文冠木及復方古日古木-7不同給藥方式下主要成分的藥代動力學性質△
馬超美,高杰,許海燕,武丹丹,葉日貴,Olusegun S.Ajala
1.內蒙古大學 生命科學學院/牧草與特色作物生物技術教育部重點實驗室,內蒙古 呼和浩特 010070;2.內蒙古醫科大學 藥學院,內蒙古 呼和浩特 010110;3.拉各斯大學 藥學院,尼日利亞 拉各斯
我國醫藥重要組成部分的蒙、藏等民族醫藥用藥特點之一是經常使用散劑,即將方劑中的藥材粉粹后直接服用。散劑的藥材用量通常較少,一般認為是游牧民族為了便于攜帶和免煎煮的原因。民族醫藥與中醫藥的另一個區別是有些與中藥相同的藥材用來治療與中醫藥用途不同的疾病,如:訶子在中醫藥中多用于久瀉、久咳,而在蒙、藏民族醫藥中則用于各種熱證、瀉痢、黃水病、肝膽病等。蒙、藏醫還認為訶子有調和諸藥和解毒等功能,使訶子成為蒙、藏醫復方中最常使用的藥材,被譽為“眾藥之王”,在民族藥中的地位與甘草在中藥中的地位相當[1-5]。紅花在蒙藥處方中出現頻率僅次于訶子,在防治肝病的復方中使用最多[1-5]。文冠木、藍盆花、黑冰片等則在中藥中很少用,而在蒙、藏藥中較常用。為闡明民族醫藥散劑用藥方式中蘊藏的科學內涵及特點,本文以蒙藥復方古日古木-7(G-7)及單味藥材文冠木的研究為例,從藥代動力學和藥效學角度綜述分析水煎劑和散劑(或甲醇提取物)的區別和原理。
1 灌胃G-7水提物、訶子水提物純成分后訶子主成分的藥代動力學性質
G-7的組成:紅花25 g、石膏15 g、麻黃15 g、紫花地丁15 g、訶子15 g、藍盆花(藍菊花)10 g、木通10 g[6]。G-7相當于藏藥中的七味紅花殊勝丸[紅花、天竺黃、獐牙菜、訶子(去核)、麻黃、木香馬兜鈴、綠絨蒿]。
從G-7的組成藥材中分離鑒定出50多種成分,包括新化合物,其結構通過多種光譜法確定[7-11]。其中藍盆花中的三萜和黃酮成分有抗α-葡萄糖苷酶活性;紅花黃酮的苷元比其苷有更強的抗氧化活性;藍盆花中的綠原酸和3,5-二咖啡奎寧酸有抗丙肝病毒作用。紫花地丁中的雙香豆素——5,5′-二秦皮乙素[5,5′-bi(6,7-dihydroxycoumarin)]有較強的抑制丙肝病毒蛋白酶作用,丙肝病毒蛋白酶半數抑制濃度(IC50)為1.4 μm;藍盆花中的熊果酸(ursolic acid)也有抑制丙肝病毒蛋白酶活性(IC50=35.0 μm)。訶子中的多酚類成分大多吸收好且具有抗丙肝病毒蛋白酶活性。訶子主要成分IC50分別為:木麻黃鞣寧(casuarinin)9.6 μm、沒食子酸(gallic acid)382.4 μm、鞣花酸(ellagic acid)56.3 μm、訶黎勒酸(chebulagic acid)5.2 μm、訶子裂酸(chebulic acid)182.6 μm、柯里拉京(corilagin)31.5 μm、訶子鞣質B(chemeinin B)67.2 μm、5-沒食子酰莽草酸(5-O-galloylshikimic acid)214.7 μm、訶子鞣質A(chemeinin A)59.7 μm、五沒食子酰葡萄糖(pentagolloyl glucose)10.6 μm。這些成分中,木麻黃鞣寧和訶黎勒酸的活性最強。
蒙藥的用藥方式包括湯劑(水提液)和散劑(藥材粉末),Gao等[12]研究了相當于湯劑的水提物在體內吸收情況。給大鼠經口給藥訶子或G-7水提物后,7種訶子活性成分吸收良好,進一步研究了訶子成分的藥代動力學性質,比較了給藥純品沒食子酸或鞣花酸與給藥訶子或G-7水提物后主要成分的藥代動力學差異。結果顯示,給藥訶子時沒食子酸和鞣花酸的AUC0~10 h分別為給藥純品化合物時的2.3和7.5倍。給藥G-7后,在血漿中可明顯檢測到沒食子酸、鞣花酸、訶黎勒酸、訶子酸、柯里拉京、訶子鞣質B及5-沒食子酰莽草酸(這7種成分的結構見圖1),其中訶子酸和沒食子酸的血藥濃度-時間曲線下面積(AUC0~10 h)最大。給藥G-7復方與單味藥材訶子相比,這7個成分的藥代動力學性質發生了明顯變化。給藥G-7復方后各成分的AUC0~10 h值分別達到給藥單味藥材訶子的倍數為:沒食子酸2.6倍,鞣花酸0.6倍,訶子鞣質B 18.1倍,訶子裂酸10.3倍,柯里拉京1.0倍,5-沒食子酰莽草酸3.7倍,訶黎勒酸3.0倍。除鞣花酸和柯里拉京外,其他5種成分在給藥G-7復方后AUC0~10 h均比給藥單味藥材訶子顯著增大。除鞣花酸外,其他6種成分的最大血藥濃度(Cmax)也在給藥G-7復方時明顯增大,達到給藥單味藥材訶子時的倍數分別為:沒食子酸2.5倍,訶子鞣質B 10.4倍,訶子裂酸20.2倍,柯里拉京3.1倍,5-沒食子酰莽草酸5.5倍,訶黎勒酸2.6倍。給藥G-7復方與單味藥材訶子相比,鞣花酸的AUC0~10 h及Cmax雖然沒有增加,但其達峰時間(Tmax)明顯縮短(復方時0.5 h,單味藥材訶子1.0 h)。其他6種成分的達峰時間也均比給藥單味藥材訶子時顯著縮短。上述結果說明G-7復方配伍后可增加多數訶子活性成分在體內的生物利用度,促進其更快更有效地吸收。

圖1 訶子主要入血活性成分的化學結構
為了探討G-7復方中的其他藥材是否含有這幾種活性成分以及是否影響這些成分的提取率,分析了這些成分在3種提取物中的含量。結果發現,G6(復方G-7除去訶子外的其他藥材配伍)提取物中檢測不到鞣花酸、訶黎勒酸、柯里拉京、訶子鞣質B及5-沒食子酰莽草酸,僅檢測到很少量的訶子裂酸和沒食子酸,分別相當于復方G-7中這2個化合物含量的0.6%和2.8%,說明復方中訶子成分體內吸收增加的主要原因不是由于其他藥材含有這些成分。比較G-7提取物及訶子單味藥材提取物中的成分含量發現,G-7提取物中含有更多的訶子裂酸、沒食子酸及5-沒食子酰莽草酸,分別是訶子單味藥材提取物中這3種成分含量的117.7%、185.2%、174.4%,說明G-7復方中的其他藥材可增加這3種訶子活性成分的溶出率,是給藥G-7比單獨給藥訶子時這3種成分體內濃度更大的主要原因之一。
分析大鼠腸內菌與訶子或G-7水提取物培養后這些活性成分的含量變化結果顯示,訶子多酚在G-7復方中被代謝分解的速率低于其在訶子中的分解速率,濃度衰減到50%初始濃度的時間均有延長,其中,訶黎勒酸從1 h延長到10 h,訶子裂酸從0.5 h延長到3.5 h。說明經口給藥G-7后復方中的其他藥材抑制了腸內菌對訶子活性成分的代謝分解速率。
上述結果說明,經口給藥G-7后訶子活性成分在體內的濃度較給藥訶子后高的原因是復方中這些成分提取率高以及在腸道內代謝分解速率減緩共同作用的結果。
2 G-7主藥材粉末及G-7甲醇提取物給藥后主成分藥代動力學性質
由于許多民族藥的主要給藥方式為散劑,即中藥粉末直接給藥,Yerigui等[13]將G-7的主要中藥紅花粉末直接灌胃大鼠,研究其主要成分的吸收情況。給大鼠灌胃紅花粉末后在血中檢測到5個主要成分:6-羥基山柰酚-3,6-二葡萄糖苷(6-hydroxykaempferol-3,6-diglucoside)、羥基紅花黃色素A(hydroxysafflor yellow A)、紅花親脂性成分(bidenoside C)、綠原酸(chlorogenic acid)、對香豆酸(p-coumaric acid)。其中,bidenoside C的AUC0~24 h面積最大,其次為羥基紅花黃色素A,前者是后者的1.39倍[13]。紅花親脂性成分bidenoside C在粉末給藥時吸收很好,因此在民族醫藥中使用含紅花的散劑時,bidenoside C在藥效方面的貢獻值得重視,同時bidenoside C在紅花散劑的質量控制中也值得受到重視。
基于以上信息,高杰[14]嘗試了G-7粉末直接灌胃大鼠,但由于G-7由7味藥材組成,定量其吸收入血成分所需粉末量超過了大鼠灌胃最大量,體積太大超過了大鼠灌胃最大量,考慮到甲醇既能提取出親水性成分又可提取出親脂性成分,因此,給大鼠灌胃G-7甲醇提取物,從而研究其主要成分的藥代動力學情況。結果顯示,經口給藥G-7復方甲醇提取物后,bidenoside C在紅花的3個成分中AUC0~10 h最大;灌胃G-7甲醇提取物后訶子主要成分的AUC0~10 h值從大到小的順序為:訶子裂酸>訶黎勒酸>鞣花酸>訶子鞣質B >5-沒食子酰莽草酸>柯里拉京>沒食子酸,而灌胃G-7水煎劑后訶子主要成分的AUC0~10 h值從大到小的順序為:訶子裂酸>訶黎勒酸>沒食子酸>鞣花酸>訶子鞣質B>5-沒食子酰莽草酸>柯里拉京。灌胃G-7甲醇提取物時,親脂性的鞣花酸的AUC0~10 h>親水性的沒食子酸,而灌胃水煎劑時沒食子酸的AUC0~10 h>鞣花酸。
3 G-7保肝活性組分的主要成分
G-7被廣泛應用于肝病的治療,但其用量較大且成分復雜,不易進行準確的質量控制以保持療效穩定。許海燕等[15]通過對G-7的甲醇提取物進行分段,找到了G-7的保肝活性部位(大孔樹脂分離的甲醇洗脫部分,MF)。研究了其對四氯化碳(CCl4)所致小鼠肝損傷的保護作用,并用高效液質聯用儀(UPLC-MS)分析了MF中的活性成分。結果顯示,連續給MF(66、132、264 mg·kg-1)4 d,每天1次,可以抑制CCl4誘導的小鼠肝臟組織病理學變化和血清轉氨酶水平的改變,并且具有一定的量效關系。給模型小鼠264 mg·kg-1的MF可顯著降低丙氨酸轉氨酶(ALT)水平(較模型組,P<0.05),極顯著降低天冬氨酸轉氨酶(AST)水平(較模型組,P<0.01)。高劑量MF給藥組的超氧化物歧化酶(SOD)較CCl4組顯著增加(P<0.01),而丙二醛(MDA)較CCl4組水平極顯著降低(P<0.01)。G-7復方的粉末3個劑量(270.84、514.68、1 083.36 mg·kg-1)直接灌胃模型小鼠時,只有1 083.36 mg·kg-1時顯著降低AST水平(較模型組,P<0.05)。說明,通過大孔樹脂可得到G-7的保肝活性部位MF,大幅降低有效劑量。
定量分析顯示,MF含有大量的鞣花酸(297.97 mg·g-1)、木犀草素與其糖苷(35.10 mg·g-1)、芹菜素與其糖苷(>30 mg·g-1)、熊果酸(14.91 mg·g-1)、bidenoside C(8.75 mg·g-1)、黃烷-3-醇聚合物(15.64 mg·g-1的原花青素A2相當量)。值得一提的是,大孔樹脂分段時,98%以上的麻黃堿類成分被甲醇-水1∶1洗脫,使得甲醇洗脫得到的MF中麻黃堿類成分的含量很少,減少了其擬腎上腺素作用。另一方面,麻黃的黃烷3-醇成分仍有較大量存在于MF部分。與G-7相比,MF的有效量和所含成分數量都大幅減少,為開發用量少并且易于質量控制的新型保肝藥物提供了科學數據。
MF為G-7的保肝活性部分,其中不僅有親水性較強的黃烷3-醇成分,更有較多的親脂性和難溶性成分,如鞣花酸、熊果酸等。鞣花酸及熊果酸是已知的保肝活性成分;黃烷3-醇及黃酮類化合物有抗氧化及清除自由基活性,也有利于保護肝臟。G-7復方含有水溶性不好的保肝及抗氧化成分,這可能是蒙藥臨床使用G-7時主要以散劑方式為主的科學基礎。
4 文冠木粉末與甲醇提取物給藥后主成分的藥代動力學性質
文冠木XanthocerassorbifoliaBunge是無患子科植物,主要分布在遼寧、河北、內蒙古等地。其干燥莖干為傳統蒙藥,用于治療風濕、痛風等。文冠木含有黃酮、三萜、縮合鞣質等成分[16-19]。Wu等[20]對文冠木提取物及全粉給藥的大鼠體內的藥代動力學性質進行研究,發現表兒茶素(epicatechin)、二氫楊梅素(dihydromyricetin)、文冠酸(xanthocerasic acid)等為主要入血成分(見圖2)。
比較了文冠木粉末及其提取物灌胃后其化學成分的藥代動力學性質[20]。由于灌胃體積的限制,可以灌胃給大鼠的最大劑量為5 g·kg-1文冠木粉。為了比較,將相應量的甲醇提取物(500 mg·kg-1)灌胃給大鼠。血漿中主要文冠木成分表兒茶素、二氫楊梅素和文冠酸的藥代動力學性質見表1。
灌胃文冠木粉末后,三萜成分文冠酸的AUC0~10 h和Cmax值比提取物小,推測是由于文冠酸的親脂性高,甲醇比消化液從藥材粉末中提取文冠酸更完全。文冠木粉末組文冠酸的Tmax比提取物組長,反映了浸提所需時間。
灌胃文冠木粉末組的表兒茶素AUC0~10 h值和Cmax顯著高于提取物組(分別為1.1和1.2倍)。在文冠木粉組中還觀察到較長的平均駐留時間(MRT)和t1/2,這表明當施用文冠木粉時,組分的吸收速率較慢。文冠木中含有以表兒茶素為延伸單元的大分子鞣質,由于其高分子特性,不能用溶劑提取出來。推測大分子鞣質在體內降解為其組成單元——表兒茶素。MRT和t1/2的延長也歸因于降解大分子釋放表兒茶素所需的時間。

圖2 文冠木的主要入血活性成分的化學結構
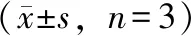

藥物代謝參數表兒茶素二氫楊梅素文冠酸FMTQFMTQFMTQAUC0~10 h/μg·L-1·h-11 367.6±23.7?1 249.6±5.2605.9±5.0602.4±5.13 339.1±149.1??6 034.8±134.1AUC0~∞/μg·L-1·h-11 373.2±26.21 250.4±5.9673.2±6.1662.6±6.13 347.6±155.4 6 375.8±183.1MRT0~∞/h 19.2±2.412.3±3.116.7±2.615.5±2.05.7±1.65.5±0.4t1/2/h 13.6±0.88.5±2.913.8±3.711.3±3.09.5±2.66.6±0.7Tmax/h0.5±0.00.5±0.00.3±0.00.5±0.02.0±0.01.0±0.0Cmax/μg·L-1186.3±9.7 151.0±4.785.9±4.972.4±1.5483.0±17.8 1 219.2±11.9 CL/F/L·h-1·kg-10.5±0.40.6±0.20.5±0.31.6±0.40.1±0.00.1±0.0
注:FM為粉末組(5 g·kg-1);TQ為提取物組(500 mg·kg-1);*與TQ組相比差異有統計學意義(P<0.05);**與TQ組相比差異有統計學意義(P<0.01)。
為了模擬大分子鞣質的體內降解過程,Wu等[20]用人工消化液對文冠木粉末和提取物分別進行了體外培養。培養5 h后,文冠木粉末在胃液培養液中的表兒茶素濃度(286.6 μmol·L-1)顯著高于提取物在胃液中的表兒茶素濃度(206.2 μmol·L-1)。說明文冠木粉中的縮合鞣質被胃液降解為其組成單位——表兒茶素(見圖 3)。
5 小結與展望
綜上,G-7含有多種活性成分,其中訶子多酚類是抗丙肝病毒蛋白酶的活性成分。大鼠經口給藥G-7后,多數訶子活性成分的吸收比給藥同量的單味藥或純品化合物時更好。復方G-7保肝活性部位MF主要含鞣花酸、熊果酸、bidenoside C、木犀草素及其葡萄糖苷、黃烷-3-醇成分等。給大鼠灌胃G-7甲醇提取物時鞣花酸的AUC0~10 h>沒食子酸,而灌胃水煎劑時親水性的沒食子酸AUC0~10 h>鞣花酸。
親脂性成分難溶于水,在水煎劑中濃度小,直接導致服用水煎劑后親脂性成分吸收少。如果某種中藥含有毒性較大的脂溶性成分,水煎劑可避免其毒性作用。對于一些基本沒有毒性的中藥,民族醫藥以中藥全粉的散劑給藥會比水煎劑給藥入血較多的親脂性成分,這些親脂性成分會對體內藥效起到不可忽視的作用。除了親脂性成分外,一些與細胞壁結合的成分或大分子成分(簡稱不可提取成分)難以被溶劑提取,但在中藥全粉的散劑給藥時能夠在體內降解吸收,如文冠木的大分子縮合鞣質受胃液作用轉化成表兒茶素吸收。中藥全粉的散劑給藥時,不可提取成分在體內消化降解產生可吸收的小分子也會對藥效有所貢獻。

圖3 文冠木不可提取的大分子縮合鞣質受胃液作用轉化成表兒茶素的示意圖
民族藥散劑的體內藥效物質基礎與湯劑有所不同,這可能是民族醫藥有時用與中藥相同的藥材治療與中藥用途不同的疾病的科學原理。民族藥散劑的體內代謝物值得深入研究;民族藥散劑的主要質量控制指標成分可能與湯劑不同,也值得深入探討。
另外,進一步研究民族藥的親脂性成分和大分子難溶性成分將有望找到新的活性物質并挖掘出民族特色藥和特色用藥方式中蘊含的深刻科學內涵。

