卵巢高級別神經內分泌癌合并高分化黏液性癌1例
趙小曉,倪海春,劉立紅,謝永輝,章宏峰
部分為惡性Brenner瘤,部分為黏液性上皮性腫瘤伴上皮增生。行經腹全子宮切除+雙側附件切除+盆腔淋巴結清掃+部分大網膜切除術。
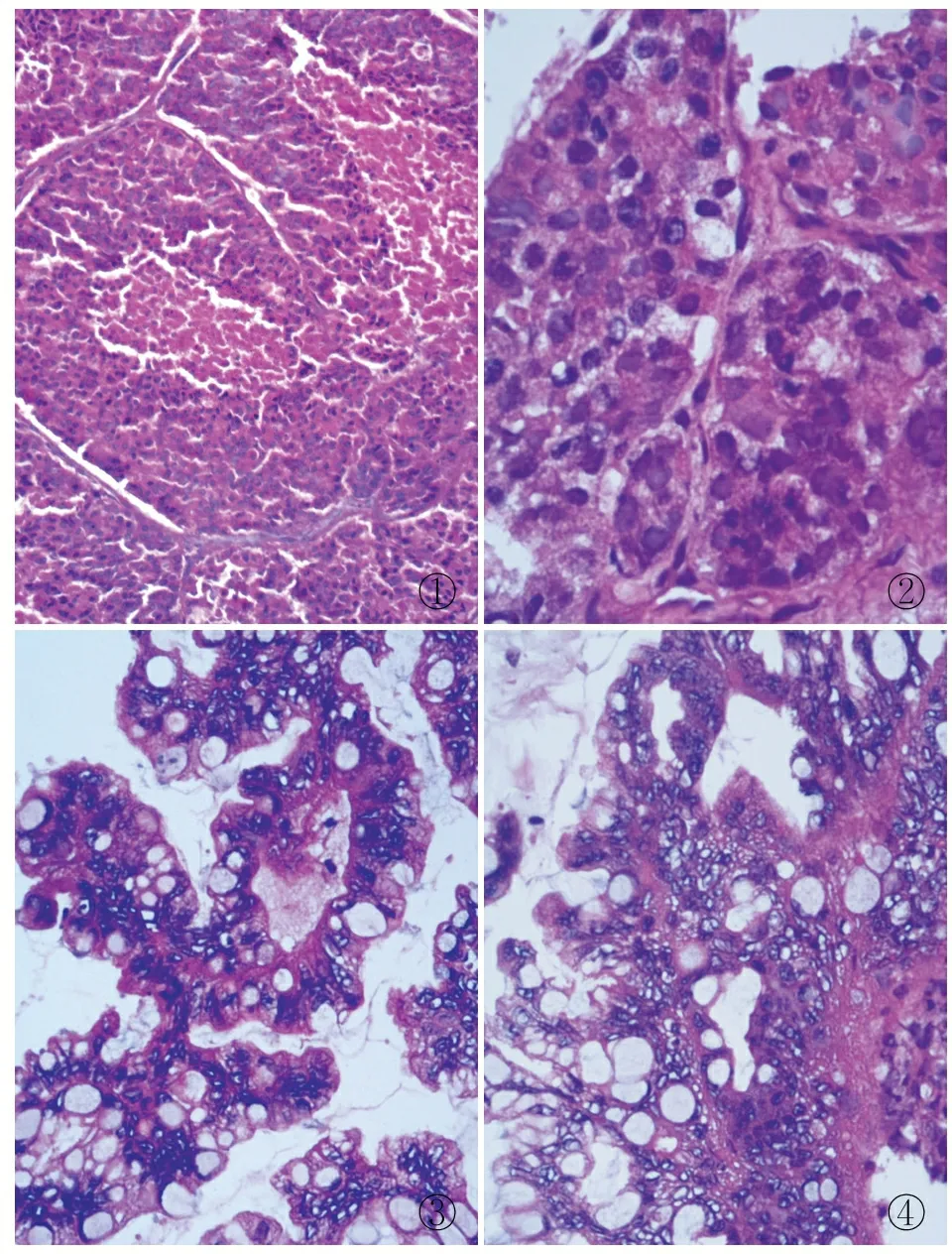
病理檢查眼觀:右側附件,輸卵管長7 cm,管徑0.5 cm,傘端可見,與之相連一已破囊實性包塊,大小11 cm×8.5 cm×6.5 cm,外壁光滑,囊性區域壁厚0.2 cm,內壁見少許囊泡樣小突起,實性區灰紅、灰黃色,乳頭狀,局部含淡黃色膠凍樣液體。鏡檢:卵巢腫瘤細胞85%呈片狀、島狀、器官樣排列,伴有壞死(圖1),細胞異型性較大,見較多核分裂(圖2);15%區域腺體密集伴間質減少(圖3),腺上皮細胞輕~中度異型,核分裂可見,呈膨脹性浸潤性生長模式(圖4)。免疫表型:神經內分泌腫瘤成分EMA、CK7、CgA、CD56和Syn均(+),p53、PAX8均部分(+),vimentin、ER、PR、p16、WT-1、PTH、TTF-1、p63、S-100和GATA-3均(-),Ki-67增殖指數約60%;黏液性腫瘤成分PAX8和CK7均(+),CDX-2和CK20均部分(+),ER和PR均(-),Ki-67增殖指數約15%。
病理診斷:右側卵巢高級別神經內分泌癌(neuroendocrine carcinoma, NEC)合并高分化黏液性癌(highly differentiated ovarian mucinous carcinoma, HDOMC);右側輸卵管示未查及明確腫瘤累及。
討論卵巢神經內分泌腫瘤(neuroendocrine neoplasm, NEN)并不常見,卵巢NEC更少見。臨床表現與其他卵巢腫瘤無明顯差異[1],診斷主要依靠腫瘤的鏡下形態特點和免疫表型。鏡下腫瘤細胞呈明顯的器官樣、實性巢狀或梁狀結構,可伴有腫瘤細胞點灶或融合片狀壞死,核分裂象>20個/10 HPF[2]。免疫表型:NEN現在應用的主要是Syn、CgA和CD56,在不同分化程度的NEN中陽性率不同,分化好的NEN可以全套神經內分泌標記陽性,分化差的NEC若形態學典型,可以僅有一個陽性,也可以全部為陰性[3]。
①②③④
圖1腫瘤細胞85%呈片狀、島狀、器官樣排列,伴壞死圖2細胞異型性較大,見較多核分裂圖315%區域腺體密集伴間質減少圖4腺上皮細胞輕~中度異型,核分裂可見,膨脹性浸潤性生長模式
鑒別診斷:(1)卵巢未分化癌:其肉眼觀察腫瘤多數呈實性,體積較大,伴出血、壞死;鏡下腫瘤細胞呈實性片塊狀分布,細胞異型明顯,分化極低,以致無法確定是何種上皮源性癌。免疫組化標記上皮性標志物陽性,但神經內分泌標志物陰性[4]。(2)低分化漿液性腺癌:鏡下腫瘤細胞乳頭結構減少或消失,呈片、巢狀,病理性核分裂象多。免疫組化標記神經內分泌標志物陰性。本例NEC伴HDOMC,需要鑒別的主要是轉移性結直腸腺癌。卵巢原發性MC以CK7+/CK20-常見,卵巢轉移性結直腸腺癌以CK7-/CK20+常見,且SATB2是鑒別卵巢原發性MC和轉移性結直腸腺癌高度特異的免疫組化標志物[5]。有研究發現MTA2可能作為一個癌基因參與卵巢上皮性癌的發展、轉移,MTA2過表達提示患者預后不良[6]。
卵巢NEC是一類高度侵襲性腫瘤,當合并HDOMC時,預后更差[7],但合并HDOMC成分時對卵巢NEC預后的影響程度的文獻報道極少。目前對于卵巢NEC治療主要方法仍以手術為主,輔助化學藥物治療以及生物治療。Natalie等[8]首次在1例卵巢非小細胞神經內分泌癌的75歲女性患者身上發現了BRCA基因突變,該研究指出卵巢癌除了高級別漿液性癌外,其它組織學類型的卵巢癌也均應該檢測BRCA1/2基因是否有突變,有BRCA1/2基因突變的患者均可使用PARP抑制劑靶向治療。本例患者術后行紫杉醇脂質體針+卡鉑針+卡鉑針方案化療,至今無瘤生存15個月,無其它不適、轉移或復發。