復(fù)方仙草顆粒的急性毒性研究
陳少鋒 梁麗清 王 河 黃 鑫 黃國(guó)東
廣西國(guó)際壯醫(yī)醫(yī)院,廣西 南寧 530001
糖尿病腎病( Diabetic Nephropathy,DN) 是指糖尿病微血管病變導(dǎo)致的腎小球硬化,又稱糖尿病腎小球硬化癥,是糖尿病的主要并發(fā)癥之一,其起病隱匿,病程進(jìn)展迅速,其患病率更是隨著糖尿病患者人數(shù)的增長(zhǎng)而逐年升高, 并成為導(dǎo)致終末期腎臟病的重要原因[1]。根據(jù)流行病學(xué)統(tǒng)計(jì)的研究,預(yù)計(jì)到2030年,世界范圍內(nèi)的糖尿病患者將達(dá)到大約3.66億人,而糖尿病腎病患者將超過1億人[2]。一但患者進(jìn)入DN蛋白尿期,進(jìn)行性發(fā)展到腎不可逆損害,最終導(dǎo)致終末期腎衰竭。因此,采用早期臨床干預(yù)防治DN具有重要意義。復(fù)方仙草顆粒由八仙草、三七、薏苡仁、制大黃、黃芪、甘草等組成,為顆粒免煎劑,10g/包,每次1包,每日3次,具有健脾益腎、清熱利濕、活血祛毒的的作用[3]。課題組前期臨床研究發(fā)現(xiàn),復(fù)方仙草顆粒在治療慢性原發(fā)性腎小球疾病及慢性腎功能衰竭和早期糖尿病腎病方面具有良好的療效[3-7],并進(jìn)行了質(zhì)量標(biāo)準(zhǔn)研究[8]。為評(píng)價(jià)復(fù)方仙草顆粒的安全性,該實(shí)驗(yàn)進(jìn)行急性毒性研究,通過觀察小白鼠的急性毒性反應(yīng),初步評(píng)價(jià)復(fù)方仙草顆粒的口服用藥安全性,為其安全性評(píng)價(jià)奠定基礎(chǔ)。
1 實(shí)驗(yàn)樣品與材料
1.1 樣品 復(fù)方仙草顆粒免煎劑,由廣西中醫(yī)藥大學(xué)附屬瑞康醫(yī)院生產(chǎn),批號(hào):20180202。
1.2 實(shí)驗(yàn)動(dòng)物 SPF級(jí)昆明種小白鼠,體重18~22g,雌雄各半,由湖南斯萊克景達(dá)實(shí)驗(yàn)動(dòng)物有限公司提供,實(shí)驗(yàn)動(dòng)物生產(chǎn)許可證號(hào):SCXK(湘)2019-0004,實(shí)驗(yàn)單位使用許可證號(hào):SYXK(桂)2019-0001。動(dòng)物分籠飼養(yǎng)、自由飲水,喂大小鼠維持飼料(北京科澳協(xié)力飼料有限公司),實(shí)驗(yàn)動(dòng)物墊料為玉米芯顆粒(東方特斯特,邳州市小河科技發(fā)展有限公司)。動(dòng)物室溫度(24±2)℃,相對(duì)濕度50%~60%,照明時(shí)間隨同自然變化。動(dòng)物室按常規(guī)定期消毒。
1.3 儀器 電子稱:型號(hào)T-2000(美國(guó)雙杰兄弟有限公司)、超純水制造系統(tǒng)(成都越純科技有限公司)。
2 方法與結(jié)果
2.1 方法
2.1.1 受試樣品的制備 取100g復(fù)方仙草顆粒,加純凈水溶解后,配制到顆粒不能繼續(xù)溶解,且剛好能通過灌胃針,配至150mL,濃度為0.67g/mL(為最大濃度),備用。
2.1.2 預(yù)實(shí)驗(yàn)情況 選取受試的SPF級(jí)昆明種小白鼠9只,禁食12h,隨機(jī)分為3組,每組各3只。第一組按照0.4mL/10g一次性灌胃給藥,第二組按照0.4mL/10g 24h內(nèi)灌胃給藥2次;第三組按照0.4mL/10g 24h內(nèi)灌胃給藥3次,1d后,觀察小鼠死亡情況。1d后,動(dòng)物均無(wú)死亡,動(dòng)物飲食和活動(dòng)正常。預(yù)實(shí)驗(yàn)結(jié)果顯示,可以進(jìn)行最大耐受量(maximum tolerated dose,MTD)實(shí)驗(yàn)。
2.1.3 MTD實(shí)驗(yàn)[8]選取受試的SPF級(jí)昆明種小白鼠40只,雌雄各半,分成空白對(duì)照組雄性組、空白對(duì)照組雌性組、給藥組雄性組、給藥組雌性組4組。實(shí)驗(yàn)前禁食12h。實(shí)驗(yàn)時(shí)稱取體重,動(dòng)物體重18~22g,空白對(duì)照組灌服純凈水,給藥組灌服受試藥物,濃度為小白鼠能耐受的最大濃度0.67g/mL,每只小鼠給藥體積均為0.4mL/10g 體重,在24h內(nèi)分3次灌服,灌胃3h后給飼料,自由飲水。連續(xù)觀察14d,每天1次,觀察記錄小鼠外觀、行為活動(dòng)、精神狀態(tài)、攝食、飲水、排泄情況,是否有中毒癥狀及死亡情況,同時(shí)在第7天、第14天稱量體重。
小鼠的最大耐受量倍數(shù)的計(jì)算方法如下[9]:

注:20g為小鼠平均體重,50000g為成人平均體重。
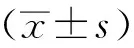
2.2 結(jié)果 MTD實(shí)驗(yàn)各組動(dòng)物給藥后均無(wú)死亡,給藥后實(shí)驗(yàn)動(dòng)物均飲食和活動(dòng)正常,未出現(xiàn)任何中毒癥狀。連續(xù)觀察14d ,未出現(xiàn)小鼠死亡。14d后稱量小鼠體重后處死小鼠,解剖后,肉眼觀察心、肝、脾、肺、腎、胸腺、卵巢、子宮、精囊、前列腺、睪丸、胃、腸及胸腔、腹腔,各臟器均無(wú)異常。實(shí)驗(yàn)前后各組動(dòng)物體重變化見表1。給藥組動(dòng)物體重在給藥前、給藥7d后、給藥14d后,分別與空白對(duì)照組比較,差異無(wú)統(tǒng)計(jì)學(xué)意義(P>0.05)。結(jié)果表明,給藥后復(fù)方仙草顆粒對(duì)小白鼠體質(zhì)量增長(zhǎng)無(wú)影響。

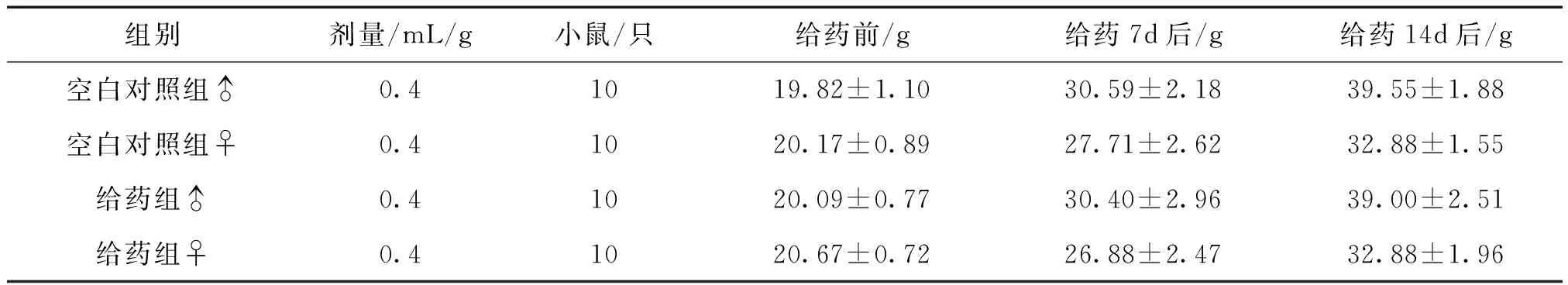
組別劑量/mL/g小鼠/只給藥前/g給藥7d后/g給藥14d后/g空白對(duì)照組♂0.41019.82±1.1030.59±2.1839.55±1.88空白對(duì)照組♀0.41020.17±0.8927.71±2.6232.88±1.55給藥組♂0.41020.09±0.7730.40±2.9639.00±2.51給藥組♀0.41020.67±0.7226.88±2.4732.88±1.96
根據(jù)臨床經(jīng)驗(yàn),復(fù)方仙草顆粒臨床推薦人用劑量為每次10g,每天3次。復(fù)方仙草顆粒最大濃度為0.67g/mL,小鼠采用40mL/kg的給藥體積,每天給藥3次,則每只小鼠的耐藥量1.608g/20g。結(jié)果經(jīng)計(jì)算,小鼠日給藥最大量為80.4g/kg。以成人每天用量30g來算,小鼠的最大耐受倍數(shù)為134倍[9],和雌雄無(wú)關(guān)。
據(jù)《中藥藥理研究方法學(xué)》,小鼠的最大耐受量倍數(shù)以耐受人用量口服100倍以上安全,本實(shí)驗(yàn)結(jié)果表明,復(fù)方仙草顆粒對(duì)小鼠的最大耐受量倍數(shù)為134倍,且受試動(dòng)物活動(dòng),飲食正常,未出現(xiàn)任何中毒癥狀,無(wú)動(dòng)物死亡,提示復(fù)方仙草顆粒無(wú)明顯毒副作用。
3 討論
中草藥毒性實(shí)驗(yàn)的目的,在于暴露藥物固有毒性,了解毒性性質(zhì)及程度,為臨床安全提供有效的科學(xué)依據(jù),也是研制新藥的基本要求。中草藥毒性實(shí)驗(yàn)根據(jù)給藥時(shí)間的長(zhǎng)短和觀察目的的不同,可分為急性毒性實(shí)驗(yàn),長(zhǎng)期毒性實(shí)驗(yàn)和特殊毒性實(shí)驗(yàn)。急性毒性實(shí)驗(yàn)又分半數(shù)致死量(LD50)測(cè)定和最大耐受量測(cè)定兩種。
據(jù)《中藥藥理研究方法學(xué)》,最大耐受量測(cè)定,即選用臨床試驗(yàn)的給藥途徑,以動(dòng)物能耐受的最大濃度,最大體積的藥量單次或24h內(nèi)2~3次給與動(dòng)物,記錄動(dòng)物反應(yīng)情況計(jì)算出總給藥量,并推算出相當(dāng)于臨床用藥量的倍數(shù)。復(fù)方仙草顆粒是中藥制劑,毒性很小,無(wú)法測(cè)出LD50,所以選用最大耐受量的測(cè)定來觀察動(dòng)物對(duì)復(fù)方仙草顆粒的耐受量,測(cè)定出復(fù)方仙草顆粒能達(dá)到人用量的134倍,和雌雄無(wú)關(guān)。從而對(duì)復(fù)方仙草顆粒的安全性做出估計(jì),為臨床用藥提供參考,也為進(jìn)一步開展復(fù)方仙草顆粒藥效學(xué)的研究提供科學(xué)依據(jù)。

