Prader-Willi綜合征患兒的臨床癥狀分析及護理干預
歐陽海梅 李娉 饒珊珊 曾靜
廣東省婦幼保健院番禺院區1遺傳代謝與內分泌科,2中藥房,3內科,4門診部(廣州511446)
Prader-Willi綜合征(Prader-Willi syndrome,PWS)是一種基因組印記遺傳性疾病,由PRADER等[1]在1956年首先報道。國外研究顯示,PWS 發病率約1/29 000,平均病死率3%[2]。目前我國尚缺乏相關統計資料。PWS臨床表型因年齡不同而存在很大差異,雖然目前已有PWS臨床篩查和診斷標準,但由于PWS臨床表現非常不特異,尤其在嬰幼兒期極容易與腦癱、脊髓性肌萎縮、低體質量兒等相混淆,確診仍依賴于分子遺傳學方法。中國PWS的文獻報道較少,且缺乏患兒的臨床癥狀回顧性分析及護理干預方面的研究。本研究分析確診為PWS的14例PWS 患兒的臨床表型特征和護理干預措施,以期讓臨床醫務人員對本病有更深層次的了解與認識[3-5],為PWS 患兒的早診斷、早治療、個性化的護理干預提供依據,從而改善患兒的生存質量,延長生命。
1 資料與方法
1.1 PWS臨床診斷及病例納入標準分別參照由GUNAY-AYGUN 等[6]和HOLM 等[7]提出的PWS臨床篩查及診斷標準,其主要診斷標準包括:(1)新生兒和嬰兒出現中樞性肌張力低下,吸吮力差,但隨年齡增加逐漸改善;(2)嬰兒期喂養困難,常需特殊喂養工具,如鼻飼、胃管等;體質量增長緩慢;(3)12個月至6歲期間,體質量迅速增加(大于兩個標準差);(4)嬰兒期特征性面容,如長顱、窄臉、杏仁眼、小嘴、上唇薄、口角向下(應含上述特征≥3 點);(5)各年齡段出現相應的性腺功能減退,生殖器官發育不全,男性有陰囊發育不良、隱睪、小陰莖和(或)小睪丸(小于同齡人第5百分位);女性有生殖器官缺如或嚴重發育不良,小陰唇和(或)小陰蒂;若不治療,16歲后仍有性腺成熟延遲和不完全,同時有青春期性征發育延遲;(6)6歲前患兒整體發育延遲,6歲以后有輕度到中度的神經發育延遲或學習障礙;(7)攝食過度/強迫攝食;(8)通過高分辨染色體分析或其他細胞或分子診斷方法確診的15q11-q13 缺失或母源性UPD。次要診斷標準包括:(1)妊娠期胎動減少,嬰兒期哭聲低,可隨年齡增長有所改善;(2)特征性行為問題:易怒、強迫行為、程序化行為等;(3)睡眠紊亂或睡眠呼吸暫停;(4)15歲時身材仍矮小(無遺傳背景,未經生長激素干預);(5)色素減退,毛發、皮膚顏色較淺;(6)與同齡兒相比手小(<P25)和(或)足小(<P10);(7)上肢尺側腕部缺乏弧度;(8)內斜視、近視;(9)唾液黏稠;(10)語言清晰度欠佳;(11)有白損皮膚的現象。本研究里,病例納入標準是:(1)我院兒童內分泌遺傳門診確診的PWS 患兒;(2)年齡<16歲。
1.2 排除標準未經PWS 基因確診、合并其他代謝性疾病、單純性肥胖、年齡>16 周歲等。
1.3 知情同意與倫理審查本研究中,所有患兒及家屬的隱私都能得到充分的保護。對所有入組患兒的家長(或監護人),均進行充分知情告知,并簽署知情同意書。本研究經廣東省婦幼保健院醫學倫理委員會審核批準,并遵守《赫爾辛基宣言》。
1.4 遺傳學檢查對納入臨床診斷標準的可疑PWS 病例,以甲基化特異性聚合酶鏈式反應(methylation-specific polymerase chain reaction,MS-PCR)方法進行初步篩查[8]。因MS-PCR 不能區分缺失型及單親二體型PWS,故對MS-PCR 篩查陽性病例,進一步以甲基化特異性多重連接探針擴增(methylation-specific multiplex ligation dependent probe amplification,MS-MLPA)方法進行確診和鑒別診斷[9-10]。MS-PCR和MS-MLPA 操作步驟分別嚴格按照CpGenome Turbo Bisulfite Modification Kit(Merckmillipore,Germany)和MS-MLPA reagents and kits(MRC-Holland,Amsterdam,the Netherlands)說明書進行。
1.5 納入研究對象的PWS患兒觀察指標 (1)基本情況:母親懷孕年齡、父親年齡、孕周、分娩方式、患兒性別、出生體質量。(2)就診情況:初診年齡、確診年齡、體質量指數、臨床癥狀、特征性行為、情緒、皮膚受損等。
1.6 護理干預護理干預的主要內容包括:醫學營養干預、行為監督和心理護理等措施進行體質量管理、改善糖脂代謝,干預周期為入院后30 d。
1.6.1 醫學營養干預(1)制定營養餐單。體質量控制是最為安全、有效、經濟的措施,而飲食管理是體質量管理的重中之重。營養師根據PWS 患兒的能量需求以及患兒的性別和年齡、體質量、糖脂等代謝情況制定科學個性化的營養餐單,飲食結構主要包括富含膳食纖維、生糖指數低具有飽腹感的全糧:燕麥、蕎麥、薏仁、小米等,選擇優質蛋白質:魚、奶、蛋以及大豆、豆腐、腐竹等[11];總能量按兒童不同年齡供給每日所需:兒童期(3~9歲)女孩700~884 kcal/d;男孩740~960 kcal/d[12],青春期按20~25 kcal/(kg·d),其中脂肪每日提供能量比例小于25%[13]。保證充足蔬菜、水果攝入。(2)飲食指導。專科護士通過參考各種文獻資料,使用通俗易懂的語言向患兒和家長介紹本疾病的基本醫學知識以及營養干預的重要性[14],詳細介紹食品交換法、發送食品交換法的圖文并茂的冊子、達到食品選擇的多樣化;食品采用電子廚房秤秤重,達到科學、準確。發放體質量管理日記本,記錄食物品種及攝入量、烹調方法、運動形式及時間、每日早晚凈體質量;建立減重微信群和添加科室微信,定時收集、評估患兒體質量管理日記,專科護士給與一對一的指導,以增強患兒和家長的信心從而改善依從性。
1.6.2 行為監督(1)改善生活方式。PWS 患兒因攝食較多,食欲旺盛、強迫攝食等行為導致中心性肥胖,嚴重影響患兒生存質量及壽命。科學安排時間,制定每日生活清單,早晚各30 min 有氧運動,快走、單車、打球、散步、游泳等中低強度的運動形式,并佩戴計步器,每日步數6 000~80 000步[15]。減少零食飲料及油炸食物攝入、定時定量進餐,減少外出進餐次數;充分的培養學習興趣、分散注意力、根據患兒不同的天賦安排跳舞、畫畫、搭積木、練字、手工、唱歌等。改善生活方式能夠有效的控制體質量快速上升。(2)食品的保管。主要目標是緩解過度的覓食行為、降低過度食物攝入,避免擺放在患兒能目視到的地方,并要求所有的食品上鎖管理;及時處理垃圾桶的食物;避免給患兒找到食品的機會從而降低患兒的覓食行為。逐漸養成良好的生活習慣,達到控制覓食行為、過度攝食的效果。
1.6.3 基礎護理(1)口腔護理。PWS 患兒口腔唾液黏稠,高腭弓,易導致食物殘留在口腔內。患兒進食后常規漱口清除殘留在口腔及咽部的食物,給予常規每天刷牙兩次,每日喝溫開水1 700~2 000 mL 以達到清潔及濕潤口腔的目的[16]。(2)皮膚護理。每日沐浴1次,及時更換汗濕衣服,并選擇寬松棉質的衣物;針對重度肥胖者且易受壓部位,采用軟墊減壓。每周修剪指甲一次,針對皮膚破損處的給予清潔消毒后止血貼外貼,可見膿點者給予百多邦外涂[17]。
1.6.4 心理護理(1)家屬方面。PWS是罕見的遺傳性疾病,家屬缺乏對疾病的認識,筆者在接診以及隨訪中需耐心講解疾病的基本醫學知識、不同年齡段的臨床癥狀、家屬照顧的重點等,讓家屬理解和接納孩子的行為,配合治療。(2)患兒方面。PWS的患兒容易沒有安全感,易出現焦慮、孤獨等負性心理[18]。在護理過程中,應主動靠近患兒,多與患兒握手、拉勾、擁抱,取得他們的依賴與信任,從而提高治療依從性。鼓勵患兒多接觸同齡人、親戚,讓他們融入社會大家庭,以樂觀心態生活,減輕心理負擔。
1.7 監測指標比較入院時與治療干預30 d 后,14例患兒的體質量、體質量指數、腰臀比,以及總膽固醇、空腹血糖、胰島素、糖化血紅蛋白等的變化情況[19-20]。
1.8 統計學方法所得監測數據指標,均采用SPSS 20.0 統計學軟件進行處理。計量資料用均數±標準差表示,組間比較方法采用t檢驗。以P<0.05為差異具有統計學意義。
2 結果
2.1 臨床資料我院兒童內分泌遺傳門診從2012年12月至2016年12月共確診14例PWS患兒,其中男11例、女3例,男女比例為4∶1。患兒出生孕周31~42周,其中足月兒10例,早產兒3例,過期產兒1例。患兒出生體質量1.55~3.80 kg,確診年齡1.5~14.6歲。患兒首次入院體檢體質量(63.13±27.89)kg;BMI(35.36±8.98)kg/m2;腰臀比(0.97±0.07),均診斷為肥胖癥[5]。病史追問和回顧性分析發現,14例患兒嬰兒期均存在中樞性肌張力低下和皮膚毛發色素減退,其他臨床表現還包括:特殊面容10例(71%),吃奶吸吮緩慢12例(86%)和唾液黏稠12例(86%)。兒童期,14例患兒均出現肥胖和智能障礙,其他臨床表現還包括:特征性行為(14例,100%)、皮膚損傷11例(79%)和外生殖器發育不良13例(93%)。見表1。
2.2 基因型14例臨床診斷的PWS 患兒均經MSMLPA 確診和分型。14例患兒基因型均為父源性15q11-q13 區域缺失型。
2.3 治療結局14例PWS 患兒經過行為監督、飲食引導和護理干預30 d 后,情緒穩定,強迫行為得到有效改善,過度的覓食行為明顯緩解。通過攝食入量限制和食品品種的優化選擇,患兒體質量、體質量指數、腰臀比等數值均出現明顯下降,糖、脂代謝紊亂得到較大改善(表2),組間比較差異具有統計學意義(P<0.05)。監測中未發現嚴重并發癥。
3 討論
PWS 屬于遺傳印跡性遺傳病,其發病機制是:在父源15q11-13 區域存在SNRPN、MKRN3 等印記基因,他們僅在父源等位基因上表達。若這些基因失去功能,便導致PWS[21]。PWS 分子缺陷類型包括:父源性15q11-q13 區域缺失(占70%~75%),母源性單親二倍體(UPD,占~25%),印記基因缺陷或基因突變(<1%)[22]。不同的缺陷類型所致臨床表型和遺傳風險存在一定差異。
PWS 發病率不低,根據國外研究報道,從1/5 000 到1/15 000 不等,平均病死率在3%[2]。但由于早期臨床表現不典型,且臨床醫師缺乏對該病的認識,容易造成漏診和誤診。因此,美國學者HOLM 等[7]于1993年總結提出了PWS的臨床診斷標準,2001年GUNAY-AYGUN 等[6]對該診斷標準進行了進一步修訂,同時提出了標準矯正建議方案,并沿用至今。本研究14例PWS 患兒主要臨床表現方面,新生兒期肌張力低下及皮膚毛發色素減退、特征性行為、兒童期肥胖和智能障礙的發生率達100%,其后依次為性腺發育不良93%、吃奶吸吮緩慢和唾液黏稠86%、皮膚受損79%等。但需要指出的是,上述臨床特點受臨床醫生主觀判斷因素影響較大,容易產生偏倚[23]。另外需要注意的是,某些臨床診斷特征,如嬰兒期中樞性肌張力低下和特殊面容,每例患兒肌張力低下程度不同,特殊面容的表現也并非每一項都一定具備,無量化標準,個體之間表現差別較大,亦存在診斷人員主觀判斷因素影響。本研究中,臨床表型的發生率與國內外相關報道[24]基本一致,提示上述臨床表型有助于PWS患兒的臨床診斷。

表1 14例PWS 患兒的臨床資料Tab.1 Clinical data of 14 children with PWS
表2 14例PWS 患兒干預前后主要監測指標Tab.2 Main monitoring indicators before and after intervention ±s
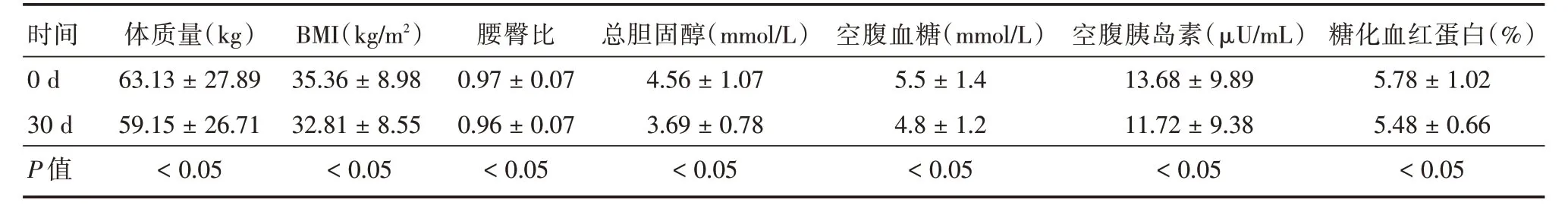
表2 14例PWS 患兒干預前后主要監測指標Tab.2 Main monitoring indicators before and after intervention ±s
時間0 d 30 d P 值體質量(kg)63.13±27.89 59.15±26.71<0.05 BMI(kg/m2)35.36±8.98 32.81±8.55<0.05腰臀比0.97±0.07 0.96±0.07<0.05總膽固醇(mmol/L)4.56±1.07 3.69±0.78<0.05空腹血糖(mmol/L)5.5±1.4 4.8±1.2<0.05空腹胰島素(μU/mL)13.68±9.89 11.72±9.38<0.05糖化血紅蛋白(%)5.78±1.02 5.48±0.66<0.05
從目前國內外關于PWS的研究內容來看,主要針對其臨床特征與遺傳學診斷,鮮有關于PWS患兒健康宣教、體質量管理及護理干預等綜合管理的研究報道。隨著年齡的增長,PWS 患兒超常的覓食行為更為顯著,研究顯示PWS 群體總體每日的能量消耗顯著降低[25],故體質量管理更為艱辛,需要醫務人員(包括臨床醫生、營養師、護理人員等)與家長、老師共同的配合。本文研究14例中最早的確診年齡為1.5歲,最大為14.6歲;BMI(35.82±9.01)kg/m2,腰臀比0.79~1.03,確診年齡普遍偏大,患兒體質量異常增加、代謝紊亂等對治療產生較為不利影響。經過30 d的體質量控制、飲食引導、行為監督引導和心理護理,患兒情緒穩定,強迫行為得到有效改善,過度的覓食行為明顯緩解,同時體質量、體質指數、腰臀比等數值均出現明顯下降,糖、脂代謝紊亂得到較大改善,說明我們的綜合治療確實有效,值得推廣。需要指出的是,目前研究的14例PWS 患兒中暫未發現母源性UPD 基因型和印記基因缺陷型,考慮可能與樣本量不夠大有關。未來準備在目前研究基礎上,進一步繼續收集PWS臨床患兒,擴大研究樣本量,以對該兩型患兒的臨床表型及治療效果進行研究。
綜上,臨床醫務人員尤其新生兒科、兒童康復科、兒保科、兒童內分泌科等科室需要加深對PWS的臨床癥狀認識,盡早診斷,及時多學科綜合模式管理干預,隨訪追蹤,以改善嬰幼兒患兒生長發育,預防學齡兒童、青少年以及成年期的體質量超重、糖脂代謝紊亂,從而提高患兒以及家屬生存質量、延長患兒壽命。

