右側外耳道多形性腺瘤一例
張爍,程敬亮,張勇
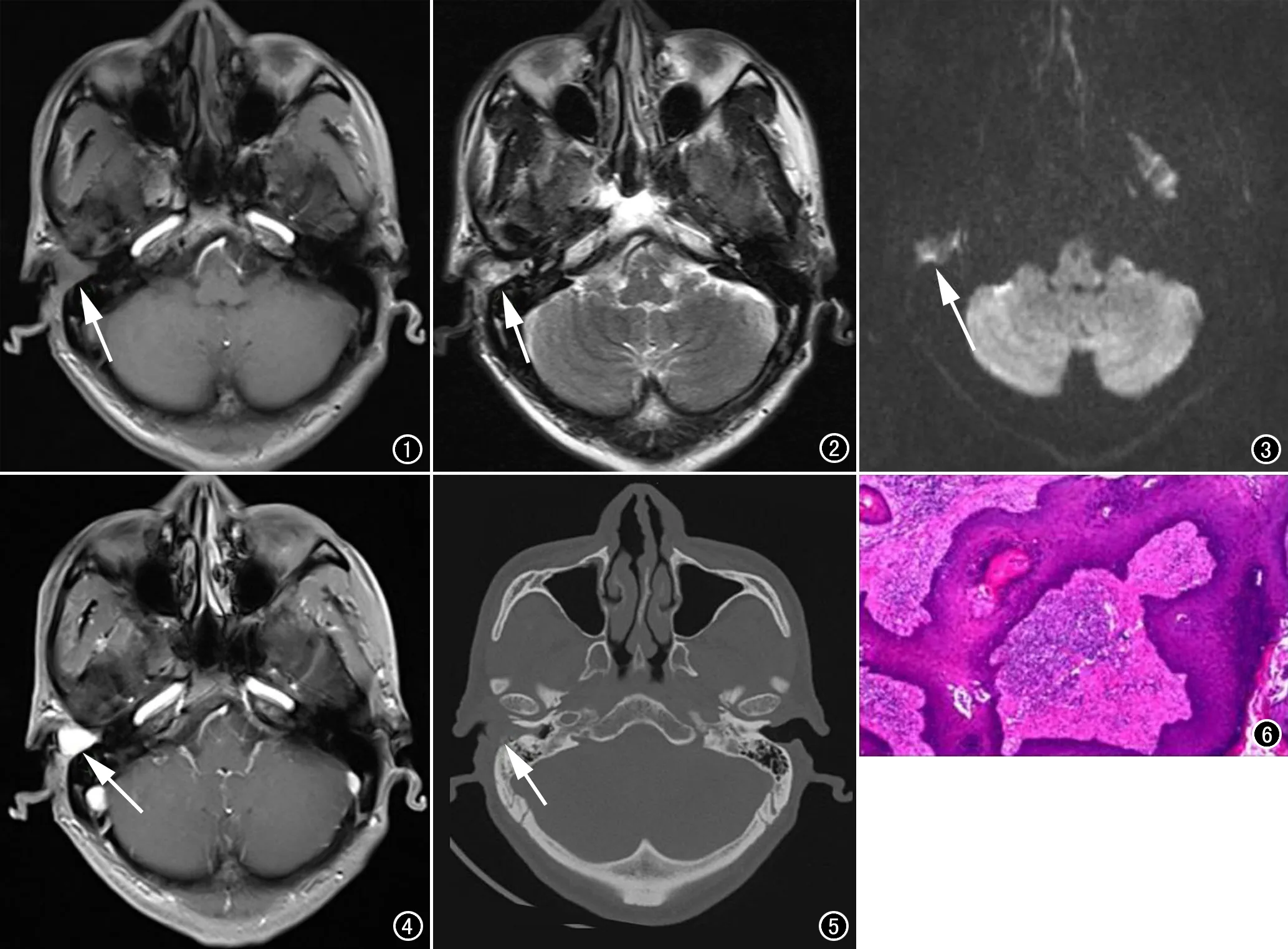
圖1 T1WI平掃示右側外耳道病灶呈等信號(箭)。 圖2 T2WI平掃示病灶呈混雜高/等信號(箭)。 圖3 DWI示病灶輕度擴散受限呈稍高信號(箭)。 圖4 T1WI增強掃描延遲期示病灶呈明顯均勻強化(箭),形態規則,邊界清。 圖5 CT平掃示右側外耳道軟組織密度影(箭),與外耳道前后壁關系緊密。 圖6 鏡下病理示上皮細胞和間質細胞混合存在,間質富含粘液(HE,×100)。
病例資料患者,男,52歲,右耳悶伴聽力下降2個月,1個多月前右耳流出淡黃色稀薄液體,無臭味,伴耳癢。查體:右側外耳道見新生物堵塞,表面不光滑,少量分泌物,鼓膜無法窺及。MRI上表現為右側外耳道等T1、混雜稍長T2信號(圖1、2),DWI上呈稍高信號(圖3);動態增強掃描示病變呈漸進性強化,延遲期強化明顯,邊界清晰(圖4)。CT上表現為右側外耳道內軟組織密度影,CT值約60HU,與外耳道前后壁關系緊密(圖5)。MRI及CT診斷:右側外耳道占位。行右側外耳道腫物切除術,術中見腫物位于右側外耳道深部,基底位于外耳道后上壁,表面不光滑,呈桑葚樣,周邊伴少量膿性分泌物;擴大切口分離腫塊,見腫塊位于外耳道皮下,與周邊組織分界清,分離外耳道皮瓣,取出腫塊;肉眼觀腫塊大小約1.5cm×1.5cm,色白,表面欠光滑,質脆。術后病理檢查鏡下見上皮細胞和間質細胞混合存在,腫瘤呈多結節生長,富含粘液,邊界不清(圖6)。免疫組化:AE1/AE3(+),CK7(+),CK8/18(+),P63(+),Calponin(+),S-100(+),SOX-10(+),Her-2(2+),Ki-67(5%+)。病理診斷:涎腺源性腫瘤,結合免疫組化,符合多形性腺瘤。
討論多形性腺瘤(pleomorphic adenoma,PA)是一種常起源于涎腺的混合瘤,主要發生在腮腺[1]、頜下腺等大涎腺及口腔、上呼吸道等處的小涎腺。原發于外耳道的PA非常罕見,僅有少數個案報道[2]。外耳道PA以鏡下結構的多形性為主要特征,多包含上皮和肌上皮細胞、粘液樣或軟骨樣等混合結構。早期臨床上多無明顯癥狀,隨著腫瘤逐漸增大,可出現傳導性聽力下降,耳部飽脹、閉塞感,部分患者可出現耳痛、耳鳴、耳漏等癥狀[3,4]。
PA可因細胞密度、組成細胞類型和比例的不同,影像學表現存在一定的差異性。MRI上多表現為長T1、長或混雜T2信號,DWI上多表現為高信號。CT平掃表現為稍低的軟組織密度,這與其富含粘液樣或軟骨樣基質有關[5];增強掃描多呈漸進性強化,可能是由于其血流不豐富,對比劑進入微血管和間質緩慢造成的[6]。本例表現為等T1、混雜稍長T2信號,DWI上呈稍高信號,MRI增強掃描呈漸進性強化,延遲期強化明顯,CT表現為稍低的軟組織密度影,符合外耳道PA的影像學表現。
外耳道PA需與以下疾病相鑒別:①膽脂瘤性中耳炎,MRI上多呈短/等T1、長T2信號,增強掃描多無強化,CT表現為團片軟組織密度影,密度多不均勻;②外耳道乳頭狀瘤,表現為乳頭狀新生物,基底較廣,多有蒂。MRI上多表現為等T1、等/長T2信號,增強掃描多表現為輕度不均勻強化。CT平掃多表現為團塊狀軟組織密度影,可伴外耳道、中耳、乳突的骨質破壞;③耵聹腺瘤:多為良性腫瘤,與發生于外耳道的多形性腺瘤臨床癥狀相似,較少侵犯周圍組織。MRI上多表現為長T1、長T2信號,增強掃描多呈不均勻強化。外耳道PA因其組成成分、臨床表現、解剖位置等具有多樣性,且發生率極低,因此誤診率較高,結合MRI和CT檢查,有助于該病的臨床診斷。

