齊墩果酸A環衍生物的合成與體外抗腫瘤活性研究
王 強, 孟艷秋
(沈陽化工大學 制藥與生物工程學院, 遼寧 沈陽 110142)
齊墩果酸(oleanolic acid,OA)是一種五環三萜類化合物,在自然界中分布廣泛,主要以游離或與糖結合成糖苷的形式存在.OA具有廣泛的生物活性,如護肝、抗病毒、抗炎、抗糖尿病、抗腫瘤等[1-4].OA結構中可供修飾的位點有限,研究主要集中在A環、C環、C-3和C-28位,對其他位點進行改造的報道不多.目前,Honda等[5-6]發現了化合物1(化合物1~3的結構見圖1)是OA研究領域的一個重大突破,其具有極強的抗腫瘤活性.化合物2和化合物3等均表現出顯著增強的抗腫瘤活性,并且能夠作用于細胞內多條信號轉導通路,是迄今為止抗腫瘤活性最強的半合成三萜化合物[5-7].因此,化合物1的結構優化也成為當前的研究熱點.WIEMANN等[8]對OA的C-3位羥基和C-28位羧基進行了結構修飾,合成的氧肟酸衍生物較OA抗腫瘤活性有了顯著增強.另有研究發現[9-11],將C-28位羧基改造成酯或酰胺,對提高OA的抗腫瘤活性有利.

圖1 化合物1~3的結構
本文結合前期OA結構改造的經驗[12-13],將A環C-2,3位改造成酮肟基,形成新型A環結構,同時C-28位羧基進行成酯或酰胺化,設計合成了兩類共10個新型OA衍生物.合成路線見圖2.
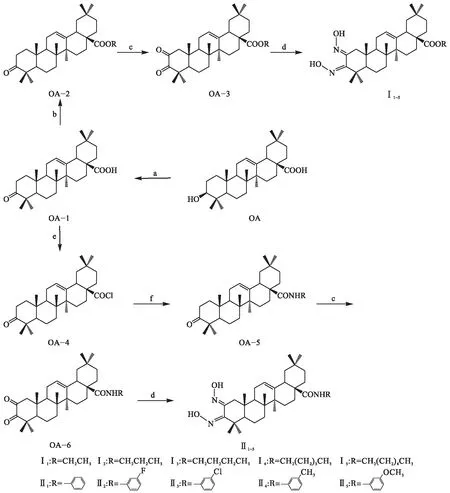
試劑和條件:a 丙酮,瓊斯試劑,室溫 b 二甲基甲酰胺,無水碳酸鉀,溴代烷 c 叔丁醇,叔丁醇鉀,50 ℃ d 鹽酸羥胺,無水吡啶 e 二氯甲烷,草酰氯,二甲基甲酰胺,室溫 f 苯酰胺,三乙胺,室溫
1 實驗部分
1.1 化學合成
1.1.1 3-氧代-齊墩果烷型-12-烯-28-羧酸的制備(OA-1)
OA(0.500 g,1.10 mmol) 溶解于50 mL丙酮溶液中,冰浴條件下緩慢滴加配制的新鮮Jones 試劑(0.64 mL,5.78 mmol),常溫反應2 h后,加入異丙醇(15 mL),常溫反應0.5 h.水洗,無水硫酸鎂干燥,減壓抽濾,蒸發溶劑.粗品分離純化[V(石油醚)/V(乙酸乙酯)=20/1],得白色固體OA-1(0.470 g,質量分數為95 %).
中間體OA-1(0.470 g,1.05 mmol) 溶解于DMF(20 mL),加入碳酸鉀(0.3g) 和溴乙烷[n(OA-1)∶n(溴乙烷)=1∶5],常溫反應5 h.過濾,水洗,無水硫酸鎂干燥,減壓抽濾,蒸發溶劑.粗品分離純化[V(石油醚)/V(乙酸乙酯)=50/1],得白色固體OA-2(0.380 g,質量分數為76 %).
1.1.3 2,3-二氧代-齊墩果烷型-12-烯-28-羧酸乙酯的制備(OA-3)
化合物OA-2(0.380 g,0.79 mmol) 溶解于叔丁醇(30 mL),加入叔丁醇鉀(25 mg,2.22 mmol) 和四氫呋喃(3 mL),50 ℃水浴反應6 h.蒸發去除溶劑,先用鹽酸進行酸洗,再用食鹽水進行水洗,無水硫酸鎂干燥,減壓抽濾,蒸發溶劑.粗品分離純化[V(石油醚)/V(乙酸乙酯)=50/1],得白色固體OA-3(0.440 g,質量分數為89 %).
1.1.4 2,3-二酮肟-齊墩果烷型-12-烯-28-羧酸乙酯的制備(Ⅰ1)
化合物OA-3(0.440 g,0.70 mmol) 溶解于無水吡啶(20 mL),加入鹽酸羥胺(0.9 g,13.00 mmol),120 ℃油浴回流1 h.冷卻到室溫時,有白色固體析出,然后過濾、干燥.粗品分離純化[V(石油醚)/V(乙酸乙酯)=20/1],得白色固體Ⅰ1(0.320 g,質量分數為86 %).
制備化合物Ⅰ2~Ⅰ5時替換為不同的鹵代烷,按上述方法操作.
1.1.5 3-氧代-齊墩果烷型-12-烯-28-酰氯的制備(OA-4)
中間體OA-1(0.470 g,1.05 mmol) 溶解于二氯甲烷(25 mL),加入草酰氯(0.85 mL,1 mmol)和DMF(20 mL),常溫反應4 h.蒸發去除溶劑,加入適量環己烷移除殘余草酰氯,減壓脫溶,得淡黃色固體OA-4(0.370 g,質量分數為74 %),直接進入下一步反應.
利用CPTU實測資料來估算土層重度,Larsson和Mulabdic(1991)通過對在瑞士、挪威和英國的試驗資料的分析,提出采用凈錐尖阻力(qt-σvo)和孔壓參數比Bq對土的密度或重度進行估計。
1.1.6 3-氧代-齊墩果烷型-12-烯-28-酰-苯胺的制備(OA-5)
化合物OA-4(0.370 g,0.76 mmol) 溶解于二氯甲烷中,加入苯酰胺[n(OA-4)∶n(苯酰胺)=1∶1.2]和三乙胺(TEA,0.6 mL),常溫下反應過夜,蒸發去除溶劑.粗品經硅膠柱色譜分離、純化[V(石油醚)/V(乙酸乙酯)=60/1],得淡黃色固體OA-5(0.280 g,質量分數為69 %).
1.1.7 2,3-二氧代-齊墩果烷型-12-烯-28-酰-苯胺的制備(OA-6)
化合物OA-5(0.280 g,0.55 mmol) 溶解于叔丁醇(30 mL),加入叔丁醇鉀(25 mg,2.22 mmol) 和四氫呋喃(3 mL),50 ℃水浴反應6 h.蒸發去除溶劑,加入適量乙酸乙酯溶液溶解,先用鹽酸進行酸洗,再用食鹽水進行沖洗,最后用無水硫酸鎂干燥、過濾、蒸發去除溶劑.粗品經硅膠柱色譜分離、純化[V(石油醚)/V(乙酸乙酯)=60/1],得淡黃色固體OA-6(0.240 g,質量分數為85 %).
1.1.8 2,3-二酮肟-齊墩果烷型-12-烯-28-酰-苯胺的制備(Ⅱ1)
化合物OA-6(0.240 g,0.40 mmol) 溶解于無水吡啶中(20 mL),加入鹽酸羥胺(0.6 g,8.63 mmol),120 ℃油浴回流1 h.冷卻到室溫時,有白色固體析出,然后過濾、干燥.粗品經硅膠柱色譜分離、純化[V(石油醚)/V(乙酸乙酯)=20/1],得淡黃色固體Ⅱ1(0.200 g,質量分數為84 %).
制備化合物 Ⅱ2~Ⅱ5時替換為不同的胺類,按上述方法操作.
1.2 初步體外活性測試
以吉非替尼和阿霉素為陽性對照物,采用MTT法對合成的目標化合物進行體外抗腫瘤活性測試.選用人胃癌SGC7901和人肺癌A549細胞為靶細胞.在96孔培養板內培養對數生長期的腫瘤細胞,每100 μL約4 000個細胞.將其置于37 ℃、體積分數為5 %的CO2全濕條件培養24 h.將含有不同濃度的合成的10個新型衍生物加入到給藥組,設置3個平行孔.陰性對照組加有等體積的溶劑(無血清的RPMI-1640培養基),并設只加RPMI-1640培養基的空白對照組,置37 ℃、體積分數為5 %的CO2溫箱中培養72 h,丟棄培養液,每孔加入MTT溶液50 μL,37 ℃ 下孵育4 h,丟棄上清液,每孔加入 DMSO 150 μL,輕度振蕩溶解甲臜顆粒.在酶標儀波長490 nm條件下測定光密度值(OD),計算所測化合物對腫瘤細胞的抑制率和IC50值.實驗重復3次,結果取平均值.
2 結果與討論
2.1 目標化合物的確證
目標化合物結構經1H-NMR、MS等確證,數據見表1和表2.
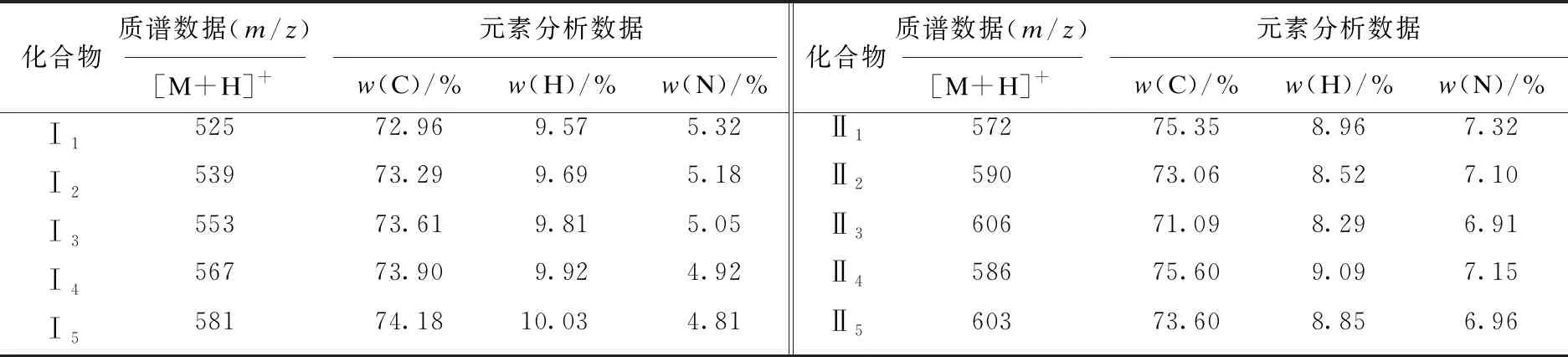
表1 目標化合物的質譜和元素分析數據

表2 目標化合物的氫譜數據
所有目標化合物結構經1H-NMR、MS等確證,為10個未見報道的新型齊墩果酸衍生物.
2.2 生物活性評價
采用MTT法對目標化合物進行初步的體外抗腫瘤活性測試.選用吉非替尼和多柔比星為陽性對照物,人胃癌細胞SGC7901和人肺癌細胞A549為靶細胞,實驗結果見表3.
由表3中分析可知:在一定濃度下目標化合物對SGC7901、A549均具有一定抑制作用,且活性強于母體OA.C-28位羧基成酯時,活性整體呈上升趨勢,表明隨著酯鏈的延長活性更佳;C-28位羧基成酰胺時,活性普遍強于成酯類;其中化合物Ⅱ5表現出良好的抗腫瘤活性,IC50值分別為10.76和13.28,與吉非替尼活性相當,可進一步研究.
3 結 論
以OA為先導化合物,對A環及C-28位羧基進行結構改造,設計合成了兩類新型OA衍生物.經體外藥理活性測試,C-28位羧基成酯或成酰胺,均能顯著提高抗腫瘤活性,表明OA的活性位點主要來自于A環,這與Honda等發現化合物1的觀點一致,說明對A環的結構改造至關重要.同時化合物Ⅱ5表現出較強的抑制活性,可能與苯環上帶有吸電子基團有關,說明在C-28位連接帶有強吸電子基團的結構更能提高抗腫瘤的活性,這也是本文的下一步研究方向.綜上所述,本研究結果對進一步OA結構修飾有一定的參考意義.

