腫瘤惡液質病人肌肉減少的分子機制
朱明星 盧宗亮 吳長蓬 許紅霞
據全球腫瘤流行病數據估計(GLOBOCAN 2018),2018年全球約有1 810萬新增癌癥病例和960萬癌癥死亡病例[1]。其中,亞洲癌癥患病人數和死亡人數分別占全球病例的60%和70%。在我國,癌癥同樣是人口死亡的主要原因,也是重大的公共衛生問題。國家癌癥中心提供的數據顯示,2015年中國約新增429.2萬癌癥病例和281.4萬癌癥死亡病例[2]。
終末期癌癥病人往往表現為極度消瘦、厭食、乏力、體能差甚至臥床,即出現惡液質(cachexia)狀態。惡液質是腫瘤最常見的并發癥之一,報道稱80%左右的胃癌或胰腺癌,50%左右的結腸癌、肺癌或前列腺癌,以及約40%的乳腺癌病人隨癌癥進展會出現惡液質[3],約30%的癌癥病人因惡液質死亡[4]。骨骼肌減少(muscle atrophy,MA)是惡液質的核心表現。惡液質的定義比較公認的是Fearon等[5]在2011年腫瘤惡液質國際大會專家共識中提出的:“以持續性骨骼肌丟失為特征,不能被營養支持完全緩解,逐步導致器官功能損害的多因素綜合征”。除惡性腫瘤,多種慢性疾病,如COPD、CHF、慢性腎功能衰竭、艾滋病等到疾病后期均可發生肌肉減少及惡液質狀態[6]。2008年在華盛頓召開的惡液質大會中,臨床醫師和研究人員對惡液質的診斷標準達成共識[7],即人體在無節食的情況下,6個月內體質量下降>5%;或BMI<20(我國<18.5)同時伴有體質量下降>2%;或四肢骨骼肌量指數(appendicular skeletal muscle index, ASMI)符合肌肉減少癥標準(男性<7.0 kg/m2,女性<6.0 kg/m2-歐洲人群)及同時伴有體質量下降>2%。
世界腫瘤惡液質年會(International Society on Sarcopenia, Cachexia and Wasting Disorders Conference)截至2019年已舉行11屆,大會每年對腫瘤惡液質最新進展和熱點問題進行探討,其中對腫瘤惡液質病人肌肉減少的分子機制研究逐年增多。肌肉減少原因歸結起來就是肌肉蛋白質降解增加與蛋白質合成受阻。研究顯示,惡液質肌肉減少涉及的蛋白質合成的信號通路主要是PI3K/AKT/mTOR信號通路,而涉及的蛋白質降解通路主要包括AKT/FOXO3a通路、Myostatin/Activin A/B信號通路、炎癥因子NF-κB通路、p38MAPK信號通路以及JAK-STAT通路等(圖1)。
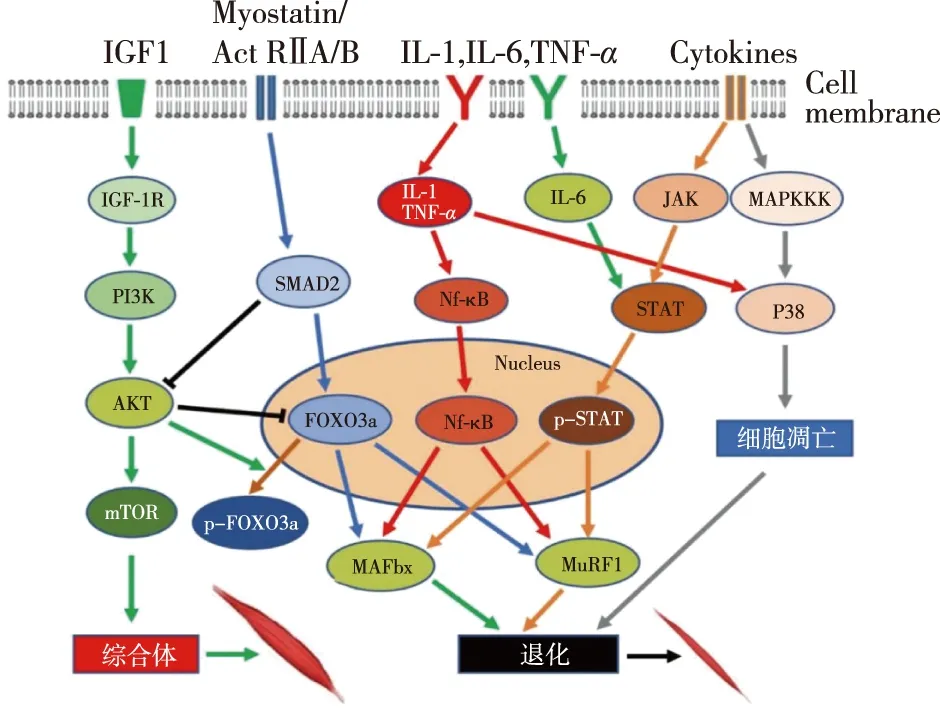
圖1 腫瘤惡液質發生肌肉減少機制示意圖
1 蛋白質合成PI3K/AKT/mTOR通路
磷脂酰肌醇3-激酶(phosphatidylinositol3-kinases,PI3Ks)是細胞內的一種磷脂酰肌醇激酶,參與多種細胞生命活動,如細胞生長、增殖、分化、運動、存活和物質轉運等。PI3Ks的作用與致癌基因PIK3CA和抑癌基因PTEN密切相關[8]。
蛋白激酶B(protein kinase B, PKB)即AKT,是一種絲氨酸/蘇氨酸特異性蛋白激酶,在多種細胞生長過程中發揮關鍵作用,如葡萄糖代謝、凋亡、細胞增殖、轉錄和細胞遷移。過表達AKT的轉基因小鼠,其骨骼肌肌量明顯增大,AKT相關信號通路被激活[9]。磷酸化的AKT可促進小G蛋白Rheb(Ras homology enriched in brain,Rheb)的正調控,從而促進Rheb集聚,激活哺乳動物雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR)復合體。這一過程激活蛋白質翻譯,進而增加骨骼肌細胞分化生長。mTOR與其他蛋白相結合,形成mTOR復合物1(mTORC1)和mTOR復合物2(mTORC2)2種不同的蛋白質復合物,他們調節不同的細胞過程,具有促進物質代謝,參與細胞凋亡、自噬的功能。
PI3K/AKT/mTOR通路主要與蛋白質的合成相關。該通路具體的分子途徑是:PI3K-AKT經PI3K生成磷脂酰肌醇三磷酸(PIP3),進一步激活磷酸肌苷依賴性蛋白激酶-1(phosphoinositide dependent proteinkinase-1,PDK1),PDK1通過磷酸化激活AKT,使AKT定位于質膜,進一步激活αNF-κB激酶抑制劑(inhibitor of nuclear factor kappa-B kinase subunit alpha,IKK-α),IKK-α磷酸化激活mTORC2。
一些因子可以激活該通路,其中包括表皮生長因子(epidermal growth factor,EGF)、類胰島素生長因子(insulin-like growth factors-1,IGF-1)、胰島素和鈣調蛋白(calcium modulated protein,CaM)等[10-12]。胰島素或IGF-1與其受體相結合后,通過胰島素受體底物(insulin receptor substrate-1,IRS-1)激活PI3K/AKT/mTOR信號通路,促進蛋白質的合成[13]。當細胞缺乏IGF-1或者發生胰島素抵抗時,會抑制PI3K/AKT/mTOR通路,從而使真核翻譯起始因子4E結合蛋白(eukaryotic translation initiation factor 4E-binding protein,4E-BP)和p70核糖體蛋白S6激酶(ribosomal protein S6 kinase beta-1,S6K1,也稱p70S6K)下調,最終導致真核翻譯起始因子(eukaryotic initiation factor 4E, eIF4E)和p70S6K等促進蛋白質合成相關過程受到抑制[13]。有研究顯示,當小鼠被敲除胰島素受體后,肌肉重量和功能下降的主要原因是蛋白合成受到抑制而非分解增加[14]。
2 肌肉AKT/FOXO信號通路
叉頭因子O蛋白家族(forkhead box class O family,FOXO)是調節骨骼肌細胞平衡的重要分子,其中FOXO1和FOXO3是調節骨骼肌蛋白質降解的主要成員。AKT可以促進FOXO磷酸化,抑制FOXO核轉位而阻止其轉錄,同時阻止E3連接酶上調,抑制蛋白水解系統激活,減少蛋白降解[15]。惡液質狀態時,FOXO通路相關基因增加,促進病人的肌肉減少。動物實驗研究顯示,骨骼肌FOXO1轉基因小鼠的Ⅰ型肌纖維基因表達下調、血糖控制受損,小鼠骨骼肌體積減小[16]。Milan等[17]發現,在肌肉減少過程中,FOXO轉錄網絡通過調節泛素-蛋白酶體系統和自噬系統發揮作用。抑制FOXO的轉錄活性可抑制肌肉蛋白質的泛素化降解。在小鼠惡液質模型中,FOXO過度激活導致肌肉減少。有證據顯示,抑制FOXO能夠挽回肌肉損失[18]。
FOXO1和FOXO3在誘導轉錄泛素化酶肌肉環狀指基因1(muscle ring finger1,MuRF1)和肌肉萎縮盒F基因(muscle atrophy F-box,MAFbx,Atrogin-1)的上調中發揮關鍵作用[19]。MuRF1和MAFbx是一種E3連接酶,為骨骼肌萎縮的蛋白標志物。肌蛋白在降解過程中,需要經過其泛素化后再被蛋白酶體降解。在去神經、糖皮質激素過量等條件下,MuRF1和MAFbx過度活化,引起惡液質[20]。MuRF1不僅能降解細肌絲中的肌動蛋白和肌鈣蛋白相關成分,而且MuRF1和MAFbx還均參與了粗肌絲肌球蛋白重鏈相關成分的分解[21]。有研究顯示,激活IGF-1/AKT/mTOR信號通路,能夠抑制MuRF1和MAFbx等的活性,從而使蛋白酶體系統中E3泛素化連接酶活性下調。將IGF-1注入小鼠體內,可以激活AKT,然后磷酸化FOXO,導致MuRF1和MAFbx表達降低,減少肌肉降解[19,22]。
一項有趣的研究發現,過氧化物酶體增殖物激活受體γ輔激活子1α(peroxisome proliferator-activated receptor gamma coactivator 1-alph, PGC-1α)與AKT作用類似,能負調控FOXO的激活[22]。在荷瘤小鼠和肌肉萎縮的條件下,PGC-1α在血液和組織中的含量下降,而過表達PGC-1α則抑制FOXO3a的表達,逆轉部分肌肉損失。同時,在運動過程中可以激活PGC-1α的表達。進一步研究發現,PGC-1α可調節肌纖維中線粒體的生物合成和氧化磷酸化[23]。在腫瘤惡液質中,肌肉萎縮針對的是Ⅱ型肌纖維,而Ⅰ型肌纖維并沒有類似的降解[24]。這有可能是由于PGC-1α抑制Ⅰ型肌纖維中的FOXO3a活性所致。嘗試尋找PGC-1α的激活劑可能是一種很有前景的、可以防止腫瘤或者其他分解代謝條件下的肌萎縮的方法。
3 Myostatin和激活素A/B信號通路
Myostatin又稱肌肉生長抑制素,是較晚發現的在生物進化中極保守的轉化生長因子-β(TGF-β)超家族成員,Myostatin主要由骨骼肌細胞合成和分泌,具有特異性抑制肌肉生成的作用,能誘導惡液質的發生[25]。Myostatin可有效抑制細胞周期由G1期向S期的過渡,使細胞生長速度顯著變慢,細胞周期蛋白CyclinD1表達下調,從而抵制成肌細胞的增殖;同時骨骼肌分化標志肌細胞生成素(Myogenin)和主要組織相容性復合體(MHC)的表達也受Myostatin抑制,導致成肌細胞不能分化為多核的融合肌管細胞。小鼠過表達Myostatin可導致骨骼肌明顯萎縮[26],相反,通過不同基因方法抑制Myostatin的表達可促進肌肉質量和肌纖維增大[27]。Myostatin的拮抗劑已被證明能夠預防Lewis肺癌(Lewis lung carcinoma,LLC)小鼠模型中的腫瘤惡液質[28]。
除Myostatin外,激活素A/B (Activin A/B)作為TGF-β家族成員,可激活TNF-α/TAK1通路,在骨骼肌細胞中可發現Activin A上調[29],阻斷該模型中的Activin A,可以逆轉肌肉萎縮。TGF-β分子通常與激活素Ⅱ型受體(ActRⅡ)相結合,激活ActRⅡ通路中肌肉萎縮關鍵的泛素連接酶MAFbx/Atrogin1,增加MuRF1的表達,可增強肌肉蛋白的泛素化作用,從而導致肌原纖維蛋白降解[30-31]。ActRⅡ拮抗劑能完全抵消上述作用[32]。最近的研究顯示,ActRⅡB受體拮抗劑可用于治療4種不同小鼠模型的腫瘤惡液質。
因此,Myostatin主要通過ActRⅡB-SMAD2/3通路阻斷骨骼肌分化增殖[33]。有趣的是,IGF-1可以顯著逆轉Myostatin對AKT的抑制[34]。但在腫瘤病人中,這顯然是存在一定問題的,因為IGF-1可能與腫瘤的發生發展有關。骨骼肌的保存是通過阻斷Myostatin和Activin A/B信號通路而實現的,但他并不一定是所有動物模型和人類發生腫瘤惡液質的原因。
4 炎癥因子通路
腫瘤惡液質常伴有全身性慢性炎癥狀態,NF-κB、CRP、 IL-1、IL-6、TNF-α等炎癥因子水平會有不同程度的升高。
NF-κB是肌肉萎縮中一種重要的轉錄因子,它參與細胞凋亡、炎癥和分化等多種細胞生命活動[35],能被許多炎癥因子所激活。研究發現,NF-κB可被TNF-α、TWEAK(TNF-related weak inducer of apoptosis)、IL-1、蛋白水解誘導因子(proteolysis inducing factor,PIF)、血管緊張素Ⅱ(AngⅡ)等通過活性氧簇誘導激活,激活的NF-κB能夠促進Myostatin的表達增加,從而使肌肉分化生長因子(myogenic differentiation,MyoD)的mRNA表達下調,導致骨骼肌的生長與分化受阻,最終破壞肌肉組織的損傷修復[36]。IL-1能通過介導NF-κB和p38-MAPK信號通路,促進E3連接酶MuRF1和MAFbx基因的表達,進而使肌纖維蛋白發生泛素化降解[37]。TWEAK通過激活NF-κB而上調MuRF1,導致MyHC消耗增加[37]。NF-κB抑制劑可以通過抑制NF-κB通路減少MuRF1和MAFbx的表達,從而顯著地降低腫瘤惡液質引起的肌肉萎縮[38]。
TNF-α由活化的巨噬細胞合成,可以誘導惡液質的發生[39]。在體外試驗中,TNF-α可使脂肪細胞從血漿脂蛋白中攝取脂肪酸減少,抑制脂肪合成,同時抑制骨骼肌細胞的分化,并在一定程度上抵抗胰島素,進而影響胰島素信號通路[40]。加入TNF-α抑制PI3K/AKT通路,可以導致培養的肌細胞肌管萎縮,還可以通過NF-κB和p38-MAPK激活MuRF1等E3連接酶誘導泛素化-蛋白酶體途徑,導致肌原纖維蛋白分解[41-43]。惡液質狀態下,骨骼肌組織中是否存在先天免疫細胞很少被報道,因此,這些細胞也不太可能在肌肉組織環境中產生TNF-α。從這個角度來說,TNF-α與腫瘤惡液質的關系就不太清楚。最近的一項研究顯示[44],對腫瘤惡液質病人使用TNF-α抗體抑制其功能后,惡液質并沒有獲得任何改善效果,在觀察的濃度下,TNF-α可能是一種促進因子,但不足以促使肌肉組織萎縮,還需要其他腫瘤或炎癥因子的協同作用。
IL-6是由活化的巨噬細胞產生的,是癌癥惡液質全身炎癥的驅動因子,多種腫瘤都會分泌IL-6[45]。IL-6可能是通過中樞神經系統引起惡液質,促進惡液質病人氧化應激的發生,抑制下丘腦脂肪酸氧化,從而引起食物攝入減少。中樞注入IL-6的拮抗劑可以改善病人食物攝入,但只有超生理劑量下的IL-6才能誘導無腫瘤或疾病狀態下的肌肉萎縮[46]。在IL-6依賴的鼠惡液質模型中,肌蛋白合成的抑制在早期即發生,與正常對照組相比,C26荷瘤小鼠腓腸肌重量減輕到對照組的84%,蛋白水解酶的活性明顯降低,說明溶酶體組織蛋白酶通路和ATP依賴性蛋白水解通路參與其中[47]。在IL-6誘導的肌肉萎縮過程中,IL-6是否直接調控E3連接酶的表達還具有一定爭議。IL-6信號通路模式是通過信號轉到受體形成的異質二聚體(gp130)和膜結合受體,激活JAK/STAT信號轉導通路下游,導致信號傳導及轉錄激活蛋白(STAT)磷酸化,進入細胞核調控基因的轉錄[48]。最近,在消瘦的肺癌病人中的試驗顯示,IL-6單克隆抗體可以逆轉厭食、疲勞和貧血,但對體質量改善無明顯影響[49]。
5 p38MAPK通路
腫瘤病人在形成惡液質的過程中,細胞對各種胞外調節信號作出特異性應答,除上述一些信號通路外,大多數細胞中還存在另外2條細胞因子通路途徑:p38MAPK途徑和JAK-STAT途徑。2條途徑獨立存在于細胞內,共同進行信號轉導。但有研究發現,絲裂原活化蛋白激酶(MAPK)可能是兩者的關鍵分子,因為當JAK激活的同時,伴有MAPK的活化[50]。
p38MAPK最早因為與應激相關而引起研究者注意,后來發現它與多種腫瘤(包括宮頸癌、卵巢癌、肝癌、淋巴瘤)凋亡的啟動、細胞周期的靜止等密切相關。p38MAPK除介導炎癥、凋亡外,還參與細胞存活、分化和發育等過程。TNF-α、IL-1和TWEAK能通過介導NF-κB和p38MAPK信號通路,促進E3連接酶MuRF1和MAFbx基因的表達,進而使肌纖維蛋白發生泛素化降解[37,51]。研究顯示,阻斷p38MAPK級聯反應,可以減輕細胞的炎癥反應[52]。在腫瘤細胞中,p38MAPK可增加TNF-α的表達,反過來,TNF-α也可以活化p38MAPK上游MAPKKK(MAP kinase kinase kinase),進而激活p38-MAPK,誘導凋亡[53]。
6 JAK-STAT通路
JAK-STAT信號途徑是由Heim在研究干擾素誘導細胞內信號傳導的過程中發現。當蛋白酪氨酸激酶(Janus activated kinase,JAK)與配體結合時,他們通過單個酪氨酸上的磷酸化激活STAT,促使STATs形成二聚體,然后轉移到細胞核內,與目標基因啟動子中的特定反應元件結合,并激活其轉錄[54]。有研究表明,STATs能調節與細胞增殖、分化、凋亡相關基因的表達。其下游基因的表達,能抑制腫瘤細胞的凋亡,促進其增殖分化,從而增強免疫逃避能力,促進腫瘤的發生發展及侵襲和轉移的能力[55]。加入STAT3蛋白抑制劑能夠阻斷STAT與DNA相結合,進而抑制腫瘤細胞的分化、增殖與生長,促進其凋亡[56]。雖然JAK-STAT信號通路與肌肉減少直接相關的研究鮮有報道,但可以發現,抑制JAK-STAT信號通路,就可抑制腫瘤的生長、轉移,促進其凋亡壞死,從而阻止病人發生腫瘤惡液質,防止腫瘤病人的肌肉減少。這為治療腫瘤惡液質提供了方向,且已成為抗癌治療研究的熱點。

