燈盞花乙素苷元結構修飾的研究進展
韓官甫 李潤濤 張偉
【摘 要】 燈盞花乙素是從燈盞細辛中提取的有藥理活性的化合物,目前主要用于治療缺血性心腦血管疾病。燈盞花乙素苷元是燈盞花乙素在人體內的主要吸收形式,但是燈盞花乙素苷元存在溶解度和穩定性差,生物利用度低、腦分布低、活性弱等缺陷。基于已有的燈盞花乙素苷元的構效關系發現,燈盞花乙素苷元A環的6、7、8位和B環的4′位對活性影響較小。對燈盞花乙素苷元在A環和B環上的結構優化進行總結,為進一步開發以燈盞花乙素苷元為先導化合物的新藥提供參考。
【關鍵詞】 燈盞花乙素苷元;溶解度;結構修飾;合成
【中圖分類號】R914.5 【文獻標志碼】 A【文章編號】1007-8517(2020)14-0060-04
Research Progress on Structural Modification of Scutellarin
HAN Guanfu1, 2LI Runtao3ZHANG Wei2 *
1.School of Pharmaceutical Science & Yunnan Key Laboratory of Pharmacology for Natural Products, Kunming
Medical University,Kunming 650500,China;
2.Kunming Longjin Pharmaceutical CO.,LTD, Kunming? 650503,China;
3.Beijing Peking University school of pharmaceutical sciences,Beijing 100191,China
Abstract: Scutellarin, which is extracted from Erigeron breviscapine, is a definitely pharmacologically active nature product. It is widely used in the treatment of ischemic cardiovascular and cerebrovascular diseases. The scutellarein is the main form of absorption of scutellarin in the human body, however, there are some defects such as poor solubility and stability, low bioavailability, low brain distribution and weak activity. Based on the existing structure-activity relationship of scutellarein, we found that 6,7,8 positions in A ring and 4′ positions in B ring of scutellarein had little effect on activity.? In this paper, the structure optimization of scutellarein in A and B rings is summarized, which provides a reference for the further development of new drugs with scutellarein as the leading compound.
Keywords:Scutellarein;Solubility; Structural Modification; Synthesis
《柳葉刀》2017全球疾病負擔研究(Global Burden of Disease Study 2017, GBD)顯示目前世界范圍內,慢性非傳染性疾病(NCD)死亡人數占全球總死亡人數的73.4%(4110萬),其中心腦血管疾病死亡的人數(1780萬)是NCD最大的死亡原因,在2007~2017年十年間,全球因心腦血管疾病造成的死亡人數同比增加21.1%,針對心腦血管疾病的防治面臨極大的挑戰[1]。
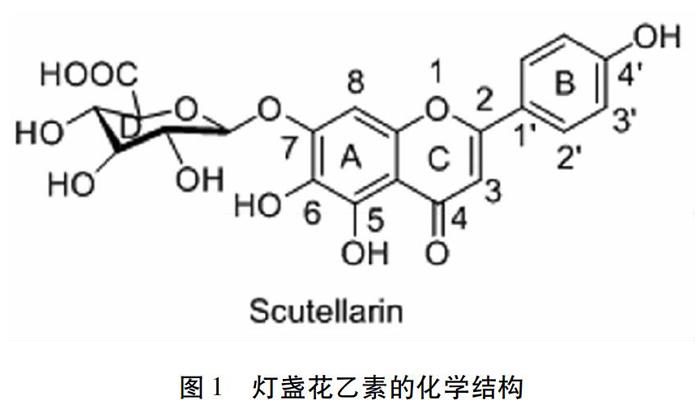
目前,中藥在心腦血管疾病的預防和治療中發揮著重要作用,我國腦血管病治療方案已經成為國際最高標準。心腦血管疾病是機體復雜因素引起,血瘀是中醫理論中心腦血管疾病的主要發病原因,中藥治療心腦血管疾病的機理主要通過改善心腦及周圍血管功能,提高靶器官血液循環,抑制組織增生,調節機體的免疫力等多靶點、多環節作用來發揮療效[2]。通過對已有的,有明確藥理活性的中藥有效成分進行結構改造是目前開發新藥的有效手段之一。自20世紀七十年代起,燈盞花乙素(圖1.1)就被制成各種制劑用于治療心腦血管疾病,有巨大的發展潛力,值得藥學工作者深入研究。
燈盞花又名燈盞細辛, 是菊科植物短葶飛蓬Erigeron breviscapus(Vant.) Hand.-Mazz.的干燥全草,以根或全草入藥, 微苦, 甘溫辛, 性溫, 歸心、肝經, 具有祛風除濕、活絡止痛功效。燈盞花主要產于我國云南、湖南、貴州等地,其中云南省能入藥的燈盞花資源占全國總資源總量的95%以上[3]。燈盞花乙素是燈盞花中含有的明確藥效成分,主要藥理作用為抗炎、抗氧化、抗凋亡、抗纖維化、神經保護、抗凝及改善循環[4],最近有報道稱其具有潛在的降血糖和保護腎臟等作用[5]。
盡管燈盞花乙素(Scutellarin)在臨床使用中有著確切的療效,但該藥物目前也存在缺點:水溶性差(0.056g/L)、脂溶性差(logP=-2.56,pH=4.2磷酸緩沖溶液)、口服生物利用度低(0.4%),半衰期短(52±29min)等缺點,這些缺點限制了燈盞花乙素類藥物在臨床中的使用。
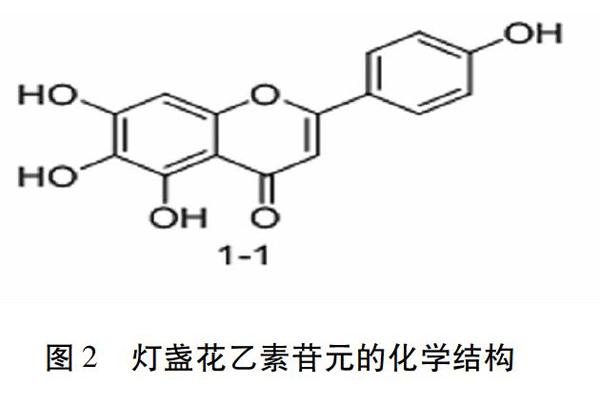
燈盞花乙素苷元1-1(圖2)是燈盞花乙素在人體內的主要吸收形式,且與燈盞花乙素相比,其口服生物利用度是燈盞花乙素的3倍[6],但是燈盞花乙素苷元也存在溶解度和穩定性差,生物利用度低和活性弱等缺陷。將有活性的天然產物作為先導化合物,對其進行結構修飾是目前新藥開發有效手段之一。因此對燈盞花乙素進行相關結構改造,希望以此獲得活性更高,溶解度更高,生物利用度改善的衍生物。目前,針對燈盞花乙素苷元的結構優化主要集中在A環和B環上,下面依次進行介紹。
1 燈盞花乙素苷元A環結構改造
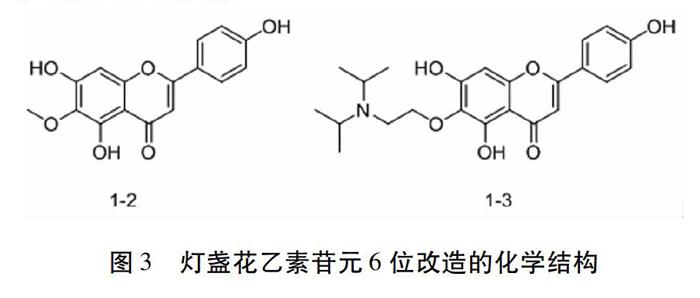
1.1 燈盞花乙素苷元A環6位結構改造 段金廒課題組[7]對燈盞花乙素苷元的四個羥基分別進行單甲基化,雙甲基化和三甲基化后發現:6-位甲基化燈盞花乙素苷元1-2(圖三)顯示出比燈盞花乙素苷元更優的抗血栓形成活性,更強的抗氧化活性以及更好的溶解性和脂水分配系數。提示化合物1-2可以作為心腦血管疾病治療的先導化合物。該課題組[8]在此前工作的基礎上,為了改善代謝穩定性及提高生物利用度,在燈盞花乙素苷元6位引入常見含氮藥效基團。結果表明,當6-位取代基為N,N-二異丙氨乙基時(圖3,1-3),該化合物的抗凝血活性、抗氧化活性及水溶性都有明顯提高。
1.2 燈盞花乙素苷元A環7位結構改造 楊麗梅[9]通過藥理活性測試初步證實燈盞花乙素結構中的葡萄糖醛酸基團對藥理活性作用不大,設計合成了18個燈盞花乙素苷元的衍生物:苷元酯類化合物3個、醚類苷元化合物14個和磺酸鈉鹽苷元化合物1個,對其進行藥理活性測試,發現化合物1-4(圖4)在保持燈盞花乙素苷元活性的同時對缺氧損傷的原代大鼠心肌細胞和SHSY5Y細胞具有更優的保護作用。并根據活性測試結果推斷燈盞花乙素4′-羥基對缺氧損傷大鼠心肌細胞的保護起決定性因素。
1.3 燈盞花乙素苷元A環8位結構改造 李念光等[10]將燈盞花乙素苷元與凝血酶(2R2M)進行分子對接發現,燈盞花乙素苷元的B環和C環能夠很好的與凝血酶S2和S1口袋相結合,但是A環只能與S3口袋結合一部分,因此他們嘗試利用曼尼希反應在A環引入一系列脂肪胺和脂環族胺制備燈盞花乙素苷元8-氨基甲基化衍生物。并通過凝血酶原時間(PT),活化部分凝血活酶時間(APTT),凝血酶時間(TT)和纖維蛋白原(FIB)的分析測試了所有化合物的凝血酶抑制活性。根據測試結果,在合成的一系列化合物中發現當8位為嗎啉基亞甲基取代化合物1-5(圖5)時與燈盞花乙素苷元相比具有更強的抗凝活性,更好的水溶性和更優的抗氧化活性,該結果對燈盞花乙素苷元進一步結構修飾提供了新思路。
隨后,該課題組[11]為了進一步解決燈盞花乙素苷元水溶性較差這一問題,繼續對8位進行結構修飾。目前,對類黃酮類化合物進行磺酸化是增加其溶解度的有效方法之一 [12]。當在燈盞花乙素苷元8位引入磺酸集團后,發現化合物1-6(圖5)的溶解度為1949.64 μg/mL,而燈盞花乙素苷元僅為6.85 μg/mL,與此同時母體化合物的生物活性仍得以保留。
2 燈盞花乙素苷元B環結構改造
藥物拼合是現代新藥開發的有效手段之一,通過將兩個不同藥效的化合物拼合在一起發揮協同作用,不但增加藥物的活性,同時能降低毒副作用等[13]。將燈盞花乙素苷元與其它藥效基團拼接也為進一步結構改造提供了方向。
2.1 燈盞花乙素苷元B環4位結構改造(連接氨基酸類) 為了設計合成有較強神經細胞氧化損傷保護作用的燈盞乙素苷元衍生物,傅曉鐘等[14] 以燈盞花乙素苷元為先導化合物,利用藥物拼合原理在其4-羥基上引入L-氨基酸酯、醚結構, 設計并合成11個衍生物。通過H2O2誘導PC12細胞氧化損傷模型對這一系列衍生物進行體外抗氧化活性評價, 同時進行了目標化合物理化性質研究。發現設計合成的系列化合物均具有抗氧化活性,溶解度也有一定提高,但通過穩定性實驗發現燈盞乙素苷元4-L-氨基酸酯類化合物可能會在體內分解為燈盞花乙素苷元致其相對生物利用度無明顯變化,尤其是在中性條件下酯類化合物降解半衰期(t1/2) 0.5 h。
隨后該課題組[15]為了解決燈盞花乙素苷元4′-L-氨基酸酯類化合物在弱酸環境下不穩定的缺點,在氨基酸的羧基和氨基中插入苯環以防止其在體內快速水解,獲得了一系列新的前藥衍生物,其中化合物1-7(圖6)的穩定性得到極大提升,并且該衍生物能在體內通過酶促反應快速釋放原藥,進一步發揮抗氧化作用,可以作為有潛力的候選藥物繼續進行研究。
2.2 燈盞花乙素苷元B環4位結構改造(連接氮芥) 氮芥是最早用于治療腫瘤且效果明顯的抗腫瘤藥物,該藥物進入人體后通過分子內成環作用,形成高度活潑的乙酰亞胺離子,一方面可以有效的發揮抗癌作用,但另一方面也有極強的致癌副作用[16]。而燈盞花乙素作為天然的多酚類化合物,有著廣譜的生物活性和低毒性。其本身也有誘導細胞凋亡[17]、抑制遷移和侵襲[18]和對敏感細胞的化療[19]等作用。
將燈盞花乙素苷元與氮芥進行拼接有可能開發出一款新的抗腫瘤新藥。基于這一原理,李大宏課題組[20]將燈盞花乙素苷元與氮芥進行拼合,得到3個化合物1-8 a-c(圖7),這三個化合物對MCF-7(乳腺癌)和Bel-7402(肝癌)細胞表現出良好的抗增殖活性,IC50值在1.50-9.07μM之間;1-8a和1-8c對A549(肺癌)細胞系表現出中等活性,IC50值分別為21.47 μM和23.51 μM。
綜合以上體外活性結果,選擇對化合物1-8 a進行MCF-7細胞系的相關研究。機理研究表明,1-8 a可以誘導MCF-7細胞凋亡,將MCF-7細胞周期阻滯在G1期,并以濃度依賴的方式引起線粒體功能障礙。此外,促凋亡蛋白caspase-9、caspase-3、Bax和cytochrome c,以及抗凋亡蛋白Bcl-2的表達降低,也都證實化合物1-8 a誘導MCF-7細胞內在的凋亡途徑。強大的抗增殖活性和良好的選擇性使化合物1-8 a做為潛在的抗腫瘤藥物被該課題組進一步開發。
3 小結與展望
對以上燈盞花乙素苷元的結構修飾進行總結,發現目前得到活性較好的新化合物集中在A環的6、7、8位和C環的4位酚羥基的醚化或酯化,對芳香環的修飾還未觸及,仍有很大的改造空間;一些新藥中常見的藥效基團如F、CF3和環丙烷等也可以作為電子等排體適當引入,以期能得到活性更好,理化性質更強的新藥;將兩個或多個相似活性的藥物進行化學拼合以找到效果更好的藥物這一新藥開發手段也可以用于該化合物進一步的結構修飾中。
參考文獻
[1]GBD 2017 Causes of Death Collaborators. Global, regional, and national age-sex-specific mortality for 282 causes of death in 195 countries and territories, 1980-2017: a systematic analysis for the Global Burden of Disease Study 2017[J].The Lancet, 2018(392):1736-88.
[2]孫德禹.臨床治療心腦血管的中藥[J].中西醫結合心血管病電子雜志,2014,2(10):92-93.
[3]王寧,楊兆祥,楊生元.燈盞細辛研究開發的回顧和展望[J].云南中醫中藥雜志,2012,33(5):69-72
[4]范婭丹,韓江全.燈盞花乙素的藥理作用及臨床應用進展[J].海南醫學,2017,28(4):627-629.
[5] LIU Y, WANG J,WANG D, et al. Scutellarin Exerts Hypoglycemic and Renal Protective Effects in db/db Mice via the Nrf2/HO-1 Signaling Pathway[J]. Oxidative medicine and cellular longevity,2019(2): 1-12.
[6]車慶明,潘麗怡,何紅.燈盞花乙素苷元的藥動學研究[J].中國藥學雜志,2007(18):1418-1421.
[7]SWI Z H,LI N G,DUAN J-A,et al. Synthesis and biological evaluation of methylated scutellarein analogs based on metabolic mechanism of scutellarin in vivo.[J]. European journal of medicinal chemistry,2015(106):95-105.
[8] DONG Z X,SHI Z H,DUAN J-A, et al. Design, Synthesis, and Biological Evaluation of Scutellarein Derivatives Based on Scutellarin Metabolic Mechanism In Vivo [J]. Chemical biology & drug design,2016,87(6):956-957.
[9]楊麗梅. 燈盞乙素的結構改造及構效關系研究[D].天津:天津醫科大學,2010.
[10] LI N G,LI S L,DUAN J-A, et al. Mannich bases of scutellarein as thrombin-inhibitors: Design, synthesis, biological activity and solubility[J]. Bioorganic & Medicinal Chemistry,2012,20(24):6919-6923.
[11]TING G,YUE Z,LI Y T, et al. Synthesis and Bioactivity Characterization of Scutellarein Sulfonated Derivative[J]. Molecules, 2017, 22(6):1028-1036.
[12] WOZ'NICKA E.? New sulfonic derivatives of quercetin as complexing reagents: Synthesis, spectral, and thermal characterization[J].J. Therm. Anal. Calorim,2015,120:351-361.
[13]吳玉梅,熊曉云,羅曉星,等.新型的治療阿爾茨海默氏癥藥物(1-二甲基磷酰基-2,2,2-三氯)-乙基-1-醇煙酸酯對體外神經細胞的作用[J].中國臨床藥理學與治療學,2005(10):1100-1103.
[14]傅曉鐘,張偉,劉影,等.燈盞乙素苷元4′-L-氨基酸衍生物的設計、合成與抗氧化活性[J].藥學學報,2011,46(5):548-555.
[15]傅曉鐘,邢鳳晶,劉影,等.燈盞乙素苷元4′-N-取代氨甲基苯甲酸酯的合成及體外抗氧化活性研究[J].有機化學,2011,31(7):1043-1048.
[16]POVIRK L F,SHUKER D E.DNA damage and mutagenesis induced by nitrogen mustards[J]. Mutation research,1994,318(3):205-226.
[17]WANG Z, YU J G,XU Z J,et al. Scutellarin protects cardiomyocyte ischemia-reperfusion injury by reducing apoptosis and oxidative stress[J]. Life Sciences,2016,157:200-207.
[18]KE Y,BAO T H,WANG L, et al. Scutellarin suppresses migration and invasion of human hepatocellular carcinoma by inhibiting the STAT3/Girdin/Akt activity[J]. Biochemical and Biophysical Research Communications,2016,483(1):509-515.
[19]GAO C, ZHOU Y,TIAN W,et al. Cytotoxic and chemosensitization effects of scutellarin from traditional Chinese herb Scutellaria altissima?L. in human prostate cancer cells Oncol[J]. Rep., 2017,38(3) :1491-1499.
[20]HAN T,WANG Y,TIAN W,et al. Synthesis of scutellarein derivatives with antiproliferative activity and selectivity through the intrinsic pathway[J]. European Journal of Medicinal Chemistry,2018(158):493-501.
(收稿日期:2020-06-16 編輯:程鵬飛)
基金項目:
作者簡介:韓官甫(1992-),男,漢族,碩士研究生在讀,研究方向為藥物化學。E-mail:934299700@qq.com
通信作者:張偉(1973-),男,彝族,碩士,正高級工程師,研究方向為藥物化學與藥物分析。E-mail:wzhangkm@sohu.com

