陽極泥還原焙燒的研究
馬曉磊 王順林
(阿克陶科邦錳業制造有限公司 阿克陶 845550)
1 前言
在電解錳的生產過程中,陽極區Mn2+不可避免的被氧化并形成Mn4+的水合氧化物(水羥錳礦),同時陽極板中的鉛錫合金亦被氧化并與錳氧水合物一起沉淀,形成典型的膠狀構造。電解錳陽極泥為黑色大小不一的固體物質,其中分散著白色結晶物(NH4)2SO4,陽極泥主要成份為MnO2,其基本結構是由1個錳原子核與6 個氧原子配位形成的六方密堆積結構,這種結構形成的復雜網絡可容納不同的陽離子。目前電解錳陽極泥的處理并沒有成熟的工業產業化方案,國內大部分的電解錳冶煉企業采用堆存、外售以及火法處理生產錳合金產品等方式進行處理。本研究利用還原焙燒技術,資源化回收利用電解錳陽極泥,實現了鉛錳分離,為電解錳陽極泥的資源化工程應用提供參考。
2 試驗原料
以新疆某電解錳冶煉企業陽極泥作為原料,還原劑選用活性炭,浸出劑選用工業硫酸(93%),其陽極泥成分見表1。

表1 陽極泥主要成分(%)
3 試驗方法
稱取10g 陽極渣,將陽極渣研磨后與石灰100:1在坩堝內混合均勻,加入一定量的活性炭(活性炭用量為理論用量的1-4.5 倍),在相關溫度下(500℃-900℃),按照要求時間(45min-4h)在馬弗爐內進行焙燒,并驗證密封性對還原的影響,待冷卻后取樣進行分析檢測,后進行硫酸浸出試驗。
試驗原理:
陽極渣主要成分為MnO2,還原劑用活性炭,主反應如下:

考慮到陽極渣中還有殘余的酸,且陽極渣高溫焙燒會有SO2酸性氣體,用石灰來中和吸收,反應如下:
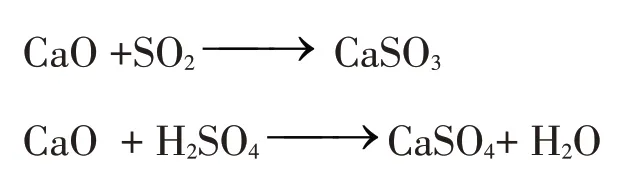
陽極渣還原焙燒后主要成分為MnO 和PbSO4,MnO 會和H2SO4發生反應生成溶于水的硫酸錳,Pb?SO4不溶于水也不和酸反應留在渣中,反應如下:

4 試驗結果與討論
4.1 溫度對還原率的影響
稱取10g 陽極渣,將陽極渣研磨后與石灰100:1在坩堝內混合均勻,加入過量1.5 倍的活性炭,溫度控制在500℃-900℃,在馬弗爐內進行焙燒1h,待冷卻后取樣進行分析檢測。
由圖1 可以看出,隨著溫度降低,錳的還原率也隨之降低,在800℃時還原率最高,可達到88.67%,且隨著溫度繼續升高,對于還原沒有明顯影響。
4.2 密封對還原率的影響
稱取10g 陽極渣,將陽極渣研磨后與石灰100:1在坩堝內混合均勻,加入過量1.5 倍的活性炭,溫度控制在800℃,對坩堝在敞開和加蓋情況下分別在馬弗爐內進行焙燒1h,待冷卻后取樣進行分析檢測。

圖1 溫度對錳還原率的影響

圖2 密封對還原率的影響
從圖2 可看出,有蓋密封時還原率較高,有蓋密封時冷卻過程中可以隔絕空氣中的氧氣,防止被還原的錳氧化再次被氧化成為二氧化錳。
4.3 活性炭加入量對還原率的影響
稱取10g陽極渣,將陽極渣研磨后與石灰100:1在坩堝內混合均勻,溫度控制在800℃,加入過量的活性炭(活性炭用量為理論用量的1-4.5倍),加蓋密封在馬弗爐內進行焙燒1h,待冷卻后取樣進行分析檢測。
由圖3 可看出,活性炭用量為理論計算的量的2-2.5倍即可獲得較高的還原率,隨著活性炭用量的增加,還原率也在增加,但增加幅度較小,為節約成本考慮,活性炭用量為理論計算的量的2-2.5倍即可。
4.4 焙燒時間對還原率的影響
稱取10g 陽極渣,將陽極渣研磨后與石灰100:1在坩堝內混合均勻,溫度控制在800℃,加入過量2.5倍的活性炭,加蓋密封在馬弗爐內進行焙燒45min-4h,待冷卻后取樣進行分析檢測。
從圖4可以看出,焙燒時間在45min—2h之間還原率逐漸升高,2h 時還原率最高,2h 后還原率下降,分析原因可能是隨著焙燒時間延長,氧化錳再次被氧化成為二氧化錳,造成還原率下降。
4.5 浸出實驗
按照還原焙燒試驗探索出的最佳條件進行還原焙燒,稱取50g 陽極泥還原渣進行浸出試驗,以陽極液為浸出劑,初始酸濃控制在100-150g/l,浸出條件為液固比10:1,浸出溫度45℃,浸出時間8h,陽極泥還原渣及陽極液成分分析見表2。

圖3 活性炭加入量對還原率的影響

圖4 焙燒時間對還原率的影響

表2 陽極泥還原渣及陽極液成分

表3 浸出實驗數據
從表3中可以看出,除第一組實驗錳浸出率較低外,分析原因為反應前總酸量不足造成浸出率較低,渣含錳較高,其余二價錳浸出率均能達到98%以上,證明該還原渣非常容易浸出。
5 結論
通過研究發現,還原焙燒可有效處置陽極泥,在溫度800℃焙燒2h,活性炭用量為理論計算的量的2-2.5 倍,保持還原氣氛的條件下,錳的還原率可達到96.56%。該還原渣極易浸出,利用稀硫酸浸出錳的浸出率可達到98%,不僅可有效回收陽極泥中錳資源,提高綜合回收率,且浸出渣中Pb可富集至45%左右,可直接作為鉛精礦計價賣出,使得資源綜合利用。

