臭氧水穴位注射聯合關節腔沖洗對KOA患者關節液中TNF-α的影響*
周友龍 李 昊 陳云杰 宋巧燕 張儒雅 吳軍尚 田明月 丁小芬 賈夢雅 李彥華
膝骨性關節炎(knee osteoarthritis,KOA)是世界范圍內最常見的成人關節疾病[1],主要臨床表現為關節疼痛,活動受限。目前KOA的發病機制尚不清楚,但是近期研究發現KOA中存在軟骨破壞,導致其破壞的重要介質是TNF-α[2]。TNF-α既能抑制軟骨組織合成,還參與破壞及分解軟骨組織,其含量的多少同炎癥的嚴重程度呈正相關[3]。臭氧治療骨性關節炎臨床療效確切[4,5],但是其作用機制不清楚,所以本研究通過觀察KOA患者的關節液的TNF-α的變化,探索臭氧水穴位注射聯合關節腔沖洗治療KOA的作用機制。
1 資料與方法
1.1 一般資料選取80例河南中醫藥大學第三附屬醫院疼痛科門診KOA患者,均符合納入標準,患者均簽署知情同意書。根據治療方案將患者隨機分為試驗組及對照組。試驗組40例中,男12例,女28例;年齡45~74歲,平均(62.47±8.05)歲;病程0.3~25個月。對照組40例中,男17例,女23例;年齡46~72歲,平均(60.19±10.23)歲;病程0.2~26個月。
1.2 診斷標準參照中華醫學會骨科學分會制訂的《骨關節炎診治指南(2007年版)》中的KOA診斷標準[6],①近1個月大多數時間有膝關節疼痛;②X線片示關節間隙有變窄、軟骨下見骨硬化和(或)囊性變、骨贅形成;③關節液檢查清亮、黏稠;④年齡≥40 歲;⑤晨僵≤30 min;⑥活動時會有骨摩擦音或骨摩擦感。符合“ ①+② ”條或者“ ①+③+⑤+⑥ ”條或者“①+④+⑤+⑥”條,均可診斷為膝關節骨性關節炎。
1.3 納入標準①符合上述診斷標準;②近期未服用鎮痛藥或其他藥物治療。
1.4 排除標準①年齡≥80歲;②懷孕和哺乳期婦女;③患者合并其他疼痛性疾病,如風濕、類風濕關節炎、關節創傷、結核、腫瘤等;④關節周圍皮膚有嚴重缺損或潰瘍;⑤膝關節畸形及關節腔消失者;⑥全身感染或傳染性疾病患者。
1.5 治療方法試驗組采用臭氧水穴位注射聯合關節腔沖洗治療。操作方法:患者取仰臥位,膝下墊枕,髖關節外旋外展,膝關節屈曲135°~145°。以髕骨中心為原點,作水平線和垂直線,在內上象限取平分角,該平分線與髕骨內側緣交點延長線上0.5 cm處定為新KP1點。常規消毒,鋪洞巾,持10 ml注射器抽取2 ml穿刺液(1%利多卡因1 ml+0.9%氯化鈉注射液1 ml),于新KP1點皮下注射麻醉,當針尖穿過關節囊時有落空感,提示進入關節腔。如果關節腔內有積液,先將積液抽出,關節積液抽取干凈后,由助手持60 ml注射器從臭氧水制備儀(濟南三氧科技有限公司制造SYZ-80A) 中抽取20 μg/ml的臭氧水,緩慢注入關節腔。盡量使臭氧水充滿整個關節腔隙,患者自覺有明顯憋脹感時,將臭氧水全部抽出。反復多次沖洗,直至沖洗液顏色清亮。沖洗結束后,于梁丘、血海、陰陵泉、陽陵泉、三陰交諸穴處注射臭氧水,3 ml/穴。治療結束后,于穿刺點處貼創可貼,囑患者休息30 min,無不適方可離開[4]。每周1次,連續治療4周。對照組采用玻璃酸鈉注射液膝關節腔內注射治療。操作方法:關節穿刺方法同試驗組,于患膝關節腔內注入玻璃酸鈉注射液(山東博士倫福瑞達制藥有限公司,2.5 ml∶25 mg/支),2.5 ml /次。治療結束后,取醫用創可貼將針眼覆蓋,并囑患者休息30 min,無不適方可離開。每周1次,連續治療4周。
1.6 觀察指標TNF-α的測定方法:于患者患側膝關節治療前后分別抽取關節液,嚴格按照TNF-α的ELISA試劑盒說明書操作,采用酶聯免疫吸附法(ELISA)檢測TNF-α的表達水平。

2 結果
2組治療前TNF-α表達水平比較,差異無統計學意義(P>0.05)。2組連續治療4周后,關節液中TNF-α的表達水平均有降低,且試驗組優于對照組(P<0.05)。見表1。
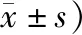
表1 2組患者治療前后TNF-α表達水平比較 (例,
3 討論
膝骨性關節炎(knee osteoarthritis,KOA)是中老年人群中常見的退行性疾病。以關節軟骨逐漸退變、骨質增生、無菌性滑膜炎癥和韌帶變性等為主要病理特征,以疼痛和功能活動受限為主要臨床表現,嚴重影響了患者生活質量。KOA屬中醫學 “骨痹”“膝痹”范疇,筆者通過多年臨床經驗及理論探討,提出了“本在肝腎空虛,治以補肝腎;標在風寒濕痹阻,治以祛風、散寒、除濕;痹有血瘀作祟,活血化瘀,貫穿始終”的學術思想,探索出用臭氧水穴位注射聯合關節腔沖洗治療KOA的方法,且臨床療效確切。
KOA病理過程是軟骨細胞的合成與分解代謝失衡,導致關節軟骨破壞以及軟骨下骨硬化、囊變以及骨贅形成。這種失衡是由于機械刺激、關節內炎癥介質共同作用于軟骨細胞的結果。已發現在KOA的發生與發展過程中起到重要作用的信號通路主要有絲裂原活化蛋白激酶(mitogen-activated protein kinase, MAPK)信號通路、NF-κB信號通路等[7,8]。關節軟骨及滑液中的TNF-α、IL-1等各種炎性因子、低氧刺激、機械應力刺激等均可啟動MAPK信號及NF-κB信號通路[9-11],從而使其下游的分解型細胞因子如白介素-1β、TNF-α等的表達增加,導致軟骨降解,造成膝關節間隙狹窄,引起膝關節疼痛,關節僵硬,最終導致KOA的發生[10, 12]。
臭氧是氧氣的同素異構體,其分子含有3個氧原子,是一種不穩定氣體,低濃度臭氧無色、有魚腥味,化學性質不穩定,常溫下的半衰期為20~40 min,在水中的溶解度是氧氣的10倍[13]。臭氧是一種強氧化劑,具有很強的氧化消毒殺菌能力,同時具有抗炎作用,其抗炎機制主要包括拮抗炎性細胞因子和免疫抑制因子的釋放;清除體內過多自由基;刺激抗氧化酶的過度表達以中和炎癥反應中過量的活性氧;刺激細胞內皮釋放一氧化氮及血小板源性生長因子等引起血管擴張,從而達到促進炎癥吸收的作用[14]。
大量基礎實驗表明,臭氧治療KOA與降低TNF-α、IL-1β等炎性介質的合成與釋放有關。臭氧治療KOA通過降低TNF-α、IL-1β等炎性因子的表達,進而調控相應炎性因子所介導的MAPK信號通路、NF-κB信號通路,從而改善軟骨細胞合成與降解代謝的失衡,進而對KOA起到治療作用[15-18]。
筆者經過多年研究研發出臭氧水制備儀,該設備以氧氣和生理鹽水為原料,通過特有的發生器,經相關化學反應生成臭氧水,并可通過相關設置調控臭氧水的濃度,可制備出濃度可控的臭氧水,保留了臭氧氣體的氧化性,具有確切的抗炎、鎮痛作用,同時臭氧溶于水后增加了穩定性、安全性。大量動物試驗表明,臭氧水能抑制KOA關節軟骨中TNF-α的生成,降低其含量,延緩KOA關節軟骨的退變[19,20]。
本研究結果表明,經過4周治療后,試驗組患者關節液中TNF-α的表達水平都降低,且優于對照組,差異有統計學意義。說明臭氧水穴位注射聯合關節腔對KOA的作用機制可能是抑制了TNF-α的表達,從而達到對KOA的治療作用。

