格利特消毒劑對高致病性禽流感病毒的抗病毒效力
霍天武 李亞雄 孟艷莉

摘? 要:根據美國國家環境保護局(EPA)制定的關于抗病毒劑類注冊產品的測試標準和方法,將格利特消毒劑稀釋至使用濃度,處理被病毒附著污染的物體表面,測定回收病毒的侵染能力和病毒侵染性的降低程度,證明1 000 mg/kg格利特消毒劑稀釋液符合EPA標準,是殺病毒劑。
關鍵詞:戊二醛;格利特消毒劑;高致病性禽流感
中圖分類號:S859.79 文獻標志碼:A 文章編號:1001-0769(2020)08-0085-04
本研究的目的是測評以戊二醛為主要有效成分的消毒劑對高致病性禽流感(Highly Pathogenic Avian Influenza,HPAI)H5N1病毒亞型的消毒效果。根據美國國家環境保護局(Environmental Protection Agency,EPA)制定的關于抗病毒劑類注冊產品的測試標準和方法,用稀釋至使用濃度的消毒劑產品處理被病毒附著污染的物體表面,測定回收病毒的侵染能力,根據病毒侵染性的降低程度來證明消毒劑的抗病毒能力。
1? 試驗方法
采用載體法獲得支持本研究結果的病毒學數據,該方法在美國官方分析化學家協會(Association of Official Analytical Chemists,AOAC)應用稀釋法的基礎上稍作修改而成。
1.1 病毒體系
HPAI病毒由美國喬治亞洲亞特蘭大疾病控制中心的亞歷山大克里莫夫博士 (Alexander Klimov) 提供。病毒毒種為禽流感病毒 H5N1 亞型的A/VN/1203/2004株,培養于雞胚尿囊腔中。將病毒以1∶20的比例稀釋到濃度為5%的尿囊溶液中用作固體載荷。
1.2 侵染性測定(侵染性的指示劑、介質、試劑和儀器)
將病毒接種于孵化9 d~11 d的長齡雞胚,以評估病毒的侵染能力。孵化? ? ? ? ? ?9 d~11 d長齡雞胚以無病原為特征,均由 Charles River 提供。雞胚運達當天記為孵化的第0天,然后置于孵化器中孵化。孵化器溫度保持在37 ℃左右,濕度為40%~70%。雞胚每3 h借助自動旋轉儀轉動一次。
使用前,所有雞胚都進行光照檢查,以確定其存活狀態。主要檢查雞胚的運動情況以及是否形成良好的血管系統。光照檢查時,如果雞胚沒有任何運動跡象,且血管系統被破壞,則可以認為已經死亡,使用前挑出死亡雞胚。接種前,在雞蛋頂部噴酒精,并用雞蛋打孔器開口,用配有1〞23 G鈍尖針頭的1 mL注射器接種。接種后,用膠水密封蛋殼開口。接種后的雞蛋不再轉動。
在進行侵染性測評時,每一份稀釋液接種4個雞胚。將0.2 mL待測液接種于雞胚的尿囊腔,孵化4 d。用雞胚的死亡情況表征病毒的侵染能力,并用Reed-Muench法計算50%雞胚致死量的滴度(ELD50)。
1.3 合成硬水
根據AOAC法的960.25條款E合成硬水。
1.4 試驗材料
1.4.1 消毒劑的準備
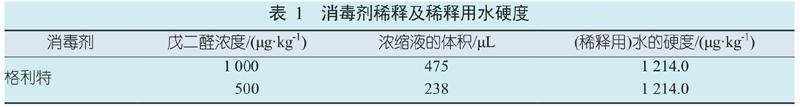
根據戊二醛產品應用指導制備消毒劑。將定量的產品加入容量瓶中,用硬水定容至100 mL,產品的使用量和水的硬度如表1所示。所有待測液的濃度均以戊二醛活性濃度為基準進行制備。
1.4.2 病毒膜的制備
用HBSS平衡鹽溶液將病毒的尿囊溶液稀釋至5%。取0.2 mL該病毒接種物均勻噴灑在23 cm2~28 cm2的玻璃培養皿底部,空氣干燥形成病毒膜,用于待測產品的消毒性測定。
1.5 病毒對照膜的處理
加入2 mL的HBSS病毒對照膜,培養 5 min。此額外加入的2 mL HBSS將病毒稀釋10倍。經過一定的接觸時間,加入2 mL中和劑(2×HBSS+50%胎牛血清),病毒被稀釋20倍。用移液管尖端來回刮擦培養皿表面數次,重懸病毒。其他的稀釋步驟均以1×HBSS為溶劑。重懸后,將病毒液以1∶5稀釋。因此,接種于雞胚中的第一個稀釋濃度為1∶100或表示為10-2,其余稀釋經1∶10梯度稀釋獲得。至于對照病毒,其毒性對照和經消毒劑樣品處理后的病毒均以相同方式處理。
1.6 中和
本試驗采用稀釋法進行中和,具體過程如下所述:經過一定時間接觸后,取? ? ?2 mL的中和劑(2×HBSS+50%胎牛血清)加入對照病毒膜和消毒劑處理后的病毒膜,形成1∶2的稀釋,隨后盡快稀釋。加入中和劑后,用移液管尖端來回刮擦培養皿表面數次,重懸病毒。除開始加入中和劑外,其余所有稀釋均以1×HBSS為溶劑。
1.7 消毒劑雞胚毒性對照(使用不含病毒的5%尿囊液干燥膜)
對于每一批待測消毒劑,各取2 mL同樣濃度產品的稀釋液處理5%尿囊液膜,以此測評消毒劑對細胞的毒性效應。以上述處理病毒對照膜和經消毒劑處理后病毒膜相同的方法處理這些培養皿。按上述操作梯度稀釋這些中和后的模擬侵染液,與病毒對照和經消毒處理的病毒樣品同步進行雞胚毒性測定。
1.8 中和劑對照
取0.2 mL中和后產品毒性對照的每一稀釋梯度與等體積相應的病毒對照稀釋液混合液,接種于雞胚以確定其效價。如果測試病毒的毒性效價小于對照病毒的效價,說明產品經中和及稀釋后仍保持活性。應從對照病毒的效價中減去中和對照的效價。從消毒劑處理后與對照病毒相比后效價的降低中減去由中和劑導致的效價降低,是消毒劑導致的病毒效價降低。由此來確定產品是否能夠將病毒效價降低3log10。
1.9 檢測標準
測試結果有效要求:(a) 至少4log10的病毒侵染能力從干燥的對照病毒膜中恢復;(b) 相較于對照組,測試產品至少可以使病毒效價降低3log10;(c) 在最低無毒稀釋液中未檢出病毒侵染性;(d) HBSS接種對照雞胚組仍然保持活性,且沒有可見的被侵染性跡象;(e) 未接種雞胚對照仍然存活。
1.10 統計學分析(效價的計算)
病毒效價和產品本身的毒性效價以50%雞胚致死量的負對數值(-log10ELD50)和50%雞胚中毒劑量的負對數值(-log10TD50)表示,采用Reed-Muench法進行計算。
1.11 測試系統的認證過程
美國南方研究所始終堅持執行有關消毒劑效力測定的標準操作規程(Standard Operating Procedures,SOPs)。SOPs涉及測試工作的諸多方面,其中包括:病毒和雞胚等生物制劑的購買發票、登記和追蹤,以備鑒定認證;病毒稀釋溶劑等化學試劑的發票及使用,等等。這些程序的制定旨在記錄消毒劑效力測試研究的每一步。此外,培養皿、稀釋管、雞胚和雞胚托盤等均根據測試病毒、試驗起始時間以及測試產品等進行標簽。這些方法旨在記錄確定測試系統。
2? 結果
測試產品的相關數據見表2。
1 000 mg/kg和500 mg/kg的格利特消毒劑稀釋液均可殺滅超過3log10的病毒量,在最低無毒稀釋液中未檢出存活的病毒。對照病毒的效價為105.3。在較高濃度的格利特消毒劑中,中和對照降低了病毒的(2log10)效價,說明加入中和劑和稀釋液后,產品依然具有活性。因此,經? ? ? ?1 000 mg/kg的格利特消毒劑處理后,病毒效價的降低扣除中和劑引起的效價降低后達不到3log10,而在500 mg/kg濃度下,產品顯然可以達到降低3log10的滴定度并且在最低無毒稀釋濃度中無病毒殘留的要求。因此,1 000 mg/kg的濃度可以視為通過測試,因為500 mg/kg的濃度可通過測試。
3? 結論
根據以上測試結果,可以做出以下結論:格利特消毒劑的1000 mg/kg稀釋液符合EPA標準,是抗病毒劑。

