PARP抑制劑致血液系統不良反應的Meta分析
黃艷華 余昉 李青宴 沈磊
摘 要 目的:系統評價聚腺苷二磷酸聚合酶(PARP)抑制劑在血液系統方面的安全性,為臨床合理用藥提供循證依據。方法:計算機檢索PubMed、Embase、Cochrane圖書館、ScienceDirect、中國期刊全文數據庫、中國生物醫學文獻數據庫、中國科技期刊全文數據庫、萬方數字化期刊全文數據庫,檢索時限為2014年5月至2019年6月。收集單用PARP抑制劑或PARP抑制劑聯合化學治療藥物(試驗組)對比單用化學治療藥物或安慰劑或化學治療藥物聯合安慰劑(對照組)的隨機對照試驗(RCT)。篩選文獻、提取資料并采用Cochrane系統評價員手冊5.1.0推薦的偏倚風險評估工具對納入文獻質量進行評價后,采用Rev Man 5.3軟件進行Meta分析,同時進行敏感性分析和發表偏倚分析。結果:共納入10項RCT,共計3 129例患者。Meta分析結果顯示,試驗組患者貧血≥3級發生率[RR=7.27,95%CI(2.74,19.27),P<0.000 1]、中性粒細胞減少≥3級發生率[RR=2.46,95%CI(1.43,4.24),P=0.001]、白細胞減少≥3級發生率[RR=1.71,95%CI(1.15,2.54),P=0.008]均顯著高于對照組;兩組患者血小板減少≥3級發生率比較,差異無統計學意義[RR=3.54,95%CI(0.66,19.05),P=0.14]。亞組分析結果顯示,單用PARP抑制劑和聯用PARP抑制劑、化學治療藥物患者的貧血≥3級發生率,中性粒細胞減少≥3級發生率以及聯用PARP抑制劑、化學治療藥物患者的白細胞減少≥3級發生率均顯著高于單用安慰劑組、單用化學治療藥物或化學治療藥物聯合安慰劑者(P<0.05)。敏感性分析支持上述結果,但存在發表偏倚的可能性較大。結論:PARP抑制劑治療癌癥可致患者發生血液系統不良反應,主要表現為貧血、中性粒細胞減少和白細胞減少。應謹慎解讀上述結果。
關鍵詞 聚腺苷二磷酸核糖聚合酶抑制劑;血液系統;不良反應;Meta分析
中圖分類號 R979.1 文獻標志碼 A 文章編號 1001-0408(2020)20-2532-07
DOI 10.6039/j.issn.1001-0408.2020.20.18
ABSTRACT? ?OBJECTIVE: To evaluate the safety of PARP inhibitors in hematological system, and to provide evidence-based evidence for rational drug use in the clinic. METHODS: Retrieved from PubMed, Embase, Cochrane Library, ScienceDirect, CNKI, CBM, VIP and Wanfang data from May 2014 to June 2019, randomized controlled trials (RCTs) about PARP inhibitors or PARP inhibitors combined with chemical treatment drugs (trial group) versus chemical treatment drugs alone, placebo alone or chemical treatment drugs combined with placebo (control group) were collected. After literature screening, data extraction and quality evaluation with bias risk assessment tool recommended by Cochrane systematic evaluator manual 5.1.0, and Meta-analysis was performed by using Rev Man 5.3 software, and sensitivity analysis and publication bias analysis. RESULTS: A total of 10 RCTs were included, involving 3 129 patients. Meta-analysis showed that the incidence of anemia≥grade 3 [RR=7.27, 95%CI(2.74, 19.27), P<0.000 1], neutropenia≥grade 3 [RR=2.46, 95%CI(1.43,4.24), P=0.001], and leukopenia≥grade 3 in trial group [RR=1.71, 95%CI(1.15, 2.54), P=0.008] in trial group were significantly higher than control group. There was no statistically significant difference in the incidence of thrombocytopenia≥grade 3 between two groups [RR=3.54, 95%CI (0.66,19.05), P=0.14]. Results of sub-group analysis showed that the incidence of anemia≥grade 3 and neutropenia≥grade 3 in the patients receiving PARP inhibitors alone, PARP inhibitors combined with chemical treatment drugs as well as the incidence of leukopenia≥grade 3 in the patients receiving PARP inhibitors combined with chemical treatment drugs were significantly higher than those receiving placebo alone, chemical treatment drugs alone or chemical treatment drugs combined with placebo(P<0.05). Sensitivity analysis supported the above results; howerer, publication bias was possibility. CONCLUSIONS: PARP inhibitor in the treatment of cancer can cause hematological system adverse drug reaction, mainly manifesting as anemia, neutropenia and leukopenia. These results should be interpreted with caution.
KEYWORDS? ?PARP inhibitor; Hematologic system; Adverse drug reaction; Meta-analysis
靶向治療是一類與多種分子靶標和信號通路作用相關的治療手段,主要通過抑制腫瘤細胞增殖、轉移,誘導細胞凋亡,調節免疫功能以及逆轉多藥耐藥等機制而發揮抗腫瘤作用[1]。絕大多數腫瘤的發展與DNA損傷及其修復、缺失有關[2]。聚腺苷二磷酸核糖聚合酶(PARP)是介導DNA修復的重要因子,可通過募集或結合其他DNA修復蛋白來修復DNA損傷[3]。在PARP家族中,PARP-1的相關研究較多,且顯示出對DNA修復和基因組穩定的特異活性[3]。PARP抑制劑是一種通過抑制PARP介導的DNA修復通路來達到合成致死目的的靶向治療藥物[2]。其可通過抑制PARP酶來抑制受損腫瘤細胞的堿基切除修復途徑,使單鏈DNA斷裂難以修復,而進一步發展為雙鏈DNA斷裂,使腫瘤細胞啟動DNA雙鏈斷裂的修復通路——同源重組修復和非同源末端鏈接[4-5],同源重組修復通路會因細胞中乳腺癌易感基因(BRCA1/2)突變而使功能受損,致使斷裂的DNA雙鏈無法被修復,導致易發生錯誤的非同源末端連接修復途徑被激活,從而引起基因組不穩定、突變積累,最終導致腫瘤細胞死亡[2,6]。
目前,PARP抑制劑如奧拉帕尼、尼拉帕尼、盧卡帕尼均已被美國FDA批準用于對鉑類藥物敏感的復發性卵巢癌的維持治療[7]。其中,奧拉帕尼是首個在我國上市的PARP抑制劑,該藥應用較廣泛,安全性數據較全,患者耐受性較好[7]。近年來,對PARP抑制劑的研究已逐漸由卵巢癌擴展到其他癌癥如乳腺癌[8]、胰腺癌[8,9]、前列腺癌[8,10]、胃癌[11]和小細胞肺癌[12]等。但有研究發現,單用PARP抑制劑并未比現有化學治療藥物更有效,但當其與化學治療藥物聯用時則可為患者帶來更多的臨床獲益[8]。然而,PARP抑制劑可引起疲勞、胃腸道反應、腎毒性及血液系統不良反應的發生[13]。其中,血液系統不良反應是一類比較常見的不良反應,一般出現在患者使用PARP抑制劑的早期,是導致患者延遲用藥、劑量調整和停藥的主要原因,主要表現為貧血、中性粒細胞減少、血小板減少、白細胞減少,這些反應可不同程度地影響著患者的生存質量[13]。雖然已有研究對奧拉帕尼致貧血和疲勞進行了系統評價[14],但未見有PARP抑制劑致中性粒細胞減少、白細胞減少和血小板減少的系統評價。為提高患者用藥的安全性,本研究采用Meta分析的方法系統評價了PARP抑制劑治療腫瘤致血液系統不良反應的發生情況,旨在為臨床用藥提供循證參考。
1 資料與方法
1.1 納入與排除標準
1.1.1 研究類型 國內外公開發表的隨機對照試驗(RCT);語種限定為中文和英文。
1.1.2 研究對象 接受過鉑類藥物治療或內分泌治療的年齡≥18歲且正在接受化學藥物治療(以鉑類藥物為基礎的化療方案)的癌癥患者;美國東部腫瘤協作組(ECOG)全身功能狀態評分為0~2分;器官和骨髓造血功能正常。
1.1.3 干預措施 試驗組患者單用PARP抑制劑或PARP抑制劑聯合化學治療藥物;對照組患者單用化學治療藥物或安慰劑或化學治療藥物聯合安慰劑。
1.1.4 結局指標 ①貧血≥3級發生率,即血紅蛋白<8.0 g/dL或需要輸血或藥物治療;②中性粒細胞減少癥≥3級發生率,即中性粒細胞計數為0.5×109~1.0×109 L-1或更低;③白細胞減少癥≥3級發生率,即白細胞計數為1.0×109~2.0×109 L-1或更低;④血小板減少癥≥3級發生率,即血小板計數為25.0×109~50.0×109 L-1或更低。不良反應分級根據美國國家癌癥研究所的常見藥物不良反應評價標準(NCI-CTCAE)確定[15]。
1.1.5 排除標準 ①綜述、會議論文;②基礎研究(包括動物研究);③個案報道、重復發表的文獻;④無以上任何一項結局指標的研究或無法獲取全文的文獻。
1.2 文獻檢索策略
計算機檢索PubMed、Embase、Cochrane 圖書館、ScienceDirect、中國期刊全文數據庫、中國生物醫學文獻數據庫、中國科技期刊全文數據庫、萬方數字化期刊全文數據庫。中文檢索詞為“奧拉帕尼”“尼拉帕尼”“盧卡帕尼”“維拉帕尼”“PARP抑制劑”“癌癥”“腫瘤”“不良反應”“血液系統”;英文檢索詞為“Olaparib”“Niraparib”“Rucaparib”“Veliparib”“PARP inhibitor”“Cancer”“Tumor”“Adverse reaction”“Hematologic system”。檢索時限均為2014年5月-2019年6月。
1.3 文獻篩選與資料提取
由兩位研究者按照納入與排除標準閱讀文獻的標題、摘要,剔除明顯與納入標準不符的文獻后,進一步閱讀全文剔除研究設計不規范、治療方案不合理、結局指標與本研究不相關、無法提取原始數據的文獻,提取完成后進行交叉核對。若存在爭議,則通過與第三方討論決定。對于無法確定的數據,通過與第一作者或通信作者聯系后盡可能收集所需資料。提取資料包括第一作者、發表年份、患者例數、年齡、臨床分期、腫瘤類型、干預措施、結局指標等。
1.4 納入文獻質量評價
采用Cochrane 系統評價員手冊5.1.0推薦的偏倚風險評估工具對納入文獻質量進行評價,具體包括隨機序列產生(分組過程中是否有隨機成分)、分配隱藏(受試者和研究者是否能夠預測分配結果)、盲法(受試者和研究者是否設盲)、結局評估的盲法(是否對結果進行盲法評估)、結果數據的完整性(是否缺失關鍵數據)、選擇性結局報告(報道研究中是否預先申明結局)、其他偏倚(是否有與特定研究設計相關的潛在偏倚)。每項均分為“高風險偏倚”“低風險偏倚”和“不清楚”[16]。
1.5 統計學方法
采用Rev Man 5.3統計軟件進行Meta分析。計數資料以相對危險度(RR)及其95%置信區間(CI)表示。采用Q檢驗和I 2檢驗進行異質性分析。若各研究間無統計學異質性(P>0.10,I 2<50%),采用固定效應模型進行分析;反之,則采用隨機效應模型進行分析。采用敏感性分析評價結果的穩定性,采用倒漏斗圖評價發表偏倚。P<0.05為差異有統計學意義。
2 結果
2.1 文獻檢索結果與納入研究基本信息
初檢共得到相關文獻476篇;按照納入與排除標準,瀏覽標題和摘要并閱讀全文后,最終納入10項研究[9-12,17-22],共計3 129例患者,其中試驗組1 890例、對照組1 239例。文獻篩選流程見圖1,納入研究基本信息見表1。
2.2 納入文獻質量評價結果
10項研究[9-12,17-22]均為RCT;9項研究[9-11,17-22]描述了隨機序列產生的方法,6項研究[10-11,18-20,22]描述了分配隱藏;9項研究[9-12,17-21]對研究者和受試者采用盲法;8項研究[9-10,17-22]在結局評估時使用盲法;9項[9-12,17-20,22]研究結局數據完整;8項研究[9,11-12,17-19,21-22]未選擇性報告結果;所有研究均不清楚是否存在其他偏倚來源,詳見圖2、圖3。
2.3 Meta分析結果
2.3.1 貧血≥3 級發生率 10項研究[9-12,17-22]報道了貧血≥3級發生率,各研究間有統計學異質性(P<0.000 01,? I 2=77%),采用隨機效應模型進行Meta分析,詳見圖4。Meta分析結果顯示,試驗組患者貧血≥3級發生率顯著高于對照組[RR=7.27,95%CI(2.74,19.27),P<0.000 1]。
按是否聯合用藥進行亞組分析。6項研究[9,17-21]報道了單用PARP抑制劑對比安慰劑患者的貧血≥3級發生率,各研究間無統計學異質性(P=0.14,I 2=40%),采用固定效應模型進行Meta分析。Meta分析結果顯示,單用PARP抑制劑患者的貧血≥3級發生率顯著高于單用安慰劑者[RR=11.75,95%CI(4.69,29.41),P<0.000 01]。4項研究[10-12,22]報道了PARP抑制劑聯合化學治療藥物對比安慰劑聯合化學治療藥物或單用化學治療藥物致患者貧血≥3級的發生率,各研究間無統計學異質性(P=0.12,I 2=49%),采用固定效應模型進行Meta分析。Meta分析結果顯示,PARP抑制劑聯合化學治療藥物致患者貧血≥3級的發生率顯著高于安慰劑聯合化學治療藥物或單用化學治療藥物[RR=2.55,95%CI(1.03,6.34),P=0.04],詳見圖4。
2.3.2 中性粒細胞減少≥3級發生率 9項研究[10-12,17-22]報道了中性粒細胞減少≥3級發生率,各研究間有統計學異質性(P=0.000 4,I 2=72%),采用隨機效應模型進行Meta分析,詳見圖5。Meta分析結果顯示,試驗組患者中性粒細胞減少≥3級發生率顯著高于對照組[RR=2.46,95%CI(1.43,4.24),P=0.001]。
按是否聯合用藥進行亞組分析。5項研究[17-21]報道了單用PARP抑制劑對比安慰劑患者的中性粒細胞減少≥3級發生率,各研究間有統計學異質性(P=0.02,I 2=65%),采用隨機效應模型進行Meta分析。Meta分析結果顯示,單用PARP抑制劑患者的中性粒細胞減少≥3級發生率顯著高于單用安慰劑者[RR=3.59,95%CI(1.40,9.21),P=0.008]。4項研究[10-12,22]報道了PARP抑制劑聯合化學治療藥物對比安慰劑聯合化學治療藥物或單用化學治療藥物致患者中性粒細胞減少≥3級的發生率,各研究間無統計學異質性(P=0.14,I 2=46%),采用固定效應模型進行Meta分析。Meta分析結果顯示,PARP抑制劑聯合化學治療藥物致患者中性粒細胞減少≥3級發生率顯著高于安慰劑聯合化學治療藥物或單用化學治療藥物[RR=1.43,95%CI(1.14,1.80),P=0.002],詳見圖5。
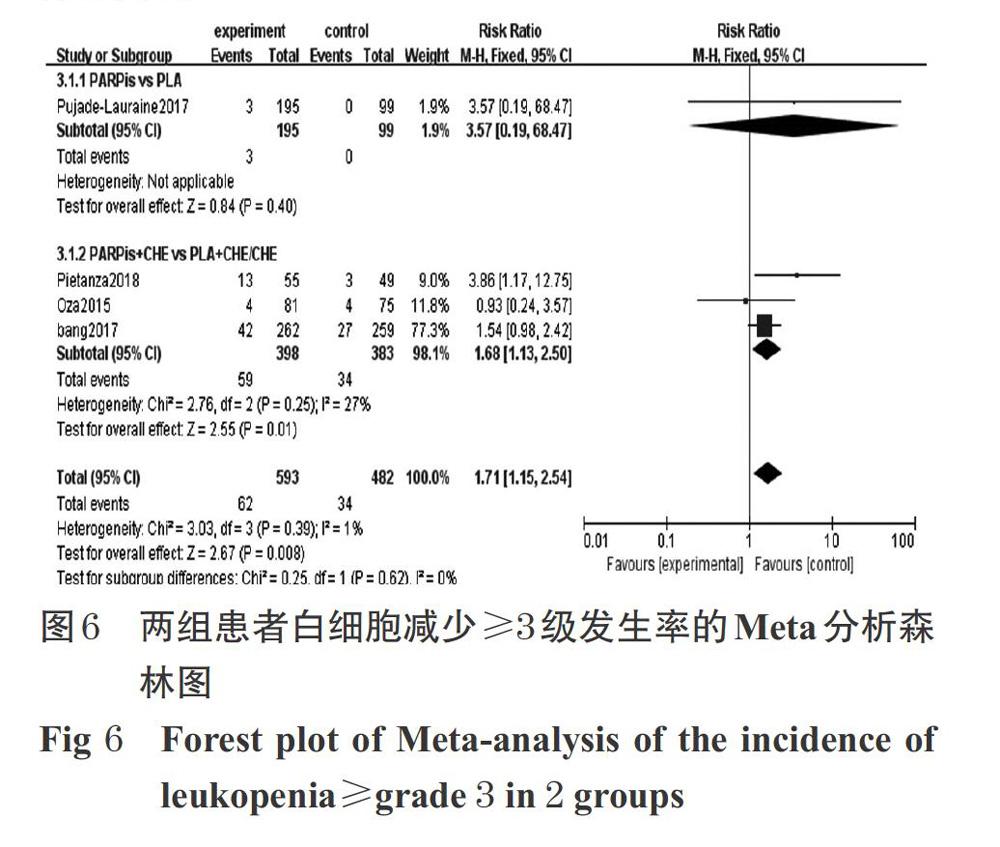
2.3.3 白細胞減少≥3級發生率 4項研究[11-12,19,22]報道了白細胞減少≥3級發生率,各研究間無統計學異質性(P=0.39,I 2= 1%),采用固定效應模型進行Meta分析,詳見圖6。Meta分析結果顯示,試驗組患者白細胞減少≥3級發生率顯著高于對照組[RR=1.71,95%CI(1.15,2.54),P=0.008]。
按是否聯合用藥進行亞組分析。1項研究[19]報道了單用PARP抑制劑對比安慰劑患者的白細胞減少≥3級發生率。Meta分析結果顯示,兩組患者白細胞減少≥3級發生率比較,差異無統計學意義[RR=3.57,95%CI(0.19,68.47),P=0.40]。3項研究[11-12,22]報道了PARP抑制劑聯合化學治療藥物對比安慰劑聯合化學治療藥物或單用化學治療藥物致患者白細胞減少≥3級的發生率,各研究間無統計學異質性(P=0.25,I 2=27%),采用固定效應模型進行Meta分析。Meta分析結果顯示,PARP抑制劑聯合化學治療藥物致患者白細胞減少≥3級的發生率顯著高于安慰劑聯合化學治療藥物或單用化學治療藥物[RR=1.68,95%CI(1.13,2.50),P=0.01],詳見圖6。
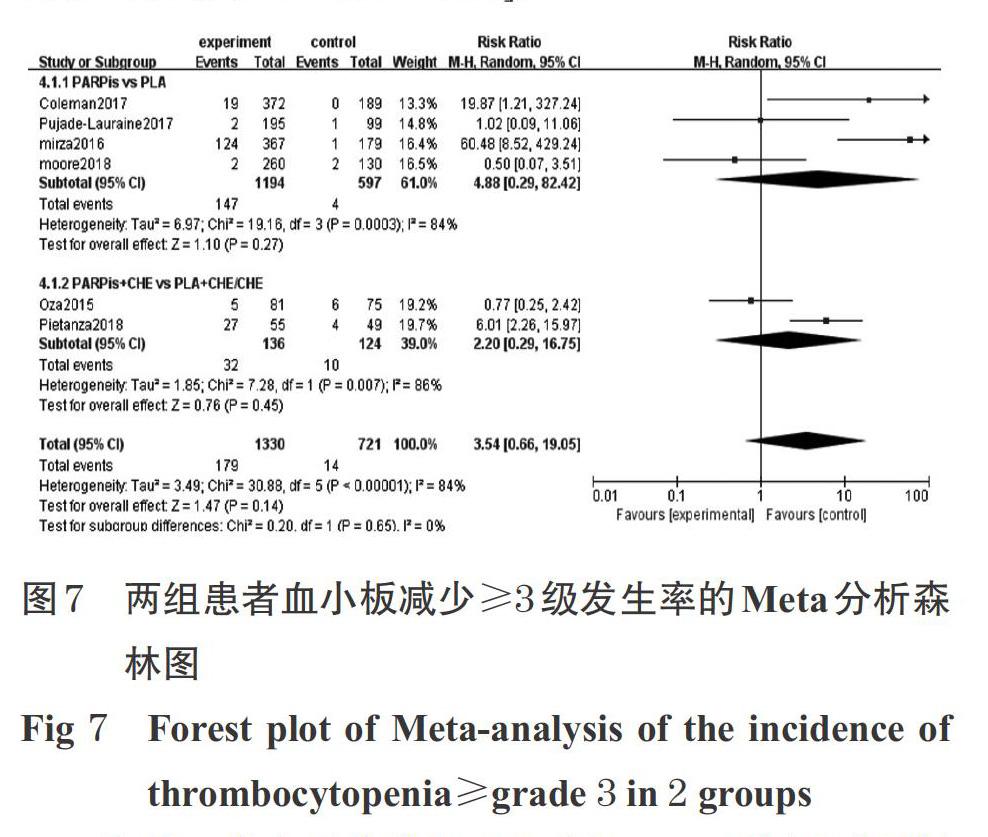
2.3.4 血小板減少≥3級發生率 6項研究[12,17,19-22]報道了血小板減少≥3級發生率,各研究間有統計學異質性(P<0.000 01,I 2=84%),采用隨機效應模型進行Meta分析,詳見圖7。Meta分析結果顯示,兩組患者血小板減少≥3級發生率比較,差異無統計學意義[RR=3.54,95%CI(0.66,19.05),P=0.14]。
按是否聯合用藥進行亞組分析。4項研究[17,19-21]報道了單用PARP抑制劑對比安慰劑患者的血小板減少≥3級發生率,各研究間有統計學異質性(P=0.000 3,I 2=84%),采用隨機效應模型進行Meta分析。Meta分析結果顯示,兩組患者血小板減少≥3 級發生率比較,差異無統計學意義[RR=4.88,95%CI(0.29,82.42),P=0.27]。2項研究[12,22]報道了PARP抑制劑聯合化學治療藥物對比安慰劑聯合化學治療藥物或單用化學治療藥物致患者血小板減少≥3級發生率,各研究間有統計學異質性(P=0.007,I 2=86%),采用隨機效應模型進行Meta分析。Meta分析結果顯示,兩組患者血小板減少≥3 級發生率比較,差異無統計學意義[RR=2.20,95%CI(0.29,16.75),P=0.45],詳見圖7。
2.4 敏感性分析
以貧血≥3級發生率為指標,逐一剔除各項研究進行敏感性分析。結果,當剔除Bang YJ 等[11]的研究后,各研究間異質性改變最顯著(P=0.003,I 2=66%),Meta分析結果顯示,試驗組患者貧血≥3級發生率顯著高于對照組[RR=8.84,95%CI(3.25,24.06),P<0.000 1]。以中性粒細胞減少≥3級發生率為指標,逐一剔除各項研究進行敏感性分析。結果,當剔除Mirza MR等[21]的研究后,各研究間異質性改變最顯著(P=0.10,I 2=42%),Meta分析結果顯示,試驗組患者中性粒細胞減少≥3級發生率顯著高于對照組[RR=1.75,95%CI(1.19,2.51),P=0.005]。以白細胞減少≥3級發生率為指標,逐一剔除各項研究進行敏感性分析。結果,當剔除Pujade-? ?Lauraine E等[19]的研究后,各研究間異質性改變最顯著(P=0.25,I 2=27%),Meta分析結果顯示,試驗組患者白細胞減少≥3級發生率顯著高于對照組[RR=1.68,95%CI(1.13,2.50),P=0.01]。以血小板減少≥3級發生率為指標,逐一剔除各項研究進行敏感性分析。結果,當剔除Mirza MR等[21]的研究后,各研究間異質性改變最顯著(P=0.01,I 2=70%),Meta分析結果顯示,兩組患者血小板減少≥3級發生率比較,差異無統計學意義[RR=1.98,95%CI(0.52,7.52),P=0.32]。上述指標的敏感性分析結果均提示本研究結果穩健、可信。
2.5 發表偏倚分析
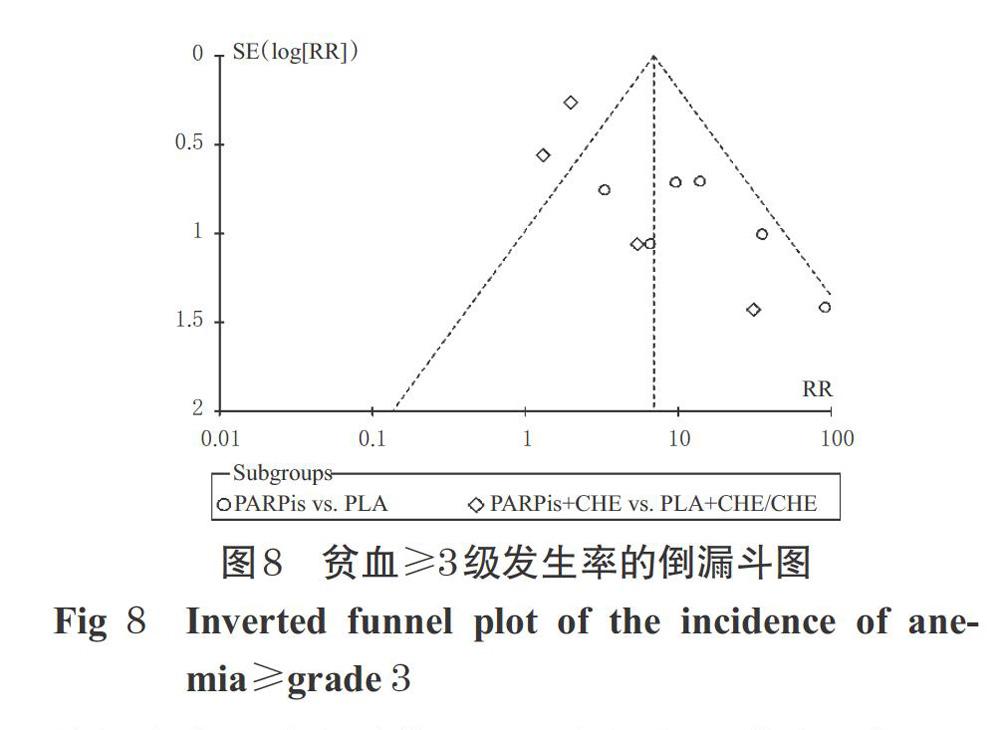
以貧血≥3級發生率為指標繪制倒漏斗圖,詳見圖8。由圖8可知,各研究散點均位于倒漏斗圖中上方,圖形不對稱且有2項研究[11,22]分布在倒漏斗圖外,提示本研究存在發表偏倚的可能性較大(其余指標所得結果相似,圖略)。
3 討論
隨著相關研究的深入,PARP抑制劑已從用于治療復發性卵巢癌延伸到其他類型癌癥,從用于BRCA基因突變的癌癥延伸到非BRCA基因相關的癌癥,PARP抑制劑的抗腫瘤活性正被研究者進一步發掘[23]。然而,該藥給癌癥患者帶來臨床療效的同時也導致了一些不良反應的發生,如疲勞、胃腸道反應、腎毒性及血液系統不良反應等[13]。而血液系統不良反應幾乎是所有PARP抑制劑較常見且較嚴重的不良反應,主要表現為貧血、中性粒細胞減少、白細胞較少和血小板減少,其中以貧血最為常見[13,24-25]。這些反應常出現在治療的早期,且多為3級和4級不良反應,極易導致患者用藥劑量調整和停藥[13,21],這使得PARP抑制劑的臨床應用受到一定限制。
PARP-1/PARP-2酶在DNA修復中被募集,且在細胞增殖、分化和轉化過程中發揮了重要作用[26],PARP-1參與了細胞晝夜代謝活動,PRPA-2在調節紅細胞生成中具有重要意義[27-30]。有研究表明,PARP-2能夠適當地維持小鼠造血功能的動態平衡;而PARP-2的缺失會損傷小鼠紅系細胞分化,增加復制壓力和溶血反應,導致慢性貧血[28-29]。由于這些是基于動物的體內研究,而PARP酶系在人體內的血液學機制尚不清楚,故還需相關研究進一步闡明。此外,PARP酶系除可在DNA損傷修復過程中發揮作用外,還與細胞能量消耗、脂質代謝、膽固醇穩態以及T細胞成熟有關[30],這些功能可能也與PARP抑制劑致血液系統不良反應有關。PARP抑制劑對腫瘤細胞和正常細胞無選擇性,會干擾正常細胞的DNA修復途徑,阻礙正常細胞的DNA修復,而致化學治療藥物的毒性(如骨髓抑制)增強,從而影響患者預后[25]。
本研究結果顯示,試驗組患者貧血≥3級發生率、中性粒細胞減少≥3級發生率、白細胞減少≥3級發生率均顯示高于對照組。亞組分析結果顯示,無論是PARP抑制劑單用還是聯合化學治療藥物,貧血和中性粒細胞減少≥3級發生率均顯著高于對照組。盡管在白細胞減少≥3級發生率的亞組分析中,單用PARP抑制劑與安慰劑比較,差異無統計學意義,但由于只納入了1項研究,因此亞組分析結果還需更多研究證實。血小板減少≥3級發生率的亞組分析結果顯示,兩組比較差異無統計學意義。敏感性分析支持上述結果,但發表偏倚分析顯示存在發表偏倚的可能性較大。這提示,PARP抑制劑可致癌癥患者發生血液系統不良反應,特別是貧血、中性粒細胞減少。因此,臨床使用PARP抑制劑時應充分考慮患者的造血功能,用藥前需對其進行用藥教育,用藥時需對患者的血液指標進行監測,必要時調整藥物劑量并輔以利血生、重組人紅細胞生成素、重組粒細胞集落刺激因子等藥物,用藥后結合飲食療法和運動療法,以減少血液系統不良反應所致的不良后果。
本研究的局限性如下:(1)部分指標相關研究間的異質性較高,分析結果具有不確定性;(2)受試對象來自不同國家、不同地區和不同種族,本文并未對不同種族間血液毒性的風險是否存在顯著性差異進行分析;(3)由于單個PARP抑制劑藥物的試驗數據有限,因此未評價單個PARP抑制劑致血液系統不良反應的風險差異,故此結論尚需更多大樣本、多中心RCT進一步證實。
參考文獻
[ 1 ] KE X,SHEN L. Molecular targeted therapy of cancer:the progress and future prospect[J]. Frontiers in Laboratory Medicine,2017,1(2),69-75.
[ 2 ] WANG Y,LUO W,WANG Y. PARP-1 and its associated nucleases in DNA damage response[J]. DNA Repair,2019. DOI:10.1016/j.dnarep.2019.102651.
[ 3 ] LORD CJ,ASHWORTH A. PARP inhibitors:synthetic lethality in the clinic[J]. Science,2017,355(6330):1152- 1158.
[ 4 ] AYMARD F,BUGLER B,SCHMIDT CK,et al. Trans- criptionally active chromatin recruits homologous recombination at DNA double-strand breaks[J]. Nat Struct Mol Biol,2014,21(4):366-374.
[ 5 ] RADHAKRISHNAN SK,JETTE N,LEES-MILLER SP. Non-homologous end joining:emerging themes and unanswered questions[J]. DNA Repair:Amst,2014. DOI:10.1016/j.dnarep.2014.01.009.
[ 6 ] WALSH CS. Two decades beyond BRCA1/2:homologous recombination,hereditary cancer risk and a target for ova- rian cancer therapy[J]. Gynecologic Oncology,2015,137(2):343-350.
[ 7 ] 高慶蕾,孔北華,尹如鐵,等. PARP抑制劑治療復發性卵巢癌專家共識[J].現代婦產科進展,2018,27(10):721- 725.
[ 8 ] KAMEL D,GRAY C,WALIA JS,et al. PARP inhibitor drugs in the treatment of breast,ovarian,prostate and pancreatic cancers:an update of clinical trials[J]. Curr Drug Targets,2018,19(1):21-37.
[ 9 ] GOLAN T,HAMMEL P,RENI M,et al. Maintenance olaparib for germline BRCA-mutated metastatic pancrea- tic cancer[J]. N Engl J Med,2019,381(4):317-327.
[10] CLARKE N,WIECHNO P,ALEKSEEV B,et al. Olapa- rib combined with abiraterone in patients with metastatic castration-resistant prostate cancer:a randomized,double-blind,placebo-controlled,phase 2 trial[J]. Lancet Oncol,2018,19(7):975-986.
[11] BANG YJ,XU RH,CHIN K,et al. Olaparib in combination with paclitaxel in patients with advanced gastric cancer who have progressed following first-line therapy(GOLD):a double-blind,randomized,placebo-controlled,phase 3 trial[J]. Lancet Oncol,2017,18(12):1637-1651.
[12] PIETANZA MC,WAQAR SN,KRUG LM,et al. Rando- mized,double-blind,phase Ⅱ study of temozolomide in combination with either veliparib or placebo in patients with relapsed-sensitive or refractory small-cell lung cancer[J]. J Clin Oncol,2018,36(23):2386-2394.
[13] LAFARGUE CJ,DALMOLIN GZ,SOOD AK,et al. Exploring and comparing adverse events between PARP inhibitors[J]. Lancet Oncol,2019,20(1):15-28.
[14] RUIZ-SCHUTZ VC,GOMES LM,MARIANO RC,et al. Risk of fatigue and anemia in patients with advanced cancer treated with olaparib: a meta-analysis of randomized controlled trials[J]. Crit Rev Oncol Hematol,2019. DOI: 10.1016/j.critrevonc.2019.06.012.
[15] TROTTI A,COLEVAS AD,SETSER A,et al. CTCAE v3.0:development of a comprehensive grading system for the adverse effects of cancer treatment[J]. Semin Radiat Oncol,2003,13(3):176-181.
[16] 谷鴻秋,王楊,李衛. Cochrane偏倚風險評估工具在隨機對照研究Meta分析中的應用[J].中國循環雜志,2014,29(2):147-148.
[17] MOORE K,COLOMBO N,SCAMBIA G,et al. Maintenance olaparib in patients with newly diagnosed advanced ovarian cancer[J]. N Engl J Med,2018,379(26):2495- 2505.
[18] LEDERMANN J,HARTER P,GOURLEY C,et al. Olaparib maintenance therapy in patients with platinum-sensitive relapsed serous ovarian cancer:a preplanned retrospective analysis of outcomes by BRCA status in a randomized phase 2 trial[J]. Lancet Oncol,2014,15(8):852-861.
[19] PUJADE-LAURAINE E,LEDERMANN JA,SELLE F,et al. Olaparib tablets as maintenance therapy in patients with platinum-sensitive,relapsed ovarian cancer and a BRCA1/2 mutation(SOLO2/ENGOT-Ov21):a double-blind,randomized,placebo-controlled,phase 3 trial[J].Lancet Oncol,2017,18(9):1274-1284.
[20] COLEMAN RL,OZA AM,LORUSSO D,et al. Rucapa- rib maintenance treatment for recurrent ovarian carcinoma after response to platinum therapy(ARIEL3):a rando- mized,double-blind,placebo-controlled,phase 3 trial[J]. Lancet,2017,390(10106):1949-1961.
[21] MIRZA MR,MONK BJ,HERRSTEDT J,et al. Niraparib maintenance therapy in platinum-sensitive,recurrent ova- rian cancer[J]. N Engl J Med,2016,375(22):2154-2164.
[22] OZA AM,CIBULA D,BENZAQUEN AO,et al. Olaparib combined with chemotherapy for recurrent platinum-? ?sensitive ovarian cancer:a randomized phase 2 trial[J]. Lancet Oncol,2015,16(1):87-97.
[23] CERRATO A,MORRA F,CELETTI A. Use of poly ADP-ribose polymerase (PARP) inhibitors in cancer cells bearing DDR defects:the rationale for their inclusion in the clinic[J]. J Exp Clin Cancer Res,2016. DOI:10.1186/s13046-016-0456-2.
[24] EVANS T,MATULONIS U. PARP inhibitors in ovarian cancer:evidence,experience and clinical potential[J]. Ther Adv Med Oncol,2017,9(4):253-267.
[25] ZHOU JX,FENG LJ,ZHANG X. Risk of severe hematologic toxicities in cancer patients treated with PARP inhibitors:a meta-analysis of randomized controlled trials[J]. Drug Des Devel Ther,2017. DOI:10.2147/DDDT.S147726.
[26] TANGUTOORI S,BALDWIN P,SRIDHAR S. PARP inhibitors:a new era of targeted therapy[J]. Maturitas,2015,81(1):5-9.
[27] ZHAO H,SIFAKIS EG,SUMIDA N,et al. PARP1 and CTCF-mediated interactions between active and repressed chromatin at the lamina promote oscillating transcription[J]. Molecular Cell,2015,59(6):984-997.
[28] FARR?S J,MART?N-CABALLERO J,MART?NEZ C, et al. PARP-2 is required to maintain hematopoiesis following sublethal -irradiation in mice[J]. Blood,2013,122(1):44-54.
[29] FARR?S J,LLACUNA L,MARTIN-CABALLERO J,? ?et al. PARP-2 sustains erythropoiesis in mice by limiting replicative stress in erythroid progenitors[J]. Cell Death Differ,2015,22(7):1144-1157.
[30] SUN QZ,GATI MI,KELLY GM. Serum-dependent and independent regulation of PARP2[J]. Biochem Cell Biol,2019,97(5):600-611.
(收稿日期:2020-05-13 修回日期:2020-08-24)
(編輯:陳 宏)

