重組枯草芽孢桿菌異源分泌表達麥芽三糖酶及其發酵優化
樓志華


摘 要:為了實現麥芽三糖酶的商業化生產,本研究以枯草芽孢桿菌為宿主,構建了木糖誘導分泌表達載體,表達了來源于Thermobifida fusca NTU22的麥芽三糖酶基因,考察重組枯草芽孢桿菌表達麥芽三糖酶的能力。搖瓶驗證了基因的功能表達之后,經過初步優化,最大發酵酶活為(108.4±2.84)U·mL-1。該研究為重組枯草芽孢桿菌發酵產麥芽三糖酶的工業化應用提供了參考。
關鍵詞:枯草芽孢桿菌;麥芽三糖酶;分泌表達
Abstract:In order to realize the commercial production of maltotriohydrolase, in this study, Bacillus subtilis was used as the host to construct a xylose-inducing secretion expression vector and express the maltotriohydrolase gene derived from Thermobifida fusca NTU22. The ability of recombinant Bacillus subtilis to express maltotriase was investigated. After the shake flask verified the functional expression of the gene, after preliminary optimization, the maximum fermentation enzyme activity was (108.4±2.84) U·mL-1. This research provides a reference for the industrial application of recombinant maltotriase produced by Bacillus subtilis fermentation.
Key words:Bacillus subtilis; Maltotriohydrolase; Secreted expression
中圖分類號:TQ925.1
麥芽三糖酶(Glucan 1,4-alpha-maltotriohydrolase),也叫麥芽三糖淀粉水解酶,可以從淀粉多糖的非還原末端連續地切割麥芽三糖殘基,其主要水解產物麥芽三糖在糖果行業、飲料行業、食品加工行業有著廣泛的應用[1]。目前,研究發現的麥芽三糖酶基因主要來源于蛾微桿菌(Microbacterium imperiale)[2]、灰鏈霉菌(Streptomyces griseus)[3]等,然而對于如何實現該酶的規模化、商業化生產鮮見報道。因此,麥芽三糖酶的高效生產菌種亟待開發,以實現麥芽三糖規模生產。
枯草芽孢桿菌是美國食品和藥品管理局、中國農業農村部認證的食品安全菌株,廣泛應用于生產各種工業酶制劑[4-5]。本研究擬構建木糖誘導的枯草芽孢桿菌表達系統,對來源于Thermobifida fusca NTU22的麥芽三糖酶基因序列優化后進行異源分泌表達,并對構建的重組枯草芽孢桿菌進行發酵條件優化,為枯草芽孢桿菌發酵生產麥芽三糖酶的工業化應用提供參考。
1 材料與方法
1.1 菌株和質粒
敲除了α-淀粉酶基因amyL的枯草芽孢桿菌模式菌株Bacillus subtilis WB600、E. coli JM109、E. coli JM109/pBSxyl、E. coli JM109/pBSG3,均購于江南大學。
1.2 工具酶、引物和試劑
Taq和Pfu DNA聚合酶、T4 DNA連接酶購于Thermo Fisher公司,各種限制性內切酶、PCR產物純化試劑盒、質粒提取試劑盒購于TAKARA有限公司。
1.3 DNA操作技術
質粒提取、DNA片段純化、回收等均參照TAKARA試劑盒說明書,PCR擴增反應、DNA瓊脂糖凝膠電泳、酶切、連接以及轉化子篩選等均參照分子克隆實驗指南[6]。
1.4 重組枯草芽孢桿菌的構建
LBY培養基過夜培養E. coli JM109/pBSxyl、E. coli JM109/pBSG3,提取重組質粒pBSxyl、pBSG3后,按文獻[7]所述方法將其轉入敲除了α-淀粉酶基因amyL的B. subtilis WB600,從而獲得重組枯草芽孢桿菌,分別命名為BSXYL和BSG3。
1.5 麥芽三糖酶酶活定義及測定
麥芽三糖酶酶活檢測方法參考文獻[8]。酶活單位(U)定義為:在pH 6.0、55 ℃的反應條件下,每分鐘水解1%可溶性淀粉生成相當于1 μmoL麥芽三糖所需的酶量。
1.6 發酵優化實驗
LBY培養基、發酵培養基以及微量元素配制方法參照文獻[9]。在進行發酵優化實驗時,均使用擋板搖瓶發酵,發酵時均加入終濃度為20 mg·L-1的四環素。初始pH為7.0,溫度37 ℃,在適當時間添加木糖進行誘導。
2 結果與分析
2.1 重組表達載體的構建
NCBI顯示,Thermobifida fusca NTU22來源的麥芽三糖酶基因序列總長為1818 bp,含木糖異構酶啟動子及其調控蛋白基因、信號肽的基因片段長度約為1507 bp。重組質粒經XbaⅠ和KpnⅠ酶切后應獲得大小為1522 bp和6789 bp的兩條核酸條帶,電泳鑒定結果符合預期(圖1),結合測序結果,表明重組表達載體構建正確。
2.2 重組麥芽三糖酶的表達
將對照菌BSXYL和重組表達菌株BSG3分別進行搖瓶發酵,接種后8 h均加入10 g·L-1木糖進行誘導,然后繼續培養30 h,離心后收集發酵液上清,分別檢測二者胞外麥芽三糖酶活力。結果顯示,只有重組表達菌株BSG3檢測到活力,而對照菌BSXYL未檢測到活力。蛋白電泳(圖2)結果顯示在約68.7 kDa處出現一明顯的表達條帶,表明枯草芽孢桿菌成功地分泌了麥芽三糖酶到發酵液中[10-11]。
2.3 發酵條件優化
2.3.1 誘導劑添加時間對發酵的影響
分別在發酵培養至4、8、12、16 h添加10 g·L-1木糖進行誘導,然后繼續發酵至48 h結束,誘導劑不同添加時間對重組菌表達麥芽三糖酶的影響如圖3所示。
如圖3所示,發酵結束時,OD600基本隨著誘導劑添加時間的延遲而增加,這表明添加誘導劑的時間越早,越不利于重組菌的生長。而且在4~12 h,誘導劑添加越晚,發酵結束時檢測到的胞外酶活也越高,當發酵12 h添加誘導劑時,發酵結束時可以檢測到最高的胞外酶活(69.2±1.67)U·mL-1。
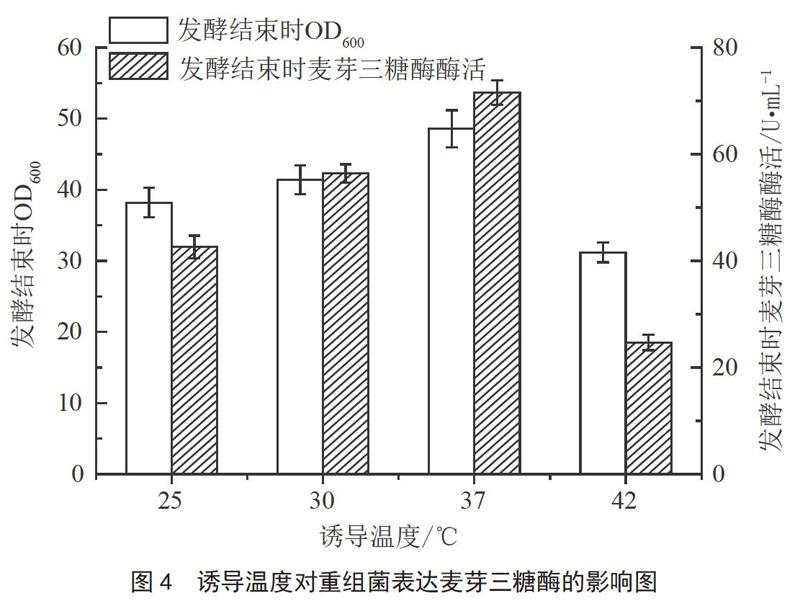
2.3.2 誘導溫度對發酵的影響
分別考察25、30、37、42 ℃誘導對產酶的影響,結果如圖4所示。可以發現,在25~37 ℃,隨著誘導溫度升高,發酵結束后的菌體量也越來越高,而42 ℃時,菌體量又有所降低,這說明重組菌最適生長溫度為37 ℃。同時,在25~37 ℃,隨著誘導溫度升高,胞外酶活力逐漸增加,誘導溫度37 ℃時,檢測到最高胞外酶活力可達(71.6±2.31)U·mL-1。
2.3.3 發酵時間對發酵的影響
在前述實驗結果基礎上進行發酵,當培養至12 h時,添加10 g·L-1木糖進行誘導,同時添加20 g·L-1麥芽糊精,發酵至24 h時補加20 g·L-1葡萄糖,發酵至36 h時添加20 g·L-1葡萄糖和10 g·L-1木糖,以后每隔12 h補加10 g·L-1葡萄糖,繼續發酵至96 h結束發酵。誘導后,每隔12 h檢測菌體量OD600和麥芽三糖酶酶活,結果如圖5顯示。可以看到,發酵至72 h時,胞外檢測到的最大酶活為(108.4±2.84)U·mL-1,之后酶活力明顯開始下降,表明重組菌發酵應在其穩定期結束時停止發酵。
3 結論
本研究以枯草芽孢桿菌為宿主,研究了來源于Thermobifida fusca NTU22麥芽三糖基因的表達方法,并且成功地實現了該酶的木糖誘導分泌表達,能夠在發酵液上清中檢測到酶活力,而且所表達蛋白大小符合理論值。對重組菌進行了發酵條件優化,獲得了最佳的發酵條件:在對數生長前中期添加誘導劑,誘導溫度37 ℃,發酵至穩定期結束停止發酵,胞外檢測到的最大酶活為(108.4±2.84)U·mL-1。
參考文獻:
[1]徐貴華,劉鐘棟,陳肇錟.小麥淀粉制備麥芽三糖的研究[J].河南工業大學學報(自然科學版),2002,23(3):1-4.
[2]Takasaki Y,Kitajima M,Tsuruta T,et al. Studies on enzymatic production of oligosaccharides. Part VI. Maltotriose-producing amylase from Microbacterium imperiale[J]. Agricultural and biological chemistry,1991,55(3):687-692.
[3]吳春森.麥芽三糖酶催化作用機制及其應用研究[D].無錫:江南大學,2017.
[4]Nakakuki T,Azum K,Kainuma K. Action patterns of various exo-amylases and the anomeric configurations of their products[J].Carbohydrate Research,1984,128(2):297-310.
[5]Yang C H,Liu W H. Purification and properties of a maltotriose-producing alpha-amylase from Thermobifida fusca[J].Enzyme & Microbial Technology,2004,35(2-3):254-260.
[6]Takasaki Y,Kitajima M,Tsuruta T,et al. Maltotriose-producing Amylase from Microbacterium imperiale[J].Journal of the Agricultural Chemical Society of Japan,2006,55(3):687-692.
[7]Yang C H,Huang Y C,Chen C Y,et al. Heterologous expression of Thermobifida fusca thermostable alpha-amylase in Yarrowia lipolytica and its application in boiling stable resistant sago starch preparation[J].Journal of Industrial Microbiology and Biotechnology,2010,37(9):953-960.
[8]Olempska-Beer Z S,Merker R I,Ditto MD,et al.Food-processing enzymes from recombinant microorganisms——a review[J].Regul Toxicol Pharmacol,2006,45(2):144-158.
[9]池亞斌.枯草芽孢桿菌發酵生產N-乙酰氨基葡萄糖條件優化控制研究[D].無錫:江南大學,2016.
[10]Tuan-Anh T,Ly L T,Viet N Q,et al. Novel methods to optimize gene and statistic test for evaluation - an application for Escherichia coli[J]. Bmc Bioinformatics,2017,18(1):100.
[11]楊韻霏,李由然,張梁,等.細菌麥芽糖淀粉酶在枯草芽孢桿菌中的誘導型異源表達[J].微生物學通報,2017,44(2):263-273.

