利用黃漿水降解甲基橙的條件優化及動力學分析
高大響 黃小忠 陳智豪

摘要:通過單因素試驗、正交試驗及動力學分析,研究不同條件對黃漿水降解甲基橙的影響,尤其考察溫度、初始pH值及濕豆渣對反應速率的影響及其動力學關系。結果表明,黃漿水放置一段時間能生成較多脂質氫過氧化物和自由基等活性成分,并且在低氧或缺氧狀態下更有利于甲基橙脫色。抗氧化劑表沒食子茶素沒食子酸酯(EGCG)和殼聚糖對甲基橙脫色產生明顯的抑制作用,在光照條件下,添加草酸銨能明顯加快甲基橙的脫色速率。溫度、pH值和濕豆渣用量對甲基橙脫色均有顯著影響效應,其脫色反應均符合準一級動力學關系。通過考察各因素對甲基橙脫色反應速率的影響發現,濕豆渣添加量的影響最顯著,當甲基橙初始質量濃度為8 mg/L時,最佳脫色工藝為溫度35 ℃,pH值5,濕豆渣添加量6 g/L。
關鍵詞:黃漿水;甲基橙 ;脫色;抗氧化劑;草酸銨;濕豆渣;反應動力學
中圖分類號:S188?? 文獻標志碼: A
文章編號:1002-1302(2020)19-0293-07
收稿日期:2020-01-06
基金項目:江蘇農林職業技術學院科技項目(編號:2019kj049)。
作者簡介:高大響(1969—),男,安徽潁上人,碩士,副教授,主要從事農業生物技術方面的研究。E-mail:1183772425@qq.com。
偶氮染料是合成染料中品種最多的一類,以甲基橙為代表的偶氮染料,被廣泛應用于紡織、造紙、印染、制藥和食品工業中,由此產生大量工業廢水。由于偶氮染料結構復雜、化學性質穩定、毒性較大,大多數傳統方法很難使其降解,從而造成嚴重的環境問題。目前,甲基橙染料廢水的處理方法主要有超聲法[1]、光催化法[2-3]、電化學氧化法[4]、Fenton法[5-6]及生物酶法[7]。超聲法、光催化法、電化學氧化法及Fenton法分別通過超聲空化、紫外光、電催化及引入化學試劑產生的自由基為主要氧化劑來氧化甲基橙等偶氮染料,這些方法存在技術復雜、設備投入大、運行費用高等問題。生物酶法主要利用漆酶的氧化作用來實現偶氮染料的生物脫色,從而消除有毒的芳香胺,但是漆酶只能對偶氮染料進行部分降解,并且對小分子偶氮染料的降解還需要介體。因此,找到一種廉價、實用的降解方法具有重要的現實意義。
脂氧合酶(lipoxygenase,簡稱LOX)廣泛分布于動植物體內,特別是在大豆種子中含量較高,豆制品加工過程中產生的廢水(如大豆乳清廢水)中含有較多高活性的LOX[8-9]。LOX可以通過分子內加氧的方式催化多不飽和脂肪酸氧化[10]。脂質過氧化過程復雜、產物多,包括脂質氫過氧化物、自由基、醛、酮等一系列生理活性物質[11],其中脂質氫過氧化物和自由基是LOX催化反應的初期產物,化學性質非常活潑,具有氧化劑作用,易與其他分子發生反應,例如可直接與蛋白質、核酸發生反應[12],利用LOX耦聯氧化降解類胡蘿卜素、葉綠素等[13],因此LOX在面粉漂白、面筋結構改變、面條加工等方面有很多應用[14-16]。目前,尚未見脂質氫過氧化物和自由基等初期產物在其他工業染料降解脫色方面的研究報道。
筆者在試驗過程中發現,豆制品加工過程中產生的黃漿廢水,在經過酶促氧化后,會產生脂質氫過氧化物、自由基等活性成分,并且這些活性成分能對甲基橙進行有效的降解脫色。本試驗對黃漿水使甲基橙脫色的條件進行研究并分析其動力學關系,旨在為有效利用豆制品廢水降解甲基橙提供依據。
1 材料與方法
1.1 材料與儀器
主要材料:大豆,市售;甲基橙、殼聚糖、草酸銨均為國產分析純;銳鈦型納米二氧化鈦,產品純度為99.9%,平均粒徑為20 nm;表沒食子兒茶素沒食子酸酯(EGCG),純度為95%。
主要儀器:九陽豆漿機;格蘭仕微波爐;高壓滅菌鍋,購自上海三申醫療器械有限公司;生化培養箱,購自江蘇天翎儀器有限公司;恒溫搖床培養箱,購自常州冠軍儀器制造有限公司;723型可見分光光度計,購自上海菁華科技儀器有限公司。
1.2 試驗方法
1.2.1 黃漿水的制備 將大豆浸泡于水中,水的質量為大豆的6倍,浸泡14 h后濾去浸泡水,按濕豆、水質量比為1 ∶6加入豆漿機中打漿,打漿結束后用80目濾網過濾得濕豆渣,備用。將過濾所得豆漿煮沸5 min后冷卻至85 ℃,加入質量為干豆質量的4%的無水硫酸鈣,靜置10 min,用80目濾網過濾,將收集的黃漿水于30 ℃下敞口靜置24 h后備用。
1.2.2 甲基橙脫色率的計算 取敞口靜置24 h的黃漿水,用雙層紗布濾除沉淀并適當稀釋后,加入甲基橙,配制成不同質量濃度(0~10 mg/L)的甲基橙溶液。利用分光光度計在可見光波段進行掃描,發現其最大吸收波長在469 nm處。在波長為469 nm 處,吸光度(y)與甲基橙質量濃度(x)呈良好的線性關系,其線性方程為y=0.071 6x-0.002 2。
黃漿水經稀釋后,調節其pH值為5。取50 mL稀釋液加入150 mL三角瓶中,并加入一定量的甲基橙,使其質量濃度為8 mg/L,混勻后,于恒溫培養箱中,在不同溫度下進行脫色反應。在不同的時間點于469 nm波長處測定吸光度并按下式計算脫色率:
脫色率=反應前后最大吸收波長處的吸光度變化值反應前最大吸收波長處的吸光度×100%。
1.2.3 抗氧化劑的選擇 取2只150 mL三角瓶,1只裝入一定量黃漿水后,添加25 mg/L EGCG,另1只裝入等量黃漿水和10 g/L殼聚糖,搖勻后沉淀10 min,用濾紙濾除沉淀物后使用。另取1只150 mL 三角瓶裝入等量黃漿水,未添加EGCG和殼聚糖處理,用于空白對照。3只三角瓶中溶液的pH值均為5,甲基橙質量濃度均為8 mg/L。在不同的反應時間點于469 nm波長處測定吸光度并計算脫色率。
1.2.4 供氧條件 分別取2只50 mL具玻璃塞磨口試管和2只150 mL三角瓶,均裝入一定量黃漿水,甲基橙質量濃度為8 mg/L。2只試管均裝滿黃漿水至管口,其中1只試管敞口,另1只加塞密封,2只試管均靜置于35 ℃恒溫培養箱內;2只150 mL的三角瓶,1只于恒溫培養箱敞口靜置,另1只敞口置于35 ℃恒溫搖床中,在轉速為120 r/min條件下振蕩,然后在不同的反應時間點于469 nm波長處測定吸光度并計算脫色率。
1.2.5 黃漿水靜置時間的選擇 在30 ℃下,分別將新制備的黃漿水敞口靜置0、12、24、36 h,取靜置后的黃漿水50 mL分別裝入150 mL三角瓶中,調pH值為5,添加甲基橙質量使其濃度為8 mg/L。混勻后,靜置于35 ℃恒溫培養箱中,在不同的反應時間點于469 nm波長處測定吸光度并計算脫色率。
1.2.6 草酸銨條件 取4只150 mL三角瓶,其中1只裝入50 mL去離子水和0.1 g草酸銨,另外3只均加入50 mL黃漿水。在3只裝有50 mL黃漿水的三角瓶中,其中1只添加0.1 g草酸銨,1只添加0.05 g的納米二氧化鈦,剩余1只做空白對照。4只三角瓶中的溶液pH值均為5,甲基橙質量濃度均為8 mg/L。將4只三角瓶均置于溫度為35 ℃、光照度為30000 lx的光照培養箱中,在不同的反應時間點于469 nm波長處測定吸光度并計算脫色率。
1.2.7 濕豆渣用量的選擇 取6只150 mL三角瓶,向每只三角瓶中加入50 mL黃漿水,然后分別添加0、1、2、4、6、8 g/L濕豆渣,調節pH值為5,甲基橙質量濃度為8 mg/L。混勻后,置于35 ℃恒溫培養箱中,在不同的反應時間點于469 nm波長處測定吸光度并計算脫色率。
1.2.8 初始pH值的選擇 取5只150 mL三角瓶分別裝入50 mL黃漿水,分別調pH值為3、4、5、6、7,在不同的反應時間點于469 nm波長處測定吸光度并計算脫色率。
1.2.9 溫度的選擇 取4只150 mL三角瓶分別裝入50 mL黃漿水,調pH值為5,甲基橙質量濃度均為8 mg/L。混勻后,分別將4只三角瓶置于25、30、35、40 ℃恒溫培養箱中,在不同的反應時間點于469 nm 波長處測定吸光度并計算脫色率。
1.2.10 動力學方程的擬合 將反應液在469 nm處的吸光度與反應時間按照反應動力學進行線性擬合,考察不同條件下的動力學關系,降解反應若屬一級反應,則速率方程如下:
dCtdt=kCt。(1)
等式兩邊積分,可得如下動力學方程:
-lnCtC0=kt+A。(2)
降解反應若屬二級反應,則速率方程如下:
-dCtdt=kC2t。(3)
對該方程進行積分后得如下動力學方程:
1Ct-1C0=kt。(4)
降解反應若屬零級反應,則動力學方程如下:
C0-Ct=kt。(5)
式中:t為甲基橙降解脫色的反應時間,min;Ct為t時刻黃漿水中的甲基橙質量濃度,mg/L;C0為黃漿水中甲基橙的初始質量濃度,mg/L;k為反應速率常數,min-1。
1.2.11 試驗數據分析方法 用Excel 2018進行數據統計和相關性分析,正交試驗采用L9(34)設計,正交試驗數據采用SPSS 17.0運用鄧肯氏法(Duncans)進行方差分析。
2 結果與分析
2.1 抗氧化劑對甲基橙脫色率的影響
如圖1所示,添加EGCG及殼聚糖沉淀處理對甲基橙脫色的影響較為明顯,加入EGCG及殼聚糖沉淀后20 h內,脫色率極低。EGCG為茶多酚類抗氧化劑,具有穩定脂質氫過氧化物和消除游離自由基的能力[17]。另外,茶多酚對LOX活性也有明顯的抑制作用,茶多酚的強還原性使得LOX的活性態Fe3+變為非活性態Fe2+,從而使酶活性喪失[18]。殼聚糖沉淀后的過濾液也未能對甲基橙實現有效的脫色,可能原因是殼聚糖的大分子鏈上分布著許多羥基、氨基及一些N-乙酰氨基等基團,能提供大量H+,具有較強的還原力以及清除自由基和抗脂質氧化的能力[19],從而阻礙了脂質氫過氧化物的氧化作用。EGCG及殼聚糖的加入抑制了黃漿水對甲基橙的脫色作用,由此可見,黃漿水中對甲基橙起降解作用的成分主要是酶促脂肪酸氧化產生的脂質氫過氧化物、自由基等產物。
2.2 供氧對甲基橙脫色率的影響
如圖2所示,具塞密封試管中的甲基橙脫色率最高,其次是無塞試管中的甲基橙,脫色率較高,并且實際觀察發現,下層甲基橙比上層甲基橙脫色快,管口處脫色最慢;而敞口三角瓶中的甲基橙脫
色率比敞口試管、密封試管中低。搖床上1個敞口三角瓶中的甲基橙脫色不明顯。盡管LOX催化多不飽和脂肪酸生成脂質氫過氧化物、自由基的反應通常在需氧條件下進行,但是甲基橙脫色反應在低氧或缺氧狀態下比在富氧狀態下快。有研究發現,在缺氧情況下,LOX也有活性,可以催化從脂肪酸中提取氫自由基的反應,這個提取出的脂肪酸自由基可接著啟動進一步的自由基反應[20]。
2.3 新制備黃漿水靜置時間對甲基橙脫色率的影響
在30 ℃下,分別將新制備的黃漿水敞口放置12、24、36 h,研究不同放置時間的黃漿水對甲基橙降解脫色的影響。如圖3所示,新制備的黃漿水對甲基橙的脫色較慢,放置時間越長,甲基橙完全脫
色所用時間越短,主要是由于經過高溫處理后,新制備的黃漿水中脂質氫過氧化物、自由基等活性成分較少,放置一定時間后,經過殘存的少量LOX促氧化,產生的脂質氫過氧化物、自由基等成分增加,使甲基橙脫色進程相應加快。考慮到時間成本及黃漿水變質等因素,本試驗中黃漿水的靜置時間選擇24 h。
2.4 草酸銨對甲基橙脫色率的影響
如圖4所示,單一的草酸銨水溶液對甲基橙的脫色并無明顯效果,但當在黃漿水中加入少量草酸銨時,在光照條件下明顯加快了黃漿水對甲基橙的脫色進程,優于單一的黃漿水處理,也優于在黃漿水中加入少量光催化劑納米二氧化鈦處理。草酸銨加快甲基橙脫色的原因可能是草酸根離子能與廢水中游離狀態的、蛋白質結合狀態的Fe3+形成草酸鐵配合物,草酸鐵是應用于光催化反應的一類光催化劑,在光催化下發生“富氧化點”的類Fenton反應[22],生成強氧化性自由基·OH,進而氧化甲基橙。已有研究發現,草酸鐵對部分450~500 nm的可見光也有少量吸收,并發生光化學反應,產生·OH[23]。
2.5 濕豆渣用量對甲基橙脫色率的影響
如圖5所示,濕豆渣的用量對甲基橙脫色有明顯影響,當濕豆渣用量為0~6 g/L時,添加量越大,甲基橙脫色越快;當濕豆渣用量增至8 g/L時,脫色
反應速率不再提高,可能是由于濕豆渣中含有一定的LOX[24],其添加量越大,酶促氧化反應產生的初級氧化活性成分越多,協同氧化甲基橙脫色反應就會同步加快[25]。
進一步考察濕豆渣用量與甲基橙脫色反應的動力學關系。由圖6、表1看出,ln(Ct/C0)與t之間呈現良好的線性關系,脫色反應符合準一級動力學關系。濕豆渣用量為2、4、6 g/L時擬合的一級動力學方程分別為ln(Ct/C0)=-0.013 1t+0.156 4、ln(Ct/C0)=-0.018 1t+0.038 7、ln(Ct/C0)=-0.022 4t-0.234。由此可見,在一定范圍內,濕豆渣的添加量越高,其反應速率常數(k)越大,脫色反應越快。
2.6 初始pH值對甲基橙脫色率的影響
如圖7所示,不同黃漿水初始pH值對甲基橙脫色反應的影響較明顯。當黃漿水初始pH值為5時,甲基橙脫色最快;其次是黃漿水初始pH值為6時的脫色速率;當黃漿水初始pH值為7時,脫色較慢;當黃漿水初始pH值為3時,脫色效果最差。pH值為4以下時,H+質量濃度較高,脂質氫過氧化物、自由基的穩定性較差;而堿性較強時,自由基的分解速度加快[26],從而限制了甲基橙的進一步降解。
另外,試驗還發現,24 h后黃漿水初始pH值為5的反應液無異味,再放置2 d仍未變質,表明混合液pH值為5時,既可保證降解脫色效果,又能保證合適的酸性環境,有利于防腐;黃漿水初始pH值為7的反應液在放置2 d后出現異味,容易腐敗變質。
進一步考察動力學關系發現,在不同pH值下,ln(Ct/C0)與t之間呈良好的線性關系,甲基橙的脫色反應符合準一級動力學關系。黃漿水初始pH值為4、5、6時,擬合的動力學方程分別為ln(Ct/C0)=-0.001 4t-0.124 7、ln(Ct/C0)=-0.019 7t+0.321 9、ln(Ct/C0)=-0.008t+0.321 9。從反應速率來看,黃漿水初始pH值為5時,反應速率常數最大,達到0.019 7 min-1(圖8、表2)。
2.7 溫度對甲基橙脫色率的影響
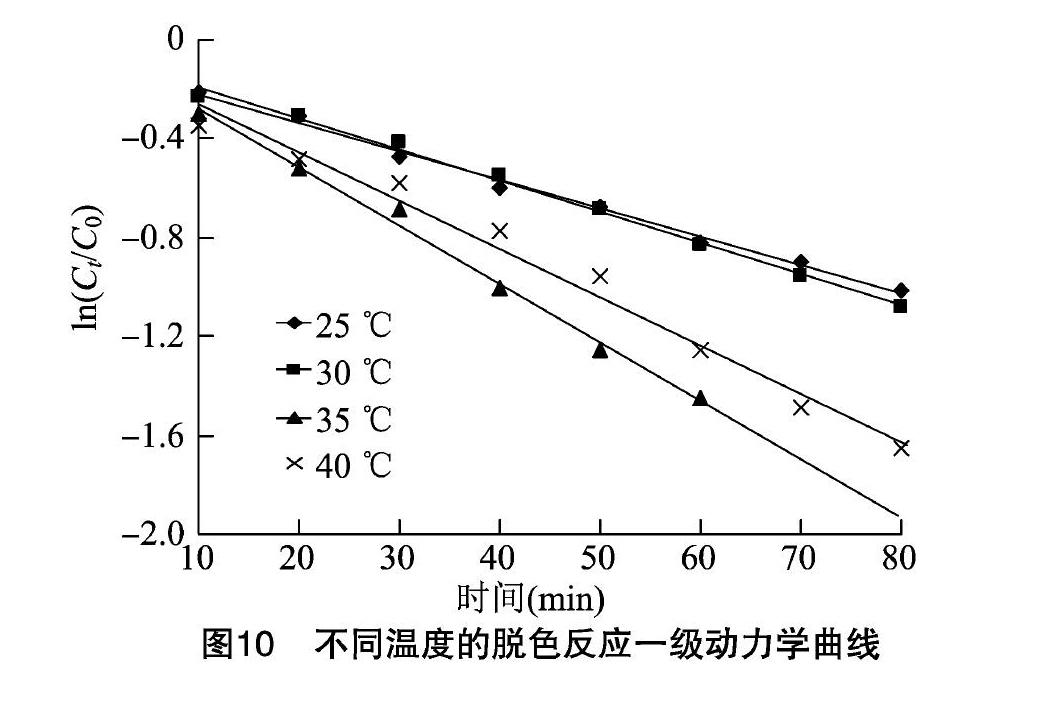
如圖9所示,溫度為35 ℃左右甲基橙脫色最快;溫度在35 ℃以下時,隨著反應溫度的提高,反應體系中甲基橙分子擴散速率加快,脫色反應相應加快;當溫度達到40 ℃時,前期甲基橙出現明顯脫色,后期脫色較慢。由此可見,反應溫度最好控制在35 ℃ 左右。
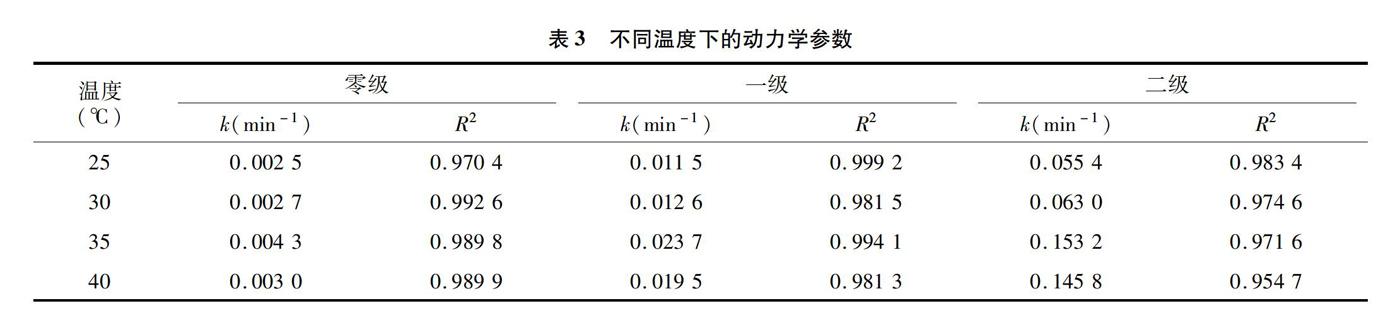
進一步考察動力學關系發現,ln(Ct/C0)與反應時間t之間呈良好的線性關系,甲基橙脫色反應符合準一級動力學關系,在溫度為25、30、35、40 ℃條件下,一級動力學方程分別為ln(Ct/C0)=-0.011 5t-0.106 4、ln(Ct/C0)=-0.126t-0.067 5、ln(Ct/C0)=-0.023 7t-0.042、ln(Ct/C0)=-0.019 5t-0.065。隨著溫度的升高,脫色反應速
率加快,k值逐漸增大,當溫度為35 ℃時,k值達到最大值,為0.023 7 min-1;當溫度為40 ℃時,反應速率開始降低,k值為0.019 5 min-1(圖10、表3)。
進一步經過高溫試驗發現,黃漿水經過微波加熱處理5 min、121 ℃高壓滅菌鍋保溫處理30 min、100 ℃恒溫水浴40 min后均不能使甲基橙脫色, 說明原有黃漿水中存在的脂質氫過氧化物等活性成分在高溫下極不穩定,易分解[27],而且LOX活性在高溫條件下受到嚴重破壞,也在一定程度上影響了甲基橙的降解脫色反應。大量研究發現,多數LOX的最適反應溫度在30~45 ℃之間,活性在低溫下能保持較高水平,溫度高于40 ℃后,活性急劇下降[28]。
2.8 正交試驗及方差分析
在單因素試驗的基礎上,分別以3個水平的溫度、pH值和濕豆渣用量設計正交試驗,試驗及方差分析結果見表4、表5。
正交試驗和方差分析結果表明,FD=346.88>FC=220.19>FB=23.89,且P<0.05,即3個因素對甲基橙脫色反應速率均有顯著效應,顯著性效應排序為A>B>C。因此,在甲基橙初始質量濃度為8 mg/L 時的最佳脫色工藝如下:溫度為35 ℃,pH值為5,濕豆渣添加量為6 g/L。
按照最佳工藝條件進行試驗,當溫度為35 ℃、pH值為5、豆渣用量為6 g/L時,經試驗得出甲基橙脫色反應速率為0.021 4 min-1。
3 結論
黃漿水敞口放置一段時間后,會產生較多脂質氫過氧化物和自由基等成分,有利于甲基橙的降解脫色,而甲基橙脫色反應的速度在低氧或缺氧狀態下比在富氧狀態下要快。EGCG和殼聚糖會明顯抑制黃漿水對甲基橙的脫色效果,而添加一定質量濃度的草酸銨后,能加快甲基橙的脫色反應。一定范圍的溫度、pH值和濕豆渣用量有利于甲基橙的脫色反應,并且對甲基橙脫色均有顯著效應,其脫色反應均符合準一級動力學關系。正交試驗和方差分析結果表明,最佳工藝條件為溫度35 ℃、pH值5、濕豆渣添加量6 g/L。
參考文獻:
[1]梁山景,程建萍,陳長琦.功率超聲處理甲基橙廢水的實驗研究[J]. 合肥工業大學學報(自然科學版),2010,33(10):1564-1565.
[2]白春華,徐志永,李光輝,等. 納米TiO2/硅藻土復合材料光催化降解甲基橙的研究[J]. 應用化工,2017,46(4):701-705.
[3]王 潔,王莉瓊,曹江平,等. WO3/BiOBr復合催化劑的制備及可見光催化降解甲基橙[J]. 工業催化,2017,25(11):44-47.
[4]孫廣垠,宋 萌.低溫等離子體技術降解甲基橙染料廢水[J]. 中國給水排水,2016,32(21):96-99.
[5]阿旺次仁,李紅娜,唐哲仁,等. 以一種黏土礦物材料為非均相類芬頓催化劑對甲基橙的降解[J]. 環境科學研究,2017,30(11):1769-1776.
[6]秦聰麗,傅吉全.植物法改性類Fenton反應催化劑降解甲基橙[J]. 化工環保,2016,36(3):312-316.
[7]Cristóvo R O,Tavares A P M,Ribeiro A S,et al. Kinetic modelling and simulation of laccase catalyzed degradation of reactive textile dyes[J]. Bioresource Technology,2008,99 (11):4768-4774.
[8]儲力前,付永彬.膜分離技術在大豆蛋白廢水處理中的應用研究[J]. 給水排水,2000,26(5):36-38.
[9]Sorgentini D A,Wagner J R. Comparative study of structural characteristics and thermal behavior of whey and isolate soybean proteins[J]. Journal of Food Biochemistry,2010,23(5):489-507.
[10]石彥國,任 莉.大豆制品工藝學[M]. 北京:中國輕工業出版社,1998.
[11]Gieseg S,Duggan S,Gebicki J M. Peroxidation of proteins before lipids in U937 cells exposed to peroxyl radicals[J]. Biochemical Journal,2000,350(1):215-218.
[12]于清峰,肖 瑩,倪坤儀,等. 脂氧合酶催化雙高-γ-亞麻酸脂質過氧化產生的碳自由基的結構確證分析化學[J]. 2009,37(12):1815-1819.
[13]胡廷章,胡宗利,屈霄霄,等. 植物脂肪氧化酶的研究進展[J]. 生物工程學報,2009,25(1):1-9.
[14]王丹丹,毛曉英,孫領鴿,等. 氫過氧化物氧化對核桃蛋白結構和乳化特性的影響[J]. 中國食品學報,2019,19(12):60-68.
[15]姜 閃,張志國.大豆乳清廢水提取脂肪氧合酶對面條加工特性的影響[J]. 食品科學,2019,40(14):48-53.
[16]Cato L,Halmos A L,Small D M. Measurement of lipoxygenase in Australian white wheat flour:the effect of lipoxygenase on the quality properties of white salted noodles[J]. Journal of the Science of Food & Agriculture,2010,86(11):1670-1678.
[17]胡秀芳,沈生榮,樸宰日,等. 茶多酚抗氧化機理研究現狀[J]. 茶葉科學,1999,19(2):93-103.
[18]熊衛東,章銀良,馬慶一,等. 脂氧合酶活性抑制劑的篩選及應用保鮮的研究[J]. 食品科技,2004(9):84-87.
[19]劉 歡,夏光輝.殼聚糖及其衍生物抗氧化活性的研究[J]. 食品科技,2015,40(5):274-278.
[20]李興軍.谷物脂氧合酶的生理生化特性[J]. 糧食科技與經濟,2011,36(3):34-37.
[21]田其英,尹貴中,華欲飛.大豆脂肪氧合酶同工酶活性的影響因素研究[J]. 食品工業科技,2008,29(1):156-157
[22]謝銀德,陳 峰,何建軍,等. Photo-Fenton反應研究進展[J]. 感光科學與光化學,2000,18(4):357-365.
[23]張 婷,吳少林,朱振興.Fe(Ⅲ) 草酸鹽絡合物的光化學性質及應用[J]. 江西化工,2008(1):26-29.
[24]秦明仁,石 琳.豆渣制備高纖維添加粉的研究[J]. 廣州食品工業科技,1993(4):39.
[25]王常青,段光明,蘇芝業.豆渣脫色及脫臭方法[J]. 食品科學,1992(9):20-25.
[26]儲金宇,樊 迪.自由基降解甲基橙溶液試驗[J]. 江蘇大學學報(自然科學版),2010,31(4):469-472.
[27]何志平,龐林江.油脂氧化檢測方法研究進展[J]. 安徽農業科學,2010,38(21):11460-11462.
[28]陳書婷,孔祥珍,華欲飛,等. 大豆脂肪氧合酶的分離純化及其性質研究[J]. 食品工業科技,2011,10(5):176-182.

