他克莫司聯合中等劑量糖皮質激素治療特發性膜性腎病的臨床分析
朱愛民,陳秋香,米俠,張策,張馳,周飛紅,王軍升
南京鼓樓醫院集團宿遷市人民醫院腎內科,江蘇宿遷 223800
特發性膜性腎病(IMN)是以腎小球基底膜上皮細胞下免疫復合物沉積伴基底膜增厚為特征性病理改變的一組腎臟疾病,又稱膜性腎小球腎炎,是導致成人原發性腎病綜合征的常見病因,占比約30%~40%[1]。 此病以中老年人多發,男女比約2:1,研究多認為發病與原位免疫復合物形成引起足細胞損傷有關, 但具體病因病機尚未完全闡明。 此病自然病程差異較大,有些患者可自發緩解或維持腎功能穩定,有些則可持續進展,出現腎功能損傷,如未接受治療,約40%的患者10 年內會發展至終末期腎臟病,危及生命[2]。 免疫抑制是臨床治療IMN 重要方法, 但對于臨床表現為腎病綜合征的IMN,有研究指出單一應用免疫抑制劑,誘導緩解及腎功能保護效果欠理想,建議聯合糖皮質激素用藥[3]。 該文方便選取2017 年1 月—2019 年12 月該院收治的47 例IMN 患者,對他克莫司與糖皮質激素聯合治療該病的效果與安全性展開研究,現報道如下。
1 資料與方法
1.1 一般資料
方便選擇該院47 例IMN 患者,隨機分為兩組。 實驗組(25 例):男18 例,女7 例;年齡26~77 歲,平均(53.21±11.60)歲;對照組(22 例):男16 例,女6 例;年齡27~76 歲,平均(52.84±9.72)歲。兩組基線資料相當,差異無統計學意義(P>0.05),具有可比性。納入標準:參照KDIGO 指南,經病史、查體、實驗室、腎穿刺活檢等綜合檢查及鑒別診斷,確診IMN;抗磷脂酶A2 抗體陽性;尿蛋白(PRO)定量>3.5 g/24 h,血清白蛋白(Alb)<30 g/L,或伴水腫、高脂血癥及其他代謝紊亂等,臨床表現為腎病綜合征; 腎小球濾過率 (eGFR)>30 mL/(min·1.73 m2),雙腎體積正常;配合治療及研究,簽署知情同意書。排除標準:各種明確病因的繼發性膜性腎病;近3 個月免疫抑制治療史;合并活動性消化道出血、腫瘤、全身感染等嚴重內科疾病及酶學指標超正常值上限2 倍以上的肝功能異常;免疫抑制劑治療不耐受;臨床資料不全。
1.2 方法
兩組均接受內科常規治療,包括臥床休息、低蛋白飲食、低鹽飲食、控制血壓、利尿消腫、降脂治療等,在此基礎上接受免疫治療。對照組單純用藥他克莫司膠囊(國藥準字H20084514),初始劑量0.05 mg/(kg·d),2 次/d,以后調整劑量至1~3 mg,2 次/d,維持血藥濃度5~10 ng/L。實驗組他克莫司用藥與對照組一致, 在此基礎上加用中等劑量糖皮質激素, 用藥醋酸潑尼松片 (國藥準字H33021207)30~40 mg 或 甲 潑 尼 龍 片 (批 準 文 號H20150245)24~32 mg,1 次/d, 以后逐漸減量至維持劑量,療程6 個月。
1.3 觀察指標與評價標準
測定兩組治療前后相關實驗室指標, 包括血清白蛋白(Alb)、24 h 尿蛋白定量(Upro)、血肌酐(Scr)、總膽固醇(TC)、甘油三酯(TG),評價兩組療效。 療效評價參照文獻擬定[4]:水腫、代謝紊亂等IMN 與腎病綜合征癥狀體征消失,24 h Upro 定量<0.3 g/24 h,Alb≥35 g/L,Scr 恢復正常—臨床治愈;水腫、代謝紊亂等IMN 與腎病綜合征癥狀體征顯著改善,24 h Upro 定量較基礎值(治療前) 下降>70%,Alb≥30 g/L,Scr 正常—顯效;水腫、代謝紊亂等IMN 與腎病綜合征癥狀體征好轉,24 h Upro 定量較基礎值下降40%~69%,Alb≥30 g/L,Scr 穩定—有效;水腫、代謝紊亂等IMN 與腎病綜合征癥狀體征及實驗室指標無改善甚或加重—無效。
另于治療前及治療達到終點時, 采集實驗組患者靜脈血樣,分離血清,以酶聯免疫吸附法測定抗磷脂酶A2 受體 (PLA2R) 抗體, 依據試劑盒說明書, 以抗PLA2R 抗體≥20 RU/mL 為陽性,比較觀察不同療效患者的指標差異。
1.4 統計方法
以SPSS 21.0 統計學軟件統計分析數據,計量資料以()表示,行t 檢驗;計數資料以頻數和百分比(%)表示,行χ2檢驗,P<0.05 為差異有統計學意義。
2 結果
2.1 臨床療效
兩組治療前實驗室指標Alb、24 h Upro、Scr、TC、TG,差異無統計學意義(P>0.05)。 實驗組治療后Alb 高于對照組,24 h Upro、TC、TG 低于對照組, 差異有統計學意義(P<0.05),見表1。 基于評價標準,實驗組治療總有效率84.00%高于對照組63.64%,差異有統計學意義(P<0.05),見表2。
表1 兩組患者治療前后實驗室指標比較()
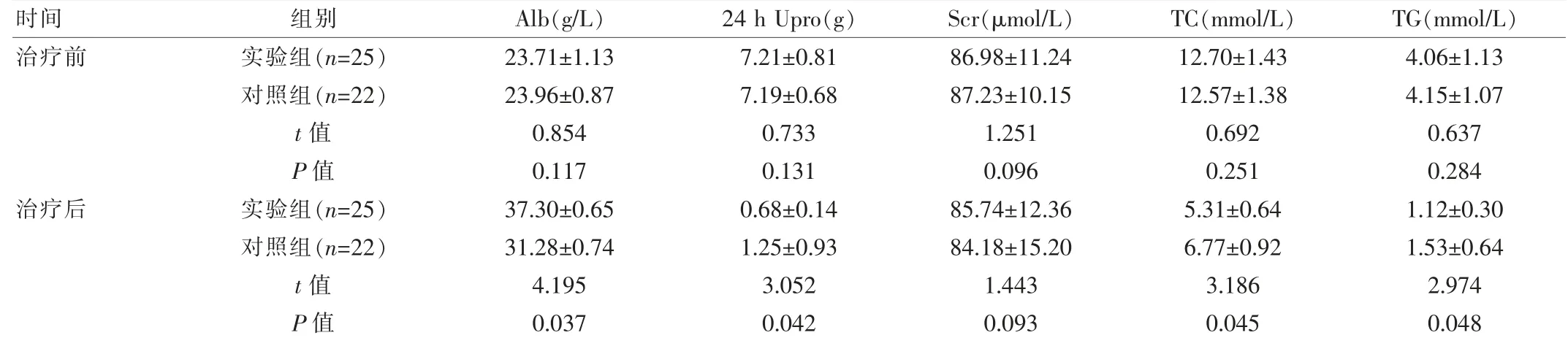
表1 兩組患者治療前后實驗室指標比較()
時間治療前治療后組別實驗組(n=25)對照組(n=22)t 值P 值實驗組(n=25)對照組(n=22)t 值P 值Alb(g/L)24 h Upro(g)Scr(μmol/L)23.71±1.13 23.96±0.87 0.854 0.117 37.30±0.65 31.28±0.74 4.195 0.037 7.21±0.81 7.19±0.68 0.733 0.131 0.68±0.14 1.25±0.93 3.052 0.042 86.98±11.24 87.23±10.15 1.251 0.096 85.74±12.36 84.18±15.20 1.443 0.093 TC(mmol/L) TG(mmol/L)12.70±1.43 12.57±1.38 0.692 0.251 5.31±0.64 6.77±0.92 3.186 0.045 4.06±1.13 4.15±1.07 0.637 0.284 1.12±0.30 1.53±0.64 2.974 0.048
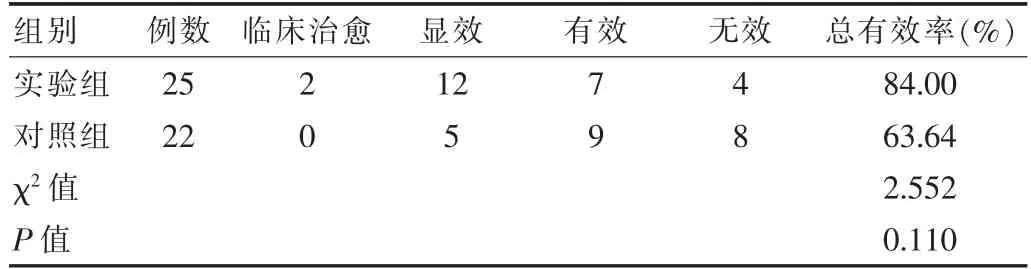
表2 兩組患者療效比較
2.2 實驗組PLA2R 抗體水平
治療前, 實驗組不同療效患者抗PLA2R 抗體水平相當,差異無統計學意義(P>0.05)。治療后,治療有效病例平均抗體水平亦顯著低于治療無效病例, 差異有統計學意義(P<0.05),見表3。 治療后實驗組治療有效病例19 例, 有4 例患者抗PLA2R 抗體轉陰, 轉陰率21.05%,治療無效病例6 例,患者抗PLA2R 抗體均未轉陰,轉陰率0.00%,組間對比,差異有統計學意義(t=5.819,P=0.026)。
表3 實驗組不同療效患者治療前后抗PLA2R 抗體水平比較[(),RU/mL]
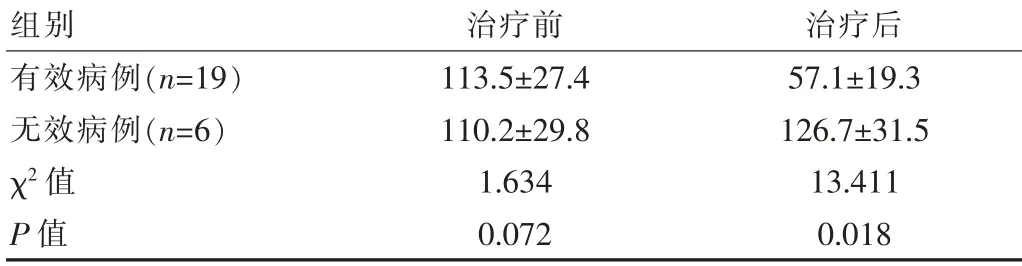
表3 實驗組不同療效患者治療前后抗PLA2R 抗體水平比較[(),RU/mL]
組別治療前 治療后有效病例(n=19)無效病例(n=6)χ2 值P 值113.5±27.4 110.2±29.8 1.634 0.072 57.1±19.3 126.7±31.5 13.411 0.018
3 討論
近年,隨著細胞分子生物學技術的應用與發展,臨床對IMN 病因病機的認識取得巨大進展。 目前已有諸多研究證實,IMN 的發生與進展同原位免疫復合物形成有關,主要靶抗原是足細胞表面的M 型磷脂酶A2 受體,其滴度與患者Upro 存在相關性[5]。 另有報道指出,抗磷脂酶A2 受體抗體與足細胞相應抗原結合,會形成損傷足細胞的C5b-9 膜攻擊復合物, 破壞腎小球濾過屏障,引起尿蛋白[6]。
對于尿蛋白過高或已經出現腎功能衰竭的磷酯酶A2 抗體陽性IMN 患者,免疫治療是控制病情的重要方法,但對于具體方案的使用和治療時機的把握,臨床存在諸多爭議[7]。 根據KDIGO 指南,以腎病綜合征為主要臨床表現,經降尿蛋白治療至少6 個月,24 h Upro 仍無下降趨勢, 持續高于4 g 或維持基線水平50%以上的IMN 患者, 以及存在嚴重致殘甚至危及生命的腎病綜合征相關臨床癥狀的IMN 患者, 應考慮進行免疫抑制治療[8]。
糖皮質激素是既往治療IMN 常用藥物, 但近年研究發現,其單一用藥在降低尿蛋白、提高腎臟功能方面均無明顯效果,加大療程或劑量可能提高緩解率,但不良反應嚴重,治療不可行,KDIGO 臨床指南亦不推薦此藥單藥治療, 臨床主要采取糖皮質激素聯合免疫抑制劑的方案[9]。 他克莫司屬大環內酯類抗生素,是一種強效免疫抑制劑,具有高度活性,既往主要用于器官移植后抗排異反應,能在分子水平與細胞性蛋白質FKBP12結合成復合物,可以通過抑制鈣調磷酸酶、干擾鈣依賴性信號傳導通路,來抑制白介素-2、γ-干擾素等淋巴因子的生成與受體表達, 進而全面抑制T 淋巴細胞增生活化,其活性在體內外實驗中均已獲得證實,作用機制同環孢素A 相似,但免疫抑制效果更強[10]。 此藥治療IMN的效果近年也在臨床得到證實, 有研究指出其短期療效優于環磷酰胺,可以幫助患者更早獲得緩解。 該研究以中等劑量糖皮質激素聯合他克莫司治療有明顯腎病綜合征的磷酯酶A2 抗體陽性IMN 患者,結果顯示患者24 h Upro 水平更低,治療總有效率84.00%明顯高于對照組他克莫司單一用藥有效率63.64%, 與文獻報道[11]兩者聯用治療IMN 有效率72.5%相當, 肯定了兩者聯合治療的有效性與安全性。
PLA2R 抗體會特異性結合腎小球磷脂酶A2 受體抗原,形成原位免疫復合物,激活補體導體,引起細胞損傷。 有數據顯示,約有70%的特發性模型腎病患者血清M 型磷脂酶A2 受體自身抗體呈陽性,是臨床診斷此病的重要實驗室指標。 另有研究發現,特發性膜性腎病患者抗PLA2R 抗體滴度減低與疾病緩解、 尿蛋白減少存在相關性,故可作為監測療效、評估轉歸的標志物[12]。該研究比較觀察實驗組用藥后不同療效患者的抗PLA2R 抗體, 結果示有效病例血清抗體水平明顯低于無效病例,其中4 例患者轉陰,提示抗PLA2R 抗體水平與特發性膜性腎病免疫治療效果存在相關性, 既可評估疾病轉歸,亦能用于指導免疫治療時機。
綜上所述, 他克莫司聯合中等劑量糖皮質激素治療特發性膜性腎病效果優于他克莫司單純用藥, 監測血清抗磷脂酶A2 受體水平能夠為療效評估提供依據參考。

