醇氨法六水氯化鎂制備無水氯化鎂的工藝研究
劉存瑞,喬秀文
(1.蘇州衛生職業技術學院,江蘇 蘇州 215009;2.石河子大學 化學化工學院,新疆 石河子 832000)
0 引言
無水氯化鎂在我國的許多領域具有廣泛用途,如冶金、化工、建筑、食品、醫藥等領域都有很好的體現。目前,國內外文獻報道用六水氯化鎂生產無水氯化鎂的工藝主要有Dow 工藝[1]、Farben 工藝、Magnola 工藝、反應結晶藕合法脫水技術等。新疆是我國面積最大的干旱、半干旱鹽湖分布區,包括鹵水湖和干鹽湖共112 個鹽湖,面積10 789 km2,可劃分為5 個鹽湖分布區:準噶爾界山- 阿爾泰山山間盆地鹽湖區、準噶爾盆地鹽湖區、天山山間盆地鹽湖區、塔里木盆地鹽湖區、昆侖山- 阿爾金山山間盆地鹽湖區[2]。鹽湖自然資源豐富,不僅有鹽類沉積資源、鹵水資源,也有鹽湖生物資源和旅游資源。其中,鹽類沉積資源和鹵水資源,是我國鹽湖的主要自然資源。近年來,我國加大了無水氯化鎂方面的研究。據有關資料報道,中科院青海鹽湖研究所就在此領域取得了新的進展:通過控制脫水進程的非平衡態熱力學和動力學條件,有效抑制了低水合氯化鎂的水解;解決了水氯鎂石流態化脫水設備的耐高溫、耐腐蝕和密封性三大難題;制得的產品完全滿足鎂電解工業對原料的質量要求。新工藝與國內外煉鎂工藝相比,具有無水氯化鎂產品制造成本低、質量高、能耗低等優點[3]。
利用醇氨法將鹽湖廢棄物中大量的六水氯化鎂來制備無水氯化鎂,成本低、毒性小,使生產工藝變為綠色工藝,生產過程幾乎無腐蝕、無三廢排放,操作過程中無需用氯氣等有毒有害氣體,減小環境污染。
試驗應用2 種制備無水氯化鎂的方法進行比較,六水氯化鎂用微波法脫水制備無水氯化鎂,脫水率隨著微波功率增大而升高,但是水解程度較大,無水氯化鎂的質量不高。醇氨法主要是將六水氯化鎂的甲醇溶液進行氨氣合成氨合氯化鎂,再進行焙燒制備高質量的無水氯化鎂的方法,此方法產量較高、質量較好。
1 儀器與試劑
1.1 儀器
海爾微波爐,青島海爾微波制品有限公司產品;X 射線衍射儀,德國布魯克公司產品;電子天平,常熟市百靈天平儀器有限公司產品;強力電動攪拌器,江蘇榮華儀器制造公司產品;真空管式高溫爐,合肥科晶材料技術有限公司產品;電熱恒溫鼓風干燥箱,上海精宏實驗設備有限公司產品。
1.2 試劑
六水氯化鎂,天津市盛奧化學試劑有限公司提供;甲醇,天津市富宇精細化工有限公司提供;氯化銨,天津市盛奧化學試劑有限公司提供;氫氧化鈉,天津市福晨化學試劑廠提供;乙二胺四乙酸二鈉,天津市巴斯夫化工有限公司提供;無水硫酸鈉,北京化學試劑三廠提供;硝酸,廣東汕頭市西隴化工廠提供。
2 試驗方法
2.1 六水氯化鎂微波加熱脫水
2.1.1 六水氯化鎂微波加熱脫水率的研究
取2.03 g 六水氯化鎂放入微波爐中加熱,研究功率分別為低火、中低火、中火,時間為210,240 s時,六水氯化鎂的脫水率。
2.1.2 六水氯化鎂微波加熱水解程度的研究
(1) 鎂含量的測定。取稀釋后的20.00 mL 待滴定溶液于錐形瓶中,加入1∶1 的氨水- 氯化銨溶液20 mL,2~3 滴鉻黑T,搖勻后,用標準EDTA 溶液滴定,溶液由酒紅色變為純藍色即為終點,對平行分析的結果取平均值。
(2) 氯含量的測定。①取標定好的AgNO3溶液50.00 mL,然后加水稀釋配成500 mL 的AgNO3溶液,C(AgNO3)= 0.009 600 mol/L。②取待測溶液25.00 mL 置于錐形瓶中,加入25 mL 蒸餾水,1 mL 5% K2CrO4溶液,在不斷搖動下用標準AgNO3溶液滴定,溶液由黃色至磚紅色即為終點。
2.2 六水氯化鎂制備無水氯化鎂的單因素試驗
2.2.1 研究不同濃度下對產物影響
分別取一定量的六水氯化鎂,配成不同濃度的甲醇溶液,分別為0.1,0.2,0.3,0.4,0.5 mol/L,將溶解后的六水氯化鎂的甲醇溶液放入三口燒瓶中,控制通入氨氣流速相同,時間相同(t=30 min)。甲醇中n(MgCl2·6H2O)∶n(NH4Cl)= 1∶6。
2.2.2 研究不同溫度下對產物影響
分別取質量相同的六水氯化鎂,配成相同濃度的甲醇溶液(濃度0.3 mol/L),將溶解后的六水氯化鎂的甲醇溶液放入三口燒瓶中,控制通入氨氣,流速相同,時間相同(t=30 min) 分別在不同溫度下反應(0,10,20,30,40 ℃)。甲醇中mNH4Cl=1.604 7 g,mMgCl2·6H2O=6.099 0 g;甲醇中n(MgCl2·6H2O)∶n(NH4Cl)= 1∶6。
2.2.3 研究氨氣的不同流量下對產物影響
分別取質量相同的六水氯化鎂,配成相同濃度的甲醇溶液(濃度0.3 mol/L),將溶解后的六水氯化鎂的甲醇溶液放入三口燒瓶中,控制通入氨氣流速不相同,時間相同(t=30 min)、溫度相同(θ=20 ℃),分別在不同氨氣的流量下反應(60,70,80,90,100 mL/min)。甲醇中mNH4Cl=1.604 7 g,mMgCl2·6H2O=6.099 0 g;甲醇中n(MgCl2·6H2O)∶n(NH4Cl)=1∶6。
2.3 六水氯化鎂制備無水氯化鎂的正交試驗
在單因素試驗的基礎上,為了確定氨合氯化鎂產率最佳條件,對濃度、溫度、氨氣流量3 個因素進行正交試驗。
正交試驗因素與水平設計見表1。

表1 正交試驗因素與水平設計
3 結果與分析
3.1 微波加熱對六水氯化鎂脫水率的影響及水解程度的影響
3.1.1 微波加熱對六水氯化鎂脫水率的影響
微波加熱的不同功率下對六水氯化鎂脫水率的影響結果見表2。
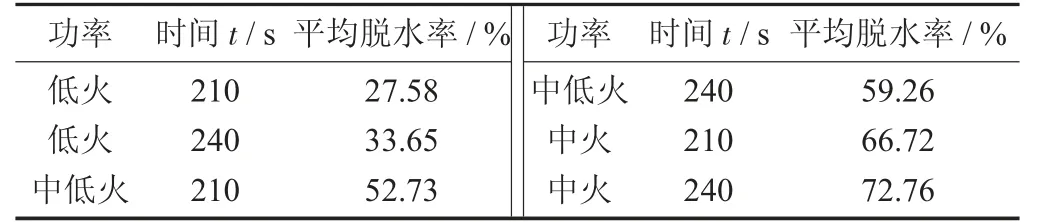
表2 微波加熱的不同功率下對六水氯化鎂脫水率的影響結果
由表2 可知,由于微波加熱功率的增大,加熱時間增加,六水氯化鎂的脫水率也逐漸增大。六水化合物和四水化合物脫水較易,水解反應的干擾不大[4]。隨著微波功率的增大、反應時間的增加,脫水率也逐漸增大。
3.1.2 微波加熱對六水氯化鎂水解程度的影響結果
t=210 s 微波加熱的不同功率對六水氯化鎂水解程度的影響結果見表3,t=240 s 微波加熱的不同功率對六水氯化鎂水解程度的影響結果見表4。
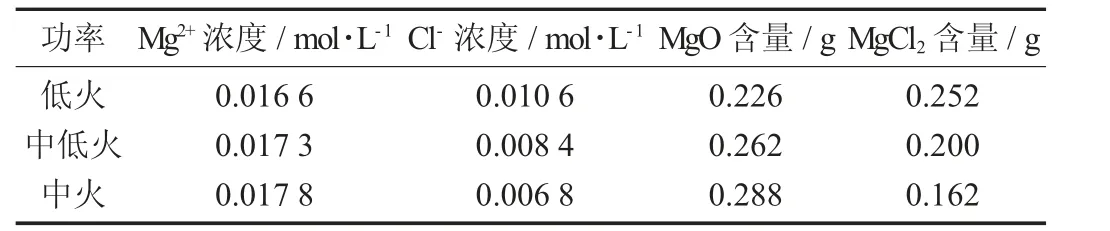
表3 t=210 s 微波加熱的不同功率對六水氯化鎂水解程度的影響結果
由表3 和表4 可知,當時間相同時,隨著功率的增加,氧化鎂的含量增加,氯化鎂的含量減少。原因:微波的另一特點是加熱點可聚集一處[5]。導致微波加熱時,六水氯化鎂受熱不均,局部溫度過高,當溫度過高時,加熱時間六水氯化鎂容易水解成堿式氯化鎂和氧化鎂等,溫度越高水解程度越大,氧化鎂的含量越多,得不到所需要的低水氯化鎂。
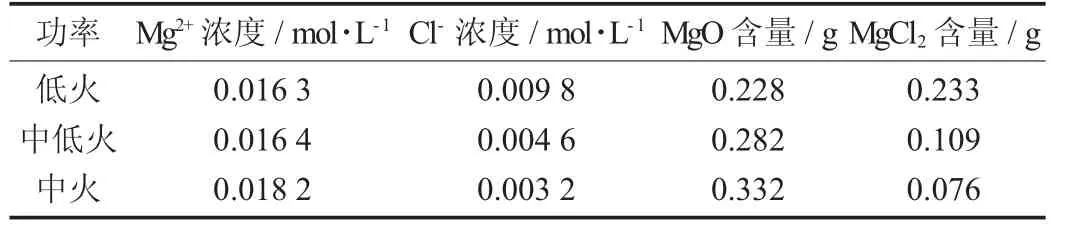
表4 t=240 s 微波加熱的不同功率對六水氯化鎂水解程度的影響結果
3.2 直接通氨氣制取氨和氯化鎂的研究結果
3.2.1 研究不同濃度下對產物影響
不同濃度下對產物影響的研究結果見表5。
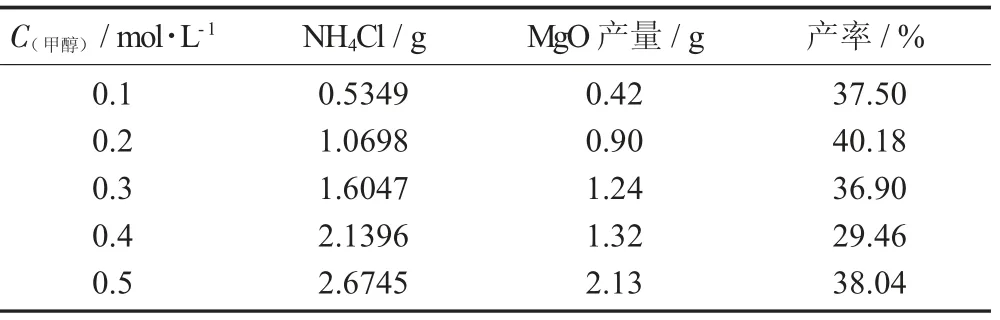
表5 不同濃度下對產物影響的研究結果
由表5 可知,在濃度為0.2 mol/L 左右,氨和氯化鎂的產量較高。
3.2.2 研究不同溫度下對產物影響
不同溫度下對產物影響的研究結果見表6。
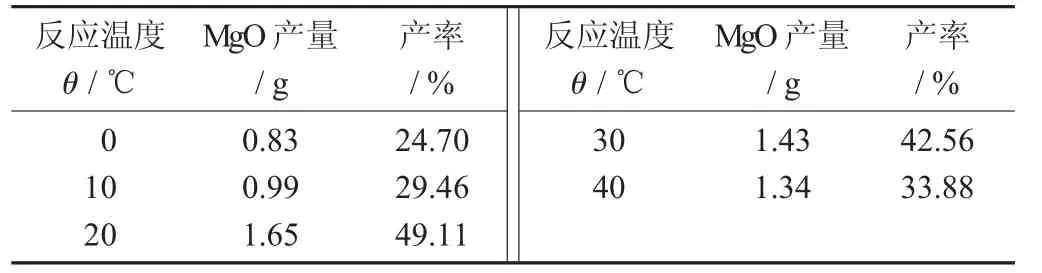
表6 不同溫度下對產物影響的研究結果
由表6 可知,在溫度為20 ℃附近,氨和氯化鎂的產量較高。
3.2.3 研究氨氣的不同流量下對產物影響
氨氣的不同流量下對產物影響的研究結果見表7。
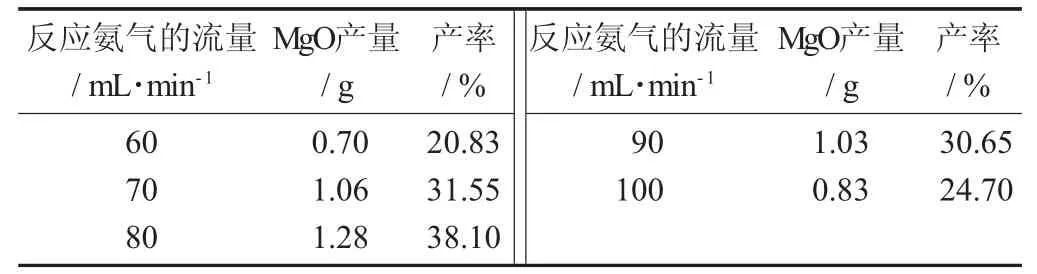
表7 氨氣的不同流量下對產物影響的研究結果
由表7 可知,在流量為80 ml/min 附近氨和氯化鎂的產量較高。
3.2.4 選取溫度、濃度、氨氣流量最佳條件下做正交試驗
溫度、濃度、氨氣流量最佳條件下做正交試驗結果見表8。

表8 溫度、濃度、氨氣流量最佳條件下做正交試驗結果
由表8 可知,影響氨和氯化鎂產率的最主要因素是甲醇溶液的濃度,其次是氨氣的流量,反應溫度影響最小。
4 結論
綜合考慮上述因素,要得到較高的氨和氯化鎂的產率,節省原料和能量,最佳制備方案為甲醇溶液濃度0.3 mol/L,反應溫度10 ℃,氨氣流量90 mL/min,得到的氨合氯化鎂產率最大,對這3 個因素來說,濃度的影響最大。通過此工藝制得的氨和氯化鎂經過焙燒后可以得到產率高,質量好的無水氯化鎂。

