腹腔鏡超聲引導下射頻消融治療原發性小肝癌的療效分析
鄭文杰,田 虎
(1.濰坊醫學院臨床醫學系,山東 濰坊,261000;2.山東省千佛山醫院肝膽外科)
原發性肝癌是目前臨床上最常見的惡性腫瘤之一,發病率高,死亡率高,愈合差。肝癌的治療方式種類較多,均可取得較好的治療效果,隨著腹腔鏡技術的不斷發展,腹腔鏡下肝腫瘤射頻消融術得到開展,具有手術時間短、術后康復快、并發癥少等優點,在臨床上得到充分體現。本研究回顧分析2016年1月至2018年6月山東省千佛山醫院完成的24例腹腔鏡超聲引導下肝癌射頻消融術的臨床數據,探討腹腔鏡下射頻消融術治療原發性肝癌的臨床療效。
1 資料與方法
1.1 臨床資料 患者術前均簽署知情同意書。納入標準:(1)術前經影像學檢查確診為原發性肝細胞性肝癌;(2)肝內腫瘤≤2個,腫瘤最大直徑≤3 cm;(3)肝功能為Child A或B級;(4)術前影像學檢查未發現血管侵犯及肝外其他臟器轉移。排除標準:(1)有嚴重黃疸或頑固性腹水;(2)心肺或其他系統嚴重功能障礙,不能耐受手術;(3)有上腹部手術史。24例患者中男18例,女6例;42~77歲,平均(62.3±8.4)歲;慢性乙型病毒性肝炎感染20例,4例無肝炎感染病史;肝功能Child A級22例,B級 2例;腫瘤最大直徑≤3 cm,平均(2.3±0.58)cm。
1.2 手術方法 全身麻醉,腹腔鏡下先確定腫瘤位置及是否發生腹腔內轉移,充分顯露腫瘤并游離腫瘤周圍韌帶。先在腹腔鏡超聲下確定腫瘤大小與位置,然后在腹腔鏡超聲探頭引導下布針,根據腫瘤大小同時布入1~3根射頻針,完全覆蓋腫瘤。布針完畢開始進行射頻消融治療,消融過程中腹腔鏡超聲觀察射頻消融效果,一般消融10~20 min,總體上消融范圍要求完全覆蓋腫瘤并超出腫塊邊緣1 cm以上,以徹底消除病灶。消融完成后即時行腹腔鏡下超聲檢查,觀察腫瘤消融的范圍是否滿足條件,如有殘留或可疑殘留再次消融,直至腫瘤完全清除。消融完畢后退針,每次退針均邊退針邊消融, 防止出血及針道腫瘤種植轉移。手術步驟見圖1~圖3。

圖1 腹腔鏡超聲下確定腫瘤大小及位置(黑色箭頭為腫 圖2 腹腔鏡超聲引導下進行消融(黃色箭頭為腫瘤) 瘤)
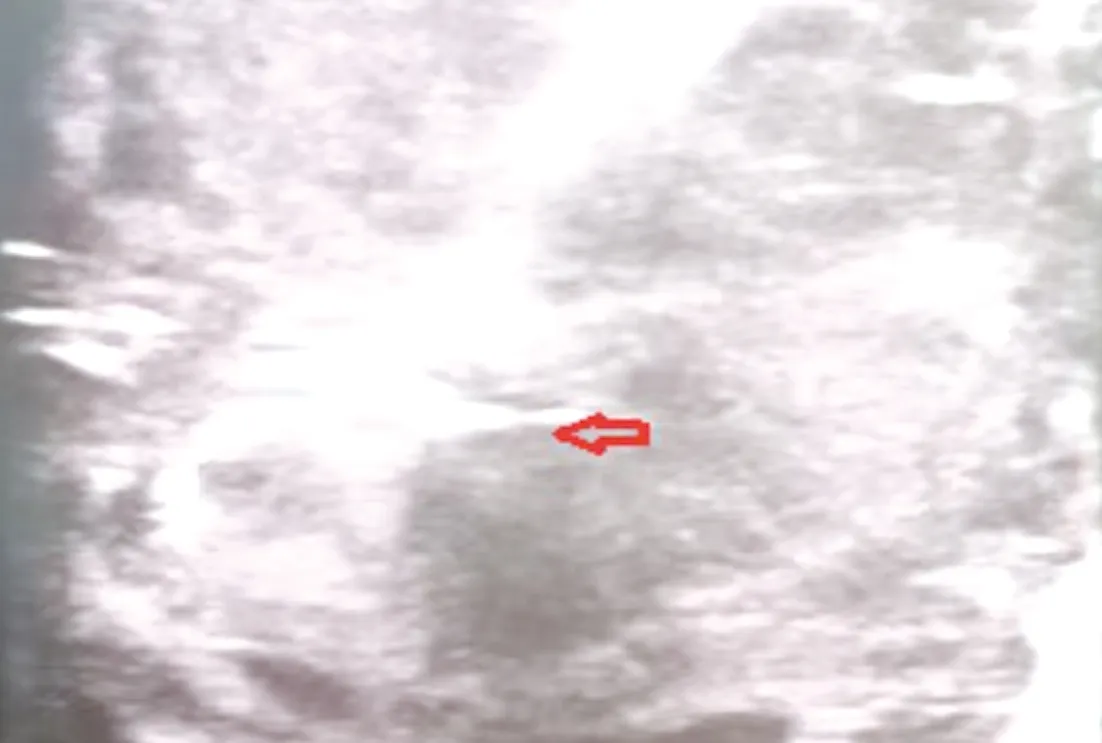
圖3 腹腔鏡超聲引導下腫瘤射頻消融圖 (紅色箭頭 為腫瘤病灶)
1.3 觀察指標及術后隨訪 (1)術前及術后第1天肝功能變化;(2)手術時間、消融時間;(3)術中出血量;(4)術后住院時間;(5)嚴重并發癥發生率;(6)甲胎蛋白(alpha fetal protein,AFP)下降率、瘤體完全消融率;術后1個月復查AFP及腹部增強CT或MRI,確定腫瘤是否完全清除及AFP下降情況;(7)術后患者總生存率與無瘤生存率;術后均定期隨訪,術后第1年每3個月復查1次腹部增強CT或MRI及血AFP,術后第2年、第3年每半年復查1次腹部增強CT或MRI及血AFP。
2 結 果
2.1 術中指標及術后情況 患者均順利完成手術,無中轉開腹,手術時間平均(156.8±58.1)min,其中消融時間(22.3±7.8)min,12例患者因合并膽囊結石或膽囊炎行腹腔鏡膽囊切除術;術中出血量平均(5.3±1.4)mL;患者術后1個月AFP[(25.4±6.2)g/L vs.(119.7±104.6)g/L]較術前下降;術后第1天,ALT[(98.6±53.2)U/L vs. (30.6±24.6)U/L]、AST[(154±91.4)U/L vs.(52.5±41.3)U/L]、TBIL[(25.8±13.8)mol/L vs.(22.6±13.4)mol/L]均較術前升高,白蛋白指標[(32.8±3.6)g/L vs.(40.4±4.6)g/L]較術前降低,肝功能各項指標均于術后2周內恢復正常;術后平均住院(10.2±6.5)d。無圍手術期死亡病例,1例患者于術后第5天因牽拉引流管導致腹腔出血,再次行腹腔鏡下止血治療,術后恢復順利,余者均未出現嚴重并發癥。
2.2 術后隨訪情況 患者均獲隨訪,隨訪24~54個月,平均(36.8±6.5)個月,均無失訪。術后1個月復查AFP及腹部增強CT或MRI,確定腫瘤是否完全清除及AFP下降情況,24例患者復查均未見腫瘤局部殘留,瘤體完全消融率為100%;23例患者AFP較術前下降,AFP下降率為95.8%。隨訪期內,10例復發,6例因腫瘤復發死亡;術后6個月、1年、2年總生存率分別為100%、91.7%、75.0%,無瘤生存率分別為83.3%、70.8%、58.3%。
3 討 論
目前對于早期原發性肝癌,肝移植、手術切除、射頻消融等是主要治療方式,均可取得較好的治療效果[1]。雖然肝移植是早期原發性肝癌最理想的治療方式,可將5年生存率增加至75%~92%[2],但由于價格昂貴及供體短缺等原因,僅少部分人能接受移植治療。手術切除是目前肝癌最有效也是應用最廣泛的治療方式,可完整切除病變組織,極大提高遠期生存率[3]。然而,許多肝癌患者由于合并肝硬化及其他并發癥,并不能耐受手術切除。經過近30年的發展,射頻消融已成為肝癌臨床上比較成熟的微創原位治療技術,可最大限度地保留肝組織并預防手術切除后的肝衰竭。尤其腹腔鏡下射頻消融術,由于精準的定位及清晰的手術視野等優勢,在臨床得到越來越多的應用。
對于無法行肝移植及肝切除術的患者,腹腔鏡下肝癌射頻消融術正逐漸成為非常理想的替代治療方式,尤其原發性小肝癌,腹腔鏡射頻消融術的治療效果良好。Na等[4]發現,對于不適合手術切除、經皮射頻消融的原發性小肝癌患者,其3個月、6個月、12個月、24個月總復發率分別為8.1%、14.4%、25%與35.7%;6個月、9個月局部腫瘤進展率分別為4.2%與8.7%。Eun等[5]的研究顯示,與經皮射頻消融術相比,腹腔鏡射頻消融術能更有效地改善原發性肝癌患者總體生存率,降低死亡率,并能更有效地限制肝內轉移復發及邊緣復發。張發鵬等[6]的研究顯示,對于原發性小肝癌,腹腔鏡射頻消融術不僅較經皮射頻消融具有更高的消融率,還具有與手術切除相當的遠期療效,同時具有微創及術后康復快的優點。本文所報道的術后6個月、12個月、24個月總復發率分別為16.7%、29.2%與41.7%,與文獻報道相近。表明腹腔鏡射頻消融術在取得較好治療效果的同時,對患者身體造成的傷害也更小。
Birsen等[7]最近發表的一篇文獻分析了1996~2012年910例共接受1 207次腹腔鏡射頻消融術治療惡性肝腫瘤患者的資料。他們發現,腹腔鏡射頻消融術后90 d并發癥發生率為4%(n=50),死亡率為0.4%(n=5)。術后并發癥主要包括胃腸道損傷、感染、出血、尿潴留、心臟損傷、肺炎、血液系統與神經系統損傷等,其中9例患者出現腹腔鏡射頻消融術后出血,由于術后肝臟(n=4)或腸系膜(n=1)出血,共5例患者需行開腹手術。發生術后出血的患者中,目標病變均位于右后方,因為這些腫瘤需要最長的針頭插入通道,因此損害血管的可能性更大。與射頻消融相關的其他研究指出,不論采用(經皮、開腹、腹腔鏡)何種射頻消融方法,并發癥發生率為0~34.7%,死亡率為0~5.2%[8-9]。與之相比,本研究24例患者中,圍手術期僅1例患者發生嚴重并發癥,無死亡病例,嚴重并發癥發生率為4.2%,基本符合文獻報道。
腹腔鏡超聲的使用對于腹腔鏡射頻消融至關重要。Asahina等[10]提出,腹腔鏡超聲可預防肝內血管與膽管的熱損傷。日常操作中,腹腔鏡超聲在確定腫瘤寬度、深度及目標病變周圍最滿意的進針位置方面具有關鍵作用,使腫瘤的消融變得更加安全、有效,避免了腫瘤破裂及消融造成的腫瘤擴散。腹腔鏡超聲可于消融術后立即評估消融效果,并對消融不滿意的結節進行第二次消融,保證了消融的成功率,可明顯減少術后局部復發[11]。因此,腹腔鏡超聲可實現目標病變的精確消融并具有更高的技術成功率。
綜上,腹腔鏡超聲引導下射頻消融術治療原發性小肝癌總體上是安全、可靠的,在取得較好遠期療效的同時還具有微創的優點,對于不符合肝臟切除術及肝移植手術治療指征的患者,腹腔鏡超聲引導下的射頻消融治療是較好的替代治療方式。

