類鋰電池體系在鹽湖提鋰中的研究進展
黃江江, 何利華, 唐忠陽
中南大學 冶金與環境學院,湖南 長沙 410083
引 言
鋰是重要的戰略金屬,廣泛應用于能源、化工、電子、冶金、醫藥等諸多領域,被譽為“21世紀的新能源金屬”。 近年來,新能源汽車產業的發展快速,動力電池的大量生產以致對鋰資源的需求量激增。全球鋰資源主要賦存于鹽湖鹵水、鋰輝石和鋰云母中,其中鹽湖鹵水鋰資源儲量占全球總量的65%。目前,全球鋰鹽產品生產所需鋰原料大多來源于鹽湖,且隨著優質鹽湖資源的開發,鹽湖的品質逐年降低。特別是對我國而言,我國是鋰資源大國,其探明鋰資源儲量510萬t,其中鹽湖鋰資源占總儲量的71.89%。但是由于我國大部分鹽湖位于青藏高原地區,且多為高鎂鋰比鹽湖,鋰資源的開發利用相較于國外優質鹽湖要面臨更多技術上的難題[1-5]。因此,如何高效、低成本地開發利用鹽湖資源是新能源汽車產業和鋰工業可持續發展亟待解決的難題。
當前鋰產品50%以上被用于鋰離子電池材料,如鈷酸鋰、錳酸鋰、磷酸鐵鋰、鈦酸鋰以及鎳鈷錳三元鋰電池等的制備。對于鋰離子電池而言(以錳酸鋰鋰離子電池為例),充電時錳酸鋰材料中的鋰離子會從晶格中脫出,并在電場驅動下插入負極層狀石墨形成層間化合物;放電過程則相反,負極中的鋰從石墨層中脫出,經電解質溶液重新進入到錳酸鋰晶格中。由于錳酸鋰獨特的晶體結構,鋰能自由地嵌入和脫出而不破壞其晶體結構,可以反復進行充放電過程,從而使電池擁有良好的循環能力,其工作原理如圖1所示[6]。
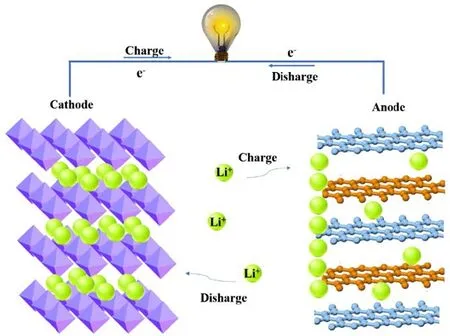
圖1 錳酸鋰電池原理示意圖[6]
實際上,鋰離子電池充放電過程中鋰的嵌入和脫出行為,亦可看作一種基于電位控制下的鋰的“電化學吸附”和“電化學解吸”。在此過程中,由于鋰離子電池材料的晶體結構具有獨特的鋰離子遷移通道、穩定的電化學氧化還原位點,因而對鋰離子嵌入表現出高度選擇性的特性。因此,如果將含鋰的鹽湖鹵水來“代替”傳統的LiPF6鋰離子電解液,采用類似于鋰離子電池的工作原理,那么在新的充放電或以化學試劑來實現的氧化/還原體系中,鹵水中的鋰將選擇性地在電極材料中進行鋰的嵌入和脫出,即鋰離子電極材料被氧化時鋰離子從電極材料中脫出(鋰的解吸過程),而再將其還原時實現鋰重新嵌入至電極材料(鋰的吸附過程)。
如果以鋰離子電池材料來進行鹽湖提鋰,面臨的首要問題就是材料的選擇問題。傳統鋰離子電池工作環境主要為有機電解液體系,而鹽湖提鋰則要求材料需要在水溶液體系(鹵水)中工作,并且材料在水溶液中應具有足夠好的化學穩定性和循環穩定性。
圖2所示為目前主流鋰離子正極材料在水溶液中的電化學工作窗口圖[7]。從圖中可以看出,磷酸鐵鋰、釩酸鋰、錳酸鋰、鈷酸鋰等材料在一定條件下能夠完全或部分在水溶液體系中實現鋰離子的電化學嵌入和脫出。基于此,研究人員利用不同的提鋰材料,提出和開發出了多種提鋰技術和提鋰模型。本文將重點闡述基于不同鋰離子電池材料形成的鹽湖鹵水提鋰體系及其基本原理。
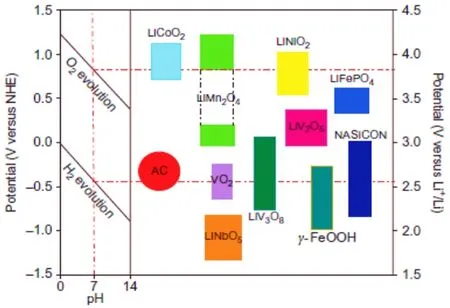
圖2 不同電極材料在水溶液中的穩定性[7]
1 錳酸鋰電化學提鋰體系
錳酸鋰作為一種對鋰選擇性極強的離子篩材料,開發之初是為了制備λ-MnO2離子篩材料,用于從鹽湖鹵水、海水等溶液中提鋰。得益于錳酸鋰材料中錳元素的氧化還原特性,錳酸鋰亦是最早被研究用于鹽湖提鋰的電極材料。
以錳酸鋰為電極材料進行提鋰,關鍵在于電極的制備。起初電極的制備是將錳酸鋰溶液漿料涂布于鉑電極上進行烘干,然后反復進行此過程制得錳酸鋰電極[8]。以制備好的錳酸鋰電極為工作電極,鉑電極為對電極,在含鋰以及其它堿金屬和堿土金屬雜質的鹽溶液進行循環伏安測試,過程脫嵌鋰反應如下:
Li++λ-MnO2+e=LiMn2O4
(1)
該研究證明了以錳酸鋰為原料、采用電化學的方法有望實現鹽湖提鋰。遺憾的是,由于所制備的錳酸鋰電極材料提鋰性能較差,對鹽湖鹵水的品位有較高的要求,難以處理低濃度鹽湖鹵水,需將鹵水進行濃縮富集,且不足以制得高品質的碳酸鋰產品[9]。特別是錳酸鋰材料存在溶損,致使循環容量快速衰減,難以長期循環使用。此外,由于采用鉑作為集流體和對電極,制造成本極高。因此,如何制備高性能、低成本的吸附電極是后續研究工作的重點之一。
1.1 (-)λ-MnO2|Brine|Ag(+) 體系
隨著鋰離子電池制備工藝技術的發展,電極材料的涂覆工藝日臻完善和成熟。錳酸鋰電極的制備工藝也有了極大的改進。如將錳酸鋰作為電極的活性物質,加入碳黑作為導電劑,聚偏氟乙烯(Poly vinylidene fluoride,簡稱PVDF)作為粘接劑,將這三者按質量比811均勻攪拌混合在NMP溶劑中,然后涂布于導電基流體上烘干[10]。這一電極制備過程完全不同于之前的反復涂覆烘干方法,且電極的整體性能得到了很大提升。新方法中導電劑的加入提高了固相電極的電導率,減少了極化現象,降低了進行提鋰反應所需的電位;粘接劑的加入則提高了電極材料的機械強度,避免了材料在水溶液中長期浸泡而脫落的現象;NMP不僅作為三者混合的溶劑,在烘干過程中其作為有機溶劑揮發后會形成一定大小的孔徑,在提高了有效反應面積的同時還能改善高黏度鹵水帶來的濃差極化問題。
此外,采用銀電極代替了最初的鉑電極作為反應的對電極。相較于鉑電極,銀電極不但擁有更好的導電能力,其電極反應電位也更低;而且在提鋰過程中,不再如鉑電極上發生陽極析氯反應(環境污染嚴重)和陰極析氫反應(改變溶液酸堿性,導致吸附材料溶解),而是鹵水中的氯離子與銀電極發生可逆吸氯和脫氯反應(如反應2所示)。在這一過程中,溶液的pH也較為穩定,有利于體系的平穩運行。
Ag+Cl=AgCl+e
(2)
該體系的提鋰工作原理如圖3(a)[10]所示,整個過程分為兩步:(1)在對體系進行充電時,鹽湖鹵水中的鋰離子進入欠鋰態錳酸鋰材料晶格,而對電極上的銀則負責捕集溶液中的氯離子,直至錳酸鋰材料中的晶格大部分被鋰離子所占據達到飽和;(2)將陰陽極對調,同時將溶液換為純凈的電解質溶液。再次對體系進行電解,錳酸鋰晶格中的鋰離子和氯化銀電極上的氯離子同時脫出進入溶液,得到純凈的氯化鋰溶液。通過反復進行這兩個步驟,能夠實現鋰元素的富集以及鋰與鹽湖鹵水中的其它雜質元素的分離。
圖3(b)所示為錳酸鋰材料在不同溶液中測得的循環伏安曲線,在1 M的氯化鋰溶液中,其在Epa=0.828 V和Epa=0.96 V分別有兩個脫鋰峰,在Epc=0.723 V和Epc=0.845 V分別對應有嵌鋰峰[11]。而在氯化鉀、氯化鈉、氯化鎂溶液中均無明顯峰形,證明錳酸鋰材料對鋰離子不僅有良好的選擇性,其嵌入脫出循環也較為穩定。這也在如圖3(c)所示的XRD圖譜中得到了證實,錳酸鋰材料通過反復地脫嵌經歷了從LiMnO4到λ-MnO2的反復變化,而其XRD峰形沒有偏移,證明了鋰離子在晶格中的嵌入脫出是可逆的[12]。圖3(d)所示為模擬的鋰離子在錳酸鋰材料晶格中的嵌入過程,研究者認為鋰離子的嵌入不會引起晶格參數較大的變化[13]。
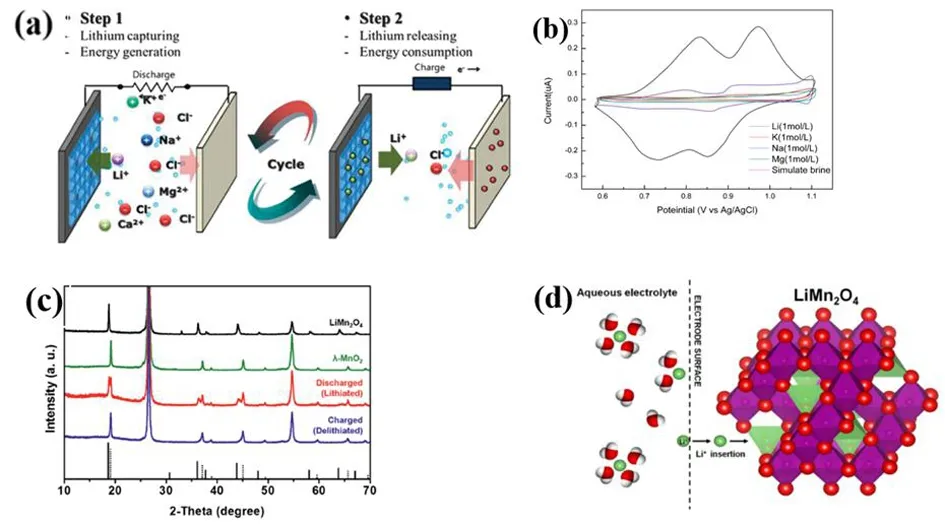
圖3 (a)錳酸鋰電極體系鹽湖提鋰原理示意圖[10];(b) 錳酸鋰在不同溶液中循環伏安曲線[11];(c)錳酸鋰在循環過程中不同形態XRD圖譜[12];(d)鋰離子嵌入錳酸鋰晶格[13]
研究者以如前文所述制得的錳酸鋰電極為工作電極,以銀電極作為對電極,通過對Acatama鹽湖鹵水模擬液(Li+=1.5 g/L、Na+=76 g/L、K+=18.5 g/L、Mg2+=9.6 g/L)以電流密度0.5 mA/cm2嵌入和脫出過程各30 min進行提鋰,4次循環后得到的富鋰溶液中,Li+濃度為18 g/L,Na+濃度為1 g/L,K+、Mg2+濃度均在0.5 g/L以下。證明該體系對鋰離子較好的選擇性和較強的分離效果[10]。采用銀電極作為反應的對電極,雖然在技術效果上取得了一定的進步,但是在實際提鋰工藝過程中,銀電極存在一定程度上的溶損,且銀電極本身較為昂貴,導致在工業應用時工藝成本大幅提高。
1.2 (-)λ-MnO2|Brine|AC(+) 體系
銀電極雖然其電化學性能相較于鉑電極有所提高,但是其高昂的成本使得其難以進行工業應用。因此有研究者[14]嘗試以活性炭為材料,通過將活性炭構筑成超級電容器來作為對電極。由于活性炭不僅對于氯離子有吸附作用,對鹽湖鹵水中其它雜質離子同樣有一定的吸附,從而降低了體系對雜質離子的分離效果以及電極在溶液中的循環能力。
為了避免這一情況的發生,研究人員設計了一套全新的鹽湖提鋰方法和裝置,其工作原理如圖4所示[14]。其提鋰過程如下:鹽湖鹵水首先從入口進入第一層,其中鋰離子在這一層中嵌入λ-MnO2電極形成LixMn2O4,其它雜質陽離子則由于陰離子交換膜阻擋,大部分無法進入負極室中留在這一層中。然后溶液繼續進入下一層中,氯離子在負極室中被活性碳吸附。在錳酸鋰達到飽和時,將溶液替換為純凈溶液,改變溶液流向和電極電位進行逆過程,活性炭上的氯離子解析下來進入溶液,同時鋰離子從錳酸鋰晶格中脫出,便可以在陽極室中得到純凈的氯化鋰溶液。

圖4 錳酸鋰—活性炭體系鹽湖提鋰裝置示意圖[14]。其中(1)為活性碳電極,(2)為陰離子交換膜,(3)為尼龍墊圈,(4)λ-MnO2電極
1.3 (-)H1.6Mn1.6O4|Brine|Pt (+) 體系
由于鹽湖鹵水礦化度高,且大都呈飽和溶液,黏度大。在傳統的吸附法和上述利用電池材料進行提鋰等工藝過程中,溶液在吸附劑或電極材料內部的擴散速度慢,路徑長,導致提鋰效率低。通過將吸附材料進行納米化,可有效降低溶液在顆粒中的擴散路徑,尤其對于成分復雜、鹽濃度較高的鹽湖鹵水來說能有效減少濃差極化,提高吸附性能。同時也減少了鋰離子在材料嵌入脫出引起的結構形變,抑制Jahn-Teller效應,改善了電池材料的循環性能[15]。
基于此,有研究通過高溫固相法合成了納米級錳系離子篩,作為工作電極進行鹽湖提鋰實驗。同時選擇使用具有良好導電性、高比表面積的石墨烯(r-GO)作為導電劑,r-GO的含氧功能團可以與粘接劑聚乙烯醇結合固定正極活性材料。在低電壓下,其反應方程式如下:
R-H++ Li+= R-Li++ H+
(3)
R-Li++ H+= R-H++ Li+
(4)
而在高電壓下,其反應方程式如下:
R-Mn(IV)+e+ Li+= R-Mn(III)-Li
(5)
R-Mn(III)-Li-e=R-Mn(IV)+Li+
(6)
其中R為正極材料中不參與反應的化合物。實驗結果證明其吸附容量達到38.78 mg/g,且在5個循環后其循環容量僅由于Mn的歧化反應降低了1%。通過選擇使用優質的導電劑改進鋰離子電池材料導電性以及合成納米級材料、混合PPy等材料降低保護材料防止溶損同時提高材料擴散性能、循環容量,將是今后鋰離子電池材料在鹽湖提鋰中應用的熱門研究方向[16]。
2 磷酸鐵鋰電化學提鋰體系
除錳酸鋰外,磷酸鐵鋰也是近年來用于鹽湖提鋰的主要材料之一。作為市場上主流的電池正極材料,相較于錳酸鋰,磷酸鐵鋰擁有更大的理論吸附容量和更低的反應電位,并且其在水環境中更為穩定。
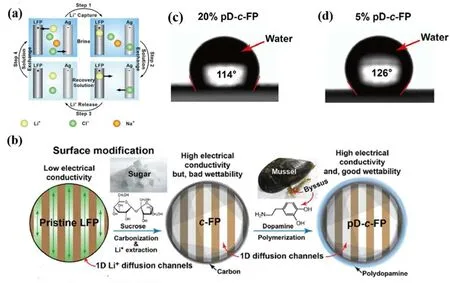
圖5 (a)提鋰循環原理示意圖[17];(b)磷酸鐵鋰和磷酸鐵的表面改性[18];(c)20%聚多巴胺涂層對磷酸鐵界面性能的影響[18];(d)5%聚多巴胺涂層對磷酸鐵界面性能的影響[18]
Mauro Pasta[17]采用磷酸鐵鋰和銀電極,構筑了(-)FePO4|Brine|Ag(+) 電化學提鋰體系,其工作原理如圖5(a)所示[17]。整個工藝同樣由兩個步驟組成:(1)磷酸鐵作為陰極在自身還原時捕集鹵水中的鋰離子,銀作為陽極通過捕集鹵水中的氯離子氧化為氯化銀,過程電極反應過程如反應(7)和(8)所示;(2)當陰極上的磷酸鐵轉變為磷酸鐵鋰時,將鋰溶液替換為純凈的電解質溶液,以磷酸鐵鋰電極作為陽極,氯化銀電極作為陰極進行電解,此時鋰離子和氯離子分別從磷酸鐵鋰和氯化銀電極中同時被釋放出來進入溶液中,得到不含雜質的氯化鋰溶液。經第二步后電極體系還原成初始形態,繼續進行下一個周期的提鋰循環。
陰極反應:Li++FePO4+e= LiFePO4
(7)
陽極反應:Ag+Cl-= AgCl+e
(8)
采用該電化學提鋰體系處理Li+濃度為0.05 M,Li/Na比為1100的模擬溶液,以0.5 mA/cm2的電流密度進行電解2 h,得到的純鋰溶液中Li+濃度為0.115 M, Na+濃度為0.021 M,能有效地分離鹽湖鹵水中的鋰離子和鈉離子。
該體系證明了使用磷酸鐵鋰材料進行鹽湖提鋰的可行性,同時相較于錳酸鋰—銀電極體系,磷酸鐵鋰電極體系消耗的電能更少,對鹽湖鹵水的適應性也更強。
由于磷酸鐵鋰本身的電子導電性比較差,通過對其表面進行改性優化處理,可顯著提高其提鋰性能。如在FePO4|Brine|C2H2IN|Pt體系中,將磷酸鐵鋰粉末與蔗糖以73的質量比混合后,在高壓反應釜中180 ℃反應12 h,使用離心分離得到沉淀物,將其置于烘箱中烘干,然后在氮氣的保護氛圍下600 ℃加熱1 h得到碳包覆的磷酸鐵鋰(圖5(b)所示[18])。通過表面碳包覆,顯著提高了磷酸鐵鋰材料的導電性,同時由于表面碳層可起到隔離電極材料與鹽湖鹵水的直接接觸的作用,使材料在水溶液中的穩定性進一步加強,循環性能得到提升。
盡管通過碳包覆可以改善材料的導電性,但碳包覆后的顆粒表面疏水性較強,溶液對電極材料的浸潤性差。為此又開發了氯化多巴胺溶液處理碳包覆后的磷酸鐵鋰材料,以改進表面疏水性。由于聚多巴胺中的兒茶酚基和氨基具有極強的極性,與材料之間有較強的作用力,可以吸附在磷酸鐵鋰材料表面,使其具有很好的浸潤性,降低了鋰離子在電極材料與電解質界面之間的傳質阻力。圖5(c)和(d)為不同聚多巴胺含量處理后的磷酸鐵鋰材料接觸角圖像對比,證明了進行聚多巴胺處理可以改善材料的潤濕性能。
除了上述所述的錳酸鋰、磷酸鐵鋰體系外,還研發了諸如(-)LiMnO4|LiCl | ZnCl2| Zn(+)[19]、(-)LiFePO4|Brine|KNiCFe(+)[20]等多種電化學提鋰體系。這些提鋰體系對電極的選擇不同,對工作電極材料的不同處理,提鋰效果有些許差異,但其工作原理大同小異,在此不再贅述。
3 三元鋰電材料電化學提鋰體系
Ni1/3Co1/3Mn1/3O2|Brine|Ag作為新一代鋰離子電池正極材料,擁有更高的理論容量(275 mAh/g)和更好的高倍率充放電能力[21],在水溶液體系中也擁有穩定的電化學窗口,可以作為新一代的水溶液體系電容器和鋰離子電池材料使用。基于LiNi1/3Co1/3Mn1/3O2材料的以上特點,有研究者[22]嘗試使用其來捕集鹽湖鹵水中Li+。在循環伏安測試中,如圖6所示,測得純鋰溶液中在Epa=0.693 V和Epc=0.587 V時分別有鋰離子的脫出和嵌入峰,而在含鋰離子的混合溶液中,脫鋰峰偏移至0.758 V,嵌鋰峰則在0.597 V。說明溶液中雜質離子的存在對提鋰過程有一定的影響。值得注意的是在不含鋰離子的混合溶液中,在Epc=0.324 V時存在的峰形可能是Mn4+的還原,而在實際操作過程中進行高倍率循環時,循環時間大于20 min會出現Mn的溶解以及其它的副反應,導致溶液中Li+純度下降,驗證了這一反應的存在。該體系在鹽湖鹵水中長時間循環的穩定性能還有待測試,但是三元材料作為鹽湖鹵水提鋰正極使用所表現出的高倍率充放電性能以及較高的吸附容量,都值得對該體系進行更深入的研究。
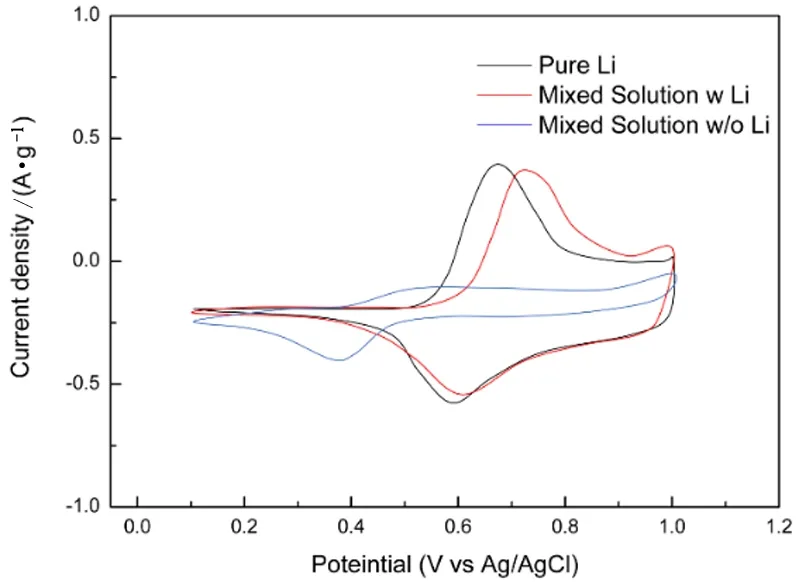
圖6 NCM材料在純鋰溶液,含鋰以及不含鋰的混合溶液的循環伏安曲線[22]
Ni0.5Mn1.5O4|Brine|Ag已經被證明在水溶液體系的鋰離子電池中,擁有147 mAh/g的高容量以及超過1 000次循環的優良循環能力。研究者[23]選用Li1-xNi0.5Mn1.5O4/Ag體系來進行鹽湖鹵水提鋰實驗,在合成材料時通過摻雜Ni元素消除Li0.5Mn1.5O4中Li離子之間的排斥能,降低了Li嵌入/脫出的能壘,使得Li+在Li1-xNi0.5Mn1.5O4結構中有著更快的傳輸速率。同時在LNMO材料中,Ni2+/Ni4+的還原反應也使得材料擁有更高的容量(1.259 mmol Li+/g)。以1.05 C電流對Uyuni鹽湖模擬鹵水進行充放電循環提鋰實驗,單次循環20 min,可以得到Li純度在98.14%的富鋰溶液。
4 電化學脫嵌法鹽湖提鋰
上述由錳酸鋰、磷酸鐵鋰或三元鋰電材料為電極吸附材料而構建的提鋰體系,實際在對鹽湖鹵水中的鋰元素進行提取和解吸的只有涂覆有吸附材料的工作電極。而對電極(如銀電極、鉑電極等)的作用更多的是匹配工作電極上的反應,起平衡電荷的作用,其上發生的電化學反應的主要是盡量避免析氫、析氯等反應而造成污染或溶液酸堿性的變化。換言之,除了工作電極本身在進行和鋰相關的反應,對電極從某種意義上而言是在“做無用功”。此外,過程中鋰的吸附和解吸分兩步進行,操作過程繁瑣。
既然吸附和解吸過程都是通過通電的方式實現,那能否將兩步合一,在同一個過程中同時完成吸附和解吸操作呢?
實際上,在鋰離子電池工作過程中,電極的陰陽極屬性隨著充放電過程的轉變也在發生相應變化。如磷酸鐵鋰和錳酸鋰在充電脫鋰時是陽極,而在放電嵌鋰時則變為陰極。換言之,如果以脫鋰后的FePO4為陰極,嵌鋰后的LiFePO4作為陽極,來構建新的提鋰體系,則有望實現陰極電化學提鋰的同時,在陽極實現鋰的同步解吸。
基于這一創新思路,中南大學趙中偉教授提出并構筑了“富鋰態吸附材料 (陽極)│支持電解質│陰離子膜│鹵水│欠鋰態吸附材料 (陰極) ”電化學脫嵌法鹽湖提鋰新體系,實現了鹽湖鹵水中鋰的高效選擇性提取和富集,并且基于不同的鹽湖鹵水和含鋰溶液,可用的吸附材料可為磷酸鐵鋰、錳酸鋰或鈦酸鋰離子篩材料等材料[24,25]。
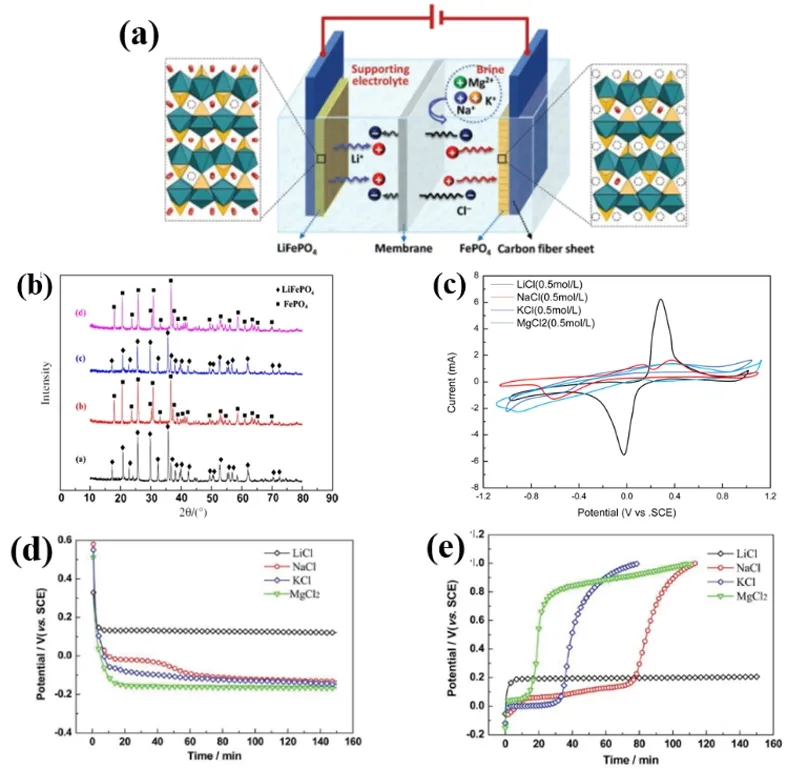
圖7 (a)鹽湖提鋰裝置結構圖[7];(b)不同階段的電極材料XRD圖譜[26];(c)磷酸鐵鋰材料在不同鎂鋰比下鋰離子的循環伏安曲線[7];(d)離子在陰極上嵌入計時電位曲線[7];(e)離子在陽極上脫出的計時電位曲線[7]
新方法的提鋰原理如圖7(a)所示[7],具體而言(以LiFePO4為例):(1)采用LiFePO4為陽極,LiFePO4脫鋰后的FePO4為陰極,用陰離子交換膜將陰陽極分割成兩個室;(2)陽極室(即富鋰室)注入NaCl等不含Mg2+的支持電解質,陰極室(鹵水室)注入待提鋰的鹽湖鹵水;(3)在陰、陽極兩端施加一定電壓,陽極LiFePO4失去電子將Li+脫出進入富鋰室(即反應 LiFePO4-e = Li++FePO4),而陰極FePO4因得到電子而迫使鹽湖中的Li+進入到FePO4晶格中以維持材料的電中性(反應Li++FePO4+e = LiFePO4),與此同時,鹵水室的陰離子則通過陰離子膜進入富鋰室以維持整個體系的電荷平衡;(4)將完成電解周期的電極對調,進行下一周期電解,實現鹽湖鹵水中鋰的不斷提取與富集,電解提鋰時陽極陰極分別如反應(9)和(10)所示。最后得到的陽極溶液中不含鎂離子等雜質陽離子,僅為富含鋰的純凈溶液,可以采用碳酸鹽沉淀法生產碳酸鋰產品。
LiFePO4-e= Li++FePO4
(9)
FePO4+Li++e = LiFePO4
(10)
值得注意的是,在該電化學脫嵌法鹽湖提鋰過程中,由于陰、陽極電極反應互為可逆反應,因此電解過程的理論槽電壓為0 V。這也意味著,其理論直流電耗為零,外電路輸入的能量主要用于過程存在電化學極化、溶液電阻和膜電阻等耗能。
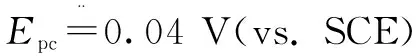
此外,通過對比磷酸鐵鋰材料在反復脫嵌鋰離子過程中的XRD圖譜可以發現,循環前后的磷酸鐵鋰與磷酸鐵峰形。沒有發生明顯的變化,可以認為鋰離子在鹽湖鹵水體系中同樣能自由地在晶格中擴散而不改變晶體結構(圖7(b)[26])。通過進一步研究鹽湖鹵水中主要陽離子在材料中的脫嵌行為,通過分析計時電位曲線,發現離子在陰極上的嵌入順序為Li>Na>K>Mg,而脫出順序則完全相反[圖7(d)和(e)],說明鋰離子相較于其他雜質陽離子會被優先吸附,且即便有雜質離子進入至磷酸鐵晶格內部,雜質離子會更容易脫出而不至于阻塞鋰離子擴散的位點影響材料的循環性能[7]。
采用該方法處理模擬的鹽湖鹵水(Li+=1.4 g/L、Na+=30 g/L、K+=3.9 g/L、Mg2+=48 g/L),在0.25 V槽電壓下經過4次循環,陽極溶液中鋰可以達到1.75 g/L。此外,以五礦青海一里坪鹽湖原鹵(成分:Li 97.5 mg/L、 Mg 13.1 g/L、K 3.5 g/L、Na 100.4 g/L、Mg/Li=134.4)為原料進行了提鋰試驗,在 0.2 V槽電壓連續電解 50 h后,鋰的回收率可達 83%,提鋰效果顯著。此時,陽極富鋰液中鋰濃度上升至 80 mg/L左右,而陰極鹵水中的鋰濃度則降至 18 mg/L。尤為突出的是,所得富鋰液中的鎂鋰比僅為 1.21,遠低于初始鹵水中的 134.41,表現出很好的鎂鋰分離效果[27]。
電化學脫嵌法鹽湖提鋰技術于2017年實現技術成果轉讓,并已完成了相關的工業化試驗,技術經濟指標優良,是極具發展潛力的綠色鹽湖提鋰技術之一。
5 結論與展望
如何實現鹽湖鹵水中鋰的綠色、高效提取是未來新能源汽車產業和鋰工業可持續發展亟待的關鍵技術難題之一[28]。利用鋰離子電池正極材料進行鹽湖提鋰越來越受到人們的重視,也是目前提鋰技術的研究熱點。
目前,已研究和開發的可用于鹽湖鹵水提鋰的材料和體系眾多,尤以錳酸鋰和磷酸鐵鋰為最。在這些提取技術中,電化學脫嵌法是最具發展前景技術之一。與傳統鹽湖鹵水提鋰工藝相比,該方法大幅度降低了可處理鹵水中鋰的濃度,避免了傳統提鋰技術因鹽田灘曬獲取老鹵原料而造成的鋰大量損失;此外,生產過程中無需調節鹵水的酸堿度、鹽度,亦無有毒有害物質的添加和產生,提鋰后的鹵水無害可直接返回鹽田,環保效益顯著。

