真空熱還原法制備金屬鋰的研究進展
沈自強, 狄躍忠, 彭建平, 王耀武, 馮乃祥
東北大學 冶金學院,遼寧 沈陽 110819
引 言
金屬鋰及其化合物廣泛應用于冶金、電子、能源電池、熱核聚變及航空航天等領域,已經成為一種對國民經濟和國防建設具有重大意義的戰略資源,被稱為“工業味精”和“21世紀的能源金屬”。
鋰礦資源的分布如表1所示,中國的鋰礦資源儲量居世界前列,僅次于智利、阿根廷和澳大利亞。單從儲量角度看,我國擁有較為豐富的鋰資源,但是由于地理位置偏遠以及礦石稟賦較差等因素,我國的鋰輝石礦開采難度較大、成本高,導致我國鋰礦石資源嚴重依賴進口。我國是全球第一大鋰鹽生產國和消費國,但原料主要依賴于進口鋰輝石精礦,且進口渠道單一,對外依存度曾達到70%左右[1-4]。同時,我國鋰工業還存在著生產工藝落后、污染嚴重以及生產成本高等問題。據統計,我國礦石提鋰的成本為全球最高[4]。因此,研發新型鋰系列產品制備工藝,降低生產成本,對于我國鋰工業發展具有重要意義。
金屬鋰的制備方法主要有熔鹽電解法和真空熱還原法兩大類,熔鹽電解法是當前工業生產金屬鋰的主要方法,1893年,Guntz提出在450 ℃下電解含有等量氯化鉀和氯化鋰的熔體,制得金屬鋰,奠定了電解法生產金屬鋰的基礎[5]。經過改進,熔鹽電解法主要是以熔融的LiCl 45%-KCl 55%為電解質,在390~450 ℃下,直流電解,在陰極得到金屬鋰。
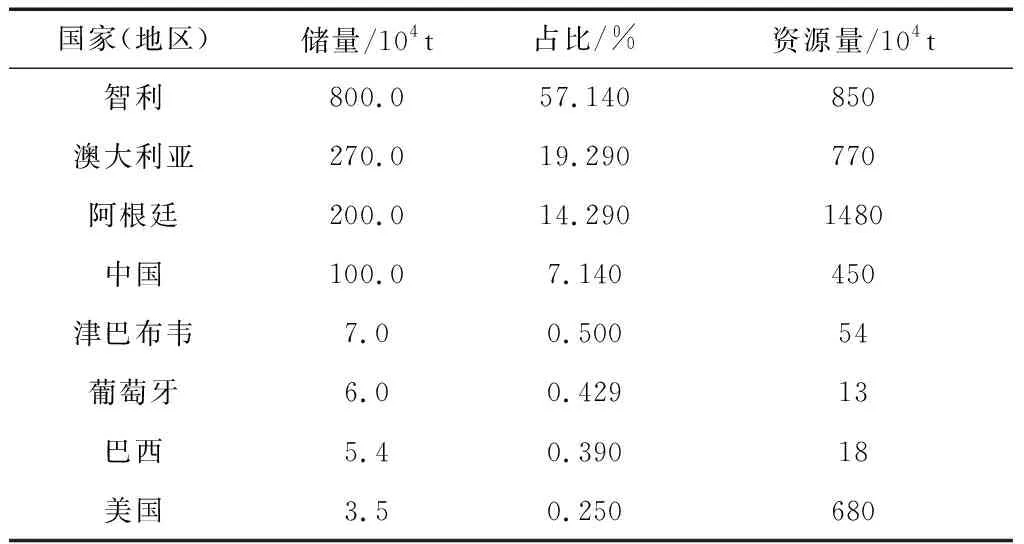
表1 2019年世界已探明鋰礦儲量與資源量概況[1]
熱還原法也是一種傳統的金屬鋰制備方法,1894年,瓦連用鎂還原氫氧化鋰,制得金屬鋰,開創了熱還原法制備金屬鋰的先河,之后鋰冶金工作者從未間斷對熱還原法煉鋰的研究工作。有學者分別用鈣和鈉還原氯化鋰,但是結果并不理想。1930年,J·Roer和 J·Broos用鋯還原鉻酸鋰,得到金屬鋰,但是生產率較低,成本較高。1936年,M·Jonnson申請了用鋁還原鋰輝石制取金屬鋰的專利。1937年,美國礦務局提出以碳為還原劑生產金屬鋰[5]。
與熔鹽電解法相比,真空熱還原法具有以下優勢:(1)熔鹽電解法的原料為高純氯化鋰,由碳酸鋰提純后氯化制備,成本較高,而熱還原法以氧化鋰熟料為還原物料,可由碳酸鋰或氫氧化鋰熱分解制備,成本較低;(2)熔鹽電解法電解質會揮發,陽極氣體氯氣污染環境、腐蝕設備,而熱還原法無腐蝕性氣體產生,過程清潔;(3)熔鹽電解法由于鉀、鈉的析出電位較低,會優先析出進入金屬鋰中,而真空熱還原法所得金屬鋰產品純度高,主要是由于飽和蒸氣壓差異,能夠避免雜質鉀、鈉混入金屬鋰中。隨著真空冶金技術裝備的不斷進步,在鎂冶金領域,真空熱還原法已經基本取代熔鹽電解法,成為工業鎂冶煉的主要方法,這為真空熱還原法煉鋰提供了堅實的理論基礎和技術儲備。在金屬鋰供不應求的形勢下,對金屬鋰制備工藝進行創新優化就顯得尤為重要,真空熱還原法煉鋰也成為鋰行業的一個重要研究方向。
本文對國內外熱還原法制備金屬鋰的工藝和研究現狀進行了綜述,主要涉及碳熱還原法和以鋁硅系還原劑為代表的金屬熱還原法。并介紹了一種以氫氧化鋰合成的Li5AlO4富鋰熟料為原料,鋁熱還原制備金屬鋰,副產高白氫氧化鋁的新工藝。
1 碳熱還原法
1937年美國礦務局首先提出用炭粉做還原劑,制備金屬鋰,基本原理如式(1)所示:
2Li2O(s)+C(s)=CO2(g)+4Li(g)
(1)
該工藝還原劑廉價,但反應溫度高,生成的鋰蒸氣易與CO發生反應,導致產品純度低。陳為亮[6]對真空碳熱還原煉鋰進行了研究,先將活性炭粉、氧化鈣以及碳酸鋰混合、壓團,置于真空爐中,加熱,制得氧化鋰熟料。然后將制得的氧化鋰熟料與活性炭粉混合壓團,進行真空熱還原,在20 Pa和1 150 ℃的條件下還原120 min,制得純度為54.34%的鋰,再進行真空蒸餾,得到了純度99.9%以上的高純鋰,從而驗證了碳熱還原制備金屬鋰的可行性,該工藝的基本流程見圖1。
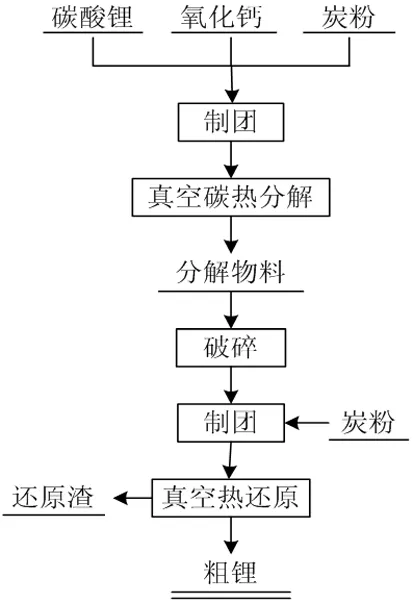
圖1 真空碳熱還原法流程[6]
真空碳熱還原法原料廉價,成本相對較低,產渣量也較少,約為0.532 kg/kg-Li,但是生成的金屬鋰易與副產物CO、CO2等發生反應,導致還原后的產物純度不高。由于碳熱還原反應溫度高,二次反應容易生成碳化物、氧化物和碳酸鹽等雜質,Kroll和Schlechten等提出以堿金屬的碳化物代替碳進行熱還原制備金屬鋰。林智群[7,8]等用碳化鈣代替碳粉,采用如圖2的工藝路線,通過優化條件制得了純度為98.28%的金屬鋰,原理如式(2)所示:
3Li2O(s)+CaC2(s)=CaO(s)+2CO(g)+6Li(g)
(2)
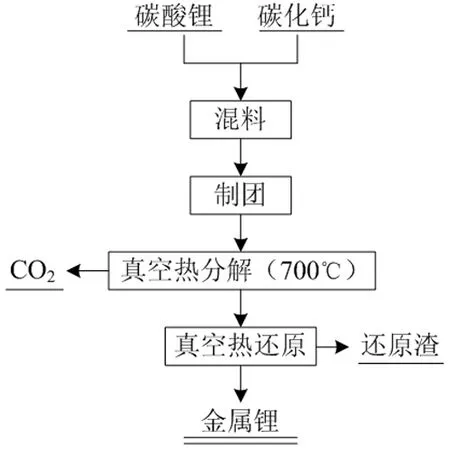
圖2 真空碳化鈣熱還原法流程[2]
相對于真空碳熱還原法,真空碳化鈣熱還原法流程簡單,還原溫度較低,只需一次配料、壓團,過程中不需要額外添加物料,就可以直接制得粗鋰,縮短了工藝周期,降低了能耗。但是,還原劑碳化鈣成本相對較高,保存條件較為苛刻,且產物中碳的含量仍然較高,可能是在真空高溫的條件下,碳化鈣分解生成碳在高溫下與金屬鋰發生反應生成碳化鋰,二次反應的問題仍然未得到有效解決。碳熱還原法制備金屬鋰,雖然具備還原劑成本低這一顯著優勢,但是從熱力學角度來看,其還原溫度較高,且極易發生二次反應,金屬鋰的純度偏低,工業應用難度極大。
2 硅熱還原法
金屬熱還原主要是用金屬為還原劑,真空熱還原制備金屬鋰,常用的金屬有鋁、硅、鐵、鎂、鈣、鋇及相關合金等,傳統方法的主要步驟分為碳酸鋰熱分解制備氧化鋰以及氧化鋰的真空熱還原,還原原理如式(3)所示。
Li2O(s)+M(s)=MO(s)+2Li(g)
(3)
式(3)中,M表示金屬還原劑,MO表示金屬的氧化物。
硅熱還原法是以硅為還原劑,高溫下還原氧化鋰制備金屬鋰的方法。Kroll[9]以碳酸鋰為原料,氧化鈣為添加劑,先制備氧化鋰物料,然后硅熱還原制得金屬鋰,通過試驗發現在950~1 000 ℃可以達到合適的金屬鋰回收率。同時,將碳酸鋰、氧化鈣和硅混合制團后,直接真空加熱分解,再升溫還原,結果發現產物氧化較為明顯。Smeets[10]以氧化鋰和鋰輝石為原料,加入氧化鈣壓塊、還原,發現了基本相同的規律。Stauffer[11]利用硅鐵還原鋰輝石,氧化鈣/鋰輝石達到2.3時,還原率可達87%,并進行了10 kg級的擴大試驗,還原溫度在1 150 ℃時,回收率為80%~85%,得到金屬鋰純度為85%~90%。日本的小林正夫也進行了硅熱法煉鋰的研究,并設計了豎式和臥式兩種真空還原爐,鋰回收率達到90%左右[12]。
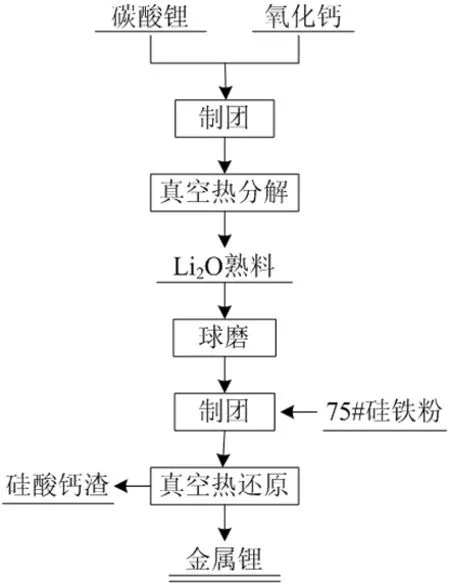
圖3 真空硅熱還原法流程圖[13]
本課題組曾系統地研究了以碳酸鋰為原料,硅鐵為還原劑,氧化鈣為添加劑的真空熱還原工藝,具體工藝路線如圖3所示。在單因素和正交試驗結合的基礎上,分析了還原溫度、還原時間、還原劑過量率、制團壓力及物料粒度對金屬鋰還原率的影響規律。確定了最優條件為真空度4 Pa、還原溫度1 020 ℃、還原時間180 min、制團壓力30 MPa、物料粒度小于80 μm、還原劑過量系數50%,在最優條件下,金屬鋰的還原率達到97.83%,純度99.24%,還原渣的主要成分為Ca2SiO4、CaO及未反應完全的FeSi[13]。還原機理如式(4)所示。
2Li2O(s)+2CaO(s)+Si(Si-Fe)(s)=Ca2SiO4(s)+4Li(g)
(4)
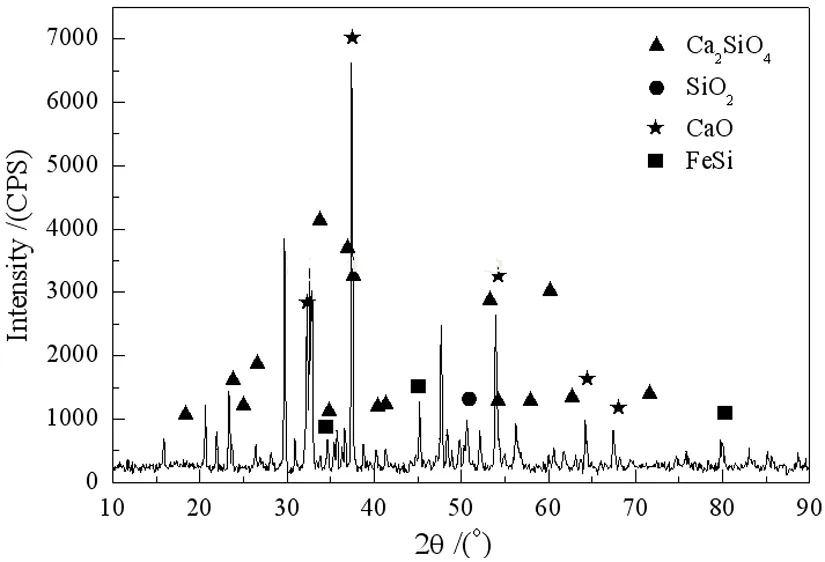
圖4 硅熱還原煉鋰所得還原渣XRD圖[13]
通過以上研究發現,雖然經過工藝條件優化可以制備出純度較高的金屬鋰,且回收率較高。但是還原過程的生產效率較低,具體表現在料鋰比非常高,約為131,同時氧化鋰熟料必須通過真空熱分解的方式來制備,能耗較高。
狄躍忠[14]等設計并建成7.5 kg/爐的新型內電阻加熱真空煉鋰中試裝置,進行了碳酸鋰真空熱分解試驗和硅熱還原制取金屬鋰的試驗。所制備的氧化鋰熟料可滿足還原過程的需要,但是由于加熱系統和結晶器的設計不完善等原因,金屬鋰的實收率較低,需要進一步優化改進。
3 鋁熱還原法
真空鋁熱還原法主要是以鋁為還原劑,真空條件下還原氧化鋰物料,制得金屬鋰。Kroll[9]在鋁粉過量10%、900 ℃、0.1 Pa的條件下,進行鋁熱還原,金屬鋰回收率為80%,還原機理如式(5)所示。
3Li2O(S)+CaO(S)+2Al(l)=CaO·Al2O3(S)+6Li(g)
(5)
Stauffer[11]進行了鋁熱還原鋰輝石制取金屬鋰的研究,在m(鋁粉)m(氧化鈣)m(鋰輝石)=21510,反應溫度1 050~1 150 ℃下還原2 h,金屬鋰的回收率為92.2%,純度85%~90%。林智群[8]研究了以碳酸鋰為原料的鋁熱還原制備金屬鋰的過程,在加入氧化鈣的條件下,通過分段加熱實現碳酸鋰先分解生成氧化鋰,再還原氧化鋰制備出金屬鋰,在該條件下金屬鋰的還原率可以達到93.37%。
李繼東[15]等通過正交試驗確定了以氧化鋰為原料,真空鋁熱還原制備金屬鋰的最佳工藝條件:溫度1 170 ℃、還原時間5 h、還原劑粒徑100目、鋁粉過量15%,在該條件下,金屬鋰還原率為92.2%。并進行了半工業試驗,從配料、成團、分解、還原到最終出爐制得金屬鋰,工藝實現了連續化,共制得金屬鋰3.26 kg,回收率為79.8%[16]。但在半工業試驗中,出現了金屬鋰的回收率較低、碳酸鋰分解較為困難以及鋰蒸氣的冷凝回收困難等問題,因此還需要進一步優化改進。
中科院青海鹽湖所用真空熱還原—蒸餾工藝,以鹵水提取的粗制碳酸鋰為原料制備了純度高達99.9%的高純金屬鋰[17]。該工藝是以碳酸鋰為原料,氧化鋁、氧化鈣為添加劑,摩爾比為1368,煅燒得到CaO和LiAlO2的混合物,然后鋁熱還原得到金屬鋰,其理論料鋰比為11.61,還原渣直接排放沒有進行循環利用。
狄躍忠[14,18]等以實現還原渣的綜合利用為目的,進行了以碳酸鋰為原料,常壓合成LiAlO2熟料,然后鋁熱還原制備金屬鋰。還原過程發生的化學反應有:
3LiAlO2(s)+3CaO(s)+Al(l)=2[CaO·Al2O3](s)+3Li(g)
(6)
21LiAlO2(s)+24CaO(s)+7Al(l)=
2[12CaO·7Al2O3](s)+21Li(g)
(7)
所得還原渣為鋁酸鈣型,如圖5所示。因此,采用混合堿液溶出—碳酸化分解的方法對還原渣進行了綜合利用研究,制備出氫氧化鋁。
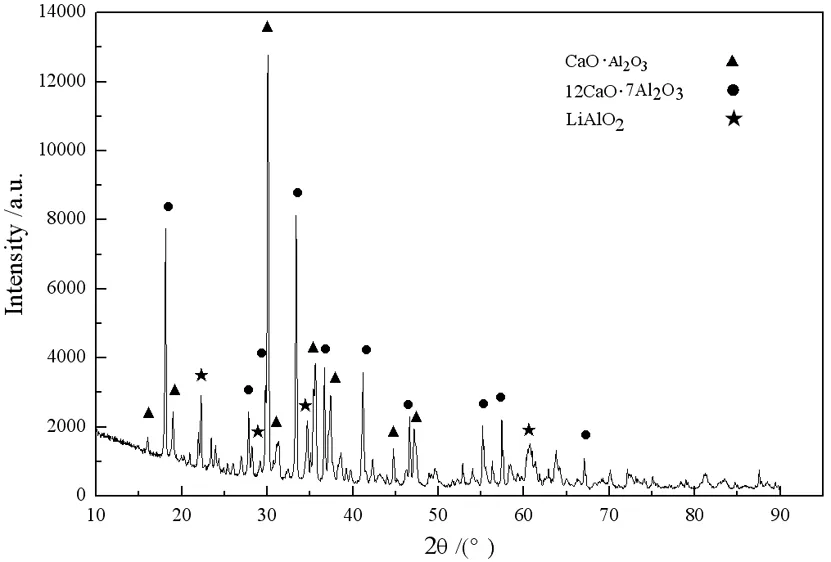
圖5 鋁熱還原所得還原渣XRD圖[14]
4 鋁硅合金熱還原法
由于鋁、硅都可以作為還原劑來還原金屬鋰,因此有學者嘗試用鋁硅合金作為還原劑來制備金屬鋰。林智群[8]以鋁粉和硅粉混合物為還原劑,按照式(8)的反應,在系統壓強為5 Pa、還原溫度900~1 100 ℃的條件下,對鋁硅合金熱還原制備金屬鋰進行了研究,在該條件下,金屬鋰的還原率最高可達97.32%,純度達到99%。
9Li2O(S)+3CaO(S)+2Al(l)+3Si(s)=
3CaO·Al2O3·3SiO2(S)+18Li(g)
(8)
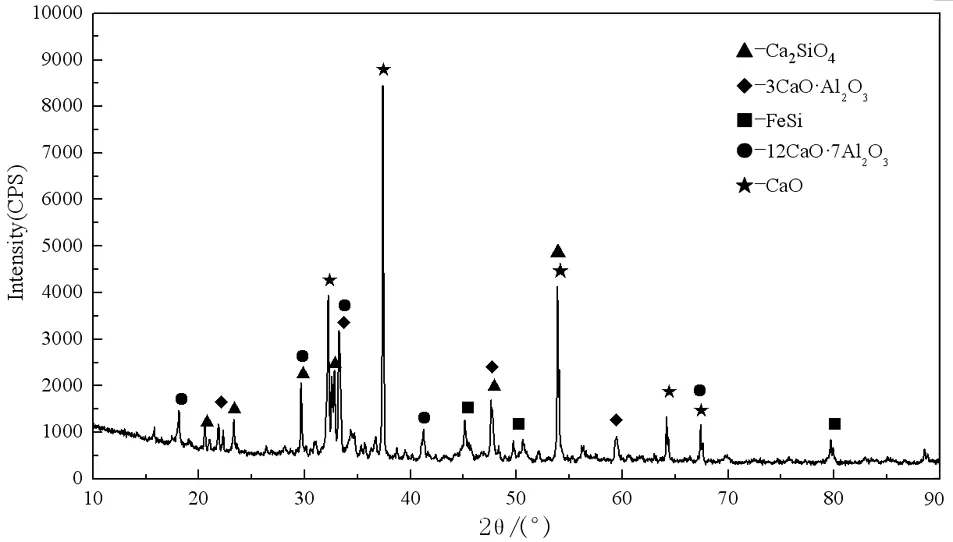
圖6 鋁硅鐵合金還原煉鋰所得還原渣XRD圖[14]
在一次鋁硅鐵合金還原氧化鋰的過程中,合金中硅是直接與氧化鈣、氧化鋰反應生成金屬鋰和硅酸鈣,鋁是在溫度較低時與氧化鋰反應生成金屬鋰和鋁酸鋰,如式(9)所示:
2Li2O(s)+Al(l)=2LiAlO2(s)+3Li(g)
(9)
當溫度逐步升高時,鋁與鋁酸鋰、氧化鋰、氧化鈣反應生成金屬鋰和鋁酸鈣,其發生的反應如式(10)和式(11)所示:
21LiAlO2(s)+24CaO(s)+7Al(l)=
2[12CaO·7Al2O3](s)+21Li(g)
(10)
3LiAlO2(s)+6CaO(s)+7Al(l)=
2[3CaO·Al2O3](s)+3Li(g)
(11)
由于鋁硅合金熱還原法在還原過程中,生成了更為穩定的固體產物,因此比用純鋁還原氧化鋰更有優勢[8]。相對而言,鋁硅合金熱還原法,還原溫度較低,金屬鋰的還原率高,產品純度高。
5 新型鋁熱還原法
基于前人及本課題組的研究成果,以鋁、硅及其合金為還原劑的真空熱還原法煉鋰工藝具有工業應用前景。但是常規工藝存在兩個問題:(1)以碳酸鋰制備氧化鋰熟料,為實現碳酸鋰的徹底分解常需添加大量氧化鈣,同時還需進行真空熱分解,造成還原過程的料鋰比較高,效率較低;(2)常規金屬熱還原工藝基本未對還原渣的回收處理進行深入研究。因此,針對上述問題開發了新型鋁熱還原煉鋰新工藝:以氫氧化鋰為原料常壓煅燒合成Li5AlO4型富鋰熟料,再與鋁粉混合真空熱還原富鋰熟料(Li5AlO4和CaO混合物)得到金屬鋰,同時獲得理論成分為12CaO·7Al2O3的還原渣,該還原渣可通過堿液溶出、碳酸化分解進行回收利用[19]。其中主要的反應為:
10LiOH(s)+Al2O3(s)=2Li5AlO4(s)+5H2O(g)
(12)
21Li5AlO4(s)+48CaO(s)+35Al(l)=5[12CaO·7Al2O3](s)+105Li(g)
(13)
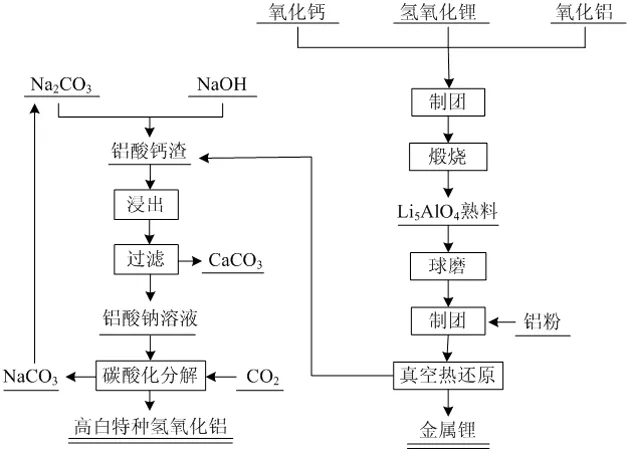
圖7 新型鋁熱還原流程[19]
唐成偉[20]對Li5AlO4熟料的制備及鋁熱還原過程進行了研究,以一水氫氧化鋰、氧化鈣和氧化鋁合成Li5AlO4熟料,其物相組成如圖8所示,其主要成分為Li5AlO4和CaO。通過工藝優化金屬鋰的還原率可以達到96%以上,還原渣物相組成如圖9所示,其主要成分為12CaO·7Al2O3和CaO·Al2O3,為鋁酸鈣型還原渣。適合用堿液溶出—碳酸化分解制備氫氧化鋁的工藝路線進行回收利用。
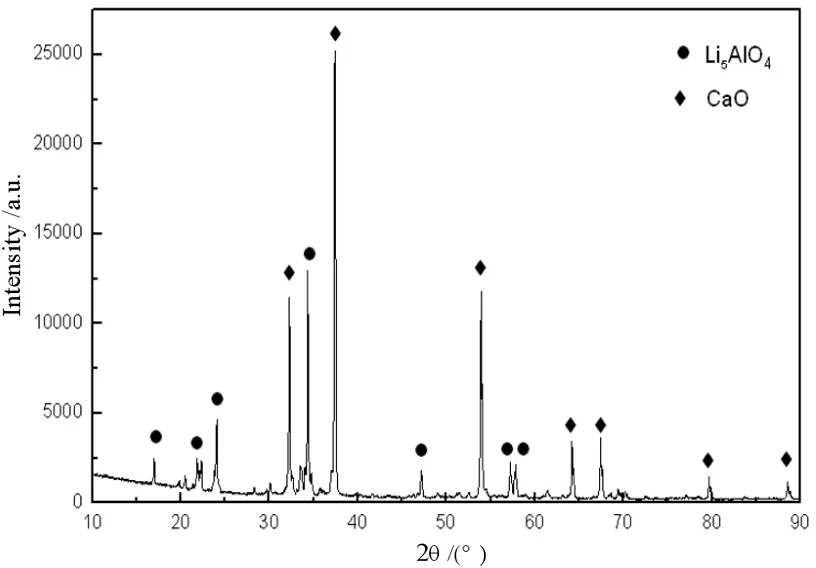
圖8 富鋰熟料的XRD
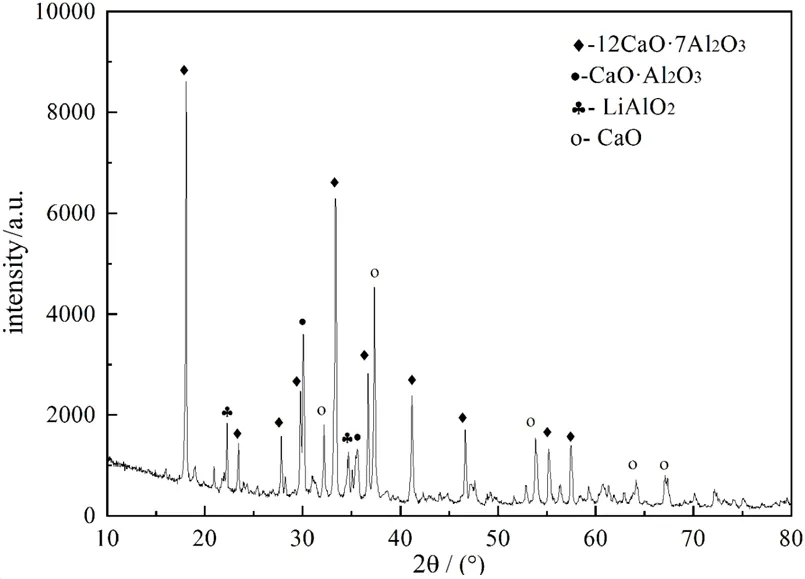
圖9 鋁熱還原所得還原渣
通過添加Na2CO3和NaOH進行堿液溶出,可以將其中的大部分氧化鋁以及過量鋁粉溶出,其溶出的主要反應如下:
CaO·Al2O3(s)+Na2CO3(l)=CaCO3(s)+2NaAlO2(l)
(14)
12CaO·7Al2O3(s)+12Na2CO3(l)+5H2O(l)=
12CaCO3(s)+10NaOH(l)+14NaAlO2(l)
(15)
2Al(s)+2NaOH(l)+2H2O(l)=2NaAlO2(l)+3H2(g)
(16)
前期通過優化條件,還原渣中氧化鋁溶出率達到85.24%,再經碳酸化分解可得產品氫氧化鋁,如圖10所示。對產品進行XRD分析可知其物相為Al(OH)3,且白度均大于95%,滿足高白氫氧化鋁國家標準要求。
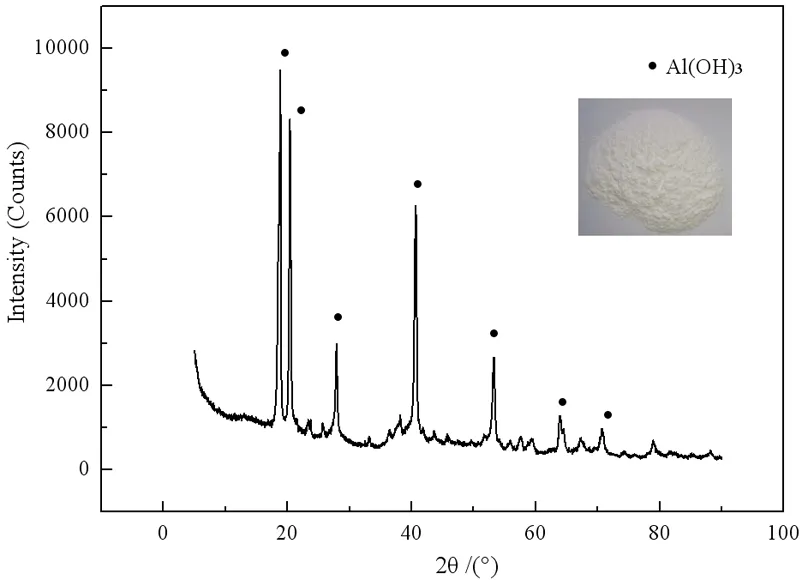
圖10 氫氧化鋁的形貌及XRD
與傳統的金屬熱還原法相比,新型鋁熱還原采用氫氧化鋰為鋰源,常壓煅燒得到富鋰熟料,從而避免了工業上碳酸鋰分解困難的問題, Li5AlO4型富鋰熟料與鋁粉混合制團,真空加熱還原過程料鋰比得到顯著降低,同時還原渣得到資源化利用,該法為真空熱還原煉鋰提供了一種新思路。
6 氫熱還原法
1972年,博恩茲(U.Bernds)以氫為還原劑,在1 100 ℃的溫度下還原制得了金屬鋰,并于1973年申請了專利。氫熱還原法主要是在高純氫氣流中加熱粉狀Li2O 與惰性金屬的混合物,反應過程生成金屬間化合物,然后在高真空的條件下將金屬化合物中鋰蒸餾分離出來,冷凝制得金屬鋰,同時惰性金屬實現循環利用。該方法較為新穎,卻由于操作困難等原因并沒有進行擴大化的試驗,未見有擴大試驗的相關報道。
7 鐵熱還原法
昆明理工大學樊粉霞[21]等在熱力學研究的基礎上,嘗試使用金屬還原劑鐵粉來制備金屬鋰。工藝流程與碳化鈣還原法制備金屬鋰相近,如圖11所示。主要是通過真空加熱使碳酸鋰分解,然后以鐵粉為還原劑與氧化鋰反應,制得金屬鋰。
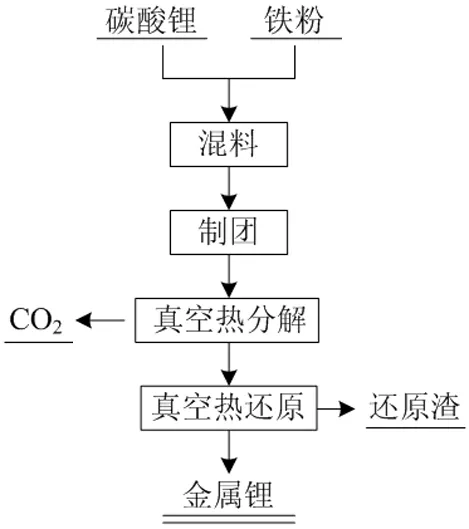
圖11 真空鐵熱還原流程[21]
試驗中金屬鋰的還原率僅為74.1%,還原過程發生的主要反應如式(17)所示。還原過程同時會生成Li2Fe3O5和Li5FeO4等化合物,相對于其它金屬熱還原工藝,鐵熱還原的還原劑比較廉價,而且該工藝將鐵粉與碳酸鋰直接混合反應,省去了碳酸鋰單獨分解的過程,節省了降溫、升溫時間,同時也降低了能耗,但是還原溫度過高,而且金屬鋰的還原率過低,筆者認為基本不具備工業應用的前景。
Li2O(s)+Fe(s)=FeO(s)+2Li(g)
(17)
8 結論
(1)真空熱還原法與熔鹽電解法相比,具有原料成本低、無腐蝕性氣體產生、產品雜質少等優點。以Al、Si及其合金為還原劑的金屬熱還原法流程短、消耗少、成本低、環境友好、最具有工業應用價值。
(2)新型鋁熱還原法以氫氧化鋰替代碳酸鋰,常壓煅燒制備Li5AlO4型富鋰熟料;還原過程理論料鋰比為8.51,可有效降低真空冶金過程的能耗,提高生產效率;且還原渣可實現增值化利用,制備高白氫氧化鋁,是一種高效綠色鋰冶金工藝。
(3)真空熱還原法有著良好的應用前景,但走向工業化還需解決的關鍵問題是:優化還原反應器的冷凝系統以實現鋰蒸氣的定向收集,促進鋰還原率與實收率的同步提升。

