自身免疫性肝炎外周血干擾素γ誘導蛋白16炎癥小體的表達及臨床價值
王建英 張偉陽 鐘建平 許文芳 陳將南 金法祥
自身免疫性肝炎(AIH)是機體對肝細胞產生自身抗體及自身反應性T細胞致肝臟炎性病變。免疫炎性反應常伴隨著炎癥細胞和免疫細胞的浸潤,炎癥因子的大量釋放和淋巴細胞的聚集。干擾素γ誘導蛋白16是干擾素誘導HIN-200家族的一員。近來研究發(fā)現(xiàn)IFI16與多種細胞活動相關,包括炎癥反應、免疫反應、細胞周期調節(jié)等,當病毒、細菌等外源物質侵襲時,IFI16作為細胞核和細胞質異常雙鏈DNA傳感器首先啟動炎病反應,傳遞信號的同時釋放炎性介質促進單核巨噬細胞、淋巴細胞到達受損部位[1],形成宿主抵御病原微生物感染的第一道防線。其在AIH患者外周血中的表達及價值尚不清楚。本文探討IFI16炎癥小體在AIH發(fā)生發(fā)展中的作用,為研究AIH炎癥小體調控機制及治療AIH提供一定的理論依據(jù)。
1 資料與方法
1.1 臨床資料 選取2016年1月至2019年6月本院就診的AIH患者43例,均經肝臟活組織檢查并經臨床確診。診斷標準參考2008年國際免疫性肝炎小組(IAIHG)提出的AIH簡化診斷積分系統(tǒng)及2010年美國肝病學會(AASLD)更新的有關AIH的診斷和治療指南[2-3]。排除肝炎病毒感染、藥物性、酒精性和遺傳代謝性肝病等。激素治療前評分≥15分明確診斷AIH。緩解是指癥狀消失,血清轉氨酶、膽紅素、IgG正常,肝組織正常或無活動性肝硬化[4]。對照組來源于本院同期健康體檢者,均取得患者同意并簽署知情同意書。
1.2 方法 采取患者及健康對照組外周靜脈血,離心后收集血清,ELISA法檢測IFI16和IL-17A的表達水平,并同時檢測炎癥效應分子Caspase-1、IL-1β和IL-18水平。其中IL-17A、Caspase-1、IL-1β和IL-18試劑盒購自eBioscience公司,IFI16試劑盒購自于美國Sigma公司。酶標儀為美國Thermo Multiskan FC。嚴格按試劑說明書操作。
1.3 統(tǒng)計學方法 采用SPSS17.0統(tǒng)計軟件。正態(tài)分布計量資料用(±s)表示,兩組間比較采用student’st檢驗,多組間比較采用方差分析,兩兩比較采用LSD法。計量資料用n(%)表示,組間比較采用χ2檢驗。相關性分析采用Pearson檢驗。P<0.05為差異有統(tǒng)計學意義。
2 結果
2.1 一般資料 43例AIH患者,29例為活動期患者,男2例,女27例;平均年齡(45.60±11.29)歲。14例為緩解期患者,男1例,女13例;平均年齡(46.18±11.56)歲。健康對照組35例,男4例,女31例;平均年齡(47.78±12.26)歲。三組性別、年齡差異無統(tǒng)計學意義(t=0.94,P=0.65)。
2.2 血清IFI16、IL-17與炎癥效應分子在AIH中的表達 見表2。
表2 IFI16、IL-17A與炎癥效應分子在AIH中的表達(±s)
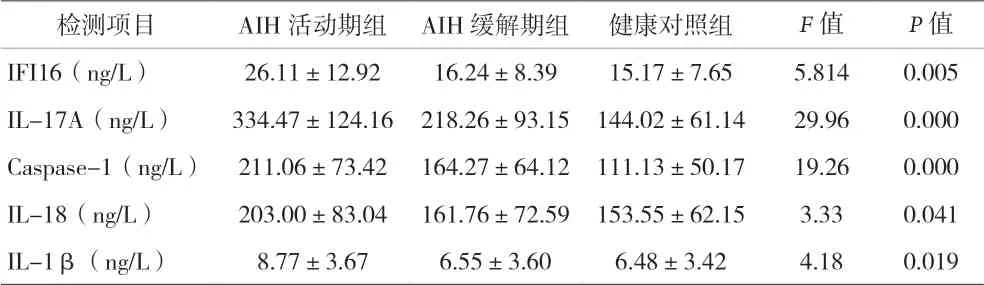
表2 IFI16、IL-17A與炎癥效應分子在AIH中的表達(±s)
檢測項目 AIH活動期組 AIH緩解期組 健康對照組 F值 P值IFI16(ng/L) 26.11±12.92 16.24±8.39 15.17±7.65 5.814 0.005 IL-17A(ng/L) 334.47±124.16 218.26±93.15 144.02±61.14 29.96 0.000 Caspase-1(ng/L) 211.06±73.42 164.27±64.12 111.13±50.17 19.26 0.000 IL-18(ng/L) 203.00±83.04 161.76±72.59 153.55±62.15 3.33 0.041 IL-1β(ng/L) 8.77±3.67 6.55±3.60 6.48±3.42 4.18 0.019
2.3 AIH患者血清IFI16與IL-17及炎癥效應分子相關性分析 AIH患者血清中IFI16表達水平與IL-17、Caspase-1、IL-18和IL-1β水平呈顯著正相關(r=0.534、0.692、0.521、0.596,P<0.001),見圖1~4。

圖1 IFI16表達水平與IL-17的相關性

圖2 IFI16表達水平與Caspase-1的相關性
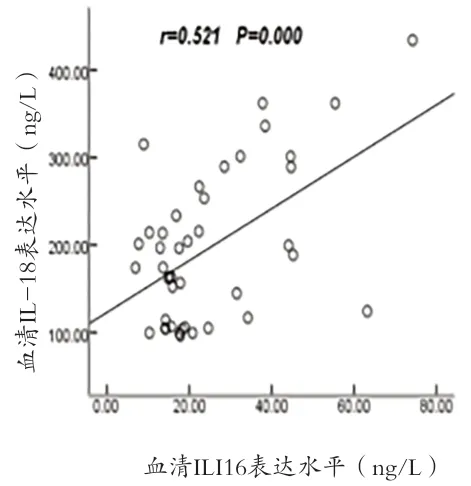
圖3 IFI16表達水平與IL-18的相關性

圖4 IFI16表達水平與IL-1β的相關性
3 討論
炎癥小體基本包含三種蛋白,分別是感受器,如NOD樣蛋白家族(NLRs)和AIM2 樣蛋白家族(ALRs),接頭蛋白凋亡相關斑點樣蛋白(ASC)和效應分子半胱天冬蛋白酶前體(pro-caspase-1)。炎癥小體感受感染性和非感染性刺激后活化Caspase-1,剪切IL-1β、IL-18前體,使其成熟并發(fā)揮促炎作用[5]。干擾素γ誘導蛋白16(IFI16)是近年新發(fā)現(xiàn)的一種細胞核內DNA感受分子,其主要位于細胞核中,識別進入核內的dsDNA,與配體相結合后介導自身炎癥小體的形成及活化[6]。有研究發(fā)現(xiàn)在自身免疫性疾病如系統(tǒng)性紅斑狼瘡中,會出現(xiàn)抗IFI16抗體和IFI16表達增高的現(xiàn)象。最新研究證實,IFI16+細胞的數(shù)量與慢性乙型肝炎(CHB)和HBV相關的慢性肝衰竭(HBV-ACLF)患者的炎癥程度顯著相關,可能是HBV-ACLF肝損傷發(fā)病機制的重要原因[7],表明IFI16可能在炎癥性肝損傷的發(fā)生和發(fā)展過程中具有重要的作用。
Th17細胞是較多類型適應性免疫中IL-17的主要來源,IL-17家族成員主要有IL-17A、IL-17B、IL-17c、IL-17D(IL-27)、IL-17E(IL-25) 及 IL-17F,IL-17家族細胞因子通過靶細胞上的表面受體介導其生物學功能。IL-17RA表達在多種細胞上,在IL-17刺激下誘導促炎分子,導致過度炎癥和明顯的組織損傷。自身免疫性肝炎發(fā)生時,Th17活化增多,并分泌一系列炎癥因子,促進肝臟炎性反應和肝臟損傷[8]。研究證實,在AIH患者血清中IL-17表達增高,在小鼠AIH模型中抑制IL-17能夠減弱炎性肝損傷[9]。研究認為IL-17及產生IL-17細胞與自身免疫性肝病密切相關[10]。Huang等[11]首次確認IL-17C/IL-17RE在AIH發(fā)生中的作用,抑制該軸的活性有可能成為治療該病的新型藥物靶點。
有報道稱IFN-γ,TNF-α,IL-17及IL-22等炎性因子誘導角質形成細胞,能夠上調IFI16的表達[12],但具體機制未明確。本資料結果顯示,AIH患者血清中IFI16、IL-17、Caspase-1、IL-1β和IFI16表達水平均顯著高于健康對照組,并隨疾病緩解而下降,提示IL-17、炎癥小體IFI16及炎癥效應分子均參與AIH炎癥性肝損傷的發(fā)生發(fā)展過程。同時通過相關性分析,發(fā)現(xiàn)外周血IFI16水平與IL-17A、 Caspase-1、IL-18與IL-1β均呈顯著正相關,因此推測在AIH發(fā)病過程中,活化CD4+T細胞向Th17細胞分化,其分泌主要效應因子IL-17誘導上調IFI16表達,促進IFI16對Caspase-1的活化,活化的Caspase-1剪切IL-1β、IL-18前體,成熟的IL-1β和IL-18發(fā)揮促炎作用,誘導肝細胞炎性應答,造成免疫失衡進一步誘發(fā)AIH,但具體機制仍需進一步研究。
綜上所述,IFI16在自身免疫性肝炎發(fā)生發(fā)展中的起重要作用,在AIH發(fā)病過程中由壞死或凋亡細胞產生的自身dsDNA的識別,進而誘導肝細胞炎性應答,但IFI16在AIH發(fā)病機制中的作用尚需探索,明確其作用有可能使其成為AIH早期診斷、治療與預后判斷的一個新的切入點。

