肢體氣壓治療不同程度2型糖尿病周圍神經病變的療效比較
徐英英 魏智利 張婉怡 王陳芳 留菁菁 周蓉
糖尿病周圍神經病變(DPN),是指在排除其他原因情況下,糖尿病(DM)患者出現周圍神經功能障礙相關的癥狀和(或)體征。常見癥狀為肢體麻木、疼痛、灼熱或其他異常感覺[1]。DPN是一種以周圍感覺神經元為早期目標的獨特的神經退行性病變,可伴軸索腫脹或皺縮,髓鞘密度不均勻,空泡變性,或部分神經纖維髓鞘脫失。該病發病機制尚未完全闡明。無癥狀DPN,依靠體征篩查,如肌肉無力和萎縮,肢體局部淺感覺減退、腱反射減弱或消失等,或神經電生理檢查方可診斷[2]。氣壓治療在2型糖尿病(T2DM)下肢神經血管病變患者中的應用目前已經得到認可,其在改善氧供、血供及神經軸索功能方面具有積極作用[3]。本文探討肢體氣壓治療不同程度DPN的療效。
1 資料與方法
1.1 臨床資料 選取2017年1月至2018年12月本院T2DM患者80例,通過振動覺閾值(VPT)測定聯合神經傳導速度(NCV)診斷DPN,結合Toronto臨床評分系統分別選取有癥狀DPN和無癥狀DPN者各40例。有癥狀DPN患者,男21例,女19例;年齡35~80歲,平均年齡(62.7±13.5)歲。無癥狀DPN患者,男20例,女20例;年齡36~78歲,平均年齡(62.1±14.3)歲。將有癥狀DPN患者隨機分A、B兩個亞組;無癥狀DPN患者隨機分C、D兩個亞組;每個亞組各20例。四組患者年齡、性別、病程等一般資料差異無統計學意義(P>0.05)。
1.2 方法 A組和C組(常規治療)均予甲鈷胺注射液500mg肌肉注射,1次/d;α-硫辛酸600mg,靜脈滴注,1次/d,連續用藥 2 周。B組和D組分別在常規治療基礎上加用肢體氣壓治療,7次/周。A、B、C、D四個亞組治療前、治療后分別記錄Toronto臨床評分,并進行肌電圖、振動覺閾值等檢查,觀察藥物安全性。治療前、后均抽血檢測空腹血糖(FBG)、胰島素、C肽、血粘度、血脂等一般生化指標。肢體氣壓治療:將治療儀套筒穿在患者肢體上,拉好拉鏈,將套筒經氣管與主機相連:設定壓力為60~90mmHg,先從低于患者舒張壓的小壓力開始,待適應后,逐漸調大壓力。1次/d,20min/次。治療期間應做好患者病情變化觀察,如出現頭暈、胸悶、心悸等異常即刻停止治療。
1.3 觀察指標 (1)應用肌電圖儀測定腓總神經及脛神經的運動神經傳導速度(MCV),和腓腸神經及腓淺神經的感覺神經傳導速度(SCV)。(2)癥狀評分:采用Toronto臨床評分系統。癥狀分:足部疼痛,發麻針刺,感無力,共濟失調,上肢癥狀;出現一項記1分,無為0分。反射分:膝反射,踝反射;每一側反射消失2分,減退1 分,正常0分,最高分4分。感覺試驗分:針刺覺,溫度覺,輕觸覺,震動覺,位置覺;每出現1次異常記1分,無異常0分;得分越高,神經功能受損越嚴重。總分最高19分。
1.4 統計學方法 采用SPSS19.0 統計軟件。計量資料以(±s)表示,治療前后比較用t檢驗,多組間比較用方差分析,組間兩兩比較用LSD法檢驗,P<0.05為差異有統計學意義。
2 結果
2.1 四組患者治療前SCV和MCV比較 治療前,無癥狀亞組(C、D)患者SCV和MCV均高于有癥狀亞組(A、B)患者,差異有統計學意義(P<0.05);但A、B兩組間及C與D兩組間的SCV和MCV差異均無統計學意義(P>0.05)。見表1。
表1 四組患者治療前SCV和MCV比較[m/s,(±s)]
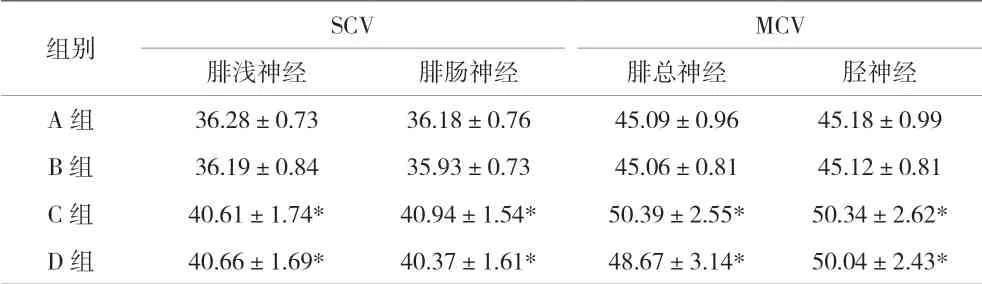
表1 四組患者治療前SCV和MCV比較[m/s,(±s)]
注:與A、B組比較,*P<0.05
組別 SCV MCV腓淺神經 腓腸神經 腓總神經 脛神經A組 36.28±0.73 36.18±0.76 45.09±0.96 45.18±0.99 B 組 36.19±0.84 35.93±0.73 45.06±0.81 45.12±0.81 C組 40.61±1.74* 40.94±1.54* 50.39±2.55* 50.34±2.62*D組 40.66±1.69* 40.37±1.61* 48.67±3.14* 50.04±2.43*
2.2 四組患者治療前、后SCV和MCV比較 治療后各組患者的SCV和MCV均高于其治療前水平,但每組治療前后差異均無統計學意義(P>0.05)。四組DPN患者,治療后NCV數值比較:B組>A組,D組>C組,但A與B兩組間及C與D兩組間,差異均無統計學意義(P>0.05)。見表2。
表2 四組患者治療前、后SCV和MCV比較[m/s,(±s)]
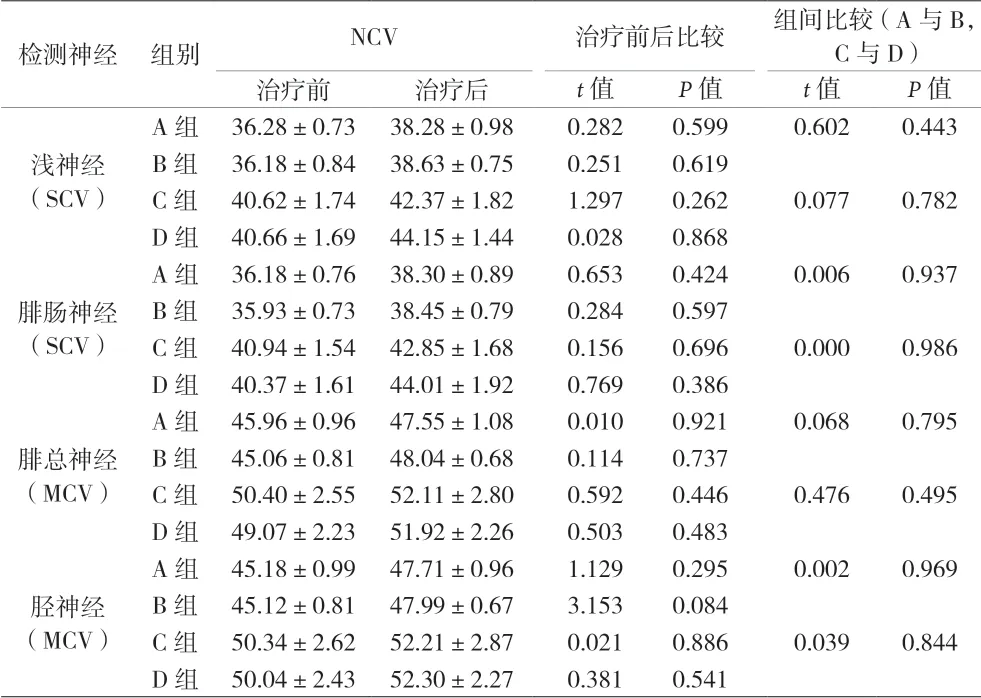
表2 四組患者治療前、后SCV和MCV比較[m/s,(±s)]
檢測神經 組別 NCV 治療前后比較 組間比較(A與B,C與D)治療前 治療后 t值 P值 t值 P值淺神經(SCV)A組 36.28±0.73 38.28±0.98 0.282 0.599 0.602 0.443 B組 36.18±0.84 38.63±0.75 0.251 0.619 C組 40.62±1.74 42.37±1.82 1.297 0.262 0.077 0.782 D組 40.66±1.69 44.15±1.44 0.028 0.868腓腸神經(SCV)A組 36.18±0.76 38.30±0.89 0.653 0.424 0.006 0.937 B組 35.93±0.73 38.45±0.79 0.284 0.597 C組 40.94±1.54 42.85±1.68 0.156 0.696 0.000 0.986 D組 40.37±1.61 44.01±1.92 0.769 0.386腓總神經(MCV)A組 45.96±0.96 47.55±1.08 0.010 0.921 0.068 0.795 B組 45.06±0.81 48.04±0.68 0.114 0.737 C組 50.40±2.55 52.11±2.80 0.592 0.446 0.476 0.495 D組 49.07±2.23 51.92±2.26 0.503 0.483脛神經(MCV)A組 45.18±0.99 47.71±0.96 1.129 0.295 0.002 0.969 B組 45.12±0.81 47.99±0.67 3.153 0.084 C組 50.34±2.62 52.21±2.87 0.021 0.886 0.039 0.844 D組 50.04±2.43 52.30±2.27 0.381 0.541
2.3 四組患者治療前后NCV差值比較 見表3。
表3 四組患者治療前后NCV差值比較[m/s,(±s)]
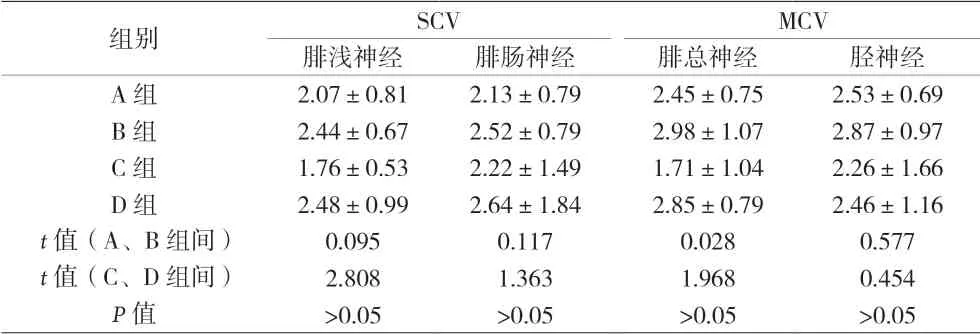
表3 四組患者治療前后NCV差值比較[m/s,(±s)]
組別 SCV MCV腓淺神經 腓腸神經 腓總神經 脛神經A組 2.07±0.81 2.13±0.79 2.45±0.75 2.53±0.69 B組 2.44±0.67 2.52±0.79 2.98±1.07 2.87±0.97 C組 1.76±0.53 2.22±1.49 1.71±1.04 2.26±1.66 D組 2.48±0.99 2.64±1.84 2.85±0.79 2.46±1.16 t值(A、B組間) 0.095 0.117 0.028 0.577 t值(C、D組間) 2.808 1.363 1.968 0.454 P值 >0.05 >0.05 >0.05 >0.05
2.4 四組患者臨床癥狀評分比較 見表4。
表4 四組患者臨床癥狀評分比較(±s)

表4 四組患者臨床癥狀評分比較(±s)
組別 n 治療前癥狀評分 治療后癥狀評分 t值 P值A組 20 9.95±0.85 7.50±1.47 7.012 <0.001 B組 20 10.05±1.03 7.15±0.98 7.486 <0.001 C組 20 7.01±0.79 5.55±0.82 5.659 <0.001 D組 20 6.95±0.83 4.85±0.67 8.732 <0.001
3 討論
DM各個階段均可發生DPN,甚至早期即可出現,是T2DM重要的慢性并發癥之一。中華醫學會糖尿病學分會(CDS)最新的流行病學調查統計發現,DPN發生率達60.3%[4],甚至有國外文獻報道高達>90%。
CDS[5]和美國糖尿病學會(ADA)糖尿病防治指南中[6],DPN診斷的基本條件及分層診斷基本一致[7]。其診斷DPN的基本條件為:(1)明確的DM病史;(2)診斷DM時或之后出現的神經病變;(3)臨床癥狀和體征與DPN的表現相符;(4)有臨床癥狀(疼痛、麻木、感覺異常等)者,5項檢查(踝反射、針刺覺、震動覺、壓力覺、溫度覺)中任1項異常,臨床診斷為DPN。DPN 發病機制尚未完全清楚,是由多種因素綜合作用的結果[8]。目前主要認為是多因素影響致使微血管內皮細胞受到較大損傷,引起血流動力學發生改變,周圍神經組織隨之發生缺氧、缺血并引發自由基增多、脂質代謝異常、神經生長因子缺乏[9-12],屬植物神經病變。中年DM患者神經活檢顯示早期原發性遠端軸突萎縮和髓鞘變性或破壞[13]。本資料結果顯示,治療前,C和D兩個無癥狀亞組DPN 患者腓淺和腓腸神經的SCV及腓總和脛神經的MCV均高于A、B兩組有癥狀亞組DPN 患者,差異有統計學意義(P<0.05);但A、B兩組間及C、D兩組間SCV和MCV差異均無顯著性意義(P>0.05)。表明不論有無癥狀的DPN患者,其NCV均有不同程度的下降,有癥狀患者NCV下降程度更嚴重。
甲鈷胺是一種活性維生素B12衍生物和蛋氨酸合成酶的輔酶,在甲基轉移中具有輔酶作用,能夠有效促進神經細胞內用于組成軸突的結構蛋白、核酸、脂質和髓鞘形成磷脂的合成,使軸突受損區域的組織、細胞修復和乙酰膽堿等神經遞質生成,促進軸索、軸漿再生,加速神經傳導,從而修復受損神經和改善NCV[14]。
硫辛酸是一種既能滲透到身體脂溶性部分又能滲透到水溶性部分的抗氧化劑,抗氧化能力更強[15]。其主要作用機制為清除自由基、降低脂質過氧化,增加神經營養血管的血流量、改善NCV、增加神經Na-K-ATP 酶活性[16]。
現代神經電生理學研究表明[17]甲鈷胺聯合α- 硫辛酸明顯提高NCV,修復受損神經,效果顯著,能夠明顯地改善患者癥狀,提升患者的生活質量,不良反應小。治療后四組患者腓淺和腓腸神經的SCV及腓總和脛神經的MCV均較治療前有升高,進一步表明甲鈷胺聯合α- 硫辛酸治療基礎上,無論是否加用肢體氣壓治療,對DPN患者均有一定的療效。
硫辛酸注射液聯合肢體氣壓治療DPN,兼顧DPN的多元醇通路亢進及神經缺血缺氧的病因,從而達到改善和恢復神經組織功能的目的[18]。本資料顯示,治療前后NCV差值組間比較:B組>A組,D組>C組,但B組與A組、D組與C組,差異均無統計學意義(P>0.05)。無論是否加用肢體氣壓治療,治療后四組患者的臨床癥狀評分均低于治療前(P<0.01)。提示治療后B組和D組的NCV改善程度高于A組和C組,表明在甲鈷胺聯合α- 硫辛酸治療基礎上,加用肢體氣壓治療可以進一步增加療效,主要表現在癥狀評分的差異,但不能明顯改善患者的NCV。
氣壓治療臨床應用較多,使用簡便。DM患者使用氣壓治療后血流灌注和氧合作用明顯增加,且提高神經的耗氧量從而達到改善功能的目的[19]。陳媛等[20]研究發現在T2DM下肢周圍神經病變患者中的應用可有效改善肢體動脈缺血及全身血液循環,利于患者神經癥狀的緩解及缺血狀態的改善,具有較高臨床價值。
綜上所述,氣壓治療為決定療效差異的主要因素,其為DPN的純物理性治療手段,將肢體氣壓治療儀應用在早期DM足疾病的治療中,可以對患者病情進行有效控制,增強治療效果,進而改善患者生活的整體質量。且肢體氣壓治療的操作方法比較簡便、安全性較高,值得在臨床中應用[21]。

