血清骨硬化蛋白 TRAP-5b在維持性血透慢性腎臟病-礦物質和骨異常診斷中的應用價值
李潤芝 祝靈英
慢性腎臟病(CKD)是一個全球性的公共衛生問 題,影響全球近5%~10%的人口。隨著腎功能的逐漸減退,礦物質代謝紊亂,表現為血清和組織中磷和鈣濃度的改變,以及甲狀旁腺激素(PTH)、維生素D等激素水平的變化[1]。腎繼發性甲狀旁腺功能亢進、CKD礦物質和骨異常(CKD-MBD)是CKD最常見的并發癥。尤其是維持性血液透析患者,隨著透析時間的延長,出現鈣磷代謝紊亂,PTH水平升高,最后導致CKD-MBD和動脈鈣化,是增加患者心腦血管死亡率的危險因素[2-3]。臨床上用于監測CKD-MBD病情的傳統標志物是血鈣、血磷、iPTH等,而在CKDMBD發生早期,血鈣、血磷等幾乎均在正常范圍內,近年有研究指出一些非傳統代謝標志物,如成纖維細胞生長因子-23(FGF-23)、骨硬化蛋白(SOST)等[4-5]變化可能早于血鈣和血磷,與傳統標志物聯合檢測有利于提高疾病診斷的敏感度。本文探討SOST、抗酒石酸酸性磷酸酶5b(TRAP-5b)輔助傳統指標血鈣、血磷及PTH對維持性血透CKD-MBD的診斷價值。
1 資料與方法
1.1 臨床資料 選擇2015年10月至2019年10月本院透析中心收治的維持性血液透析患者210例。(1)納入標準:①年齡18~65歲,符合最新KDIGO關于CKD G5期的診斷標準者[6];②神志清楚,無認知能力下降,能正常溝通交流;③透析時間>3個月,透析2~3次/周,且近2周透析干體質量平穩。(2)排除標準:①意識模糊或有嚴重精神疾病;②合并嚴重心腦血管疾病以及其他感染性疾病;③合并腫瘤及自身免疫性疾病者。
1.2 方法 收集入選維持性血液透析患者的一般資料和臨床生化指標。一般資料主要包括年齡、性別、BMI、基礎腎病、飲食習慣、磷酸鹽結合劑藥物服用的持續時間等。臨床生化指標主要包括血紅蛋白(Hb)、血尿素氮(BUN)、血肌酐(SCr)、腎小球濾過率(eGFR)、血鈣、血磷、PTH、血清SOST和TRAP-5b。其中,血清SOST和TRAP-5b水平均采用酶聯免疫吸附法測定,試劑盒均購自上海江萊生物,嚴格按照試劑盒說明書進行。對納入維持性血液透析的CKD患者進行統計分析,按照CKD-MBD診斷標準[7]計算其發病率,并將發生CKD-MBD的患者設為觀察組,未發生的設為對照組。
1.3 統計學方法 采用SPSS20.0統計軟件。計量資料以(±s)表示,用t檢驗;計數資料以%表示,用χ2檢驗,采用ROC曲線下面積分析診斷價值。以P<0.05為差異有統計學意義。
2 結果
2.1 一般情況 210例維持性血液透析CKD患者中,CKD-MBD 152例(72.3%)。男97例,女55例;年齡(46.65±17.35)歲。慢性腎炎42例,糖尿病腎病42例,高血壓腎病37例,其他腎病28例。而未發生CKDMBD的對照組男35例,女23例;年齡(47.24±15.21)歲。慢性腎炎19例,糖尿病腎病18例,高血壓腎病14例,其他腎病7例。兩組患者一般情況比較,差異無統計學意義(P>0.05)。
2.2 兩組患者臨床生化指標比較 見表1。
表1 兩組患者臨床生化指標比較(±s)
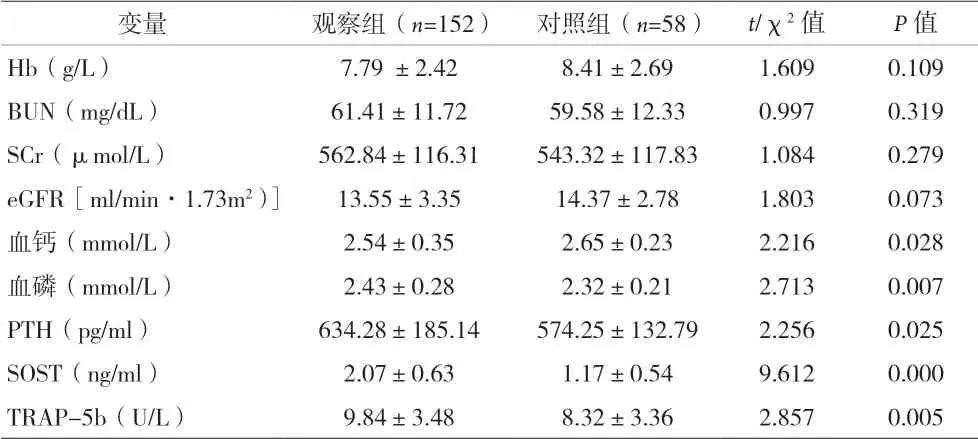
表1 兩組患者臨床生化指標比較(±s)
變量 觀察組(n=152) 對照組(n=58) t/χ2值 P值Hb(g/L) 7.79 ±2.42 8.41±2.69 1.609 0.109 BUN(mg/dL) 61.41±11.72 59.58±12.33 0.997 0.319 SCr(μmol/L) 562.84±116.31 543.32±117.83 1.084 0.279 eGFR[ml/min·1.73m2)] 13.55±3.35 14.37±2.78 1.803 0.073血鈣(mmol/L) 2.54±0.35 2.65±0.23 2.216 0.028血磷(mmol/L) 2.43±0.28 2.32±0.21 2.713 0.007 PTH(pg/ml) 634.28±185.14 574.25±132.79 2.256 0.025 SOST(ng/ml) 2.07±0.63 1.17±0.54 9.612 0.000 TRAP-5b(U/L) 9.84±3.48 8.32±3.36 2.857 0.005
2.3 SOST、TRAP-5b聯合血鈣、血磷及PTH檢測在維持性血透CKD-MBD中的診斷效能 ROC曲線結果,SOST、TRAP-5b聯合血鈣、血磷及PTH檢測在維持性血透CKD-MBD中的ROC曲線下面積最大為0.902,差異有統計學意義(P<0.05),聯合檢測的診斷敏感性為82.24%,特異性為87.93%。見表2、圖1。
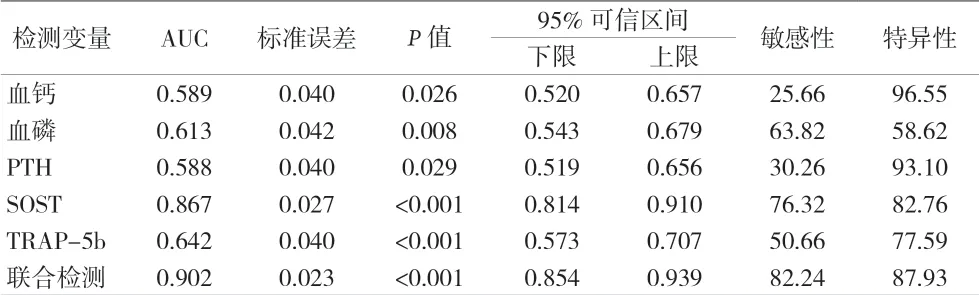
表2 SOST、TRAP-5b聯合血鈣、血磷及PTH檢測對維持性血透CKD-MBD的診斷效能

圖1 SOST、TRAP-5b聯合血鈣、血磷及PTH檢測在維持性血透CKD-MBD中的ROC曲線分析
3 討論
CKD-MBD是由于慢性腎臟病導致的礦物質及骨代謝異常綜合征,臨床上常表現為鈣、磷、PTH或維生素D代謝異常,骨線性生長或骨強度異常,血管或其他軟組織鈣化。雖然骨活檢是診斷CKD-MBD的金標準,但由于臨床操作困難,對于CKD G3-G5期患者不要求進行常規骨活檢,而是結合多項生化指標的監測[8]。鈣磷、PTH和骨化三醇紊亂是CKD的常見癥狀,與CKD-MBD的發生密切相關。CKD早期,確保從食物中吸收的磷能完全排泄出去,FGF-23水平增加,1,25-D水平下降,腸道鈣磷吸收減少,為維持礦物質動態平衡,FGF23、骨化三醇、PTH與礦物質鈣磷相互作用[9]。PTH主要由甲狀旁腺的主細胞產生,參與礦物質的代謝。高鈣血癥不僅減少PTH的整體分泌,且有助于PTH片段的釋放,而低鈣血癥刺激PTH的整體分泌,有利于PTH片段的釋放。當腎功能進一步減退,腎小球的濾過率下降,維持礦物質動態平衡與正常骨骼轉運能力進行性丟失,血鈣水平下降,血磷升高,刺激PTH分泌,促成甲狀旁腺功能亢進的惡化,腎單位進一步減少,1-α羥化酶受阻,維生素D代謝異常,對骨的作用減少,引起骨病[10]。
此外,與CKD礦物質及骨代謝異常密切相關的還有SOST和TRAP-5b。有研究表明,血清SOST水平隨著CKD分期的進展而升高,尤其是維持性血液透析患者[11]。本資料結果顯示,觀察組血鈣水平低于對照組,而血磷、PTH、SOST及TRAP-5b水平均高于對照組(P<0.05)。近年來,CKD的總體預后欠佳,其并發癥和病死率增加,人們也越來越擔心CKD的礦物質和骨代謝紊亂以及用于糾正這些異常的治療可能導致骨骼外鈣化。大量研究表明,CKD患者礦物代謝紊亂與骨折、心血管疾病和死亡率間存在關聯[12-13]。
與此同時,CKD G5期患者高轉化性骨病診斷中,對于該病的陽性預測,SOST優于iPTH;而該病的陰性預測,則iPTH優于SOST,即同時考慮這兩種激素血清水平更有助于CKD患者骨轉化的準確評估[14]。SOST是一種主要由骨細胞分泌的糖蛋白,目前被認為是骨形成的負性調節因子,缺乏可致人骨密度增高。SOST已被證明是堿性磷酸酶活性的主要抑制劑,可以減少骨形成和血管鈣化,提示血清中SOST可能是抗血管鈣化的保護性因素[15]。而TRAP-5b由破骨細胞產生,并在各種代謝性骨疾病中表現為血清濃度增加。將CKD合并骨折的患者與無骨折的患者進行比較,發現TRAP-5b在骨折患者中高29%[16]。因此,本研究為評估SOST、TRAP-5b輔助傳統標志物對CKDMBD的診斷價值,采用ROC曲線分析不同臨床指標對CKD-MBD的診斷效能,結果顯示SOST、TRAP-5b聯合血鈣、血磷及PTH檢測在維持性血透CKD-MBD中的ROC曲線下面積最大為0.902,有統計學意義(P<0.05),聯合檢測的診斷敏感性為82.24%,特異性為87.93%。總之,SOST、TRAP-5b聯合血鈣、血磷及PTH檢測在維持性血透CKD-MBD中能獲得較高的診斷效能,對疾病的治療和預防具有重要意義。

