病毒是什么
fam
病毒,一種地球上最微小同時又是數量最多的生命形式。據估計,如果把地球上的病毒首尾相接,能連成一條2億光年的長鏈。病毒無處不在,空氣、大海、土壤乃至南極冰層中都能找到它們的身影。
病毒的定義通常是:一類非常小的、寄生在細胞中的非細胞結構,一般由單一類型的核酸(DNA或RNA)組成的基因組和包裹著核酸的蛋白質構成,有些病毒還含有由脂質和蛋白質組成的包膜。
衡量病毒大小的單位通常是納米(nm)和微米(μm),典型的病毒大小在0.02μm~0.2μm間,無法用普通光學顯微鏡看到。(作為對比,典型的細菌直徑在0.5μm~5μm之間。)菜豆畸矮病毒是最小的病毒之一,直徑僅10nm左右。而從阿米巴原蟲體內分離得到的潘多拉病毒則是目前發現的最大的病毒,它呈橢圓形,長徑可達1μm。
研究病毒的病毒學
病毒學(Virology)是以病毒(virus)這一特殊的生命形態為研究對象的自然科學,有時被視為微生物學的下級學科。病毒學研究的內容包括病毒的結構、分類和進化、感染和利用宿主細胞繁殖的方式、與宿主在生理和免疫方面的相互作用、病毒引起的疾病、分離和培養病毒的技術及其在研究和治療中的應用等。
雖然病毒的概念直到19世紀末期才出現,但病毒病自古就有記載。隨著科學技術的進步,病毒研究獲得了巨大的發展,病毒學的發展歷程大體上可分為三個階段——
經驗認識階段
病毒病在古代就有相關記載。
公元前1400年——在公元前1400年古埃及首都的一塊石碑上,刻畫了一位牧師布道的場景,牧師的腿呈現出脊髓灰質炎導致的殘疾。
公元前4世紀——公元前4世紀,古希臘的亞里士多德記述了患狂犬病的犬表現出瘋狂、暴怒的癥狀,并可通過噬咬將類似的病狀傳給其他動物和人。
公元前1144年——逝世于公元前1144年的埃及法老拉美西斯五世,其木乃伊顯示他曾感染天花病毒。
公元2世紀——公元2世紀,奧勒里安努斯對患狂犬病的表現做了清楚的描述:被咬傷后,起初常有莫名的焦躁、易怒、厭水,最后發展到恐水。
宋代——在昆蟲病毒方面,我國宋代農學家陳旉在《農書》中記載了家蠶“高節”“腳腫”等病癥,現在我們知道這是由家蠶核型多角體病毒①引起的疾病。
16世紀——天花在我國流行也有數千年的歷史,到了16世紀,我國先人發明了人接種法來預防天花。明朝隆慶年間,人痘法從我國傳到了俄國、日本、朝鮮、土耳其、英國等國。當時的人痘接種有很嚴重的副作用,且接種死亡率很高。
1796年——1796年,英國醫生愛德華-詹納發明了用牛痘接種預防天花的方法,并留下了豐富、詳細的記錄。牛痘被認為是世界上最早的疫苗,詹納發明牛痘也被認為是現代免疫學的奠基事件。
17世紀早期——在17世紀早期,荷蘭人發現有些郁金香開出了具有條斑的花朵,他們認為這樣的花比原本單色的花朵更美。這被認為是第一個被記載的植物病毒病——郁金香碎色花病。
1884年——法國人巴斯德在1884年發明了狂犬病疫苗,對狂犬病的治療做出了巨大貢獻。
人類對于諸如此類的病毒性疾病的認識和研究,都為病毒的發現創造了條件。
①核型多角體病毒一種特異性針對昆蟲的病毒,其加工制劑被人類用作殺蟲劑,已有近半個世紀的歷史。
LINK
為了追求具有條斑的特殊郁金香花朵,當時一株受感染植株的球莖或種苗,可以換到數頭公牛、豬或綿羊,幾噸谷物,甚至一個磨坊。由于當時并不知道郁金香花出現條斑的具體原因,無法確保后代花朵的顏色,球莖買賣也就帶上了賭博的性質,并由此引發了全球第一次經濟泡沫。荷蘭阿姆斯特丹的博物館至今還保存著1619年荷蘭畫家所繪制的一幅得病的郁金香靜物畫。
病原研究階段
19世紀中葉——19世紀中葉,顯微鏡被發明出來后,人們逐漸認識到了細菌、真菌等微生物。
1840年——1840年,德國科學家雅各布-亨勒提出了一個假說,認為還存在一種比細菌更小的、顯微鏡看不到的、有感染性的微生物。19世紀后期——19世紀后期,病原發生學說已經得到了普及,亨勒的學生羅伯特·科赫提出了著名的科赫法則②。很快,科赫法則成了主導醫學微生物學實驗的經典方法,而一些不符合科赫法則的現象,促使人們思考,進而發現了病毒。
1879年——煙草花葉病毒的發現在病毒學發展史上有著劃時代的意義,這可以歸功于三位科學家的重要貢獻。
1886年
1892年
1898年
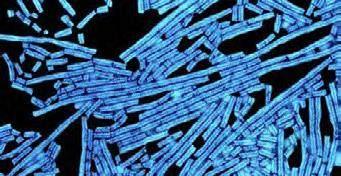
煙草花葉病毒
煙草花葉病毒
1898年——在接近的歷史時期,1898年,德國微生物學家洛菲爾和菲洛施發現,引起牛口蹄疫的病原也可以通過細菌濾器。
1911年——1911年,美國生物學家勞斯發現了引起雞惡性腫瘤的勞斯肉瘤病毒。
1915年——1915年,托沃特觀察到了葡萄球菌會產生噬菌斑的現象。
1917年——1917年,代列耳發現了細菌裂解現象,并將裂解因子命名為噬菌體。
20世紀20年代——接下來的幾十年間,流感、脊髓灰質炎、狂犬病、兔黏液瘤、馬鈴薯卷葉病、馬鈴薯條斑病、黃瓜花葉病、小麥花葉病等的病原體相繼被發現。
②科赫法則
要證實某種微生物是某種疾病的病原,需要滿足四個條件:1.在每一病例中都出現相同的微生物;2.這種微生物可以通過培養被分離出來;3.用培養出來的微生物接種敏感宿主,會引發同樣的疾病;4.從實驗中發病的宿主體內能再次分離培養出這種微生物。
1879年,德國科學家阿道夫-邁耶應荷蘭農民的請求,開始研究煙草的一種疾病,他將其命名為煙草花葉病。這種病可以通過患病葉子的汁液傳播,但卻無法從中分離培養出細菌或真菌,因此,1886年他發表文章指出,煙草花葉病的病原可能是一種類似酶樣的可溶物。
幾年后,俄國科學家伊萬諾夫斯基重復和證實了邁耶的實驗,并進一步發現,用可以過濾掉細菌的陶瓷濾器將病葉汁過濾之后,葉汁仍然具有感染性。1892年,他向圣彼得堡科學院報告,認為通過細菌濾器的病原是一種毒素。
1898年,邁耶的荷蘭同事馬丁努斯·拜耶林克在不了解伊萬諾夫斯基工作的情況下,也進行了過濾的實驗,此外他還進行了稀釋、瓊脂擴散等實驗,總結出煙草花葉病的病原有三個特點:1.比細菌更小,能通過細菌濾器;2.只能在細胞內繁殖;3.不能在培養基等體外非生命物質中生長。據此,拜耶林克將這種病原稱為“有感染性的活的液體”,并將其賦予拉丁名“virus”,從而開啟了病毒學獨立發展的歷程。
現代病毒學研究階段
20世紀30年代——20世紀30年代,生物化學界掀起了“蛋白質熱”,人們開始了對病毒的化學本質和結構的研究。
1935年——1935年,美國生物化學家德溫爾·斯坦利得到了煙草花葉病毒的晶體,X射線衍射顯示它由重復的單元構成,斯坦利因此獲得了1946年的諾貝爾化學獎。這也為后來的沃森和克里克提出“多數簡單的病毒都是由一種或幾種蛋白質重復所構成的”這一理論打下了基礎。
1956年——1956年,煙草花葉病毒的遺傳物質被證實為RNA,這也是首次證明RNA可以作為遺傳物質。
1950年后——1950年后,分子生物學迅速興起、飛躍發展,噬菌體的研究也帶動了整個病毒學和分子生物學的發展。病毒學輻射發展出了疫苗、抗病毒藥物、病毒載體、病毒與腫瘤等許多不同的方向。
③支原體
是一種沒有細胞壁,只有細胞膜的簡單原核生物,能在無生命的人工培養基上生長繁殖。支原體直徑一般是0.1~0.3μm,僅為細菌的1/10,可以通過細菌濾器。
④衣原體
是一類在細胞內寄生、有獨特發育周期的原核細胞性微生物,它也能通過細菌濾器,直徑為0.3~0.5μm。
⑤立克次體
是一類嚴格細胞內寄生的原核細胞型微生物。立克次體可以是球桿狀或桿狀,還有時出現長絲狀體,通常體長為0.3~0.8μm,寬0.3~0.5μm。它比支原體和衣原體更大,無濾過性,一般可在光學顯微鏡下觀察到。
病毒的分類
病毒是嚴格的細胞內寄生物,幾乎可以感染所有的細胞生物。且病毒具有高度的宿主特異性,某一種病毒只能感染特定的一類宿主,甚至只能感染特定的一種宿主。根據病毒的宿主性質,可以將其劃分為微生物病毒、植物病毒和動物病毒。細菌病毒也叫噬菌體,是較早就被發現的一類病毒。隨著研究的發展,人們發現真菌、支原體⑨、衣原體④、立克次體⑤等也有被病毒感染的情況。
需要指出的是,按照宿主性質來劃分,界限有時是模糊的,例如一些脊椎動物病毒、植物病毒能以無脊椎動物、真菌為傳播介體,有的只是機械地將病毒從一個宿主體內帶到另一個宿主體內,有的卻能支持病毒的增殖。感染人類的病毒屬于動物病毒,其中有一些只能感染人類,更多的則是人和動物共患的病毒。
20世紀70年代,病毒學家巴爾的摩根據病毒基因組的存在形式和轉錄特征,將病毒分為6類:雙鏈DNA病毒、單鏈DNA病毒、正鏈RNA病毒、負鏈RNA病毒、逆轉錄病毒和擬逆轉錄病毒。這套分類系統對病毒的復制類型進行了科學歸類,至今仍在使用。
為了讓病毒的分類命名標準化,病毒學家們成立了國際病毒分類委員會(ICTV),建立了一套復雜、完善的命名系統,以拉丁文命名病毒的域、門、綱、目、科、屬、種。ICTV給病毒分類命名主要依據以下8個方面的內容:1.核酸的類型、結構和相對分子質量;2.病毒的形狀和大小;3.病毒的形態和結構;4.病毒對脂溶劑的敏感性;5.病毒的抗原性質和血清學關系;6.病毒在宿主體內活動和細胞培養方面的特性;7.病毒對除脂溶劑外,其他化學和物理因素的敏感性;8.病毒的流行病學特性。
人們推測,地球上真核生物的種類可能有8700萬,按每個物種攜帶10種病毒計算,目前ICTV已經登記的病毒種類,也就是人類已經發現的病毒種類,可能只占實際病毒種類數的百分之一。
病毒感染
人一生中可能被多種病毒攻擊,已知的人類傳染病中約80%的病原體是病毒。天花、流感、普通感冒、肝炎、水痘、帶狀皰疹、脊髓灰質炎、狂犬病、埃博拉病毒病和艾滋病等等,都是病毒性疾病的例子,甚至某些類型的癌癥也與病毒感染有關。
病毒的感染由接觸敏感細胞開始,因此,對于讓人類患病的病毒來說一一如果敏感細胞分布在呼吸道,病毒就通過飛沫、氣溶膠等形式傳播;如果敏感細胞分布在消化道,病毒就通過口—口、糞—口等途徑傳播;如果敏感細胞是血細胞,病毒就需要通過輸血或污染的傷口等途徑才能感染新宿主……以此類推。病毒根據自身特點,會在最適合其復制和傳播的組織器官來完成其主要復制過程,這種對靶器官的選擇性被稱為組織嗜性。決定病毒組織嗜性的因素至少包括:病毒對宿主細胞的可接觸性、病毒感染所需受體在宿主細胞表面的分布、病毒復制對細胞內差異性表達產物的依賴程度、細胞自身的天然免疫特性。
但病毒不一定都是導致我們患病的,事實上,人人體內都有病毒。在人類基因組中,有50%的DNA來源于逆轉錄病毒、逆轉座子⑥、DNA轉座子⑦、假基因等,其中人類內源性逆轉錄病毒(HERV)約占8%,這些HERV被認為起源于一些已經消失了的逆轉錄病毒,它們在距今4000萬至1億年前整合到了靈長類祖先的生殖細胞中,并在進化中產生了重要影響。例如,HERV-W的一種包膜蛋白Env可特異性地在人體胎盤組織中表達,其表達產物合胞素被認為在人類的胚胎發育中發揮重要作用。
⑥逆轉座子
在基因組內存在著通過DNA轉錄為RNA后,再經逆轉錄成為cDNA并插入到基因組的新位點上的因子,就被稱為逆轉座子。
⑦DNA轉座子
DNA轉座即移位,DNA轉座子是一類可在基因組上自由移動的遺傳元件。
⑧Western blot
即蛋白質印跡法(免疫印跡試驗),是分子生物學中研究蛋白的經典方法,應用于從蛋白質混合物中檢出目標蛋白質、定量或定性確定細胞或組織中蛋白質的表達情況,以及用于蛋白質一蛋白質、蛋白質-DNA、蛋白質-RNA相互作用的后續分析。

病毒檢測
病毒學的檢測方法很多,但有一項傳統、經典的方法一直到今天都是金標準,那就是從細胞培養物中分離病毒,其他檢測方法必須與之進行對比參照。動物細胞的培養通常使用含有鹽類、葡萄糖、維生素、氨基酸、抗菌藥物、緩沖劑以及血清的培養基,它提供了必要的細胞生長的條件。
直接觀察病原體
這是最直接的病毒檢測和鑒定方法。大多數病毒的形態特征足以將圖像識別為病毒,并將新發現的未知病毒歸入相應的家族。此外,某些暫時沒能成功培養的病毒也可以通過電子顯微鏡檢測出來。
血清學試驗
這種檢測方法也是比較常用的,通常是檢測特定病毒抗體的存在與否。某些抗體的存在表明被試者已經暴露于該病毒了。一些可以用來鑒定病毒抗體的實驗方法包括紅細胞凝集試驗、補體結合試驗、放射免疫試驗、免疫熒光、酶聯免疫吸附試驗、放射免疫沉淀和Western blot⑧等。
分子技術
如聚合酶鏈式反應,也被廣泛用于檢測病毒。PCR檢測的一些不同應用可以在診斷性臨床病毒學中實施,也可以用于研究目的。這種以核酸為中心的技術使用在病毒檢測方面取得了實質性進展,并且可以通過某些核酸雜交技術的結合而得到進一步加強。
人體免疫系統
免疫系統有三大基本功能:免疫防御、免疫監視、免疫自穩。
一、免疫防御:指機體抵御病原體的入侵、攻擊已入侵的病原體和其他有害物質。
1.免疫防御功能過低或缺陷
這時,就會被正常情況下不能感染人體并致病的病原體感染,并表現出癥狀,或發生正常情況下不會發生的腫瘤。
艾滋病的診斷標準之一就包括出現卡波西肉瘤等腫瘤或是卡氏肺囊蟲肺炎等機會性感染,必須要HIV感染后幾年甚至十幾年,免疫系統功能已經被損害了,出現這些情況,才叫作艾滋病患者,而不是被HIV感染后立刻變成艾滋病患者。
“我體質差、我容易感冒、我容易拉肚子、我容易口腔潰瘍”,這些都不能成為判定“免疫防御功能過低或缺陷”的充分條件,因為疲勞、感冒、腹瀉和口腔潰瘍都是正常情況下在健康人身上可能發生的,對特定傳染病或自限性疾病的易感性與基因和環境有關。
2.免疫防御功能過高
①免疫應答強度過高或持續時間過長,在清除病原體的同時,免疫應答過程中被激活的免疫細胞和高表達的免疫分子就會導致機體損傷,通俗點說,就是正常情況下殺敵一千自損八百,功能過高則殺敵一千自損八萬。
②功能異常,發生過敏等超敏反應,對不必攻擊的外來對象發動了攻擊,且因為不必要的殺敵行為導致了只要殺敵就必然發生的自損副作用。
二、免疫監視:指機體識別和清除體內的異常物質的能力,這些異常物質包括表達新抗原的突變細胞(包括腫瘤細胞)、被病毒感染的細胞等。
當這一功能出現異常時,將不能正確識別、及時清除異常,可導致腫瘤、持續性病毒感染等情況的發生。
三、免疫自穩:指機體通過自身免疫耐受和免疫調節兩種主要的機制來達到免疫系統內環境的穩定。
如果這一功能出現異常,將不能正確識別“自我”與“非我”,免疫調節功能紊亂,可導致自身免疫病的發生,也就是免疫系統把自身正常組織細胞視為敵人發動攻擊。
疫苗的工作原理
我們前面說到,人體免疫系統的功能之一是識別外來者并加以清除,每個人的細胞表面都有自身獨有的一套識別分子,就像是一套通行證一樣,免疫系統不會攻擊持有全套自有通行證的細胞。
當細菌、病毒侵入人體,免疫系統就會發現它們的通行證和自己不同,于是發起進攻。可是當入侵者足夠多時,免疫系統來不及阻攔,人就該生病了。免疫系統為了提高自己防御外敵的能力,會把曾殺死的病原體的通行證記錄下來,一旦同樣的敵人再次入侵,就能快速調集防御大軍。
這就是疫苗的工作原理,先送幾個奄奄一息的敵人,或者敵人的通行證到體內,讓免疫系統認識認識,以后再來的敵人就難逃堵截了。
由于疫苗是讓一批危害很小的物質入侵人體,激活人體對這種物質的特異性免疫,從而在之后的數年或數十年內,體內都能快速調集針對這種物質的防御大軍,所以注射疫苗后,一部分人出現低燒、局部疼痛、紅腫等程度較輕微的不良反應屬于正常現象,這些反應是免疫系統積極工作造成的。

抗原與抗體
各種病原體表面的特征分子被稱為“抗原”,免疫系統召集的防御戰士則是“抗體”,抗體可以與抗原特異性結合,啟動一系列免疫反應。抗原-抗體反應具有高度特異性,每種抗體只能識別一種抗原,但一個抗原分子的不同部位可以分別被不同的抗體識別。
抗體組成了“免疫球蛋白”,共有五種類型,分別是IgM、lgG、IgE、IgA和IgD。有時人們會接受“免疫球蛋白”注射,實質上就是注入抗體,相當于外來的援軍,幫助我們擊退入侵的病原體。
我們體內的淋巴細胞主要分為T淋巴細胞和B淋巴細胞兩大類,每類淋巴細胞又分成許多小類,其中“記憶B細胞”和“記憶T細胞”是主要負責記錄接觸過的抗原,而“漿細胞”負責在接到信號后大量產生針對特定抗原的抗體,還有很多其他細胞也用不同方式參與到這場保衛戰中。
人體第一次接觸某種抗原時,需要經過一系列抗原識別、呈遞等過程,才能產生抗體來應對這陌生的敵人。所以感染一段時間后,血液中才能出現抗體,這就是抗體檢測的窗口期。
最早出現的抗體主要是IgM,對抗原的結合能力弱,而且含量低,維持時間短,濃度很快下降。這叫“初次免疫應答”。
在這之后,體內的抗體濃度降到非常低的水平,但記憶細胞會將抗原信息記錄下來。
如果再次被同樣的抗原入侵,免疫系統就能很快被激活,記憶細胞迅速分裂增殖,產生大量漿細胞,分泌抗體,潛伏期顯著縮短。這叫“再次免疫應答”。
再次免疫應答的抗體主要是IgG,結合抗原的能力強,含量高,維持時間長。接種疫苗之所以能預防疾病,正是因為我們的免疫系統倚仗著這些抗體來戰勝病原體。
在醫院檢查是否罹患傳染病時,檢查項目通常就包括IgG和IgM。如果IgM為陽性,提示近期感染了該病原體;如果IgM是陰性,而IgG是陽性,則說明以前得過這種病,或者曾接種過相應的疫苗。
病毒入侵與人體識別
病毒由核酸和蛋白質組成,有些還有脂質膜。核酸分RNA和DNA,還可細分為單鏈、雙鏈、正鏈、反鏈。

通俗來說,核酸是遺傳物質,蛋白質負責生理功能。比如病毒蛋白質中,有些負責當鑰匙,能匹配人體細胞表面的鎖(受體),鑰匙開了鎖,病毒才能進入人體細胞。因為鑰匙和鎖的對應關系,每種病毒都有自己盯準了感染的細胞。
還有些蛋白質負責障眼法,逃避人體免疫系統的監視,有些負責劫持人體細胞內的細胞器,有些負責調控復制裝配增殖,等等。病毒雖然很小,卻十分精巧。
病毒自己是沒有細胞結構的,也不能獨立生活,只有進入人體細胞后才能復制增殖。所以被病毒污染的無活細胞的產品,里面的病毒也不會增殖。而且大多數病毒離開人體后,都挺脆弱的,太陽曬曬啦、晾晾干啦、洗手液洗洗啦……很多病毒經歷這些就失去活性了。
當只有一兩個病毒顆粒進入人體,是不能構成感染的,一般來說,起碼要成千上萬個才行,這個數還受到不同毒株的感染活性不同的嚴重影響。所以,雖然病毒有顆粒,是一個一個的,但我們用“滴度”而不是“個”來描述,可以理解為滴度是跟濃度差不多的一個概念。
人體各種不同細胞表面有著不同的分子標志,免疫系統認識自己的分子標志,不會對自身發起攻擊(這里先不管自身免疫)。細菌和病毒、花粉什么的,也有各自獨有的分子標志,這些分子標志就是抗原,抗原通常是蛋白質的片段,經過折疊其序列和空間結構能被人體免疫系統識別并產生對應的抗體。一個蛋白質分子上可以有多個抗原(這里暫不論表位啊折疊啊什么的)。一種病毒當然也往往有多種可被人體識別的抗原。
足夠的病毒進入人體,構成感染后,人體的免疫系統就會偵測到陌生的抗原,并發起攻擊,這個過程中就會產生抗體。抗體相當于人體的衛兵,一方面攻擊外來物,一方面通風報信啟動后續更復雜更強大的免疫反應。
當然也有例外,狂犬病病毒就是個奇葩。它進入人體后不進入血液循環,不引起免疫反應,人體直到發病都不產生抗體,目前人類還沒研究出在發病前診斷一個人是否感染了狂犬病病毒的技術。
免疫系統對接觸過的外來抗原,有時會建立免疫記憶,等到再次見到,就能更快、更高、更強(此處不是修辭手法)地產生免疫應答。疫苗的原理就是模擬病原體的抗原,讓人體免疫系統預先認識一下這個抗原。
關于一些專業詞匯
通過在實驗室對病毒檢測,才能確定患者到底感染了何種病毒,才能更好地對患者進行針對性治療。××檢測就是檢測××的存在與否和含量多少。樣本姑且默認為最適宜檢測的樣本,病原姑且只說病毒。
任何檢測技術,都有檢出限,比如檢出限是每毫升1 000個病毒(實際上,病毒不能按個算,要按滴度),那么不管是0個還是200個、800個,都檢不出。
從形成感染,到病毒增殖,直到檢測指標達到檢出限水平,這段時間叫窗口期。
從形成感染,到表現出癥狀,這段時間叫潛伏期。
這時又有例外了,那就是HIV感染,在和其他傳染病一樣的潛伏期結束后,先有一個急性感染期,癥狀通常是發燒、乏力等,但并不是每個感染者都有明顯癥狀;這些癥狀通常持續2~3周后自行消失;之后進入無癥狀感染期;2~15年的無癥狀感染期之后,才顯現出艾滋病的癥狀。人們常常忽略HIV感染的急性感染期,而將漫長的無癥狀感染期視為潛伏期,所以常說“艾滋病的潛伏期特別長”。HIV攜帶者在發生特定的癌癥或機會性感染(也就是確診為艾滋病的標準)之前,只能被稱為“HIV感染者”,而不能被稱為“艾滋病患者”。
還有一個例外就是潛伏性感染,最常見的是單純皰疹病毒,剛感染的時候病毒增殖會讓患者長皰疹,之后病毒就躲起來,形成潛伏性感染,沒有癥狀,等患者免疫系統功能紊亂壓不住它了,又跑出來再次作妖,于是有些人的皰疹總是反復發作。
抗原檢測一一陽性 基本就是感染了對應病毒(罕見情況暫且不論)。陰性,可能是感染窗口期,可能是沒感染過,也可能是感染過,免疫系統已經清除或暫時壓制了病毒。
抗體檢測一一陽性 可能是感染了對應病毒,也可能是接種過該病的疫苗,還可能是輸注了外源抗體比如狂免(狂犬病特異性免疫球蛋白)、破免(破傷風特異性免疫球蛋白)。陰性,可能是剛感染窗口期,可能是沒感染過,也可能是感染過,免疫系統已經清除或暫時壓制了病毒。
核酸檢測一一陽性 基本就是感染了對應病毒(罕見情況暫且不論)。陰性,可能是剛感染窗口期,可能是沒感染過,可能是感染過,免疫系統已經清除了病毒。
半數組織培養物檢測 把樣本和敏感細胞放在一起養,如果樣本里面有病毒,病毒會感染細胞,然后根據樣本不同稀釋倍數對應的細胞被感染的比例,可以計算樣本中病毒的真實感染活性與數量的綜合實力。稍微改一下也能檢測樣本中的抗體搞定病毒的綜合實力。這種方法一般不用于判斷某人是否罹患某種疾病。

