超聲造影與CT/MRI肝臟影像報告與數據系統對肝細胞癌診斷評分的一致性分析
劉媛,李晨,吳明曉,羅曉捷,陳秀華,許靜涌
(北京醫院,a超聲科,b放射科,c普外科 國家老年醫學中心 中國醫學科學院老年醫學研究院,北京 100730)
肝細胞癌(HCC)是我國常見的惡性腫瘤之一,其病死率居第3位[1],因此早期診斷和治療尤為重要。超聲造影(CEUS)可實時動態顯示微血管及組織血流灌注狀態,分辨率較高,且無腎毒性及輻射,已廣泛應用于肝臟病變的診斷[2]。美國放射學院(ACR)2016年8月首次發布了針對HCC高危人群的肝臟影像報告和數據管理系統(LI-RADS),目前仍在不斷修訂及更新,其臨床應用價值尚需進一步探討[3]。以往的研究[4-5]大多探討CEUS-LI-RADS對于HCC的診斷效能,對于不同醫師之間診斷評分的一致性及CEUS-LI-RADS與CT/MRI-LI-RADS對HCC診斷效能的比較研究較少。本文旨在比較CEUS-LI-RADS與CT/MRI-LI-RADS對HCC的診斷效能以及不同醫師之間診斷評分的一致性。
1 資料與方法
1.1 臨床資料 回顧性分析2016年7月至2019年5月在北京醫院就診的具有HCC高危風險的肝局灶性病變患者的超聲造影及CT/MRI資料。經過篩選,最終35例患者共47個病灶納入本研究,其中男28例,女7例;年齡范圍53~81歲,年齡(64±8.2)歲;所有患者均接受CEUS檢查,其中16例患者(21個病灶)接受增強CT檢查,19例患者(26個病灶)接受增強MRI檢查。
1.2 納入與排除標準 納入標準:①肝硬化患者;②慢性乙型病毒性肝炎患者;③診斷為HCC的患者;④病灶均經病理證實。排除標準:①CEUS或增強CT/MRI資料不完整;②病灶接受過介入或手術治療。
1.3 儀器與方法
1.3.1 超聲造影 采用GE Logic E9、Toshiba Aplio 500超聲診斷儀,C1-5凸陣探頭,頻率2~5 MHz,具有低機械指數超聲造影技術。造影劑采用Sono Vue(意大利Bracco公司)。
患者取平臥位或左側臥位,選擇最佳切面,啟動超聲造影模式,經肘正中靜脈彈丸式注射Sono Vue 2.4 mL,隨后快速推注5 mL 0.9%氯化鈉注射溶液沖管。對病灶進行實時、動態觀察3~5 min,并存儲動態圖像。
1.3.2 CT 使用GE HD750、Toshiba Aquilion one多排螺旋CT。掃描參數:120 kVp,300 mAs,層厚5 mm,層間距5 mm。常規行平掃及增強三期(動脈期、門脈期及延遲期)掃描,經高壓注射器靜脈團注碘海醇80 mL,注射流率3.5 mL/s,分別于注射對比劑后25~30 s、60 s及3 min掃描獲得動脈期、門脈期及延遲期圖像。
1.3.3 MRI 掃描設備為3T磁共振掃描儀,包括GE Signa Pioneer、GE Discovery MR750,用8通道體部相控陣線圈采集信號。常規行T1WI、T2WI、DWI、同反相位及動態增強掃描。MR對比劑為釓噴酸二甲基葡胺(Gd-DTPA),標準劑量(0.1 mmol/kg),注射速率2.5~3 mL/s,采用高壓注射器經靜脈注射。掃描方位均為軸位。
FSPGR脂肪抑制T1WI掃描參數:TR 3.89 ms,TE 1.74 ms,層厚≤6 mm,層間距≤ 1.5mm,矩陣512×512,FOV 38 cm×(34.2~38)cm。
化學位移同反相位成像掃描參數:TR 3.89 ms,同相位TE 2.32 ms,反相位TE 1.16 ms,層厚≤6 mm,層間距≤1.5 mm,矩陣512×512,FOV 38 cm×(34.2~38)cm。
脂肪抑制FSE T2WI掃描參數:TR為2~3個呼吸周期,TE 86.2ms,回波鏈<20,層厚≤6 mm,層間距≤1.5 mm,矩陣512×512,FOV 38 cm×28.5 cm。
DWI掃描呼吸觸發單次激發自旋回波-回波平面成像(SE-EPI)序列:b值為0,600s/mm2,擴散方向為3個,并行采集加速因子為2,TR為2~3個呼吸周期,TE默認為最短(56.2 ms),矩陣256×256,采用選擇性水激勵技術進行脂肪抑制,其他參數同T1WI。
LAVA動態增強掃描參數:TR為最短,TE為最短,層厚4 mm,層間距0,FOV (32~38)cm×(32~38)cm,矩陣512×512。掃描期相:包括平掃、動脈早期、動脈晚期、門靜脈期及平衡期。注射對比劑后15~20 s及25~30 s連續采集動脈早期及動脈晚期,注射對比后50~60 s及3 min分別采集門靜脈期及平衡期。
1.4 圖像分析
1.4.1 超聲造影 由2位不同年資的超聲科醫師(分別具有5年及10年以上腹部超聲診斷經驗)對所有病灶的超聲圖像進行獨立盲法閱片,參照CEUS-LI-RADS V2017對病灶進行分類,不提供任何臨床及病理資料。
1.4.2 CT/MRI 由2位熟悉腹部影像診斷的醫師(分別具有腹部閱片經驗4年及10年)對所有病灶的超聲圖像進行獨立盲法閱片,參照CT/MRI-LI-RADS V2018對病灶進行分類,不提供任何臨床及病理資料。
1.5 統計學處理 應用SPSS 19.0統計學軟件進行分析。以病理為金標準,計算超聲組和CT/MRI組2名高年資醫師利用CEUS及CT/MRI對HCC的診斷符合率,應用χ2檢驗分析,P<0.05為差異有統計學意義。應用Kappa檢驗分析超聲組和CT/MRI組2名不同年資醫師組內診斷的一致性。Kappa值定義為:0.81~0.99,一致性非常高;0.61~0.80,一致性良好;0.41~0.60,一致性中等;0.21~0.40,一致性一般;≤0.20,一致性差。
2 結果
2.1 病理結果 47個病灶最大徑線范圍為0.9~6.8 cm,最大徑線(2.7±1.5)cm;經病理證實31個為HCC,2個為膽管細胞癌,2個為轉移癌,7個為肝硬化結節,2個為血管瘤,1個為局灶性結節增生(FNH),1個為肝膿腫,1個為復雜囊腫。
2.2 超聲造影LI-RADS與CT/MRI-LI-RADS對病灶診斷評分的一致性比較 超聲組兩名醫師利用CEUS-LI-RADS對病灶的評分一致性為中等,Kappa值為0.481(表1)。評分不一致的情況主要為:醫師1評為LR-5而醫師2評為LR-M的病灶有5個,醫師1評為LR-M而醫師2評為LR-5的病灶有6個,醫師1評為LR-4而醫師2評為LR-5的病灶有2個,醫師1評為LR-3而醫師2評為LR-M的病灶有1個。
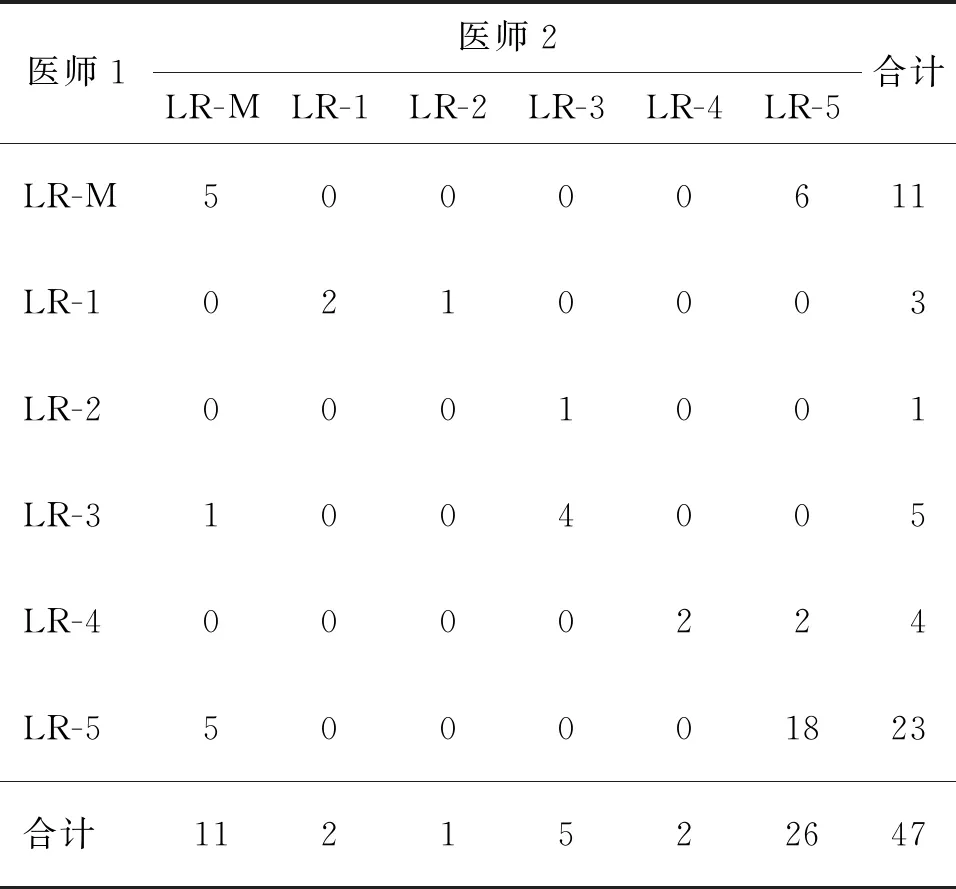
表1 超聲組兩名醫師利用CEUS-LI-RADS 對病灶的分類結果(個)
CT/MRI組兩名醫師利用CT/MRI-LI-RADS對病灶的評分一致性為中等,Kappa值為0.467(表2)。評分不一致的情況主要為:醫師1評為LR-3而醫師2評為LR-4的病灶有3個,醫師1評為LR-4而醫師2評為LR-3的病灶有1個,醫師1評為LR-4而醫師2評為LR-5的病灶有4個,醫師1評為LR-3而醫師2評為LR-5的病灶有3個。
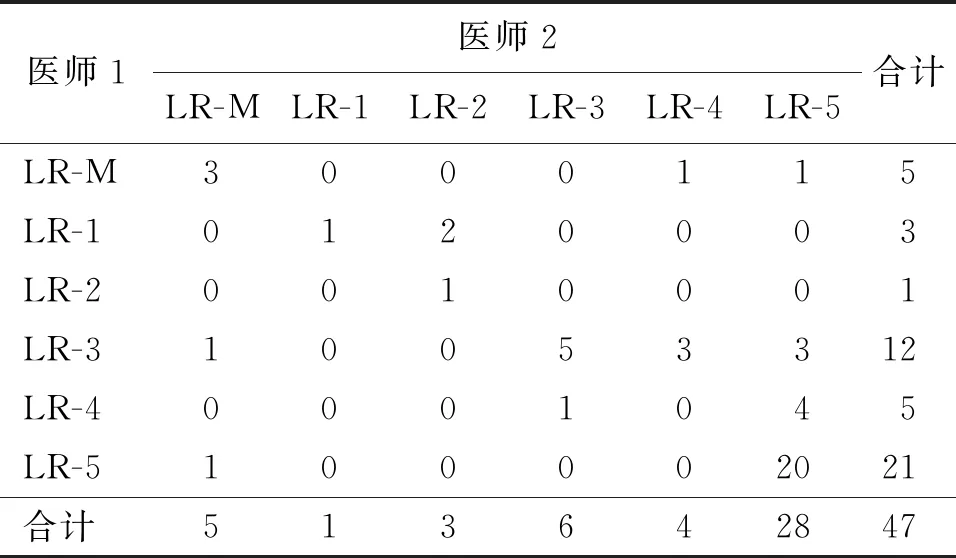
表2 CT/MRI組兩名醫師利用CT/MRI-LI-RADS 對病灶的分類結果(個)
將LI-RADS 4~5類歸為陽性,以病理結果為金標準,超聲組和CT/MRI組兩名高年資醫師分別利用CEUS和CT/MRI對HCC的診斷符合率分別為80.9%(38/47)、89.4%(42/47)(表3,4),經χ2檢驗,其差異無統計學意義,χ2=1.571,P=0.240。某典型病例影像圖片見圖1。
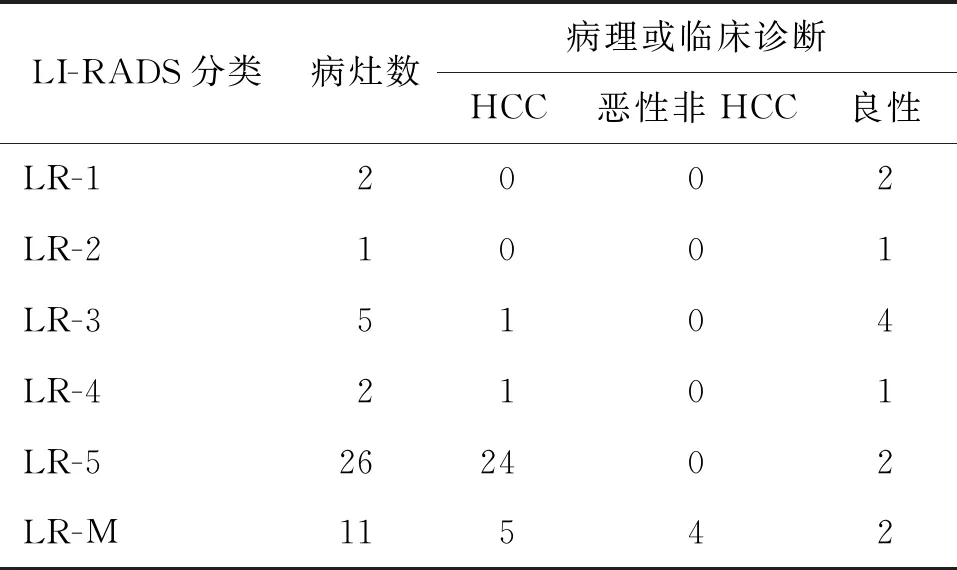
表3 47個病灶CEUS-LI-RADS分類與病理或臨床 診斷情況(個)
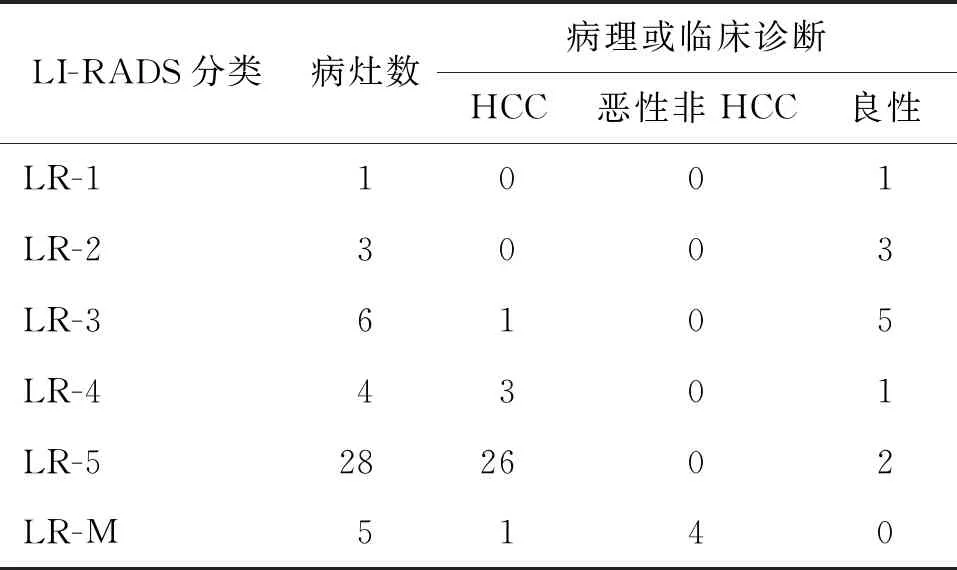
表4 47個病灶CT/MRI-LI-RADS分類與病理或臨床 診斷情況(個)
3 討論
肝癌是最常見的惡性腫瘤之一,其中HCC占85%以上,多發生于肝硬化背景[6]。由于HCC影像學表現具有一定特征,因此影像學檢查成為HCC常用的無創性監測和診斷方法。美國放射學院(ACR)于2011年首次發布了基于CT/MRI的LI-RADS分類標準,目前已發布v2018[7],而超聲造影LI-RADS由ACR于2016年8月發布,并更新至v2017,其分類原則與CT/MRI保持一致,目前仍處于不斷更新及驗證中[3]。既往研究表明將LR-4類及LR-5類歸為陽性,利用CEUS-LI-RADS診斷HCC的準確度較高[8],但關于不同醫師之間的診斷一致性研究較少。有研究顯示利用CT/MRI-LI-RADS,高年資醫師之間的一致性高于低年資醫師[9]。本研究分別比較了不同醫師利用CEUS-LI-RADS及CT/MRI-LI-RADS分類評分的一致性及兩者對HCC的診斷符合率。
本研究顯示超聲組兩名醫師利用CEUS-LI-RADS分類評分的一致性為中等,Kappa值為0.481,較文獻中(Kappa值為0.218)一致性高[10]。這可能是因為本組病例中HCC比例較高,而非HCC惡性腫瘤中轉移瘤較多,病灶多≥1.0 cm,并且在閱片前兩名醫師對CEUS-LI-RADS分類標準進行了嚴格學習和實踐,盡量減少由于不熟練導致的不一致。醫師之間不一致主要集中在LR-M與LR-5之間、LR-4與LR-5之間,這主要是由于兩名醫師對病灶是否廓清和廓清時間的判斷存在爭議。對于評分存在爭議的大多數病灶,2名醫師都認為病灶具有動脈期高增強,其中9個病灶1名醫師認為廓清時間<60 s,而另1名醫師認為廓清時間≥60 s,另外2個病灶伴有中央壞死,1名醫師認為病灶環形強化,而另1名醫師認為病灶為動脈期非環狀高增強,因此造成了LR-M與LR-5的差異。另外3個病灶一名醫師認為有動脈晚期輕度廓清,而另一名醫師認為未見明顯廓清,因此造成了LR-4與LR-5的差異。這點與文獻[11-12]一致。本研究中的主要差異為廓清時間的判斷,并且有2個HCC病灶廓清時間<60 s,因此筆者認為對于廓清時間的界定尚需要進一步探討。
關于CT/MRI組2名醫師利用CT/MRI-LI-RADS分類評分的一致性,本研究結果與文獻報道(Kappa值為0.398~0.537)基本一致,其一致性為中等,Kappa值為0.467[13]。本研究中兩名醫師的評分差異主要集中在LR-3與LR-4之間、LR-4與LR-5之間,造成差異的一個重要原因是對次要征象的認識不同,其次對于強化或廓清不明顯的病灶在判讀上存在分歧。
本研究中超聲組和CT/MRI組兩名高年資醫師利用CEUS-LI-RADS與CT/MRI-LI-RADS診斷HCC的診斷符合率分別為80.9%(38/47)、89.4%(42/47),CT/MRI組略高于超聲組,但其差異無統計學意義。由于CT/MRI-LI-RADS發布較早且不斷修正更新,并且MRI軟組織分辨率較高,序列較多,次要征象較多,為診斷提供的信息較多。尤其對于肝轉移、膽管細胞癌等LR-M類病灶以及肝膿腫等,MRI多序列能提供更多信息,提高診斷的準確性。本研究中5個HCC在CEUS上被診斷為LR-M類,僅1個HCC在CT/MRI上被診斷為LR-M類。既往研究顯示CEUS-LI-RADS對HCC的診斷準確率較高[8,14],但其發布時間短,臨床實踐較少,僅利用主要征象進行診斷評分,可利用的信息較少,且尚需要進一步驗證和探討。
本研究尚存在一定的局限性,比如樣本量較小,且僅對醫師之間的診斷評分進行探討,未對影像征象進行具體分析。
總之,不同醫師利用CEUS-LI-RADS對病灶診斷評分之間的一致性與CT/MRI-LI-RADS接近,不一致的主要原因是對于是否廓清以及廓清時間的判定,這尚需要進一步研究來探討。CEUS-LI-RADS對HCC的診斷具有重要參考價值,但仍需要大量研究來驗證及修正,不斷提高其診斷效能。

