超聲、細針穿刺細胞學及BRAFV600E基因對甲狀腺結節的診斷價值
趙媛 趙永剛 張春芳 陳昊 張智弘
1南京醫科大學臨床醫學院連云港市第一人民醫院(江蘇連云港222002);2南京醫科大學第一附屬醫院(南京210029)
甲狀腺結節是甲狀腺最常見的疾病之一,在人群中的發生率為20% ~76%,其中惡性結節占5%~15%[1-2];甄別甲狀腺結節的良惡性及其生物學行為,進而做出正確的臨床決策是臨床的首要任務和當前研究的熱點之一。
超聲(ultrasound,US)在甲狀腺結節良惡性鑒別診斷中具有不可替代的優勢,是首選檢查方法。以此為基石,超聲引導下細針穿刺細胞學(fine?needle aspiration cytology,FNAC)是術前診斷甲狀腺結節良、惡性的“金標準”,其使用Bethesda 報告甲狀腺細胞病變系統,該報告系統分級明確,有助于改善患者管理,亦存在一定局限性,其中19.7% ~30%無法明確診斷[3-5]。2015年美國甲狀腺協會(ATA)指南建議使用分子標志物來進一步診斷和管理不確定結節。近年來,分子標志物大量應用到術前FNAC 檢測中,BRAFV600E是當前研究熱點之一,大約40% ~83%的PTC 存在BRAFV600E突變,其診斷PTC 的陽性預測值接近100%,稱其是PTC 的特異性標記物[6]。
1 資料與方法
1.1 臨床資料收集2015年1月至2018年12月在南京醫科大學第一附屬醫院經US 檢查同時行FNAC、BRAFV600E基因突變檢測并且有術后病理的512 例甲狀腺結節病例資料,包括61 例良性病變和451 例甲狀腺惡性腫瘤,入選病例中男122 例,女390 例,年齡17 ~77 歲,平均(43.4±12.4)歲,結節最大直徑3 ~73 mm,平均(13.3±9.4)mm。
1.2 方法
1.2.1 超聲檢查常規描述甲狀腺影像和報告系統(the thyroid imaging reporting and data system,TIRADS)分類中的五個方面:結構、回聲水平、形態、邊緣和鈣化,同時描述結節位置、大小、數量、血供情況、與周圍被膜組織的關系,以及評估頸部淋巴結情況,根據TIRADS 分類將結節分為6 類。
1.2.2 細針穿刺細胞學檢查超聲探查目標結節,確定穿刺路徑;局部0.5%碘伏消毒,戴無菌手套,左手固定結節,右手在超聲引導下將帶5 mL針筒的25G 穿刺針沿預定路線刺入結節內,反復抽吸3 次左右,將注射器內穿刺物打入BD 公司一次性保存液中并反復抽吸幾次,送至病理科,使用BD 公司沉降式液基細胞自動制片設備進行制片和巴氏染色,后透明、封片和鏡檢。
1.2.3 BRAFV600E基因突變檢測取材方法同細針穿刺細胞學,將注射器內穿刺物打入BD 公司一次性保存液中,送至病理科分子室后轉移到裝有裂解液的EP 管中,采用擴增阻滯突變系統多聚酶鏈式擴增法檢測BRAFV600E基因突變結果。
1.3 結果判讀
1.3.1 超聲結果判讀術前超聲評估甲狀腺結節均按照KWAK 等[7]提出的甲狀腺影像和報告系統分為6類。TIRADS 1類:正常甲狀腺;TIRADS 2類:良性甲狀腺結節;TIRADS 3 類:可能良性甲狀腺結節;TIRADS 4A 類:低度可疑惡性結節;TIRADS 4B類:中度可疑惡性結節;TIRADS 4C 類:高度可疑惡性結節;TIRADS 5 類:典型惡性征象;TIRADS 6類:已行活檢并有惡性病理診斷。
1.3.2 細胞學結果判讀細針穿刺細胞學按照2007年美國國家癌癥協會制定的Bethesda 報告甲狀腺細胞病變系統進行報告,將診斷結果分為6 類:Ⅰ類:標本無法診斷或不滿意;Ⅱ類:良性病變;Ⅲ類:意義不明確的細胞非典型病變/濾泡性病變;Ⅳ類:濾泡性腫瘤/可疑濾泡性腫瘤;Ⅴ類:可疑惡性腫瘤;Ⅵ類:惡性腫瘤。
1.3.3 BRAFV600E 基因突變結果判讀若樣本的FAM 信號Ct 值≥28,則樣本為陰性(BRAFV600E野生型);若樣本的FAM 信號Ct 值< 28,則樣本為陽性(BRAFV600E突變型)。
1.3.4 聯合診斷結果判讀聯合診斷時,幾種方法均診斷為良性,則判定為良性;若診斷不一致,則其中一種診斷為惡性,即判定為惡性。
1.4 統計學方法采用SPSS 20.0軟件對數據進行統計分析。以術后病理為金標準,構建US、FNAC、BRAFV600E及不同聯合診斷方法的ROC 曲線,聯合診斷使用二元Logistic 回歸分析計算聯合預測因子;通過ROC 曲線確定US 和FNAC 的最佳截斷點并計算AUC,比較不同方法的診斷效能;計數資料組間比較采用行×列卡方檢驗;計量資料以均數±標準差表示。P<0.05 時差異有統計學意義。
2 結果
2.1 術后切除512 例甲狀腺結節US、FNAC 及BRAFV600E突變測定結果512 例結節的US 診斷結果(表1):TIRADS 3 類結節23 個,其中惡性2 例;TIRADS 4A 類結節100 個,其中惡性72 例;TIRADS 4B類結節146個,其中惡性136例;TIRADS 4C類結節171個,其中惡性169例;TIRADS 5類結節72個,均為惡性;FNAC 診斷結果(表2):Bethesda Ⅰ類結節27 個,其中4 例術后被診斷為PTC;BethesdaⅡ類結節25 個,其中1 例被診斷為PTC;BethesdaⅢ類結節42 個,其中29 例被診斷為PTC,1 例為濾泡癌(follicular thyroid carcinoma,FTC),1 例為髓樣癌(medullary thyroid carcinoma,MTC);Bethesda Ⅳ類結節6 個,其中4 例被診斷為FTC;Bethesda Ⅴ類結節133 個,其中惡性132 例,包括126 例PTC,2 例淋巴瘤,1 例FTC,1 例MTC,1 例未分化癌,1 例嗜酸細胞癌;Bethesda Ⅵ類結節279 個,均被診斷為PTC;BRAFV600E診斷結果(表3):BRAFV600E野生型78 例,其中惡性19 例,包括8 例PTC,5 例FTC,2 例MTC,2 例淋巴瘤,1 例未分化癌,1 例嗜酸細胞癌;BRAFV600E突變型434 例,其中被診斷為PTC 431 例,FTC 1 例。
2.2 比較US、FNAC 及BRAFV600E突變檢測及不同方法聯合的診斷效能構建三種診斷方法及不同聯合診斷方法的ROC 曲線(圖1),ROC 曲線表明US 的最佳診斷截斷點是4B,即TIRADS 1?4A 類為良性,TIRADS 4B?6 類為惡性;FNAC 的最佳診斷截斷點是Ⅴ,即BethesdaⅠ?Ⅳ類為良性,BethesdaⅤ?Ⅵ類為惡性;以術后病理為標準,US 診斷甲狀腺惡性腫瘤的敏感性、特異性、陽性預測值、陰性預測值和AUC 分別為83.59%、80.33%、96.92%、39.84%和0.888;FNAC 診斷對應的指標分別為91.13%、98.36%、99.76%、60.00%和0.980;BRAFV600E基因檢測為95.79%、96.72%、99.54%、75.64%和0.963;US+FNAC 診斷為94.46%、80.33%、97.26%、66.22% 和0.986;FNAC+BRAFV600E基因檢測為98.45%、96.72%、99.55%、89.39%和0.995;三種診斷方法聯合的指標分別為98.89%、78.69%、97.17%、90.57%和0.993(表4)。
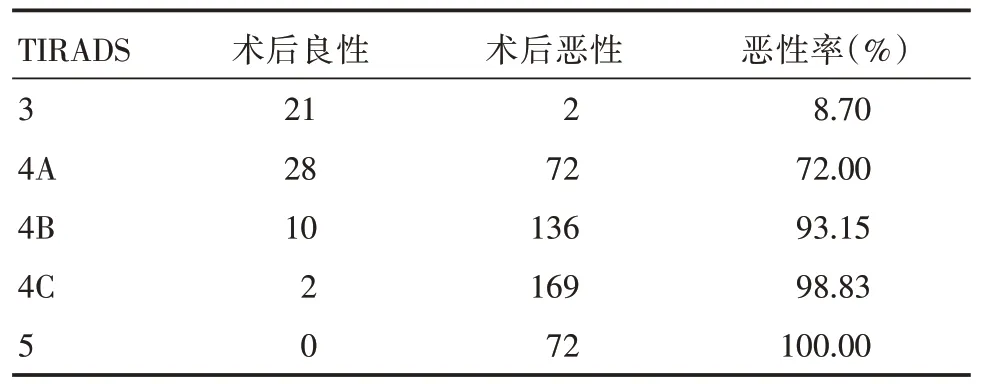
表1 TIRADS 分類結果與術后結果比較Tab.1 Comparison of TIRADS classification results with postoperative results 例
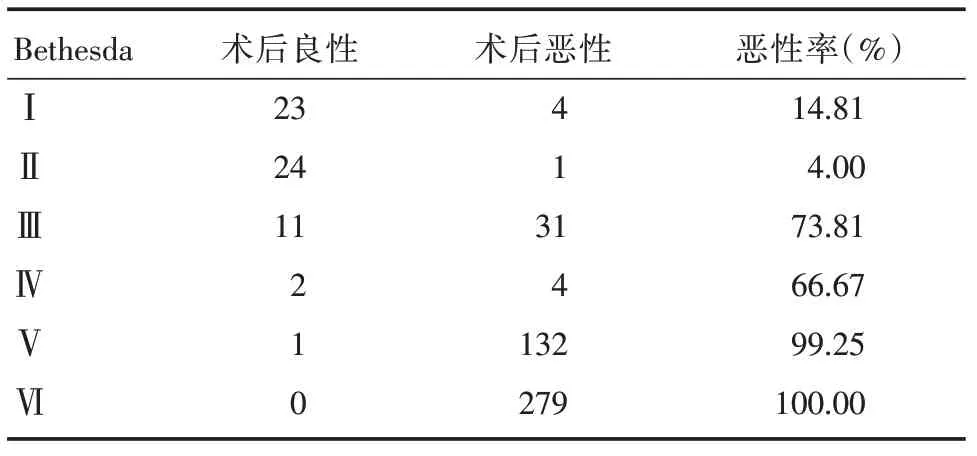
表2 Bethesda 報告結果與術后結果比較Tab.2 Comparison between the results reported by Bethesda and postoperative results例

表3 BRAFV600E檢測結果與術后結果比較Tab.3 Comparison of BRAFV600E detection results and postoperative results 例
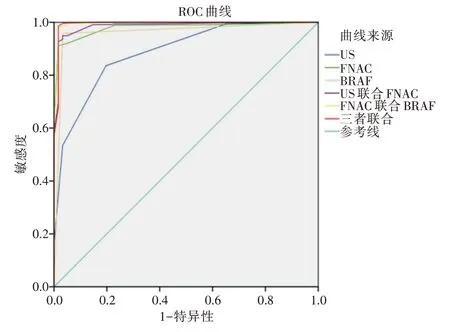
圖1 US、FNAC、BRAFV600E及不同聯合診斷方法的ROC曲線Fig.1 ROC curves of US,FNAC,BRAFV600E and differentcombined diagnostic methods
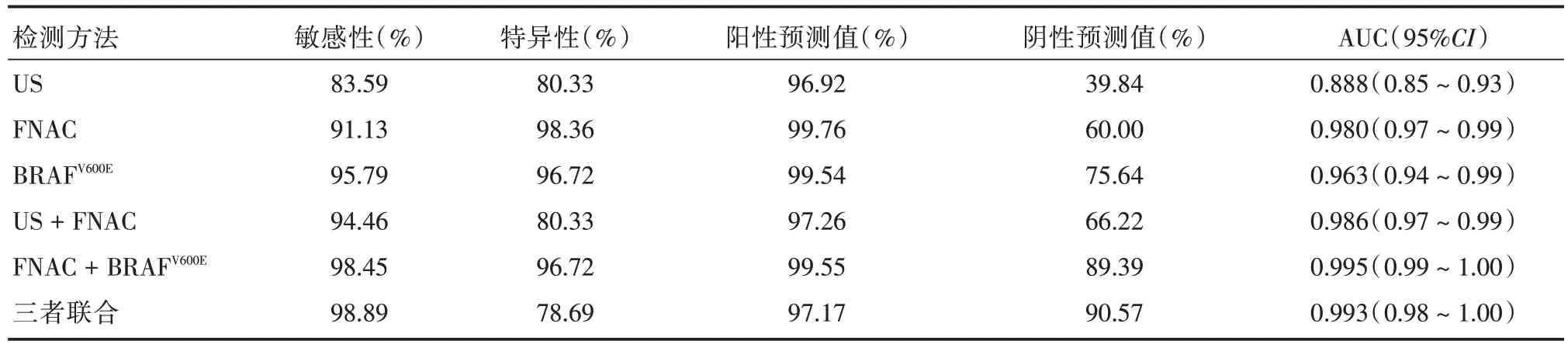
表4 US、FNAC、BRAFV600E及不同聯合診斷方法的診斷效能Tab.4 Diagnostic efficacy of US,FNAC,BRAFV600E and different combined diagnostic methods
2.3 FNAC、BRAFV600E 突變檢測與術后病理結果比較BethesdaⅠ?Ⅳ類共100 例,其中BRAFV600E突變率35%(35/100),BethesdaⅠ?Ⅳ類惡性率為40%;BethesdaⅤ?Ⅵ類共412 例,其中BRAFV600E突變率96.84%(399/412),BethesdaⅤ?Ⅵ類惡性率為99.76%;512 例標本中BRAFV600E 基因突變型434 例,占84.77%;野生型78 例,占15.23%(表5)。
2.4 US、FNAC、BRAFV600E與FNAC聯合BRAFV600E突變檢測診斷率的比較US 診斷陽性病例389例,陰性病例123 例;FNAC 診斷陽性病例412 例,陰性病例100 例;BRAFV600E診斷陽性病例434 例,陰性病例78 例;FNAC 聯合BRAFV600E診斷陽性病例446 例,陰性病例66 例;FNAC 聯合BRAFV600E診斷優于單獨US,差異有統計學意義;兩者聯合診斷亦優于單獨FNAC(表6)。
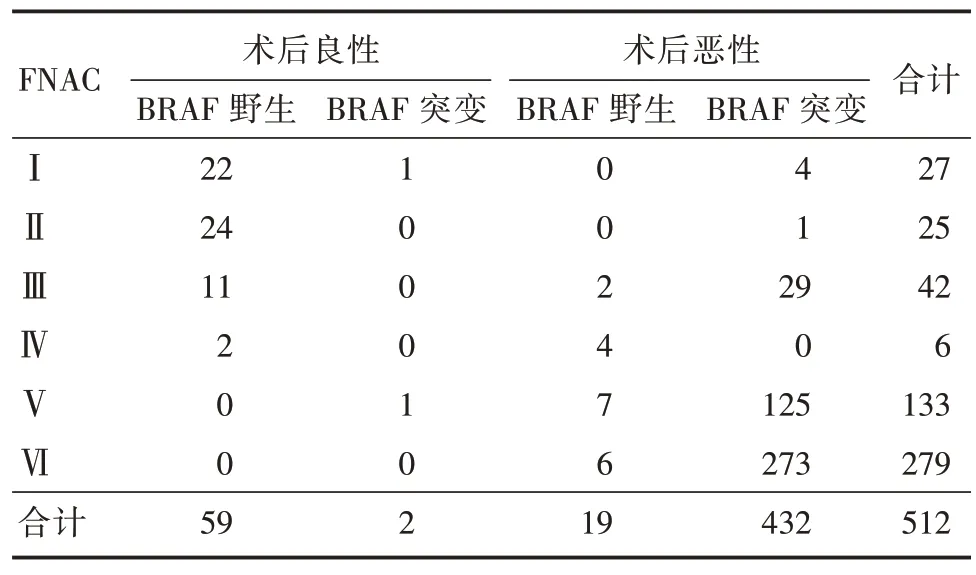
表5 FNAC、BRAFV600E與手術病理結果比較Tab.5 Comparison of FNAC,BRAFV600E and surgical pathological results 例
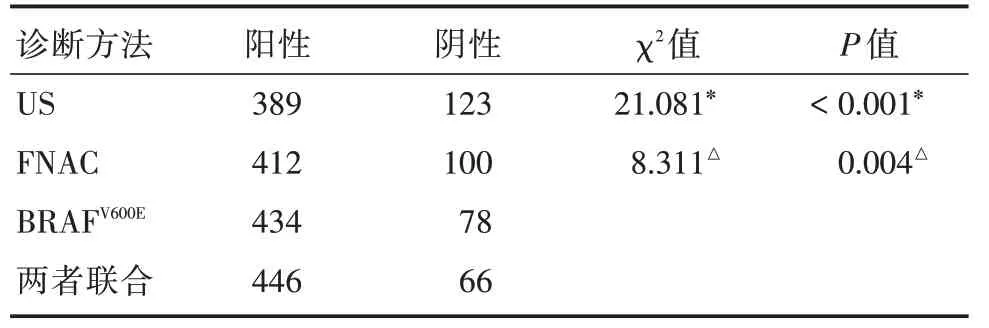
表6 US、FNAC、BRAFV600E 與兩者聯合診斷的比較Tab.6 Comparison of US,FNAC,BRAFV600E and their combined diagnoses 例
3 討論
CHEN 等[8]進行流行病學統計顯示2000年至2011年我國甲狀腺癌的發病率由4.9%上升到20.1%,是內分泌系統最常見的惡性腫瘤。術前鑒別甲狀腺結節良惡性的方法有很多,超聲是最便捷、最經濟的方法,KWAK 等[7]提出五個惡性特征對其進行分類,盡管這些特征具有較高的特異性,但敏感性相對較低;FNAC 是在超聲引導下通過細針對結節進行穿刺診斷的方法,具有創傷小、效率及準確性高等特點[9],但其中約10% ~40%的結節受大小、位置、穿刺及病理醫生的經驗水平等影響而不能明確診斷[10];BRAFV600E作為PTC 的特異性標記物,FNAC 基礎上進一步檢測BRAFV600E可確診部分無法明確性質的結節[11-12]。本文以術后病理為標準,比較US、FNAC、BRAFV600E及聯合診斷對甲狀腺結節的診斷價值。
本研究結果顯示US 診斷甲狀腺惡性腫瘤的敏感性、特異性、陽性預測值和陰性預測值分別為83.59%、80.33%、96.92%、39.84%,與MISTRY 等[13]研究相比,其陽性預測值偏高而陰性預測值偏低,顯示出影像科醫生對于惡性特征把握太緊,判斷相對保守;FNAC 診斷甲狀腺惡性腫瘤的敏感性、特異性、陽性預測值和陰性預測值分別為91.13%、98.36%、99.76%和60.00%,陰性預測值明顯偏低,原因為Bethesda Ⅲ和Ⅳ類惡性率明顯偏高;WU 等[14]根據細胞形態學將Bethesda Ⅲ類分為四個亞組:AUS 未指定、AUS 不能排除濾泡性腫瘤、AUS 不能排除Hurthle 細胞腫瘤和AUS 不能排除PTC,這四個亞型的惡性腫瘤風險分別為44%、81%、53%及63%。本文Bethesda Ⅲ類惡性率高的主要原因是細胞診斷醫生使用較多“AUS 不能排除PTC”的診斷術語;Bethesda Ⅳ類惡性率高是細針穿刺細胞學的局限性造成的,濾泡性腫瘤與濾泡性癌的鑒別要點在于是否存在包膜或血管的侵犯,僅僅細針穿刺細胞學很難對這兩類腫瘤進行鑒別診斷[15];本研究經術后證實PTC 共439 例,其中431 例發生BRAFV600E突變;其他類型惡性腫瘤共12例,僅有1例FTC 發生BRAFV600E突變;上述結果顯示BRAFV600E檢測對PTC 的診斷意義較大,對其他類型惡性腫瘤幫助不大,由于甲狀腺惡性腫瘤中約99%為PTC[16],因此BRAFV600E對甲狀腺結節仍然具有很高的診斷價值。
通過繪制ROC 曲線,顯示FNAC 聯合BRAFV600E的AUC 最大,診斷效能最高,敏感性、特異性、陽性預測值和陰性預測值分別為98.45%、96.72%、99.55%、89.39%。BEI?A 等[17-20]報道FNAC 聯合BRAFV600E基因檢測可改良單獨FNAC 的診斷效能。本研究中BethesdaⅠ類發生率為5.27%,其中BRAFV600E突變率為18.52%,惡性率為14.81%;Bethesda Ⅲ類發生率為8.20%,其中BRAFV600E突變率為69.05%,惡性率為73.81%;由此可以看出,BRAFV600E檢測可以明確診斷FNAC 中性質不確定的大部分結節,從而減少不必要的外科手術[21-22];術后病理診斷為其他類型惡性腫瘤12 例,其中BRAFV600E突變僅1 例,而FNAC 診斷Bethesda Ⅴ類5 例,Bethesda Ⅳ類4 例,Bethesda Ⅲ類2 例,并且給出了傾向性腫瘤類型,可見FNAC 可以降低BRAFV600E的假陰性率,兩者相互補充,顯著提高了診斷性能。
綜上所述,US 對甲狀腺惡性腫瘤有良好的預測作用,可以篩選出高危甲狀腺結節,進而進一步行細針穿刺和基因診斷。FNAC 聯合BRAFV600E可提高術前甲狀腺良惡性結節的診斷。本研究亦存在局限性,總樣本中良性標本比例偏低,可能存在一定的選擇偏倚,期待后期擴充樣本量進行深入研究探討甲狀腺結節術前最佳診斷方法,為患者管理和臨床決策提供更科學的依據。

