乳制品中食源性致病菌檢測技術研究進展分析
趙國婧,謝國陽,肖芳斌,姜華祥,許恒毅*
(1.南昌大學食品科學與技術國家重點實驗室,330047,南昌;2.南昌市青云譜區市場和質量監督管理局個體私營經濟協會辦公室,330001,南昌;3.南昌市青云譜區檢驗檢測中心,330001,南昌)
0 引言
乳制品營養豐富,是人類膳食中蛋白質、鈣、磷、維生素A和維生素B2的重要來源。最近幾年,隨著國民經濟水平的持續進步,我國人民的生活質量逐步提高,國內的家庭膳食層次已經普遍地改善了,對于乳制品消費水平呈現明顯的上升趨勢。目前普遍的乳類品種主要包含液態乳、粉態乳和其他種類乳制品。由于乳制品營養豐富,極易被微生物污染,成為其生長繁殖的營養介質。在所有發生的大規模乳制品安全事件中,大部分是由致病菌污染所引起的乳制品中毒事件。乳制品污染后的食源性致病菌主要包括金黃色葡萄球菌、沙門氏菌和克羅諾桿菌等,金黃色葡萄球菌,因其廣泛存在于自然界中,可以通過乳制品加工人員、加工過程、運輸過程等途徑污染乳制品,造成乳制品腐敗變質;沙門氏菌是一種引起細菌性食物中毒的重要致病菌,生鮮乳中少量的沙門氏菌就可能導致感染,引發沙門氏菌病等;克羅諾桿菌又稱阪崎腸桿菌,是奶粉中最常見的食源性致病菌,嬰幼兒是該菌感染的高危人群且感染后致死率較高,因此對其預防和檢測尤為重要。本文介紹了常見致病菌的檢測方法,并重點介紹了基于核酸的檢測方法,以期為乳制品中食源性致病菌的檢測提供參考。表1總結了不同的檢測方法在致病菌分析測定中的應用。
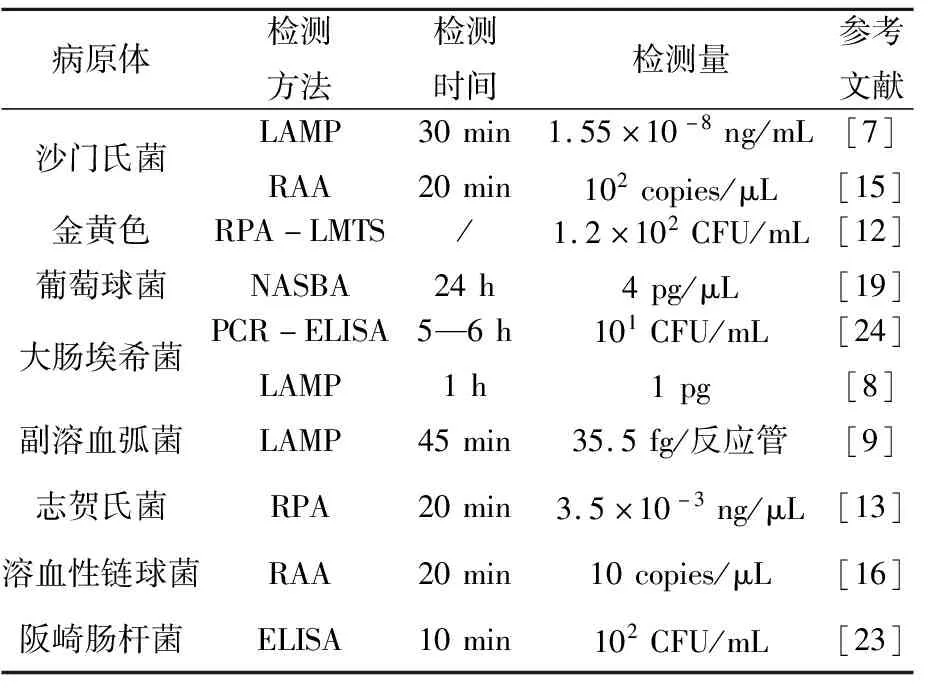
表1 不同的檢測方法在致病菌分析測定中的應用
1 基于培養的檢測方法
目前國家標準對于乳制品檢測有詳細的檢驗方法和限定范圍,如GB 4789.18—2010《乳與乳制品檢驗》[1]、GB 4789.4—2010《沙門氏菌檢驗》[2]、GB 4789.10—2016《金黃色葡萄球菌檢驗》[3]、GB 4789.40—2010《阪崎腸桿菌檢驗》[4]等。一般來說,在一定的培養條件下(相同的培養基、溫度以及培養時間),同種微生物表現出穩定的菌落特征,這些特征包括菌落的形狀、顏色等方面,因此可以通過觀察菌落的形態特征對微生物種類進行判斷。這些基于細菌培養的檢測方法都可以從樣品中得到致病菌定性和定量的檢驗結果,但都需要經過樣品處理、增菌、分離、生化鑒定等過程,具有操作簡單、成本低、準確度高等優點,卻也存在周期長、操作復雜、鑒定微生物種類有限等缺點,難以滿足市場需求。因此出現了一些特異性更好、檢測更快速靈敏的致病菌檢測技術。
2 基于分子生物學技術的檢測方法
隨著分子生物學技術的發展,已經有多種核酸檢測方法應用于食源性致病菌的檢測。如經典的聚合酶鏈式反應(PCR,Polymerase chain reaction),該技術具有靈敏度高、特異性強的特點。Rahn[6]等根據沙門氏菌的侵襲蛋白A(invasion protein A,invA)基因設計引物,用PCR技術對沙門氏菌進行了檢測,共檢測了630株沙門氏菌和21個屬的142株非沙門氏菌,準確率為99.4%。但PCR技術需要核酸擴增儀作為輔助工具,對操作人員技術水平要求較高,因而在實驗室之外的應用有一定局限。近年來核酸等溫擴增技術逐步發展,以環介導等溫擴增(Loop-mediated Isothermal Amplification,LAMP)、重組酶等溫核酸擴增(Recombinase Polymerase Amplification,RPA)、重組酶介導的等溫核酸擴增(Recombinase Aided Amplification,RAA)、依賴核酸序列的擴增(Nuclear Acid Sequence-based Amplification,NASBA)為主的一類核酸技術逐漸應用于食源性致病菌的檢測,同樣具備一定的應用前景。
2.1 環介導等溫擴增技術
環介導等溫核酸擴增技術是一種目前較新的DNA擴增方法,其可以針對靶基因上的特異性區域設計引物,從而利用Bst DNA聚合酶在恒溫條件下完成對靶基因的大量擴增,具有靈敏度高、特異性強等優點,但也容易污染,出現假陽性問題。該技術已廣泛應用于細菌類病原微生物檢測、病毒類病原微生物檢測、病原寄生蟲檢測、轉基因產品檢測等領域。關玉婷[7]等以沙門氏菌腸毒素stn基因為靶基因設計引物,應用DNA聚合酶鏈置換活性和羥基萘酚藍(HNB)在LAMP反應中顏色變化特征,建立了可視化LAMP檢測技術,其靈敏度可達1.55×10-8ng/μL,實現了原料乳中沙門氏菌的檢測。林芳明[8]等發明了不耐熱型產腸毒素,即大腸埃希菌的LAMP快速檢測方法,結果顯示,此方法能夠準確地從生鮮牛乳中檢測到1 pg當量的產腸毒素大腸埃希菌的DNA,且與其他類型的大腸埃希菌及細菌不發生交叉反應,檢測所需時間約1 h,具有特異性強、敏感性高、快速的特點,對保障生鮮牛乳食品安全有十分重要的意義。程曉艷[9]等根據副溶血弧菌的毒力基因tdh保守序列設計引物,建立了LAMP快速檢測技術,結果表明,該細菌的DNA最低的檢出限是35.5 fg/反應管,該方法的靈敏度比PCR高10倍,只需約45 min左右完成。同時利用此方法對扇貝樣品中的副溶血弧菌進行檢測,結果顯示,此LAMP方法對檢測致病性的副溶血弧菌安全、可靠。
2.2 重組酶等溫核酸擴增技術
比如重組酶等溫核酸擴增技術是一種體外恒溫核酸擴增新技術。該技術主要模仿T4噬菌體內的核酸復制機制[10]依賴重組酶UvsX[11]與Gp32單鏈結合蛋白在體外的恒溫環境下實現DNA模板特異性結合和識別,同時通過鏈置換DNA聚合酶Bsu實現了模板DNA的擴增。此方法檢測優點是時間短、操作方便、靈敏程度高,缺點是該技術對某些特定的短序列核酸無法檢測。該技術在食源性病毒、食源性致病菌、動物源性成分檢測等方面均有廣泛應用。高建欣[12]等建立了一種RPA與乳膠微球試紙條(Latex Microsphere Test Strips,LMTS)相結合的方法,根據金黃色葡萄球菌的基因nuc保守區序列設計特異性的引物,經過RPA的擴增,完成了金黃色葡萄球菌快速檢測,其靈敏度為1.2×102CFU/mL。劉立兵[13]等依照志賀氏菌侵襲性質的粒抗原H基因(ipaH)保守區序列的設計和exo探針,建立了志賀氏菌實時熒光重組酶聚合酶擴增技術的檢測方法。該方法特異性擴增志賀氏菌,在39 ℃恒溫下20 min即可完成檢測,檢測的靈敏度為3.5×10-3ng/μL,該方法在人工污染樣本中的檢測時間僅需7—12 min。GAO[14]等建立了一種快速檢測沙門氏菌的RPA-LFD檢測方法,在30~45 ℃下,只需要8 min的擴增就可達到相關擴增子的檢測閥值,該方法特異性強并且靈敏度高。RPA技術可以為食源性的致病菌檢測提供一類快速且簡便的方案。
2.3 重組酶介導的等溫核酸擴增技術
重組酶介導的等溫核酸擴增技術也是一種恒溫擴增方法,與RPA不同的是,RAA擴增法利用的是從細菌或真菌中獲得的重組酶,在37 ℃的恒溫環境下,該重組酶可以和引物的DNA緊密結合,形成酶與引物的復合體,當引物不斷在模板的DNA上搜尋到和它完全互補的序列時,并且在單鏈DNA的結合蛋白輔助下,展開模板DNA的內部雙鏈結構同時使引物和模板相配對,隨后在DNA的聚合酶作用下,組成了新的DNA互補鏈,擴增產物以指數級增長。該技術用時少,操作簡單,已廣泛應用于微生物檢測、醫學檢測等領域。張小平[15]等人按照沙門菌的invA基因來設計引物與探針,并且采用重組酶介導核酸擴增方法對沙門菌進行快速檢測。結果顯示,建立的方法在39 ℃下進行,檢測時間在20 min以內,檢測下限為102copies/μL。魏瑩[16]等建立了RAA技術用于溶血性鏈球菌的檢測,檢測時間小于20 min,靈敏度為10 copies/μL,具有良好的特異性。
2.4 依賴核酸序列的擴增技術
依靠核酸相關序列的擴增技術是一類擴增RNA的新技術種類,依靠一對特異性引物來介導的,并且以3種酶來催化的,以單鏈RNA為模板等溫擴增[17]。該技術具有操作簡單、靈敏程度高、特異性較強的特點,已廣泛應用于多種病毒的檢測當中,但仍然還存在假陽性、靈敏度低等問題,需要進一步優化改進反應條件。楊蜜[18]等人設計了一對具有隱球類菌屬特異性的引物,并且建立了NASBA擴增隱球菌的RNA方法,結果表明該方法靈敏度可達10 CFU/mL。鐘響[19]等人按照金黃色葡萄球菌的核酸酶nuc1基因設計相關的引物,進行了NASBA檢測,同時采用了人工添加菌來污染樣品進行驗證。結果顯示,實驗中未出現假陽性和假陰性結果,靈敏度高,檢出限達到4 pg/μL的總RNA;檢測時間短,24 h即可完成樣品中目標菌的篩選,非常適合口岸快速檢出金黃色葡萄球菌。
2.5 核酸交聯染料相結合等溫擴增技術
等溫擴增技術來檢測乳制品中致病菌方法是具有靈敏度高、特異性強、快速便捷等優點的方案,已廣泛應用于食源性致病菌的檢測。然而,細胞死亡后,由于DNA分子能保留較長時間,從樣品中提取的死菌DNA同樣能作為模板進行特異性擴增,因此檢測過程中難以區分“死菌”和“活菌”容易出現假陽性結果[20]。核酸交聯染料即含有2個或2個以上烷基化官能基團的烷基化試劑,核酸染料可以通過受損的死菌細胞膜,在特定光激活后與DNA結合,從而抑制DNA擴增,這樣可以消除死菌的影響。GAO[21]等食品中的活的但不可培養的副溶血性弧菌(VBNC)進行檢測時發現:當VBNC菌濃度小于104CFU/g時,PMAxx處理樣品后結合qLAMP法與qPCR比檢測結果更精確。減少了普通核酸檢測在食品中VBNC微生物含量低的情況下,可能導致的假陽性結果。
3 基于免疫學技術的檢測方法
在1959年,研究者yalow和Berson同時將發射性同位素示蹤方法和免疫反應相結合創建了現代的發射免疫測定法,從而開創了免疫分析這一嶄新領域,免疫學技術發展至今,具有簡便、快速、靈敏度高、特異性強等特點[22],已經在微生物相關的檢測方面取得了廣泛的應用。免疫學技術的主要原理是抗原與相應抗體,無論在體內或體外相遇,均可以發生各種抗原抗體反應,包括中和反應、沉淀反應或溶解反應等,由于特定抗原(抗體)的量與反應的強度呈現明顯的函數關系,可以依此對樣品進行定性或定量的分析,主要包括酶聯免疫吸附技術、免疫層析技術、酶聯熒光免疫分析技術等。
3.1 酶聯免疫吸附技術
酶聯免疫吸附技術(Enzyme Linked Immunosorbent Assay,ELISA)的基本原理是將可溶性抗原或抗體吸附到某種固定載體表面,采用添加酶標的抗體或抗原,產生抗原和抗體反應,從而形成抗原抗體的復合物,經過洗滌后,游離的酶標抗體和抗原被沖洗掉,然后再加入酶底物和載體上的抗原抗體復合物相結合進行免疫酶染色,通過定性或定量分析有色產物量就可確定樣品中的待測物質含量。周鶴峰[23]等構建了阪崎腸桿菌的特異性抗體相關間接ELISA檢測方法,最后確定37 ℃顯色10 min,檢測靈敏度達到102CFU/mL,該檢測方法具有高效快速、特異性強等特點,為食品中的阪崎腸桿菌的相關檢測創立了研究基礎。胡金強[24]等人選用金黃色葡萄球菌的耐熱核酸酶nuc基因作為靶標,采用地高辛來標記引物擴增的PCR產物和用生物素標記的探針進行雜交,然后與ELISA平板上的鏈霉素雜交,通過抗地高辛抗體顯色建立PCR-ELISA檢測技術,應用結果表明采用PCR-ELISA技術來檢測人工污染金黃色葡萄球菌的牛奶檢測敏感性為101CFU/mL,比普通PCR檢測的敏感性(103CFU/mL)高100倍,實驗全過程只需要5—6 h。該研究建立的PCR-ELISA方法具有良好的特異性與敏感性,能夠特異、敏感、準確地檢測牛奶的金黃色葡萄球菌。
3.2 酶聯熒光免疫分析技術
酶聯熒光免疫分析技術ELFIA(Enzyme-Linked Fluorescent Immunoassay)是在酶聯免疫吸附技術基礎上發展創立的用酶系統和熒光免疫分析相互結合的微生物的快速檢測方法。它利用理想的熒光底物來代替顯色底物,使得分析靈敏度顯著提高,從而達到擴大測量范圍和減少試劑用量的目的。劉新亮[25]等通過以下3個步驟完成沙門氏菌的快速檢測:首先采用全自動熒光酶免疫分析儀(mini VIDAS)來進行初篩,隨后采用沙門氏菌顯色培養基來復篩,最后采用全自動的微生物鑒定儀(VITEK 2 Compact)來進行陽性菌株的生化性狀的鑒定。該聯用法初篩時能在45 min之內準確鑒定出陽性菌株,陽性菌株經沙門氏菌顯色培養基分離純化后按照VITEK檢測的結果與血清學凝集試驗結果相結合即可以判斷它是否屬于沙門氏菌。采用該方法對395種食品和水產品中的目標菌同時檢測的結果與國標法完全一致,其準確性好,并且還具有快捷高效、自動化程度高的特點。
4 結束語
傳統國標法檢測乳制品中的相關致病菌具有特異性差、操作繁瑣、效率低等不足,很難實現快速有效的檢測。免疫學方法存在靈敏度低、對抗體依賴、價格高昂等缺點,而分子生物學,由于特異性強靈敏度高,逐漸應用于致病菌的快速檢測,但其也存在以下不足需要改進:1)需要購買昂貴的儀器設備;2)等溫核酸擴增技術適用于現場做大量樣品的快速檢測,反應簡單,但存在易產生假陽性和假陰性的缺點;3)新開發的PMAxx-RAA方法實現了在死菌存在的環境下檢測出活的致病菌,避免了常規分子生物學方法的缺點。在今后的研究中對于等溫核酸擴增技術存在假陽性、假陰性等問題,需要進一步加強對此技術反應體系和反應條件的不斷優化,相信RAA技術能利用其優勢,成為乳制品中致病菌檢測的重要方法。

