檳榔下腳料中檳榔堿的提取工藝及應用研究
陳 娟 盧克強 朱門君 蔣雪薇
(1.湖南皇爺食品有限公司,湖南 湘潭 411228;2.長沙理工大學,湖南 長沙 410000)
食用檳榔是指以檳榔干果(也稱檳榔原籽)為原料經甜味劑及香精發制而制成的一類休閑食品[1]。據報道[2],截至2017年底,僅湖南省湘潭市天易全區的檳榔年制成品就超過10萬t,而檳榔在加工過程中會產生檳榔核、檳榔蒂及報廢檳榔片等下腳料,其中下腳料約占檳榔成品量的10%~15%,然而目前這些下腳料常常作為廢棄物或生活垃圾以焚燒等方式處置,不僅浪費了資源,也易造成環境污染。有研究[3-4]表明,檳榔果的各個部位均含有檳榔堿,其中鮮果檳榔核的檳榔堿含量為0.118%、檳榔殼的含量為0.043%,且檳榔堿含量隨熟度的增加而增加。因此可將檳榔下腳料用作提取檳榔堿的原料。
目前,檳榔堿的提取方法有有機試劑提取法[5-6]、超聲波輔助提取法[7]、微波輔助提取法[8]、超臨界CO2流體萃取法[9-10]、亞臨界水提取法[11]等,在大規模生產過程中,低沸點易燃的有機試劑有一定的安全隱患,超聲波、微波、超臨界和亞臨界CO2流體萃取等方法的輔助設備的造價過高。研究擬采用酸水提取法提取檳榔堿,并將經響應面法優化的最佳提取工藝得到的提取物應用于檳榔產品中,以期低成本高值化利用檳榔下腳料這一資源。
1 材料與方法
1.1 材料與儀器
1.1.1 材料與試劑
檳榔加工下腳料:湖南皇爺食品有限公司;
甲醇:色譜純,默克股份兩合公司;
乙腈:色譜純,國藥集團化學試劑有限公司;
鹽酸、磷酸、乙二胺:分析純,國藥集團化學試劑有限公司;
檳榔堿氫溴酸鹽:色譜純(純度98.5%),國家計量標準物質網。
1.1.2 主要儀器設備
烘箱:DKN412C型,日本雅馬拓公司;
粉碎機:RRH-A350型,上海緣沃工貿有限公司;
超聲波:KQ-500E型,昆山市超聲儀器有限公司;
高效液相色譜儀:RF-20A型,日本島津公司;
水浴恒溫振蕩器:SHZ-A型,上海博訊醫療生物儀器股份有限公司。
1.2 方法
1.2.1 檳榔下腳料的選擇 將收集的檳榔下腳料于50 ℃ 干燥至水分含量為10%~15%,再按核、蒂、廢棄檳榔片分類分開,粉碎機分別粉碎后,測定其檳榔堿含量。每組試驗重復3次。
1.2.2 檳榔堿的提取 稱取5 g過60目篩的檳榔核,按照試驗方案加入一定量的溶劑,在恒溫振蕩水浴鍋(105 r/min)中以一定的溫度處理一定時間后,過濾,收集濾液,測定濾液中檳榔堿含量。
1.2.3 單因素試驗
(1) 粉碎粒度對檳榔堿提取量的影響:檳榔核經粉碎機處理后過20,40,60,80,100,120目篩,分別測定不同粉碎粒度下檳榔核提取物的檳榔堿含量。
(2) 提取時間對檳榔堿提取量的影響:在粉碎粒度60目,鹽酸質量濃度0.00%,料液比(m檳榔∶V水)為1∶15 (g/mL),提取溫度70 ℃,提取次數1次的條件下測定提取時間為15,30,45,60,75 min時濾液的檳榔堿含量。
(3) 提取溫度對檳榔堿提取量的影響:在粉碎粒度60目,鹽酸質量濃度0.00%,料液比(m檳榔∶V水)為1∶15 (g/mL),提取時間30 min,提取次數1次的條件下測定提取溫度為50,60,70,80,90 ℃時濾液的檳榔堿含量。
(4) 料液比對檳榔堿提取量的影響:在粉碎粒度60目,鹽酸質量濃度0.00%,提取時間30 min,提取溫度70 ℃,提取次數1次的條件下測定料液比(m檳榔∶V水)分別為1∶5,1∶10,1∶15,1∶20,1∶25 (g/mL)時濾液的檳榔堿含量。
(5) 鹽酸質量濃度對檳榔堿提取量的影響:在粉碎粒度60目,料液比(m檳榔∶V水)為1∶15 (g/mL),提取溫度70 ℃,提取時間30 min,提取次數1次的條件下測定鹽酸質量濃度分別為0.00%,0.15%,0.30%,0.45%,0.60%時濾液的檳榔堿含量。
(6) 提取次數對檳榔堿提取量的影響:在粉碎粒度60目,鹽酸質量濃度0.00%,料液比(m檳榔∶V水)為1∶15 (g/mL),提取溫度70 ℃,提取時間30 min的條件下測定提取次數分別為1,2,3,4,5次時濾液的檳榔堿含量。
每組試驗3次重復。
1.2.4 響應面試驗設計 根據中心試驗設計原理,在單因素試驗結果的基礎上,考察提取時間、提取溫度、鹽酸質量濃度對檳榔堿提取量的影響,確定最佳提取工藝。
1.2.5 檳榔堿含量的測定及提取量的計算 根據文獻[12]修改如下:
(1) 樣品處理方式:取適量樣品于比色管中,加甲醇定容至25 mL。混勻后超聲波處理1 h,過0.45 μm有機膜,進樣。
(2) 標準曲線的制定:配制0.1 mg/mL的氫溴酸檳榔堿對照品溶液,分別吸取0.06,0.20,0.40,0.80,1.60,3.20,4.00 mL對照品溶液加流動相定容至4 mL,混勻后進樣。根據試驗所得結果以氫溴酸檳榔堿標準品的峰面積為縱坐標,氫溴酸檳榔堿的濃度(mg/mL)為橫坐標,繪制檳榔堿標準曲線,得到線性關系式:y=2×107x+173 859。
(3) 檳榔堿提取量計算:按式(1)計算。
(1)
式中:
Y——檳榔堿提取量,mg/g;
X——檢測樣品的檳榔堿含量,mg/g;
C——檢測樣品對應的標準曲線的濃度,mg/mL;
V——檢測樣品的定容體積,mL;
m1——檢測樣品的質量,g;
m2——濾液質量,g;
m3——檳榔核的質量,g。
1.2.6 檳榔提取物對檳榔產品品質的影響 按檳榔原籽→煮籽→發制→烤籽→悶香→壓籽→上膠→切籽→去核→點鹵→晾片→包裝的工藝流程制作檳榔產品。其中試驗樣品在發制步驟中用檳榔堿最優提取方案得到的提取物濃縮5倍后等量替代熬料用水,其余不變。測定試驗樣品與對照樣品中的檳榔堿含量,并組織10名經過訓練的品評人員對樣品按照表1中的項目打分,最后統計各項的平均得分。
1.3 數據處理與分析
數據均使用SPSS、Design-Expert 8.0.6軟件進行分析處理。
2 結果與分析
2.1 檳榔下腳料的選擇
檳榔核、檳榔蒂和廢棄檳榔片中檳榔堿含量見圖1。由圖1 可知,檳榔核中的檳榔堿含量遠高于檳榔蒂和廢棄檳榔片,與劉蕊等[13]試驗得出的鮮檳榔中檳榔堿含量檳榔核>纖維層>表皮基本一致。由于檳榔在高溫水洗、烘烤的加工過程中會破壞檳榔殼、蒂中的檳榔堿,而檳榔核被殼包裹能較好地保留檳榔堿,而且檳榔下腳料中檳榔核占總量的90%左右,因此選擇檳榔核作為檳榔堿的提取原料。
2.2 單因素試驗
由圖2~7可知,最佳的單因素參數為:粉碎粒度60目,料液比(m檳榔∶V水)1∶15 (g/mL),提取時間30 min,提取溫度70 ℃,鹽酸質量濃度0.15%,提取次數2次。
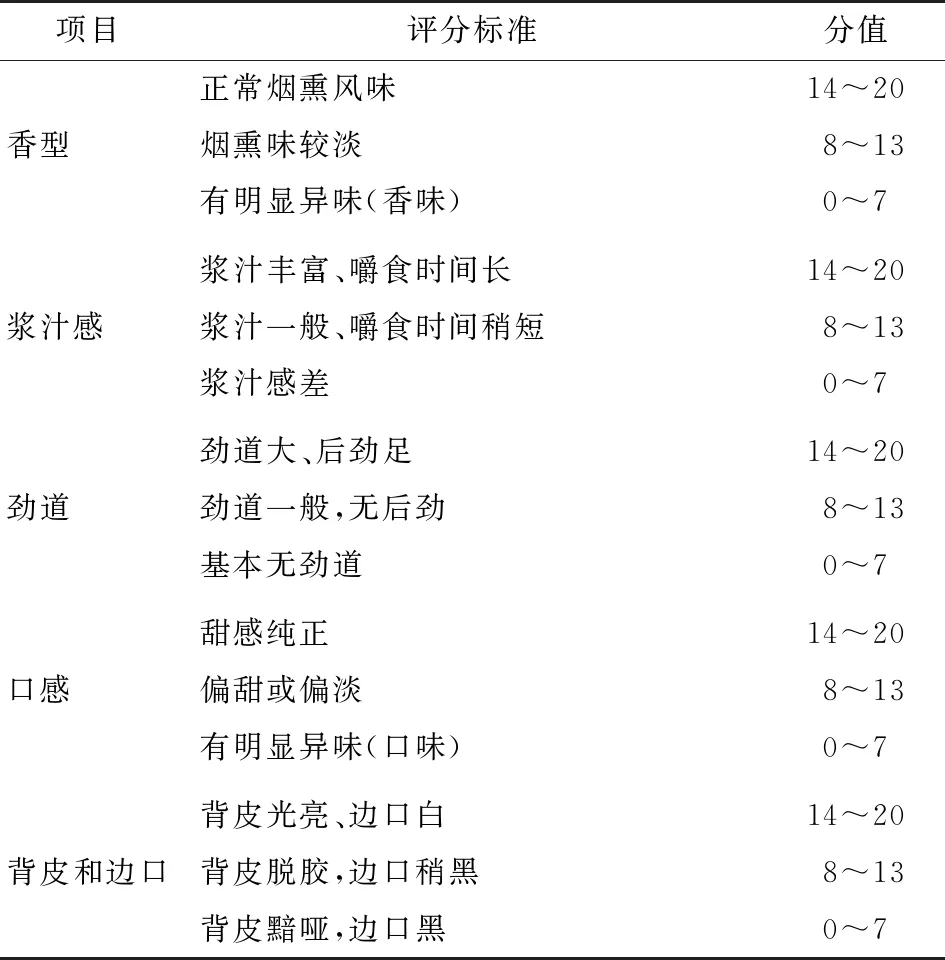
表1 感官品評表Table 1 Sensory evaluation table
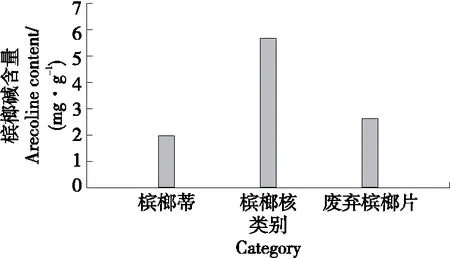
圖1 不同類別檳榔下腳料的檳榔堿含量對比Figure 1 Arecoline content at different catagory of the betel-nut waste

圖2 不同粉碎粒度下提取的檳榔堿含量Figure 2 Extracted arecoline content at different grinding particle sizes
2.3 響應面優化試驗
2.3.1 試驗設計及結果 根據SPSS軟件進行單因素方差分析,結果表明粉碎粒度、提取時間、提取溫度、料液比、提取次數、鹽酸質量濃度對于檳榔堿提取量的影響都是極顯著的(P<0.01)。試驗得出的料液比與提取次數的結果與相關研究[14]的結果基本一致,考慮到粉碎粒度、料液比、提取次數與試驗設備、操作難易和成本耗費緊密相關,在選定粉碎粒度60目,料液比(m檳榔∶V水)1∶15 (g/mL),提取次數2次的基礎上,選擇提取時間、提取溫度及鹽酸質量濃度作為響應面優化的因素,試驗因子與水平表見表2。具體試驗設計與結果見表3。

圖3 料液比對檳榔堿提取量的影響Figure 3 Impact analysis of solid-liquid ratio
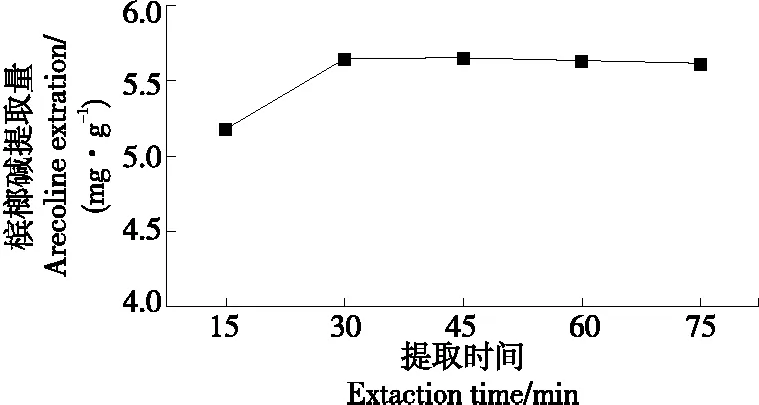
圖4 提取時間對檳榔堿提取量的影響Figure 4 Impact analysis of extraction time

圖5 提取溫度對檳榔堿提取量的影響Figure 5 Impact analysis of extraction temperature

圖6 鹽酸質量濃度對檳榔堿提取量的影響Figure 6 Impact analysis of hydrochloric acid concentration

圖7 提取次數對檳榔堿提取量的影響Figure 7 Impact analysis of extraction times
2.3.2 模型與數據分析 運用Design-Expert 8.0.6軟件試驗數據進行統計分析,得到檳榔堿提取量與提取參數的二次回歸方程為:
Y=7.84+0.30A+0.25B+0.65C-0.075AB+0.035AC+0.24BC-0.12A2-0.14B2-0.71C2。
(2)

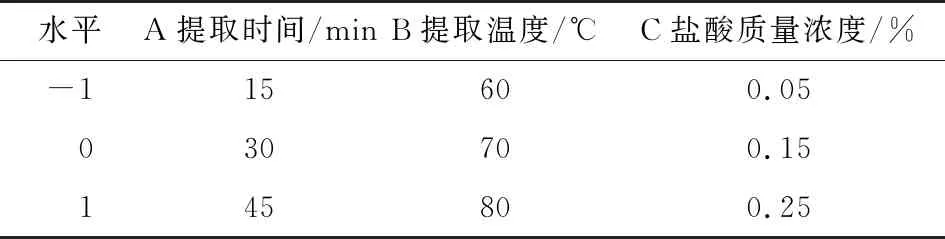
表2 響應面試驗因素水平表Table 2 Factors and levels of response surface experiment

表3 響應面試驗設計和結果Table 3 Design and results of response surface experiment

表4 響應面模型方差分析?Table 4 ANOVA for the response surface quadratic model
由圖8~10可知,3個因素對檳榔堿提取量的影響大小依次為:鹽酸質量濃度>提取時間>提取溫度。當鹽酸質量濃度固定為0.15%時,檳榔堿提取量隨著提取時間和提取溫度的增加而緩慢增加,可能是作為主要影響因素的鹽酸質量濃度還未達到最佳濃度,此時,增加提取時間和提取溫度有助于提高提取效率。當提取溫度固定為70 ℃時,提取率隨鹽酸質量濃度的增加先升高后降低,隨提取時間的增加呈緩慢上升的趨勢;當提取時間固定為30 min時,提取量隨鹽酸質量濃度和提取溫度的增加先上升后降低,可能是高鹽酸質量濃度可大大提升檳榔堿的提取量,但長時間的高溫會導致被提取檳榔堿損失,造成其提取量下降。因此,在確定適當的鹽酸質量濃度后,尤其要控制好提取溫度以使檳榔堿提取量達到最大值。

圖8 提取時間與鹽酸質量濃度交互作用的等高線圖和響應曲面圖Figure 8 Response surface and contour plots for interaction effects of time and hydrochloric acid concentration
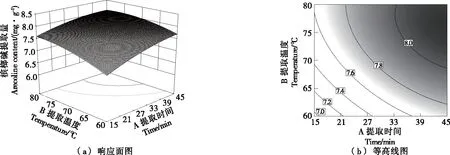
圖9 提取時間與提取溫度交互作用的等高線圖和響應曲面圖Figure 9 Response surface and contour plots for interaction effects of time and temperature

圖10 提取溫度與鹽酸質量濃度交互作用的等高線圖和響應曲面圖Figure 10 Response surface and contour plots for interaction effects of temperature and hydrochloric acid concentration
2.3.3 最優工藝條件的驗證 由Design-Expert 8.0.6軟件分析得出的最優工藝條件為:提取時間45 min,提取溫度80 ℃,鹽酸質量濃度0.22%,此優化條件下預測的檳榔堿提取量為8.365 mg/g。對其進行3次重復實驗,得到檳榔堿提取量的平均值為(8.330±0.109) mg/g,與理論提取量的相對誤差為0.42%,說明該工藝條件合理可行,能用于實際生產。
2.4 應用試驗
水的極性大,除了能提取檳榔堿外,也能較全面地提取出具有檳榔風味的物質。由表5可知,添加了檳榔提取物的檳榔產品風味更加濃郁且無異味,嚼食時更有漿汁感和勁道,說明檳榔提取物的加入可以提升檳榔產品的品質。其次,測定的試驗樣品的檳榔堿含量和勁道評分高于對照產品,表明樣品勁道的提升可能與檳榔堿有關。

表5 試驗樣品與對照樣品的對比Table 5 Comparison between experimental products and control products
3 結論
采用酸水提取法提取檳榔核中檳榔堿的最佳提取工藝條件為粉碎粒度60目、料液比(m檳榔∶V水)1∶15 (g/mL)、提取次數2次、提取時間45 min、提取溫度80 ℃、鹽酸質量濃度0.22%,該條件檳榔堿提取量為(8.330±0.109) mg/g,與傳統乙醇提取法(提取率1.90 mg/g[15])相比,檳榔堿的提取效率大幅提高。
將檳榔提取物添加至檳榔產品可以提升其品質,并且能夠提高檳榔下腳料的附加值,具有極大的應用前景。檳榔提取物不僅可以應用于檳榔產品中,還可以應用于醫藥領域。因此,下一步可根據其具體的應用領域來開發適宜的提取、純化方法,以充分利用檳榔下腳料這一資源。

