GP方案結合PD-1抑制劑治療NSCLC的療效及對Survivin蛋白、免疫細胞水平的影響
王利民,羅 敏,胡 萍,高 利
四川省成都市中西醫結合醫院醫學檢驗科,四川成都 610041
肺癌是最常見的惡性腫瘤之一,已成為我國城市人口惡性腫瘤死亡原因的第1位[1-2]。非小細胞肺癌(NSCLC)包括鱗狀細胞癌(鱗癌)、腺癌、大細胞癌,與小細胞肺癌相比,其癌細胞生長、分裂速度較慢,擴散、轉移相對較晚。NSCLC約占所有肺癌的80%,約75%的患者發現時已處于中晚期,5年生存率很低[3-4]。化療是肺癌的主要治療方法,90%以上的肺癌患者需要接受化療,尤其是NSCLC患者。化療治療NSCLC的腫瘤緩解率為40%~50%,但是化療一般不能治愈NSCLC,只能延長患者生存時間和改善患者生活質量。程序性細胞死亡蛋白-1(PD-1)是一種重要的免疫抑制分子[5],通過向下調節免疫系統對人體細胞的反應,以及通過抑制T細胞介導的炎癥活動來調節免疫系統并促進自身耐受。PD-1可以預防自身免疫性疾病,也可以阻礙免疫系統殺死癌細胞[6]。筆者采用PD-1抑制劑聯合GP化療方案治療NSCLC,以探討其對NSCLC患者療效的影響,現報道如下。
1 資料與方法
1.1一般資料 選取2018年3月至2019年3月本院收治的105例NSCLC患者,按照隨機數字表法將其分為對照組(52例)及觀察組(53例)。對照組年齡31~75歲,平均(62.3±7.5)歲;體質量51~65 kg,平均(56.43±5.12)kg。觀察組年齡31~76歲,平均(62.5±7.3)歲;體質量53~66 kg,平均(56.84±5.51)kg。兩組患者性別、年齡、TNM分期比較,差異無統計學意義(P>0.05),具有可比性,見表1。以上患者均于本院確診為NSCLC。本研究經本院倫理委員會批準,患者及家屬均知情并同意本研究。
1.2納入與排除標準 納入標準:未合并嚴重營養不良及貧血;無嚴重傳染性疾病;無精神系統疾病;符合內科學(第8版)中NSCLC的診斷標準[7]。排除標準:長期服用免疫抑制劑者;肝腎功能障礙者;合并急性感染者;入院前經系統性化療者;無法耐受本研究化療方案者;因各種原因無法完成本研究者;腫瘤肺外轉移者。

表1 兩組患者一般資料比較
1.3方法 對照組患者給予吉西他濱(國藥準字:H20123362;生產企業:連云港杰瑞藥業有限公司;日劑量為1 000 mg/m2)+順鉑(國藥準字:H20023461;生產企業:齊魯制藥有限公司;日劑量為75 mg/m2)進行治療,靜脈滴注。治療周期為20 d,共治療6個周期。觀察組在對照組基礎上給予PD-1抑制劑(國藥準字:S20180019;生產企業:美國默沙東公司;2 mg/kg)靜脈滴注,21 d為1個周期,共治療6個周期。若患者出現不適及不良反應,應及時報告上級醫師,并采取相應治療措施。比較兩組患者治療前及治療后6個月血清Survivin蛋白水平,治療前及治療后6個月CD4+、CD8+、CD4+/CD8+、自然殺傷(NK)細胞水平。觀察兩組患者治療后6個月的療效,治療前及治療后1、3、6個月的生存質量評分,以及不良反應發生情況。血清Survivin蛋白采用ELISA法進行測定。CD4+、CD8+、CD4+/CD8+、NK細胞采用流式細胞儀(HPC-150)進行檢測。所有操作均由本院檢驗科醫師按照說明書進行操作。
1.4療效評價 根據世界衛生組織(WHO)實體瘤的效果評價標準進行評價[7],將療效分為完全緩解(CR)、部分緩解(PR)、病情穩定(SD)和病情進展(PD)。疾病控制率=CR率+PR率+SD率;總有效率=CR率+PR率。

2 結 果
2.1兩組患者治療前后Survivin蛋白水平比較 兩組患者治療前Survivin蛋白水平比較,差異無統計學意義(P>0.05),治療后6個月兩組患者Survivin蛋白水平均明顯降低(P<0.05),觀察組患者Survivin蛋白水平明顯低于對照組(P<0.05)。見表2。
2.2兩組患者免疫功能比較 兩組患者治療前CD4+、CD8+、CD4+/CD8+、NK細胞水平差異無統計學意義(P>0.05),治療后6個月兩組患者CD4+、CD4+/CD8+、NK細胞水平與治療前比較,均明顯升高(P<0.05),觀察組患者治療后6個月的CD4+、CD4+/CD8+、NK細胞水平明顯高于對照組(P<0.05)。見表3。

表2 兩組患者治療前后Survivin蛋白水平比較
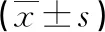
表3 兩組患者免疫功能比較
2.3兩組患者治療后6個月的療效比較 兩組患者治療后6個月的療效差異有統計學意義(P<0.05),觀察組總有效率及疾病控制率明顯高于對照組(P<0.05)。見表4。

表4 兩組患者治療后6個月的療效比較
2.4兩組患者治療前后的生存質量評分比較 治療前,兩組患者的生存質量評分差異無統計學意義(P>0.05),治療后1、3、6個月的生存質量評分比較,差異有統計學意義(P<0.05)。隨著治療的進行,兩組患者的生存質量評分均有明顯改善。治療后1、3、6個月觀察組患者的生存質量評分明顯高于對照組(P<0.05)。見表5。

表5 兩組患者的生存質量評分比較分)
2.5兩組患者不良反應比較 兩組患者均未出現嚴重不可逆不良反應。觀察組出現骨髓抑制6例,肝功能損傷3例,腎功能損傷2例。對照組出現骨髓抑制5例,肝功能損傷5例,腎功能損傷6例。兩組不良反應發生率比較,差異無統計學意義(P>0.05),且兩組患者的不良反應經調整藥物劑量后均得到顯著改善。
3 討 論
隨著生活污染的加重,肺癌的發病率呈逐年升高的趨勢[8-9]。近年來,化療逐漸成為NSCLC治療的重要手段,并取得了良好的治療效果。隨著分子生物學技術的不斷發展,越來越多的分子生物學靶點被用于NSCLC的治療,并被證明具有積極的治療效果。PD-1是一種重要的免疫抑制分子,為免疫球蛋白超家族成員。有研究發現,以PD-1為靶點的免疫調節對抗腫瘤、抗感染、抗自身免疫性疾病及促進移植器官的存活等均具有重要的意義[10-11]。其配體PD-L1也可作為靶點,相應的抗體可以起到相同的作用。PD-1和PD-L1結合啟動T細胞的程序性死亡,使腫瘤細胞獲得免疫逃逸。PD-1抑制劑是阻斷PD-1的一類新藥,可激活免疫系統以攻擊腫瘤,并用于治療某些類型的癌癥。
Survivin是凋亡抑制蛋白家族的新成員,Survivin具有腫瘤特異性,只表達于腫瘤和胚胎組織。有研究發現,Survivin與NSCLC患者腫瘤細胞的分化、增殖及浸潤轉移密切相關,其水平的升高提示腫瘤的快速增殖[12-13]。同時Survivin蛋白的表達也與NSCLC患者預后密切相關。為此,筆者將Survivin蛋白與CD4+、CD8+、NK細胞等免疫因子納為NSCLC患者預后的評價指標。本研究中,兩組患者治療前Survivin蛋白水平比較,差異無統計學意義(P>0.05),治療后6個月兩組患者Survivin蛋白水平均明顯降低(P<0.05),觀察組患者Survivin蛋白水平明顯低于對照組(P<0.05)。
兩組患者治療前CD4+、CD8+、CD4+/CD8+、NK細胞水平比較,差異無統計學意義(P>0.05),治療后6個月兩組患者CD4+、CD4+/CD8+、NK細胞水平與治療前比較,均明顯升高(P<0.05),且觀察組明顯高于對照組(P<0.05)。此結果表明,GP方案聯合PD-1抑制劑相對于GP方案更能有效改善NSCLC患者的免疫功能。CHEN等[14]也在研究中得出相似結論,可能與PD-1抑制劑有效抑制了PD-1導致的自身免疫細胞功能下調有關,這在很大程度上改善了人體的自身免疫對腫瘤細胞的殺傷能力。兩組患者療效比較,差異有統計學意義(P<0.05),觀察組總有效率及疾病控制率明顯高于對照組(P<0.05)。隨著治療的進行,兩組患者的生存質量評分均明顯改善,治療后1、3、6個月觀察組患者的生存質量評分明顯高于對照組(P<0.05)。此結果表明,GP方案聯合PD-1抑制劑相對于GP方案更能有效提升NSCLC患者的療效。CHEN等[15]也在研究中發現,GP方案聯合PD-1抑制劑能顯著改善NSCLC患者預后及生活質量,這可能與PD-1抑制劑有效減少了腫瘤細胞的免疫逃逸,顯著改善患者自身免疫功能有關,與本研究結果基本一致。兩組患者不良反應發生率比較,差異無統計學意義(P>0.05),且兩組患者不良反應較輕,經調整藥物劑量后均得到顯著改善。此結果表明,PD-1并不會顯著增加GP方案治療患者的相關不良反應,具有較高的安全性。本研究還存在不足之處,需擴大樣本量進一步證實其安全性。
綜上所述,GP方案結合PD-1抑制劑治療能有效提升NSCLC患者療效及改善免疫功能,提高患者生活質量,值得臨床推廣。

