2型糖尿病患者體質(zhì)量指數(shù)、血脂與胰島β細胞功能的相關(guān)性研究
薛 敏,馮 帆,姜國良,王 萍,湯智勤
上海市嘉定區(qū)南翔醫(yī)院內(nèi)分泌科,上海 201802
胰島素抵抗及胰島素分泌不足是2型糖尿病(T2DM)發(fā)病的重要病理生理機制[1],而胰島β細胞功能在其中發(fā)揮著至關(guān)重要的作用。胰島β細胞功能惡化的過程常伴隨著脂代謝的異常,包括血清三酰甘油(TG)、總膽固醇(TC)、低密度脂蛋白膽固醇(LDL-C)水平升高及高密度脂蛋白膽固醇(HDL-C)水平降低。脂代謝紊亂又可引起肥胖、高血壓等糖尿病慢性并發(fā)癥[2]。既往研究發(fā)現(xiàn),肥胖者常伴有明顯的內(nèi)臟脂肪蓄積、代謝紊亂、胰島素抵抗等癥狀,其糖尿病患病率為正常體質(zhì)量者的3倍[3]。而當(dāng)體質(zhì)量減輕后,組織對胰島素的敏感性會提高,血液中胰島素濃度降低,胰島β細胞的代償性分泌現(xiàn)象將會得到改善,胰島素抵抗水平降低[4]。因此,血脂異常及肥胖在胰島素抵抗和胰島β細胞分泌功能缺陷上可能起著重要的作用。
本研究通過對比T2DM患者的年齡、病程、體質(zhì)量指數(shù)(BMI)、血脂、空腹血糖(FBG)及空腹胰島素(FINS)水平,評估胰島素抵抗與胰島β細胞功能,探討T2DM患者胰島素抵抗及胰島β細胞分泌功能與BMI、血脂的相關(guān)性。
1 資料與方法
1.1一般資料 選取2018年12月至2019年12月本院內(nèi)分泌科門診收治的334例T2DM患者作為研究對象,其中男213例,女121例;平均年齡(58.62±14.27)歲;平均BMI(25.06±4.40)kg/m2。TC水平升高者164例,TG水平升高者169例,LDL-C水平升高者180例,HDL-C水平降低者219例。納入標準:患者均符合WHO推薦的T2DM診斷標準[5],且正在接受降糖治療,或者FBG≥7.0 mmol/L,同時排除妊娠期糖尿病、1型糖尿病和其他特殊類型糖尿病;近半年未接受胰島素治療。排除標準:有自發(fā)性酮癥酸中毒傾向;有嚴重的心臟、肝、腎、腦功能不全;近期服用嚴重影響糖代謝及脂代謝藥物;近期有感染或應(yīng)激情況;惡性腫瘤者。本研究通過本院倫理委員會審查,研究對象簽署知情同意書。
1.2方法 收集患者一般資料。受試者空腹8 h以上,于次日清晨取靜脈血樣。應(yīng)用Cobas e 601全自動生化免疫分析儀測定FBG、FINS、TC、TG、LDL-C、HDL-C,所有試劑均為配套試劑。根據(jù)《中國2型糖尿病防治指南》[5],TC<4.5 mmol/L,TG<1.5 mmol/L,LDL-C<2.6 mmol/L,HDL-C>1.1 mmol/L認為達到糖尿病患者的血糖控制目標,血脂水平正常。統(tǒng)一由專人測量患者脫鞋、穿單衣下體質(zhì)量、身高,并計算BMI=體質(zhì)量/身高2(kg/m2)。依據(jù)《中國成人超重和肥胖癥預(yù)防控制指南》建議[6],18.5 kg/m2≤BMI<24.0 kg/m2為正常,24.0 kg/m2≤BMI<28.0 kg/m2為超重,BMI≥28.0 kg/m2為肥胖。使用穩(wěn)態(tài)模型評估法(HOMA)評估胰島素抵抗指數(shù)(HOMA-IR):HOMA-IR=FBG(mmol/L)×FINS(mIU/L)/22.5;胰島β細胞功能指數(shù)(HOMA-β):HOMA-β=20×FINS(mIU/L)/[FBG(mmol/L)-3.5]×100%;胰島素敏感指數(shù)(HOMA-ISI)=1/[FBG(mmol/L)×FINS(mIU/L)]。
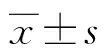
2 結(jié) 果
2.1胰島β細胞功能與各指標的相關(guān)性分析 Pearson相關(guān)分析結(jié)果顯示,HOMA-IR與BMI呈正相關(guān)(r=0.121,P=0.028),HOMA-ISI與HDL-C呈正相關(guān)(r=0.114,P=0.036),HOMA-β與年齡、病程、BMI、血脂水平均無相關(guān)性。見表1。

表1 胰島β細胞功能與各指標的相關(guān)性分析
2.2不同BMI水平患者臨床指標的比較 根據(jù)BMI將患者分為3組,即正常組、超重組、肥胖組。組間對比發(fā)現(xiàn),3組患者FBG、HOMA-IR差異有統(tǒng)計學(xué)意義(P<0.05)。多元線性回歸分析結(jié)果顯示,BMI是HOMA-IR的獨立影響因素(β=0.002,t=13.674,P<0.001)。見表2。

表2 不同BMI水平患者臨床指標的比較
2.3不同HDL-C水平的患者臨床指標的比較 根據(jù)HDL-C水平將患者分為兩組,即HDL-C正常組(HDL-C>1.1 mmol/L),HDL-C異常組(HDL-C≤1.1 mmol/L),組間對比發(fā)現(xiàn)兩組患者年齡、病程、FINS、HOMA-ISI差異有統(tǒng)計學(xué)意義(P<0.05)。多元線性回歸分析結(jié)果顯示,HDL-C是HOMA-ISI的獨立影響因素(β=0.001,t=2.281,P=0.023)。見表3。
3 討 論
胰島功能的進行性變化在T2DM發(fā)生與發(fā)展中起到至關(guān)重要的作用:早期由于脂肪因子、炎性介質(zhì)的作用,以及胰島素自身信號傳導(dǎo)異常,可導(dǎo)致機體對胰島素的敏感性降低、胰島素抵抗,使得胰島β細胞超負荷分泌胰島素。胰島β細胞功能長期失代償,最終導(dǎo)致β細胞衰竭、凋亡,T2DM患者病情逐漸惡化[7-8]。既往研究表明,脂代謝紊亂既是胰島素抵抗的結(jié)果,也會加重患者胰島素抵抗的病情,并引起胰島素分泌不足[9]。而肥胖患者具有明顯的糖脂代謝紊亂。因此,本研究選用穩(wěn)態(tài)模型,即HOMA-β、HOMA-IR、HOMA-ISI評估胰島β細胞功能及胰島素抵抗,并探討其與BMI、血脂的相關(guān)性。
本研究結(jié)果發(fā)現(xiàn),在T2DM患者中,BMI與HOMA-IR呈正相關(guān),HDL-C與HOMA-ISI呈正相關(guān)(P=0.036)。將患者按BMI水平分為正常、超重、肥胖3組,組間對比結(jié)果顯示FBG、HOMA-IR差異有統(tǒng)計學(xué)意義(P<0.05)。相較于健康人群,肥胖及超重人群FBG水平更高,胰島素抵抗更明顯。多元線性回歸分析顯示,BMI是T2DM患者胰島素抵抗的獨立影響因素。肥胖影響血糖及導(dǎo)致胰島素抵抗的可能機制為肥胖者脂肪體積較大,體內(nèi)脂肪累積較多,脂肪細胞容易產(chǎn)生缺氧,易引起細胞的炎性反應(yīng)和死亡,其產(chǎn)生的炎癥因子進一步干擾胰島素信號傳導(dǎo)通路,導(dǎo)致骨骼肌、脂肪組織和肝臟發(fā)生功能障礙[10],并且,肝內(nèi)脂肪變性能夠?qū)е赂闻K分泌激素的功能發(fā)生異常,從而不同程度地影響胰島素的效應(yīng),降低機體對胰島素的敏感性,導(dǎo)致胰島素抵抗[11]。此外,脂肪細胞分泌抵抗素降低細胞對葡萄糖的攝取量,使得胰島β細胞無法攝取葡萄糖,進而抑制了胰島β細胞分泌胰島素。然而本研究并未觀察到BMI與HOMA-β的相關(guān)性,原因可能為T2DM前期胰島素分泌能力降低不明顯,但是當(dāng)病程超過10年后,其胰島β細胞分泌胰島素的能力會下降31.5%~39.1%[10]。
本研究還發(fā)現(xiàn),以HDL-C為1.1 mmol/L作為界值將患者分為兩組,兩組年齡、病程、FINS、HOMA-ISI差異均有統(tǒng)計學(xué)意義(P<0.05)。HDL-C低于標準值的T2DM患者年齡更大、病程更長、FINS更低,且胰島素敏感性顯著低于HDL-C正常的T2DM患者。多元線性回歸分析顯示,HDL-C是T2DM患者胰島素敏感性的獨立影響因素。既往研究發(fā)現(xiàn),HDL-C水平直接影響新診斷T2DM患者的胰島β細胞功能[12],且在糖代謝受損的患者中,HDL-C水平與胰島素生成指數(shù)及HOMA-ISI高度相關(guān)[13]。本研究證實了上述理論,血脂代謝紊亂導(dǎo)致胰島β細胞功能障礙的可能機制有:(1)HDL-C參與TC逆向轉(zhuǎn)運。HDL-C降低會使TC等脂質(zhì)過量蓄積于機體胰島素敏感組織中,產(chǎn)生局部炎性反應(yīng)及巨噬細胞浸潤,導(dǎo)致外周胰島素抵抗[14-15]。(2)TC等成分在脂肪組織中沉積,可導(dǎo)致脂肪細胞體積增大、數(shù)量增多,使得胰島素受體數(shù)目相對減少,活性相對降低,導(dǎo)致胰島素敏感性降低[8]。(3)HDL-C降低及高膽固醇血癥可引起血清可溶性P-選擇素水平升高,后者可通過影響細胞代謝及介導(dǎo)免疫炎性反應(yīng)而導(dǎo)致并加重胰島素抵抗,進一步影響機體血糖水平[16]。
既往研究發(fā)現(xiàn),LDL-C可以參與胰島素抵抗,影響胰島β細胞增殖、凋亡及胰島素分泌[17],LDL-C水平升高是糖尿病發(fā)病的獨立危險因素。國內(nèi)研究發(fā)現(xiàn),口服降糖藥物治療的老年T2DM患者中LDL-C與HOMA-IR具有相關(guān)性[18],而在本文中并無此發(fā)現(xiàn),這可能是由于本研究樣本量相對較小,可能影響研究結(jié)果。針對LDL-C與T2DM患者胰島β細胞功能的相關(guān)性研究仍有待后續(xù)大樣本臨床試驗驗證。