冷/熱榨紫蘇子油氧化穩定性及其α-亞麻酸氧化動力學探究
易 醒,羅俊溢,易孜成,李 娟,袁弋婷,夏小華,桂靜芬,肖小年*
(南昌大學a.中德食品工程中心;b.中德聯合研究院,江西 南昌 330047)
紫蘇(Perilla frutescens)是一年生的可食用植物[1],廣泛種植于我國的西南和華中一帶[2]。紫蘇的干燥成熟果實為紫蘇子,將其壓榨后可得紫蘇子油,研究表明,紫蘇子油是一種高度不飽和的天然油脂,有抗氧化[3]、抗腫瘤[4]、抗菌以及抑制真菌[5]、抗炎[6]、抗過敏[7]、抗抑郁[8-9]的作用,此外還具有降低低密度脂蛋白所載膽固醇的作用[10]。紫蘇子油中含有大量的α-亞麻酸(ω-3脂肪酸),占脂肪酸總量的61.1%~64.0%[11-13],其次為亞油酸和油酸,含量差異不大,分別占脂肪酸總量的15.0%左右,此外還有少量的三酰基甘油、甾醇和磷脂類物質[14]。
紫蘇子油中含有較多不飽和脂肪酸,在儲藏過程中易受到光、熱、氧氣、微生物、重金屬等因素的影響,繼而分解成酮類、醛類化合物以及其它氧化物,不利于食用。通過現代科技手段,可有效的控制紫蘇子油的氧化。對紫蘇子油氧化的控制,可從改善制油工藝及添加抗氧化劑兩方面著手進行。有研究表明紫蘇子油的萃取方法對紫蘇子油的氧化穩定性有重要影響,Jung Dongmin等[13]比較了二氧化碳萃取法、壓榨法以及溶劑提取法對紫蘇子油氧化穩定性的影響,發現使用二氧化碳萃取的紫蘇子油在60 ℃黑暗條件下的氧化穩定性低于壓榨萃取和己烷萃取法,使用不同萃取方法所得的紫蘇子油中的脂肪酸組成成分大致相同。
Zhao Tingting等[15]比較了紫蘇種子經過180 ℃,200 ℃,220 ℃烘烤預處理,再用烘烤后的種子進行榨油,發現隨烘烤溫度的升高,壓榨油脂中的反式脂肪酸的含量逐漸上升,在60 ℃貯藏條件下,未經烘烤預處理較經過烘烤預處理所得紫蘇種子油,其生育酚損失速率較快。除了在提取工藝上進行優化創新以外,添加抗氧化劑提高植物油脂氧化穩定性是常用方法,天然的抗氧化劑一般選擇VE、VC以及植物甾醇等[16-18],合成抗氧化劑主要有2,6-二叔丁基-4-甲基苯酚(BHT)、丁基化羥基茴香醚(BHA)、特丁基對苯二酚(TBHQ)等[19-20]。
為了研究冷、熱榨不同加工方式對油脂品質的影響,本文以冷、熱榨紫蘇子油為研究對象,探討溫度、光照、抗氧化劑及增效劑對紫蘇子油過氧化值(POV值)的改變,并考察其主要成分α-亞麻酸的氧化動力學。
1 材料與方法
1.1 原料與試劑
冷榨、熱榨紫蘇子油(實驗室自制);TBHQ、BHT、檸檬酸(CA)、異抗壞血酸鈉(D-VcNa)均為食品級,廣州泰邦食品添加劑有限公司;VE軟膠囊(食品級),天之海藥業;α-亞麻酸對照品(HPLC≥98%),上海源葉生物科技有限公司;甲醇、乙腈均為色譜純,天津市永大化學試劑有限公司;磷酸為分析純級,天津市永大化學試劑有限公司。
1.2 儀器與設備
KOMET冷榨油機,德國IBG公司;Agilent1200高效液相色譜儀,安捷倫科技有限公司;EYELAN-1100旋轉蒸發儀、EYELAOSB-2100油浴鍋,上海愛郎儀器有限公司。
1.3 試驗方法
1.3.1 紫蘇子油中α-亞麻酸含量測定方法建立
根據參考文獻建立測定方法[21],精確吸取α-亞麻酸對照品儲備液(2 mg·mL-1,甲醇配制)0.4,0.8,1,2,4 mL,定容至10 mL棕色容量瓶中(甲醇),于液相色譜儀中測定(檢測波長:205 nm,柱溫:30 ℃,流動相:乙腈/0.1%磷酸=90:10,V/V,色譜柱:Marchal C18(250 mm×4.6 mm,5 μm))。
1.3.2 測定紫蘇子油的氧化穩定性
(1)紫蘇子油過氧化值的測定。采用GB 5009.227[22]中所述方法測定紫蘇子油的POV值。
(2)溫度對氧化穩定性的影響。將等質量(30 g)冷榨和熱榨紫蘇子油分別于室溫下避光(25 ℃)和630±1 ℃烘箱中避光保存。每隔1 d測定其POV值,每組試驗重復3次。
(3)光照對氧化穩定性的影響。分別將等質量(30 g)冷榨和熱榨紫蘇子油置于室溫下避光(25 ℃)和光照下(250Lx)保存。每隔1 d測定其POV值,每組試驗重復3次。
(4)不同抗氧化劑對氧化穩定性的影響。分別取等質量(20 g)冷榨以及熱榨紫蘇子油,添加等量的VE、BHT、TBHQ,使用Schaal烘箱法對樣品進行處理[23]后測定其POV值(隔3 d測1次),每組試驗重復3次。
(5)抗氧化劑復配對氧化穩定性的影響。將抗氧化劑按0.01%TBHQ+0.01%BHT、0.01%TBHQ+0.01%VE和0.01%BHT+0.01%VE進行復配后分別加入到等質量(20 g)的冷榨和熱榨紫蘇子油中,按文獻所述方法對樣品進行處理和測定[21],每組試驗重復3次。
(6)抗氧化增效劑對氧化穩定性的影響。將0.015%TBHQ+0.005%CA、0.015%TBHQ+0.005%D-VCNa、0.015%BHT+0.005%CA、0.015%BHT+0.005%D-VCNa進行復配后分別加入到等質量(20 g)的冷榨和熱榨紫蘇子油中,按文獻所述方法對樣品進行處理和測定[21],每組試驗重復3次。
1.3.3 紫蘇子油α-亞麻酸氧化動力學研究
根據加速氧化實驗探究加速氧化過程中冷/熱榨紫蘇子油中α-亞麻酸含量的變化。分別取等質量(20 g)冷榨和熱榨紫蘇子油,使用Schaal烘箱法對樣品進行處理,隔1 d取1次樣,共20 d。取樣后,對樣品甲酯化處理,測定α-亞麻酸含量,考察α-亞麻酸氧化動力學[21]。反應動力學模型擬合方程:
零級反應動力學方程:Y0=Yx=k0x
一級反應動力學模型:lnYx=-kt+lnY0式中:Y0—初始α-亞麻酸濃度,Yx—氧化x時α-亞麻酸的濃度,x—氧化時間,k0、kt—反應速率常數。
1.4 數據分析
實驗數據采用Origin2017軟件進行處理及作圖。
2 結果與分析
2.1 冷/熱榨紫蘇子油的系統適應性和α-亞麻酸含量的標曲建立
α-亞麻酸對照品冷榨紫蘇子油、熱榨紫蘇子油的色譜圖可得(圖1),冷/熱榨紫蘇子油中α-亞麻酸的保留時間與標準品保持一致,且α-亞麻酸的色譜峰與相鄰色譜峰的分離度大于1.5。擬合后的α-亞麻酸的線性回歸方程為Y=35 639X+162.82,R2=0.999 4,α-亞麻酸含量測定在0.04~0.4 mg·mL-1范圍內線性良好。
2.2 溫度對冷/熱榨紫蘇子油氧化穩定性的影響
紫蘇子油在室溫避光和烘箱避光下的POV值隨時間變化情況如圖2所示。由于熱能可能引發自由基的大量產生,使冷/熱榨紫蘇子油的過氧化值在烘箱貯存中變化明顯,而在室溫條件下兩種工藝制備的紫蘇子油POV值改變不大,說明溫度可顯著影響紫蘇子油的氧化速率。GB 2716規定,植物原油的POV值應小于19.7 meq·kg-1。根據文獻報道[24],在60 ℃貯存24 h相當于20 ℃下放置384 h。因此,烘箱避光保存條件下,冷榨油的儲存期限為176 d,熱榨油的儲存期限為112 d。
2.3 光照對冷/熱榨紫蘇子油氧化穩定性的影響
由圖3結果表明,光照對冷/熱榨紫蘇子油POV值的增加有較大影響,可能是光照促進了紫蘇子油中氫過氧化物的降解,從而使紫蘇子油的氧化速率增加。冷榨和熱榨紫蘇子油的氧化穩定性在光照條件下較避光時差,因此光照對紫蘇子油的氧化影響較大。
2.4 單一抗氧化劑對冷/熱榨紫蘇子油氧化穩定性的影響
采用Schaal烘箱法進行測定,試驗結果如圖4所示。TBHQ和BHT對紫蘇子油的POV值的升高具有抑制作用,可能是因為TBHQ和BHT能與自由基穩定結合,中止自由基的連鎖反應。VE的加入對紫蘇子油POV值的變化表現為促進作用,可能原因試驗添加的VE稍有過量,過量的VE在猝滅單線態氧的同時,其自身化極易被單線態氧所氧化,產生氫過氧化物,從而起到促進氧化的作用[25]。通過比較TBHQ和BHT對紫蘇子油氧化穩定性的影響,發現添加了TBHQ的紫蘇子油其POV值上升速率慢于BHT,說明TBHQ與自由基結合的能力要強于BHT[26]。通過冷、熱榨紫蘇子油的儲藏時間進行考察,表明添加TBHQ將冷、熱榨紫蘇子油的儲藏時間分別延長了304和416 d,而添加BHT的儲藏時間分別延長了304和272 d。
2.5 復配抗氧化劑對冷/熱榨紫蘇子油氧化穩定性的影響
采用Schaal烘箱法測定,試驗結果如圖5所示,復配抗氧化劑對紫蘇子油POV值上升的抑制作用要強于單一抗氧化劑,將TBHQ與BHT復配對紫蘇子油的氧化穩定性表現為較好的促進作用,可能是TBHQ與BHT之間可通過電子轉移等方式提供和維持了抗氧化劑的含量,從而使抗氧化能力增強[27-28]。TBHQ和VE的復配效果次之,可能是因為TBHQ在該體系中占據了主導作用,而作為次抗氧化劑的VE可能將TBHQ·還原為TBHQ,使體系中主抗氧化劑的有效濃度增加,提高了復配抗氧化劑的抗氧化活性[29]。BHT和VE復配對紫蘇子油的氧化穩定性的促進作用相對較差,可能是因為VE不能有效的將BHT·還原為BHT所致。
2.6 抗氧化增效劑對冷/熱榨紫蘇子油氧化穩定性的影響
由圖6和圖7可得,D-VcNa和CA對冷、熱榨紫蘇子油都表現出較好的抗氧化作用,且在相同條件下,相對于D-VcNa,CA對抗氧化劑的增效作用較好,可能原因是紫蘇子油中存在某些對油脂氧化具有催化作用的金屬離子(如Cu2+、Fe2+、Mu2+、Ni2+)[30],從而賦予了抗氧化劑良好的抗氧化增效作用,但是CA比D-VcNa更容易絡合油脂中的金屬離子,有效降低了油脂中催化劑的含量,從而阻止了油脂中自由基大量的誘發[31]。通過TBHQ和CA復配結果可得,冷榨紫蘇子油的儲藏時間延長了352 d,熱榨紫蘇子油的儲藏時間延長了432 d;通過BHT和CA復配結果可得,冷榨紫蘇子油的儲藏時間延長了288 d,熱榨紫蘇子油的儲藏時間延長了208 d。
2.7 加速氧化過程中冷/熱榨紫蘇子油中α-亞麻酸含量的變化
表1和2顯示,隨氧化時間的增加,冷、熱榨紫蘇子油中α-亞麻酸的含量有顯著降低。通過20 d的考察發現,其中冷榨紫蘇子油和熱榨紫蘇子油中α-亞麻酸含量分別減少了14.59%和19.47%。
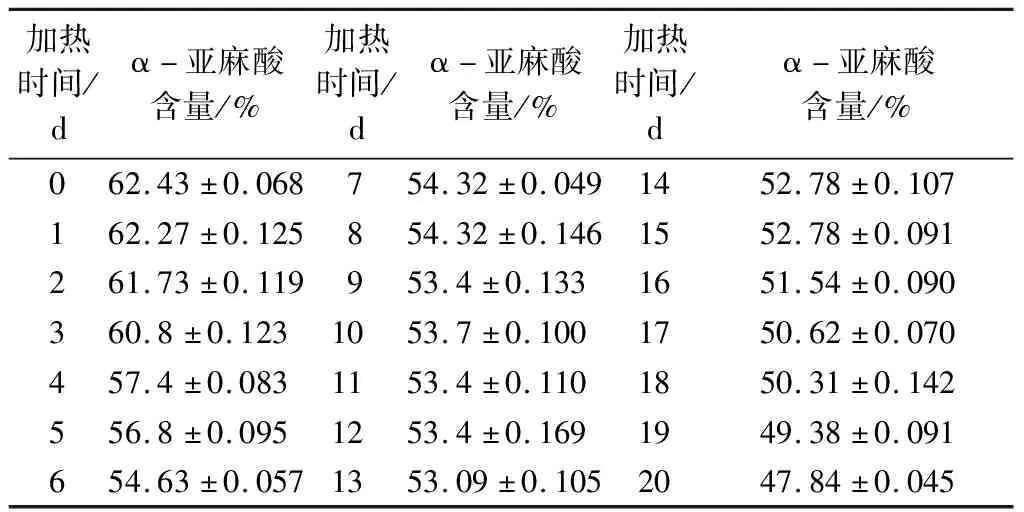
表1 加速氧化過程中冷榨紫蘇子油中α-亞麻酸含量的變化
2.8 α-亞麻酸氧化動力學模型
表3為α-亞麻酸氧化動力學數據分析結果。冷榨紫蘇子油α-亞麻酸含量的變化模型最佳擬合方程為一級反應動力學方程,其擬合優度(R2)為0.908,呈指數變化趨勢,其方程可表示為lnY=61.183-0.012x;熱榨紫蘇子油α-亞麻酸含量的變化模型最佳擬合方程為零級反應動力學方程,其擬合優度(R2)為0.930,呈線性變化趨勢,其方程可表示為Y=62.334-1.151x。兩種擬合模型的擬合優度都大于0.85,因此可以用這兩個方程來分析α-亞麻酸的氧化動力學。

表2 加速氧化過程中熱榨紫蘇子油中α-亞麻酸含量的變化

表3 α-亞麻酸反應動力學模型的參數及相關系數值
3 結論
本文主要探討了冷/熱榨紫蘇子油的氧化穩定性及α-亞麻酸的氧化動力學。在63 ℃避光保存條件下,冷/熱榨紫蘇子油的過氧化值達19.7meq·kg-1所用時間分別為11和9d,在250Lx光照室溫保存下,冷/熱榨紫蘇子油的過氧化值達19.7meq·kg-1所用時間分別為6和4d。因此相對于光照,溫度對紫蘇子油的氧化性有顯著影響,因此紫蘇子油貯存需低溫避光。通過比較單一抗氧化劑TBHQ和BHT對紫蘇子油氧化穩定性的影響,添加了單一抗氧化劑TBHQ的冷/熱榨紫蘇子油,其過氧化值達19.7meq·kg-1所用時間分別為33和30d。添加了單一抗氧化劑TBHQ的冷/熱榨紫蘇子油,其過氧化值達19.7meq·kg-1所用時間分別為18和12d,說明TBHQ與自由基結合的能力要強于BHT。復合抗氧化劑TBHQ+BHT對紫蘇子油的抗氧化性的增加效果最好,冷/熱榨紫蘇子油的過氧化值達19.7meq·kg-1時所用時間均為36d。增效劑(CA和D-VcNa)與抗氧化劑之間表現為協同作用,且CA對抗氧化劑的增效作用均優于D-VcNa。通過分析紫蘇子油中α-亞麻酸含量隨時間變化情況可得,冷榨法制備的紫蘇子油中α-亞麻酸的氧化過程符合一級動力學方程lnY=61.183-0.012x,其擬合優度為R2=0.908,熱榨法制備的紫蘇子油中α-亞麻酸的氧化過程符合零級動力學方程Y=62.334-1.151x,其擬合優度為R2=0.930。

