二甲雙胍對伴胰島素抵抗的多囊卵巢綜合征患者血清Asprosin水平的影響*
郭婭棣 高燕燕 劉建國 鄧玉杰
(1.中國石油大學(華東)醫院內分泌科,山東 青島 266580;2.青島大學附屬醫院內分泌科,山東 青島 266580;3.中國石油大學(華東)化學工程學院,山東 青島266580)
多囊卵巢綜合征 (polycystic ovary syndrome,PCOS)是育齡期女性常見的一種內分泌及代謝紊亂性疾病,臨床表現為多毛、痤瘡、肥胖、閉經及不孕等。流行病學調查發現,PCOS患者中35%~60%合并肥胖[1-2]。肥胖可由脂肪組織堆積及功能異常導致。脂肪組織可分泌多種細胞因子,其分泌異常可引發胰島素抵抗(IR)、糖尿病和心血管疾病等。近年來,脂肪因子與PCOS的關系成為研究熱點[3-5]。Asprison是在 2016年被發現的一種新型脂肪因子[6],由白色脂肪細胞分泌,作用于肝臟,可促進肝糖元分解和釋放,升高血糖[6]。最新一項國外研究發現,Asprison與PCOS患者的IR有一定的相關性[7]。研究證實,二甲雙胍可以改善IR[8],是治療PCOS較有效的藥物。本研究觀察二甲雙胍對PCOS患者血清Asprosin的影響,并探討其作用機制,為PCOS的治療提供新的理論依據。
1 資料與方法
1.1 一般資料 選取中國石油大學醫院2019年1月~2019年10月門診及住院的55例初診PCOS患者,年齡18~75歲,均符合PCOS的診斷標準[9]。排除標準:①其他可導致月經周期不規則的疾病。②其他內分泌與代謝性疾病,如原發性甲狀腺功能減退癥、庫欣綜合征等導致繼發性肥胖的疾病及藥物引起的肥胖。③冠心病、糖尿病、高脂血癥、高血壓等并發癥。④急慢性感染,自身免疫性、遺傳性及傳染性疾病。⑤嚴重肝腎功能不全者。⑥臨床資料不全者。⑦精神疾病史及家族史者。⑧惡性腫瘤史者。⑨妊娠和哺乳者。⑩近半年內接受任何外科手術患者。本研究已通過本院倫理委員會批準,所有受試者均簽署知情同意書。
1.2 方法
1.2.1 資料收集 詳細記錄受試者的一般情況、既往史、個人史、家族史等臨床資料。由專業固定人員測量身高、腰圍、臀圍、體質量、坐位血壓(包括收縮壓和舒張壓)。計算腰臀比(WHR)=腰圍(cm)/臀圍(cm);BMI=體質量(kg)/身高(m2)。給予患者二甲雙胍(中美上海施貴寶制藥 有限公司;國藥準H20023370;規格:0.5g×20s)口服,0.5g/次,3次/d,共治療3個月。
1.2.2 指標測定 禁酒,禁高糖、高脂飲食1月;已閉經者于任意一天,有月經者在月經周期第3~5 d,隔夜空腹至少8 h,于次日清晨7∶00~9∶00采集外周靜脈血,室溫(20~25 ℃)下靜置30 min,離心,取上清液,-80 ℃以下冷凍保存。治療前后分別采用全自動生化儀測定總膽固醇(total cholesterol,TC)、TG、高密度脂蛋白(HDL-C)、低密度脂蛋白(LDL-C)、FBG采用化學發光法測定FINS、LH、卵泡刺激素(FSH)、T、硫酸脫氫表雄酮(dehydroepiandrosterone sulfate,DHEA-S)、SHBG。計算一般穩態模型下HOMA-IR=FINS(μU/mL)×FBG(mmol/L)/22.5和FAI=[T(nmol/L)×100]/SHBG(nmol/L);采用酶聯免疫吸附法測定(Abcam公司,英國)PCOS患者血清Asprosin的濃度。
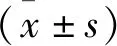
2 結果
2.1 一般臨床資料及相關指標比較 55例入選患者中,兩例病例因不耐受二甲雙胍胃腸道反應中斷用藥并退出實驗;3例患者因病情需要改用其他藥物治療。PCOS患者治療后BMI、TG、FBG、FINS、HOMA-IR、LH、T、FAI、Asprosin顯著低于治療前(P<0.05);SHBG顯著高于治療前(P<0.05);治療前后患者收縮壓、舒張壓、腰圍、臀圍、WHR、TC、HDL-C、LDL-C、FSH、Estradiol、DHEA-S差異無統計學意義(P>0.05),見表1。
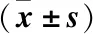
表1 治療前后各指標比較Table 1 Comparison of indicators before and after treatmen
2.2 治療后血清Asprosin的變化與其他指標的變化的相關性
2.2.1 相關分析 分析提示治療后較治療前PCOS患者血清Asprosin濃度的下降分別與BMI、TG、HOMA-IR、FAI的下降均呈正相關(r為0.287、0.865、0.425、0.291,P<0.05或0.01),見表2。

表2 治療前后血清Asprosin的變化與各指標變化的相關性分析Table 2 Correlation analysis of serum Asprosin changes and the changes of each indicator before and after treatment
2.2.2 多元逐步回歸分析 以血清Asprosin的下降為因變量,BMI、TG、HOMA-IR、FAI的下降為自變量進行多元逐步回歸分析顯示,HOMA-IR及TG的下降為血清Asprosin的下降的獨立相關因素(β=0.208、0.810,P<0.05),見表3。

表3 治療前后血清Asprosin的下降與相關因素變化的多元逐步線性回歸分析Table 3 Multiple stepwise linear regression analysis of the decrease of serum Asprosin and the changes of related factors before and after treatment
3 討論
PCOS在育齡期婦女中發病率為5%~10%,在無排卵性不孕患者中可高達30%~60%[10]。以高雄激素水平、持續無排卵、胰島素抵抗等癥狀為主要特點,嚴重威脅婦女的健康[11]。PCOS發病病因尚不明確[12],目前仍是各相關專業學科的研究熱點。
PCOS臨床特點之一為高胰島素血癥,并伴有IR狀態。二甲雙胍屬于胰島素增敏劑,可糾正高胰島素血癥,可改善PCOS患者高胰島素血癥及IR,改善卵巢的排卵功能[13-14]。目前二甲雙胍成為治療PCOS無排卵型的一線用藥。此外,二甲雙胍還能改善肥胖,一半以上的PCOS患者使用二甲雙胍后體重減輕[15]。過半的PCOS患者中伴有肥胖,而IR是聯系肥胖與糖脂代謝紊亂的樞紐。其中,脂肪組織因子分泌異常是肥胖引起IR的一項重要因素。脂肪細胞可以分泌多種脂肪因子,例如,網膜素、脂聯素、趨化素、內脂素等,脂肪因子的改變可影響PCOS患者的胰島素分泌和作用[3-5]。Asprosin是由白色脂肪細胞分泌,為FBN1基因的第65及66位外顯子編碼而成的原纖維蛋白前體(profibrillin)C末端裂解分子片段[6]。Asprosin的靶器官為肝臟,可通過肝細胞G蛋白-cAMP-PKA信號通路,調節肝糖代謝,引起血糖升高。Asprosin水平的升高與胰島素抵抗的PCOS的患病風險有一定的相關性,可以作用于大腦下丘腦,調節食欲和體重[6-7]。本研究發現,二甲雙胍治療后BMI降低,而且與Asprosin的降低正相關,推測PCOS患者體內Asprosin濃度變化與肥胖密切相關。另外,Zhang等[16]研究發現在2型糖尿病患者中,空腹血糖是Asprosin升高的獨立相關因素。PCOS患者多伴有糖代謝紊亂,而本文發現,二甲雙胍治療后FBG較前降低,與二甲雙胍降糖作用有關。PCOS患者多伴有脂代謝異常,TG為PCOS患者血清Aspersion的獨立相關因素,血清Asprosin參與PCOS患者的脂質代謝,并可能引起其代謝紊亂[6]。本研究發現,二甲雙胍治療后TG的下降與Asprosin的下降呈正相關,且與其獨立相關。而肝臟作為脂肪因子Asprosin的靶點,由此推測,二甲雙胍可能通過改變脂質代謝進而減低Aspersion的水平。
PCOS發病的首要特點為雄激素明顯升高。PCOS患者高雄激素水平與IR正相關,共同參與PCOS的發生發展。雄激素可以通過抑制肝臟對血胰島素的清除和外周組織對胰島素的降解。而反過來,胰島素可以直接刺激腦垂體,增加黃體生成素的生成,促進卵泡膜細胞的增生,進而提高雄激素的合成;并通過減少性激素結合球蛋白的分泌,提高雄激素的利用度。研究證實,二甲雙胍通過胰島素增敏的作用進而改善高雄激素血癥,并通過降低胰島素水平進而減少睪酮的分泌及調節其他性激素水平[17]。Zhang等[16]研究顯示,Asprosin在男、女性體內的含量無明顯差異。而Murat[7]認為,FAI及HOMR-IR為Asprosin的獨立相關因素。FAI可以反映IR水平,其敏感性較游離睪酮更高[18]。診斷高雄激素血癥首選FAI,其較單純查總睪酮或游離睪酮優越[19]。FAI用于檢測PCOS患者高雄激素血癥的陽性率最高,能更好的指導PCOS臨床診斷和治療[20-21]。本研究推測二甲雙胍降低Asprosin水平,可能與改善胰島素抵抗有關,而與其改善性激素分泌無明顯相關性。二甲雙胍改善PCOS患者胰島素抵抗通過脂肪因子方面又增添新的成員,進一步完善臨床數據分析。但今后仍需進行大量的臨床及基礎研究探討其分子作用機制,為PCOS的治療提供新的理論支持。
4 結論
二甲雙胍可降低 PCOS患者血清Asprosin濃度水平,可能與其改善胰島素抵抗及降脂作用有關。

