氣相分子吸收光譜法測定水中硫化物的不確定度評定
孫洪梅,李 陽,馬清書,張 昊
(國家飲用水產品質量監督檢驗中心,吉林白山 134300)
硫化物是指水中溶解性無機硫化物和酸溶性金屬硫化物的總和。包括溶解性的H2S、HS-、S2-,以及存在于懸浮物中可溶性硫化物和酸可溶性金屬硫化物[1]。利用氣相分子吸收光譜儀對水中硫化物進行測定,前處理過程簡單,所需試劑少,儀器操作過程方便,大量節省時間[2]。本文采用氣相分子吸收光譜法對水中硫化物進行測量[3],并對測定結果不確定度進行評定。
1 水中硫化物不確定度評估
1.1 水中硫化物不確定度來源
水中硫化物測量不確定度來源有以下幾方面。①由最小二乘法原理進行擬合校準曲線引入的不確定度u1。②硫化物標準溶液引入的不確定度u2。③稀釋配制標準使用溶液引入的不確定度u3。④氣相分子吸收光譜儀性能產生的不確定度u4。
1.2 水中硫化物不確定度分量評估
1.2.1 由最小二乘法原理進行擬合校準曲線引入的不確定度u1[4]
由表1可知,由最小二乘法進行擬合求得校準曲線:y=0.068 61x+0.000 35,r=0.999 9,a=0.000 35,b=0.068 61。7個標準濃度點的均值為=0.642 86,樣品測定結果x=0.380 mg/L。

表1 擬合校準曲線的不確定度分量的相關計算結果表
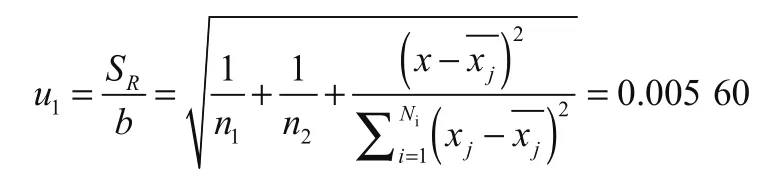

式中:sR-標準溶液響應信號殘差的標準差;n2-標準溶液的測定次數;n1-試樣中待測物質含量的測定次數;X-待測物的測定結果;xj-參加擬合的每一次測量的標準溶液含量;-標準溶液的平均值。
1.2.2 硫化物標準溶液引入的不確定度u2
硫化物標準溶液濃度為(100±5%) μg/mL,證書給出的擴展不確定度為5%,即5 μg/mL,并指出K=2,其帶來的不確定度分量為:U2=5/2=2.5 μg/mL。
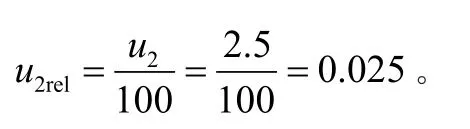
1.2.3 稀釋配制標準使用液引入的不確定度
(1)5 mL移液管引入的相對不確定度分量。5 mL移液管容量允差為:(5.00±0.015) mL[5],試驗時溫度為:22 ℃。5 mL移液管容量允差引入的不確定度計算為:溫度引入的不確定度計算為:
上述2項不確定度分量引入的體積的不確定度計算為:

(2)250 mL容量瓶引入的相對不確定度分量。250 mL容量瓶容量允差為:(250.0±0.10) mL,試驗時溫度為:22 ℃。250 mL容量瓶容量允差引入的不確定度計算為:溫度引入的不確定度計算為:
稀釋配制標準使用溶液引入的相對不確定度為:

1.2.4 氣相分子吸收光譜儀性能產生的不確定度
不確定度評定的方式可實際進行測量,求出測量儀器重復性的標準不確定度U4。
濃度為0.40 mg/L的測試水樣(經標準溶液配制),經氣相分子吸收光譜儀重復測定8次,根據表2數據,其標準偏差計算為:,標準不確定度為:相對不確定度為:

表2 水樣重復測定結果表
1.3 合成標準不確定度
根據上述水中硫化物不確定度的各個分量,相對合成標準不確定度為:
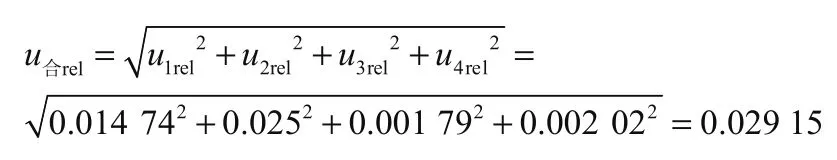
合成不確定度為:

1.4 擴展不確定度
擴展不確定U=k×u合,包含因子k=2,U=2×0.011 08=0.022 mg/L。
2 水中硫化物檢測結果
根據HJ/T 200—2005方法對試驗樣品進行測定,得到水中硫化物的檢測結果為ρ=(0.380±0.022) mg/L(k=2)。
3 結論與討論
根據《水質硫化物的測定氣相分子吸收光譜法》(HJ/T 200—2005)進行硫化物的測定,測得濃度為0.380 mg/L的水樣,其擴展不確定度為0.022 mg/L。通過以上不確定度分析、合成、計算可知,氣相分子吸收光譜法進行硫化物的測定中,最大不確定度是由硫化物標準溶液引入的,其次是由校準曲線擬合的影響。

