高血壓患者視網膜病變與血清脂蛋白相關磷脂酶A2的相關性
吳玉呈,張青青
泰州市人民醫院心內科1、內分泌科2,江蘇 泰州 225300
目前,高血壓病已逐漸成為我國最嚴重的慢性病之一[1]。高血壓相關并發癥已嚴重降低高血壓患者的生活質量。高血壓性視網膜病變(hypertensive retinopathy,HRP)是高血壓常見的并發癥,是由長期高血壓所引發的眼底相關疾病,其患病時間越長,則視力受損越嚴重,疾病越難以康復。高血壓視網膜病變已成為成人失明的最主要原因之一,但其發病機制仍未完全闡釋清楚[2-3]。
脂蛋白相關磷脂酶A2 (Lp-PLA2)是一種具有血管特異性的新型生物標志物。相關研究顯示Lp-PLA2水平與高血壓腎病的發生發展具有一定的相關性[4-5],而同屬于高血壓微血管病變的視網膜病變與Lp-PLA2水平是否也存在關聯,仍有待研究。本研究旨在探討高血壓患者視網膜病變與Lp-PLA2的相關性。
1 資料與方法
1.1 一般資料 選取2019 年1 月至2020 年8 月在南通大學附屬泰州市人民醫院心內科住院的116例高血壓患者為研究對象,所有患者均符合1999年世界衛生組織/國際高血壓學會(WHO/ISH)高血壓診斷標準[6],所有患者均行免散瞳眼底照相(德國蔡司VISUCAM 200 無散瞳眼底照相機),根據免散瞳眼底照相結果分為高血壓合并視網膜病變52例(觀察組)和單純高血壓64例(對照組)。排除標準:(1)繼發性高血壓患者;(2)合并腦血管意外等急性并發癥;(3)急、慢性感染者;(4)不能配合研究者;(5)合并嚴重肝、腎功能不全或其他相關眼部疾病。本研究獲得南通大學附屬泰州市人民醫院醫學倫理委員會批準,所有研究對象均簽署知情同意書。
1.2 研究方法 收集入選者的一般情況,包括性別、年齡、既往史、個人史等,由專業護士測量其空腹狀態下的身高、體質量,并計算身體質量指數(BMI)=體質量/身高2,同時測量入院時收縮壓(SBP)、舒張壓(DBP)。研究對象需空腹10~12 h,于次日清晨抽取靜脈血檢測下列指標:采用全自動生化分析儀(上海德賽日立7600)檢測總膽固醇(TC)、高密度脂蛋白膽固醇(HDL-C)、低密度脂蛋白膽固醇(LDL-C)、甘油三酯(TG)、載脂蛋白AI(Apo-AI)、載脂蛋白(Apo-B)、ApoAI/ApoB、脂蛋白(a)、載脂蛋白E(ApoE),采用高壓液相色譜法檢測糖化血紅蛋白(HbA1c),采用雙抗體夾心免疫層析法檢測Lp-PLA2 (北京熱景生物技術有限公司)。所有患者均行免散瞳眼底照相(德國蔡司VISUCAM 200無散瞳眼底照相機),由經過培訓的內分泌科醫生查看眼底。觀察組患者視網膜病變程度按照WONG等[7]提出的HRP 4級分類法進行分級。
1.3 統計學方法 應用SPSS18.0 軟件進行數據統計學分析。計量資料以均值±標準差()表示,兩組間比較采用t 檢驗。定性資料采用率表示,兩組間比較用χ2檢驗。Lp-PLA2 與各檢測指標相關性采用Spearman法分析,視網膜病變與各指標的相關性采用二元Logistic 回歸法分析。檢驗水準=0.05,以P<0.05表示差異有統計學意義。
2 結果
2.1 兩組患者的臨床資料比較 116例高血壓患者中,HRP共計52例,其患病率為44.83%,其中男性患病率為36.36%,女性患病率為56.00%。觀察組患者的女性比例、高血壓病程、糖尿病患病率、Lp-PLA2水平明顯高于對照組,差異均具有統計學意義(P<0.05),見表1。
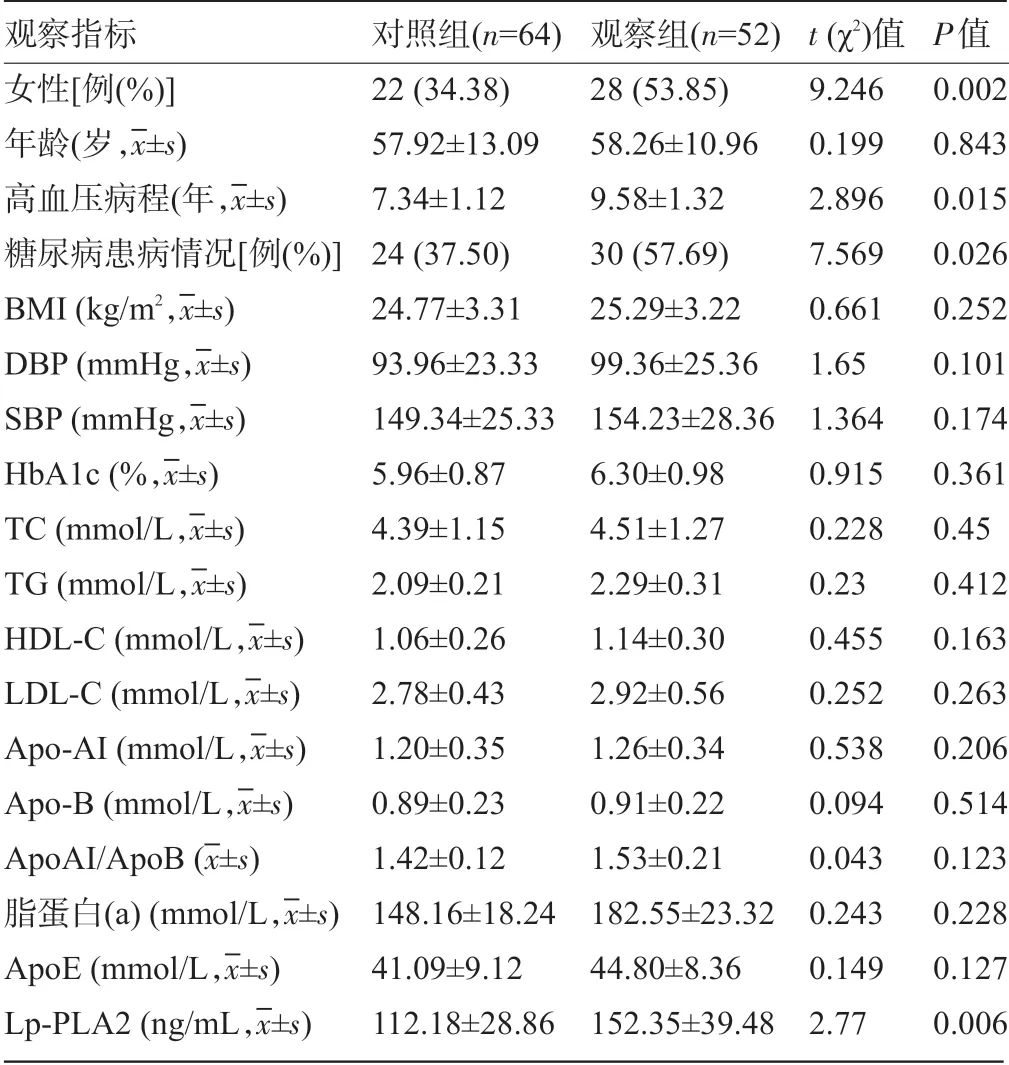
表1 兩組患者的臨床資料比較
2.2 Lp-PLA2 與各檢測指標的相關性 根據Spearman 相關分析結果顯示:Lp-PLA2 與TG、脂蛋白(a)、ApoAI/ApoB、HRP 呈正相關,與HDL-C 呈顯著負相關,見表2。
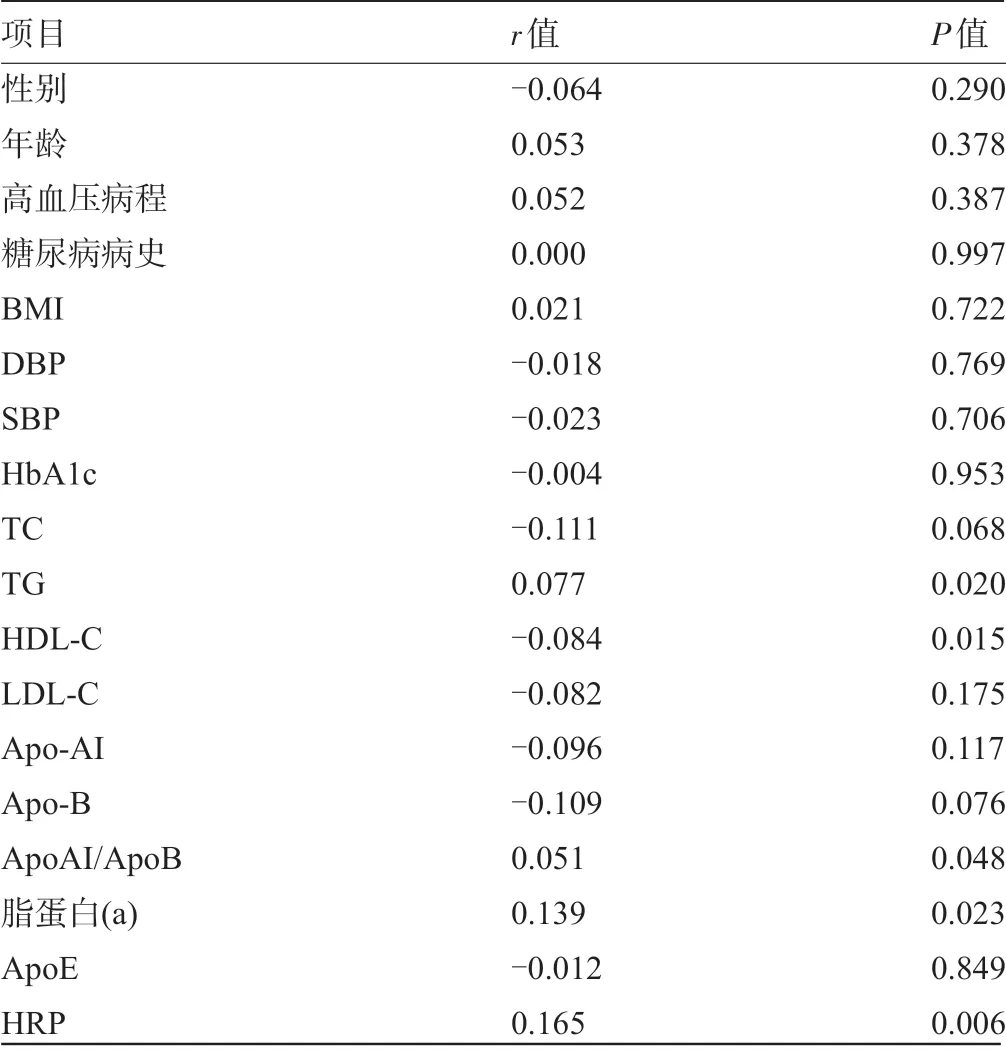
表2 Lp-PLA2與各檢測指標的相關性
2.3 HRP 的危險因素 將HRP 作為因變量,將性別、高血壓病程、糖尿病、Lp-PLA2 納入自變量,進行二元Logistic回歸分析。結果顯示,性別、糖尿病病史、Lp-PLA2均為HRP的危險因素,且校正性別、糖尿病病史、高血壓病程后,Lp-PLA2 仍是HRP 的獨立危險因素(P<0.05),見表3。
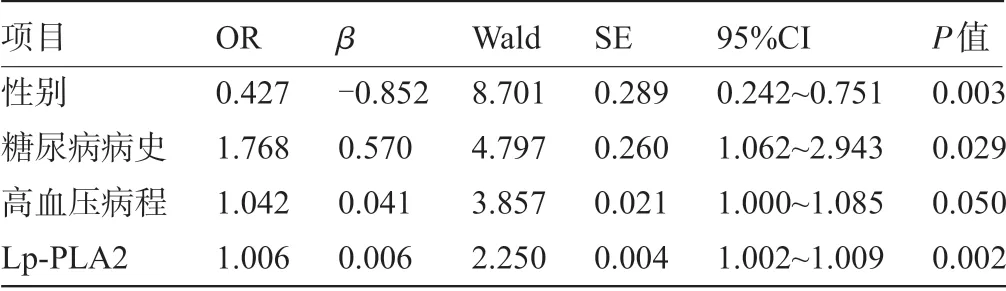
表3 二元Logistic回歸分析HRP危險因素
3 討論
高血壓患者例數逐年增加,已成為危害人類健康、加重經濟負擔的最主要慢性病之一。HRP 作為高血壓病最常見的并發癥之一,已成為導致成人失明的最主要原因之一,而如何預防及治療HRP 仍困難重重[8-9]。本研究首次探討Lp-PLA2 水平與HRP 關系,共納入116 例高血壓患者,HRP 共計52 例,其患病率為44.83%。國外研究顯示,高血壓患者中HRP患病率可達20.5%~46.9%[10]。本研究HRP患病率與上述研究結果相符合。
本研究結果顯示女性HRP發生率顯著高于男性,考慮與性激素參與調節有關。已有大規模臨床研究證實雌激素對女性血管內皮有保護作用[11]。本研究平均年齡在58 歲,多數為絕經后女性,雌激素對血管內皮的保護作用明顯減弱,故可能引起HRP發生率顯著高于男性。
本研究結果顯示觀察組Lp-PLA2 水平顯著高于對照組,且相關性分析結果顯示Lp-PLA2 水平與HRP 呈正相關。HRP 的主要病理基礎為視網膜微血管損傷,包括視網膜缺血、內皮損傷、玻璃體機化等一系列發生發展過程。目前關于HRP 的具體發病機制仍不清楚,一些細胞因子(VEGF,Ang2,NP1,RSR)可能參與其中[12-13]。此外,有研究發現炎癥因子與HRP 的發生發展密切相關,其中,TNF-α能激活中性粒細胞和淋巴細胞,使血管內皮細胞通透性增加,刺激柔軟和未硬化的視網膜動脈血管,經自調節作用使其張力增高、血管迂曲、動靜脈壓陷;IL-8 能刺激中性粒細胞、T 淋巴細胞和嗜酸性粒細胞的趨化,促進中性粒細胞脫顆粒,釋放彈性蛋白酶,損傷內皮細胞,使微循環血流淤滯,引起視網膜神經纖維的微小梗塞,導致了血-視網膜屏障破壞,血管壁破損和血流異常[14-15]。新近研究顯示Lp-PLA2 是具有血管特異性的炎癥標志物[16-17],Lp-PLA2 可水解氧化低密度脂蛋白中的氧化磷脂,從而生成脂類促炎物質,進而產生內皮細胞死亡,導致內皮功能異常,最終促進黏附因子和細胞因子的產生。通過趨化炎癥細胞,這些因子進一步反饋循環,從而最終生成更多的促炎物質[18-19]。
本研究結果顯示Lp-PLA2 是HRP 的獨立危險因素,原因可能為血漿Lp-PLA2作為一種炎性因子參與了HRP 的發生發展。既往有基礎研究顯示高血壓腎病小鼠Lp-PLA2活性明顯升高,提示Lp-PLA2作為炎性因子參與高血壓微血管病變的發生發展[20]。此外,本研究存在一些不足,包括納入人數較少,未進行相關的機制研究等。大樣本的隨機對照研究以及探討相關機制的動物試驗研究需要進一步開展。
綜上所述,Lp-PLA2 與HRP 具有相關性,是HRP的獨立危險因素,提示早期檢測Lp-PLA2 水平對預測高血壓患者視網膜病變的發生具有一定的臨床價值。

