工業氫氧化鋁重溶重結晶制備高純氧化鋁試驗研究
李中林,李思佳,耿繼業,林杰榜,李義兵,蘇積波,黃桃娥
(1.桂林理工大學 材料科學與工程學院,廣西 桂林 541000;2.百色百礦集團有限公司,廣西 百色 533000; 3.廣西田東錦鑫化工有限公司,廣西 田東 531500)
高純氧化鋁(HPA)在高溫下具有較高的轉化率、較低的鈉含量[1]及較強的收縮性能,廣泛用于制備單晶材料、發光載體、激光材料、透明陶瓷材料等[2-3]。
目前,已有多種制備HPA工藝,但都存在一些優缺點:結合有機鋁醇鹽水解法[4-6]可以獲得平均粒徑25 nm、分散性好、尺寸均一、球形顆粒α-Al2O3粉體,但制備條件要求極高,生產成本高;碳酸鋁銨結晶熱解法[7-8]和硫酸鋁銨結晶熱解法[9]工藝相對簡單,反應母液可循環利用[10],但制備過程中會產生大量廢氣造成環境污染,且K、Ga、鹵素等雜質很難去除;水熱合成法[11]生產周期短,成本低,是制備超細粉體的一種新工藝,但其反應條件較為苛刻,需高溫高壓,反應時也會產生氫氣,易發生爆炸,難以實現產業化生產[12-13];在拜耳法[14]基礎上,采用石灰法對拜耳法生產的高純鋁酸鈉溶液進行深度脫硅,再脫鈉[15-16]、煅燒,所得Al2O3純度在99.9%左右[17],鈉、硅雜質含量有所降低[18],但生產效率較低,燒結溫度過高。因此,研究在簡單生產條件下,用低成本原料生產HPA有重要意義。
試驗研究了以氫氧化鈉溶液溶解工業氫氧化鋁(Al(OH)3),然后重結晶氫氧化鋁,焙燒制備高純氧化鋁。
1 試驗部分
1.1 試驗材料及設備
試驗原料:工業氫氧化鋁(w(Al(OH)3)≥96.0%)由廣西某公司提供。
試驗試劑:氫氧化鋁、氫氧化鈉,分析純;鹽酸,購自廣東西隴科學股份有限公司。
試驗設備:高純水處理器,集熱式恒溫加熱磁力攪拌器,紫外可見分光光度計,反應釜,電熱恒溫鼓風干燥箱,熒光光譜儀。
1.2 試驗原理及方法
在一定溫度下,工業Al(OH)3用NaOH重溶為鋁酸鈉溶液(NaAl(OH)4),此時,只有微量Fe2O3雜質與NaOH反應生成NaFe(OH)4進入溶液;而溶于水中的SiO2與苛性堿在重溶和種分階段反應生成的可溶性硅酸鈉(Na2SiO3)則繼續與NaAl(OH)4反應生成水合鋁硅酸鈉沉淀(Na2O·Al2O3·1.7SiO2·nH2O)。種分所得Al(OH)3粉末中Na2O含量較高,這是Al(OH)3晶體慢慢長大后發生團聚,晶間和晶體內會殘留和吸附一定量Na2O雜質所致;最后,在酸性水熱條件下,用超聲沖擊使晶體中殘留的Na2O脫落,進一步降低產物中Na2O含量。超聲波波長短,近似直線傳播,能量較集中,對微粒具有分散沖擊作用,能夠滲透到Al(OH)3晶粒微孔中,且其產生的高壓、高強沖擊波可大幅度降低分子間的作用力,能有效阻止Na2O發生團聚和吸附。整個過程中的主要化學反應如下:

(1)

(2)

(3)

(4)
稱取219.4 g NaOH和281.4 g工業Al(OH)3,用400 mL高純水在95 ℃水浴中攪拌至全部溶解,過濾后定容至1 000 mL。NaAl(OH)4溶液中,Na2O和Al2O3質量濃度分別為170、184 g/L。加入5 g分析純Al(OH)3作為晶種,種分后過濾干燥,以熒光光譜法分析中間產物Al(OH)3粉末中主要雜質含量;種分后中間產物Al(OH)3粉末經過焙燒再與稀鹽酸一起加入反應釜中,在200 ℃下反應4 h,沉淀物洗滌過濾后干燥、磨細;在900 ℃下焙燒1.5 h,并在酸性環境下超聲加熱0.5 h,之后洗滌至中性,干燥后測定產物Al2O3中Na2O雜質含量。
2 試驗結果與討論
2.1 工業Al(OH)3重溶及晶種分解除雜
2.1.1 水質的影響
分別用去離子水和高純水配制1 000 mL NaAl(OH)4溶液,其中Na2O和Al2O3質量濃度均為170、184 g/L。用鉬藍光度法和鄰菲啰啉分光光度法測定NaAl(OH)4中Si、Fe吸光度,結果見表1。

表1 水質對溶液中雜質含量的影響
由表1看出:2種水質所得NaAl(OH)4溶液的Fe吸光度基本相等,表明去離子水不影響Fe2O3雜質含量;去離子水配制的NaAl(OH)4溶液Si吸光度低于參比組溶液Si吸光度,這是因為去離子水中Si含量較高,且配制參比溶液所用去離子水量高于配制NaAl(OH)4溶液,導致參比組中Si含量較高。綜合考慮,確定整個制備過程使用高純水。
2.1.2 分級過篩及洗滌的影響
取一定體積Na2O和Al2O3質量濃度分別為170、184 g/L的NaAl(OH)4溶液,加入適量Al(OH)3晶種,于30 ℃下種分48 h。對種分后的部分溶液分級過篩(用325#945 μm網篩),篩上和篩下的中間產物Al(OH)3分別干燥后,以熒光光譜法測定Al(OH)3中主要雜質質量分數;剩余溶液分別洗滌一次和多次,過濾干燥后分析雜質質量分數。試驗結果見表2。
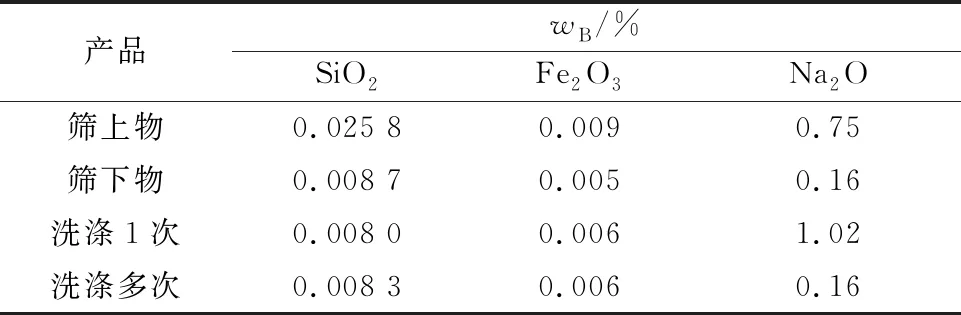
表2 分級過篩及洗滌對產品中雜質質量分數的影響
由表2看出:篩下物Al(OH)3中SiO2和Na2O雜質質量分數明顯低于篩上物,這是因為未分級過篩的Al(OH)3顆粒較大,晶間和晶體中殘留的雜質更多;洗滌對SiO2和Fe2O3雜質質量分數的影響較小,這是因為洗滌僅能洗去溶液中大部分未反應的Na2O,無法脫除殘留在晶體中的雜質。
2.1.3 Na2O和Al2O3初始質量濃度的影響
將Na2O和Al2O3質量濃度170、184 g/L視為D,配制Na2O和Al2O3初始質量濃度分別為0.50D、0.75D、1.00D和1.25D的NaAl(OH)4溶液各1 000 mL,每組加入5 g晶種,30 ℃下種分48 h, 考察Na2O和Al2O3初始質量濃度對Al(OH)3產物中雜質質量分數影響,試驗結果如圖1所示。
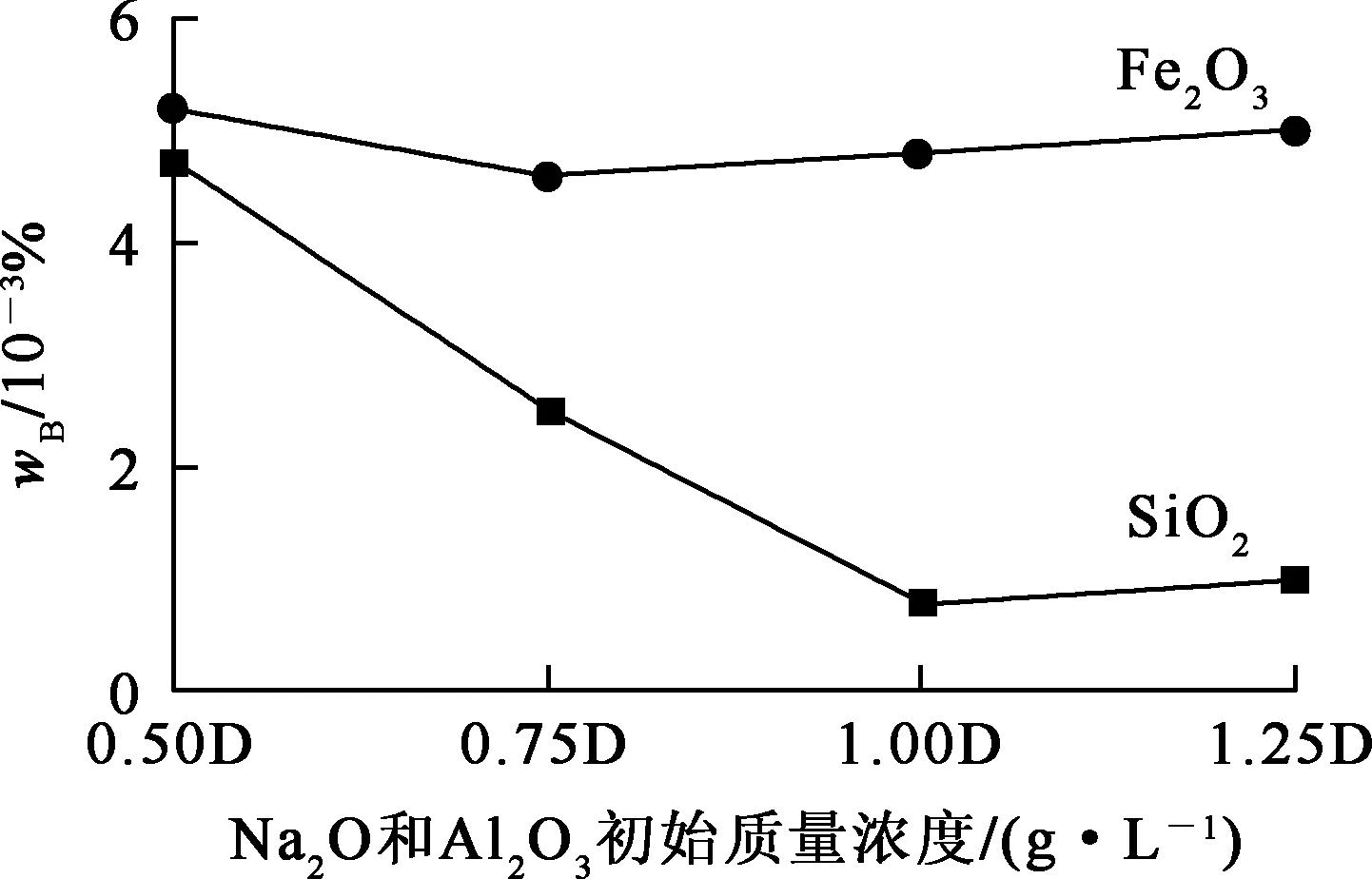
圖1 Na2O和Al2O3初始質量濃度對產物Al(OH)3雜質質量分數的影響
由圖1看出:隨Na2O和Al2O3初始質量濃度升高,中間產物Al(OH)3干粉中SiO2質量分數先降低后略有升高,而Fe2O3質量分數變化較小;NaAl(OH)4溶液中Na2O和Al2O3初始質量濃度為170、184 g/L時,Al(OH)3干粉中SiO2質量分數最低,僅為8.0×10-4%。這表明:在溶解和種分過程中,只有微量Fe2O3進入溶液,而可溶性SiO2與NaOH生成的Na2SiO3則與NaAl(OH)4反應生成沉淀;隨溶液中Na2O和Al2O3初始質量濃度升高,溶液苛性比增大,對去除SiO2更有利;但Na2O和Al2O3初始質量濃度過大,則溶液黏度會增大,容易發生團聚,反而不利于雜質的去除。
2.1.4 種分溫度的影響
配制5份1 000 mL NaAl(OH)4溶液,其中Na2O和Al2O3初始質量濃度均為170、184 g/L,在不同溫度下種分48 h。種分溫度對中間產物Al(OH)3干粉中SiO2和Fe2O3雜質質量分數的影響試驗結果如圖2所示。
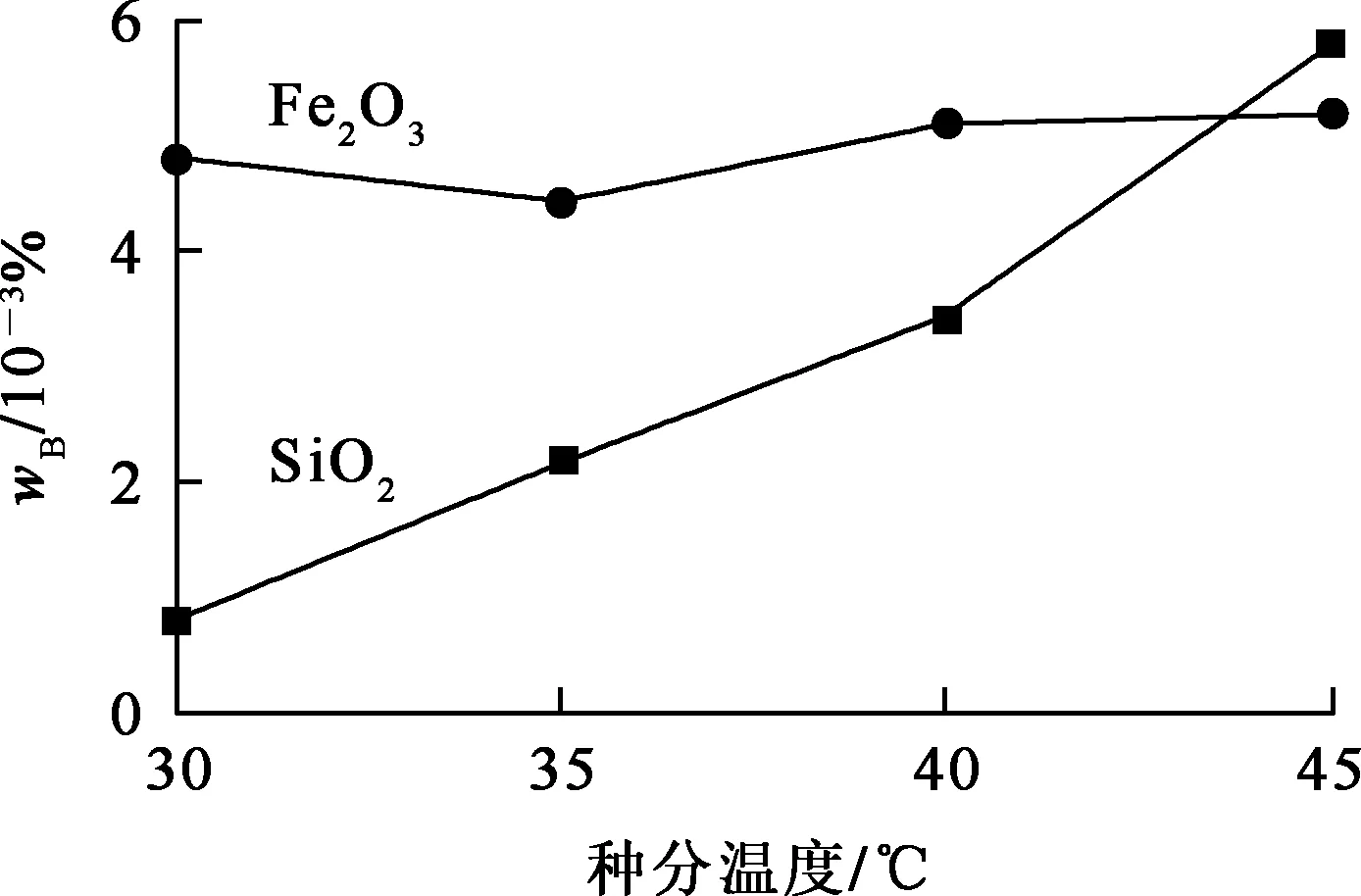
圖2 種分溫度對Al(OH)3產物中雜質質量分數的影響
由圖2看出,種分溫度在30~45 ℃條件下,種分溫度較低時,雜質含量較低,Al(OH)3純度更高。體系溫度較低時,溶液黏度較大,晶核較多,形成的Al(OH)3顆粒較小,晶體對雜質的作用力較小,雜質殘留和吸附得更少;但溫度過低,漿料黏度過大,不利于雜質的去除。為提高分解速度、降低中間產物Al(OH)3干粉中雜質質量分數,需要采用起始始溫度較高并逐漸降溫的控溫方式進行種分。
2.1.5 種分時間的影響
配制5份1 000 mL NaAl(OH)4溶液,其中Na2O和Al2O3初始質量濃度分別為170、184 g/L,在30 ℃下進行種分。種分時間對中間產物Al(OH)3干粉中SiO2和Fe2O3雜質質量分數的影響試驗結果如圖3所示。
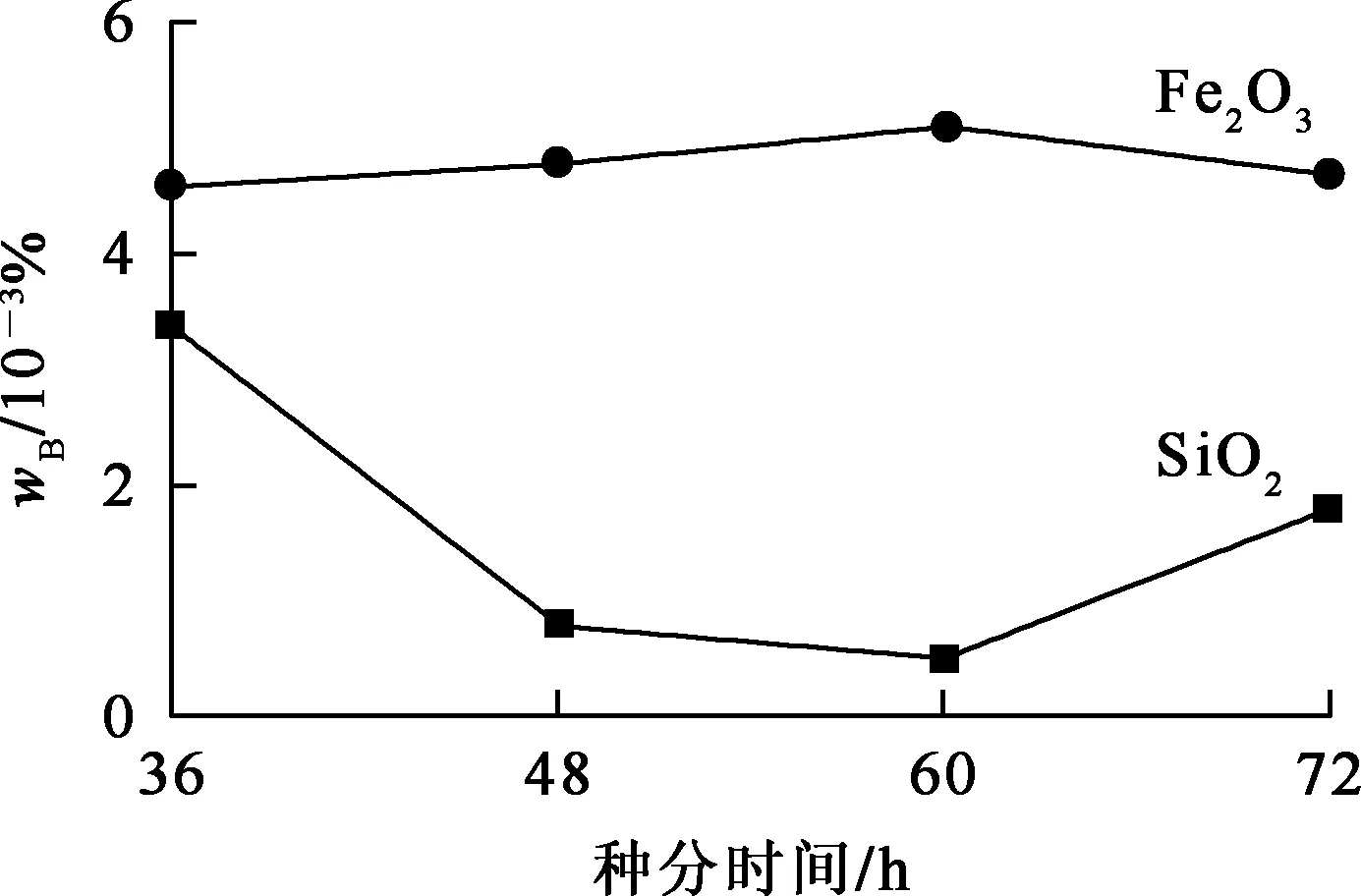
圖3 種分時間對Al(OH)3產物中雜質質量分數的影響
由圖3看出:中間產物Al(OH)3干粉中SiO2雜質質量分數隨種分時間延長先降低后升高,在36~60 h時間范圍內去除效果較好;Fe2O3質量分數變化不大。在一定時間范圍內,溶液苛性比隨種分時間延長而增大;種分時間過長,晶體顆粒過大,晶間和晶體對雜質作用力增大,晶間和晶體包裹的雜質會更多;但過早停止種分不僅會降低Al(OH)3產率,也會降低溶液苛性比,使SiO2和Fe2O3雜質質量分數提高。綜合考慮,種分時間以60 h為宜。
2.2 料液酸度的影響
表3為料液酸度對最終產物Al2O3中雜質質量分數的影響試驗結果。可以看出:與高純水(鹽酸質量濃度為0)相比,料液中添加適量鹽酸,最終產物Al2O3中Na2O質量分數會顯著降低;隨鹽酸質量濃度增大,Al2O3產物中Na2O雜質質量分數降低;用質量濃度100 g/L的鹽酸溶液深度脫鈉效果最好,Al2O3產物中Na2O質量分數可低至3.8×10-2%。在超聲波沖擊下,熱的酸性環境中,焙燒中間產物Al(OH)3得到的Al2O3晶間和晶體中殘留的Na2O發生脫落,但脫落Na2O的物質的量是一定的。

表3 鹽酸質量濃度對最終產物Al2O3中Na2O質量分數的影響
2.3 種分產物的形貌
圖4為Al(OH)3種分產物的SEM照片。可以看出,Al(OH)3晶體形貌為塊狀顆粒上附著類似于金字塔的細小圓錐形顆粒。結合Al(OH)3結晶機制可知:結晶早期,NaAl(OH)4溶液處于過飽和狀態,主金字塔側面通過填充扭結部位形成次金字塔并繼續生長,次生金字塔出現在前核簇中,金字塔底部則通過填充螺旋結構的方式逐漸展開;結晶后期,溶液過飽和度慢慢降低,側面僅通過填充扭結部位而生長,螺旋結構也逐漸收縮變形,初始階段的錐形顆粒漸漸變形為最終的塊狀顆粒。

圖4 Al(OH)3種分產物的SEM照片
3 結論
Al(OH)3重溶時,只有微量Fe2O3會與苛性堿反應進入到溶液中,而可溶性SiO2在重溶和種分過程中與NaOH反應生成的NaSiO3則會與NaAl(OH)4反應生成沉淀。采用起始溫度較高并逐漸降低的控溫方式,將較高濃度NaAl(OH)4溶液置于30 ℃溫度下進行種分,延長種分時間至60 h左右,中間產物Al(OH)3晶體中SiO2雜質質量分數低于3.0×-3%,Fe2O3雜質質量分數低于5.0×10-3%, 但殘留和吸附的Na2O雜質含量相對較高,需要進一步去除。在超聲波的沖擊下,熱稀酸中晶體殘留的部分NaAl(OH)4被脫除,最終的Al2O3產物中Na2O質量分數可降至3.8×10-2%左右,純度可達99.9%。

