頸動脈粥樣硬化性大血管閉塞與心源性栓塞性大血管閉塞患者側支循環(huán)及臨床預后的比較研究
楊 蕾, 付勝奇, 石寶洋, 秦歷杰, 王龍安
頸動脈粥樣硬化性大血管閉塞與心源性栓塞性大血管閉塞是臨床較為常見的病因亞型。研究發(fā)現(xiàn),心源性栓塞性卒中患者較其他原因引起的缺血性卒中患者臨床預后更差,復發(fā)及死亡風險更高[1,2];而對接受血管內治療(endovascular treatment,EVT)的由顱內動脈閉塞引起的卒中患者,側支循環(huán)評分與臨床預后有關[3~5]。可能原因是側支動脈(如軟腦膜)有助于延緩缺血腦組織的壞死[6]。由于心源性栓塞卒中不伴有慢性腦灌注障礙,這些患者側支循環(huán)較差。因此,本研究將比較頸動脈粥樣硬化性與心源性栓塞性大血管閉塞對側支循環(huán)的影響,同時評估不同病因是否與患者的臨床預后有關。
1 資料與方法
1.1 研究對象 連續(xù)納入2014年1月1日-2020年11月30日在我院接受EVT治療的前循環(huán)缺血性卒中患者,共318例。納入標準:(1)入選患者均符合中國急性缺血性診治指南2014診斷標準;(2)動脈狹窄程度經計算機斷層血管造影(CTA)證實;(3)年齡≥18歲;(4)患者具備完整的影像學資料及實驗室檢查資料。排除標準:(1)小血管閉塞性病變;(2)大動脈粥樣硬化導致的單發(fā)皮質下小梗死;(3)其他非動脈粥樣硬化原因如顱/頸血管夾層、高凝狀態(tài)或血液疾病導致的卒中;(4)其他未明確診斷的卒中或合并嚴重全身性疾病的患者。
1.2 研究方法 所有患者均接受頸動脈CTA(介入治療前及90 d后)、動態(tài)心電圖檢查、心臟彩超、頸動脈彩超、肝腎功能、糖化血紅蛋白、空腹血糖、葉酸、維生素B12等常規(guī)檢查。按照TOAST病因分型將患者分為大動脈粥樣硬化性、心源性、其他明確原因或原因不明型(包括兩種或多種病因,到目前為止未找到病因等)。如果癥狀側頸動脈有>50%的動脈粥樣硬化狹窄或閉塞,且經影像學證實,該患者被認為是由于頸動脈粥樣硬化引起的卒中;有高危或中危心源性栓塞風險的患者則被歸類為心源性栓塞性卒中[7]。基線NIHSS評分與入院后24 h或48 h的最大NIHSS評分差(δNIHSS);90 d時的mRS評分;90 d時的良好功能結局(mRS評分:0~2分);90 d時基于CTA的側支循環(huán)評分;90 d時的死亡率和癥狀性顱內出血。癥狀性顱內出血是指患者的出血與死亡或出現(xiàn)神經功能惡化(NIHSS至少下降4分)有關[8]。主要結局指標是基于CTA進行的側支循環(huán)評分,包括4個等級,分別是0~3分:0分表示無側支循環(huán)(動脈支配區(qū)完全無血流灌注);1分表示側支循環(huán)不良(僅有少量的血流灌注,小于正常的50%);2分表示側支循環(huán)中度不良(有一點的血流灌注,但較正常差,側支循環(huán)大于正常的50%);3分表示側支循環(huán)好(側支循環(huán)與正常側相同為100%)[9]。放射學結局指標是腦梗死再灌注程度(eTICI)評分≥2B患者比例[10]。首次通過效應[11]定義為單次使用取栓設備導致LVO及其下游區(qū)域的完全再灌注(eTICI 3),并且在使用該設備后不再進行其他操作;EVT手術持續(xù)時間是從腹股溝穿刺到成功再灌注(eTICI≥2B)或最后一次造影劑推注(EVT未能成功完成再灌注或手術期間未觀察到目標閉塞)的時間。在CTA上進行血栓密度測定(單位是Hounsfield單位,HU),其血栓衰減增加(TAI或δ)(δ=ρ血栓CTA-ρ血栓NCCT)[12]。
1.3 統(tǒng)計學分析 統(tǒng)計學采用IBM SPSS 24.0分析,定量資料描述其中位數(shù)與四分位數(shù),組間比較采用非參秩和檢驗。定性資料描述其例數(shù)與百分比,組間比較采用卡方檢驗或Fisher精確概率法。對于兩組的臨床結局變量(δNIHSS、mRS、功能預后和死亡率)的比較,采用回歸模型校正年齡、外周動脈疾病史、既往心肌梗死史、既往使用抗凝藥物史、閉塞位置、發(fā)病到腹股溝穿刺時間和動脈高密度征象。P<0.05為差異有統(tǒng)計學意義。
2 結 果
2.1 一般情況 納入符合條件的頸動脈狹窄大于50%的動脈粥樣硬化性前循環(huán)LVO患者132例,心源性栓塞引起的前循環(huán)LVO患者186例。入組患者中,頸動脈粥樣硬化性卒中患者較心源性栓塞患者年齡更小,男性更常見;卒中前mRS評分更低,頸內動脈/頸內動脈末端閉塞的發(fā)生率更高(見表1)。

表1 頸動脈粥樣硬化性卒中患者與心源性栓塞患者基線資料比較
2.2 預后結局指標比較 頸動脈粥樣硬化性卒中患者在90 d時的中位mRS低于心源性栓塞卒中患者。而兩組間90 d時mRS評分0~2分的患者所占比例無統(tǒng)計學差異,兩者死亡率也無統(tǒng)計學差異。另外,與心源性栓塞患者相比,頸動脈粥樣硬化卒中患者首過效應較少見,手術時間更長(見表2)。
2.3 側支循環(huán)改善情況比較 頸動脈粥樣硬化性卒中患者較心源性栓塞卒中患者的側支評分有顯著改善。此外,將側支循環(huán)分為良好(2~3分)和不良(0~1分)評估時,頸動脈粥樣硬化性卒中患者側支循環(huán)良好所占比例高于心源性栓塞性卒中患者(見圖1)。
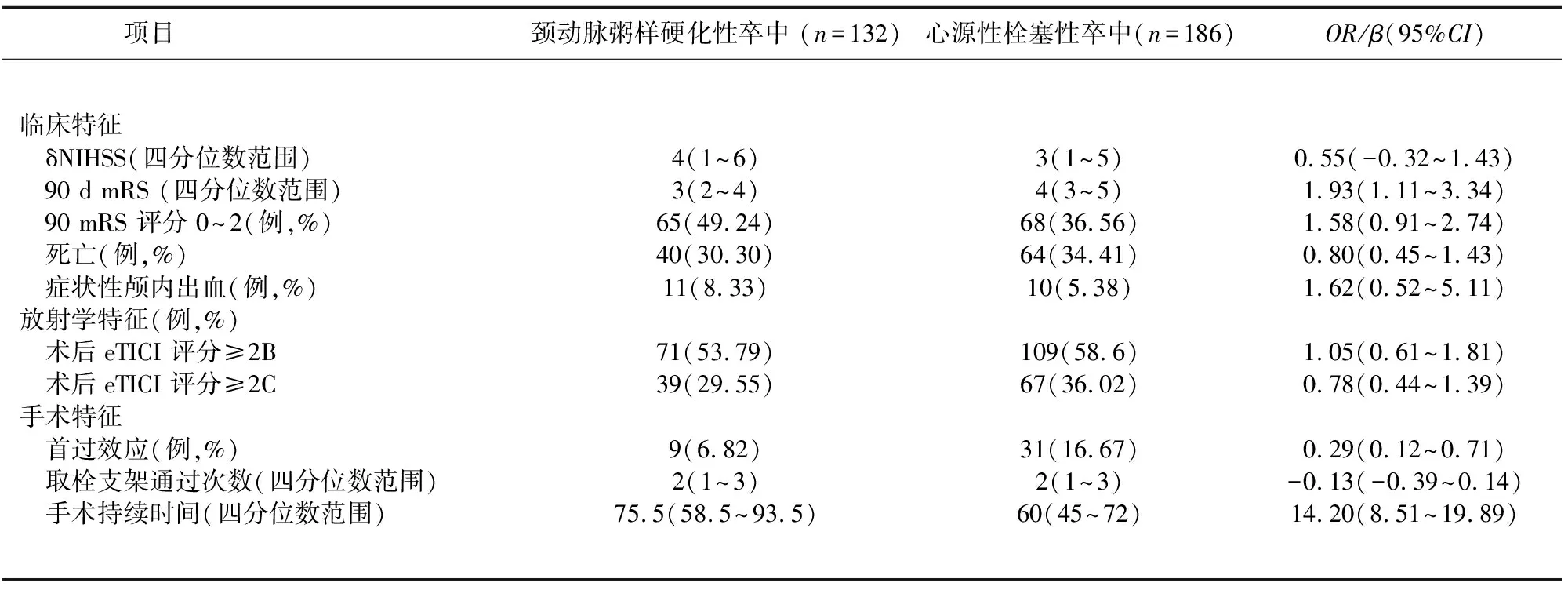
表2 頸動脈粥樣硬化性卒中患者與心源性栓塞患者臨床、影像及手術結果比較

圖1 頸動脈粥樣硬化性卒中患者與心源性栓塞患者側支循環(huán)比較
3 討 論
研究發(fā)現(xiàn)心源性栓塞性卒中患者側支循環(huán)更差,而頸動脈粥樣硬化性卒中具有更好的側支循環(huán)[13,14]。但是,既往研究均沒有對混雜因素進行校正,且部分研究的心源性栓塞患者僅納入了房顫患者,而未納入其他心源性栓子引起的心源性栓塞患者。本研究彌補了既往研究的不足,不僅納入了除房顫以外其他栓子引起的心源性栓塞患者,而且對混雜因素進行了校正。我們發(fā)現(xiàn),接受EVT治療的由頸動脈粥樣硬化引起的前循環(huán)LVO患者比心源性栓塞引起的前循環(huán)LVO患者在90 d時側支循環(huán)更好,功能結局更佳。
本研究中頸動脈粥樣硬化性卒中患者比心源性栓塞性卒中患者更年輕,男性更多,這與既往研究一致[15]。而本研究中頸動脈粥樣硬化性患者卒中前mRS評分更低,可能部分是由于患者年齡較小和合并癥較少。另外,兩組之間的良好功能結局或死亡率無統(tǒng)計學差異,而頸動脈粥樣硬化性卒中患者比心源性栓塞患者接受靜脈溶栓的比例更高,這可能與心源性栓塞性卒中患者接受口服抗凝治療比例較高有關。與既往研究不同的是,本研究中頸動脈粥樣硬化性和心源性栓塞性卒中患者的基線NIHSS評分無顯著差異。Arboix研究表明[16],在非EVT人群中,與其他原因導致的卒中相比,心源性栓塞性卒中患者表現(xiàn)出更嚴重的神經功能缺損,因為心源性卒中通常與相對較大的血栓形成有關,更常導致LVO。而由于我們的研究人群僅由LVO患者組成,這可能解釋了為什么我們沒有觀察到兩類患者卒中嚴重程度(NIHSS評分)的差異。
既往已有研究表明,側支循環(huán)決定了缺血半暗帶、梗死體積大小、腦缺血時嚴重程度以及血管閉塞后是否發(fā)生卒中,良好的側支循環(huán)能縮小急性期梗死體積、降低靜脈溶栓或血管內治療后出血轉化風險,提高急性血管再通治療獲益率,有效改善臨床預后[17,18]。本研究發(fā)現(xiàn)頸動脈粥樣硬化性卒中患者在90 d時的中位mRS低于心源性栓塞性卒中患者,在90 d時側支循環(huán)也更好,但兩組患者在良好功能結局和死亡率均無統(tǒng)計學顯著差異,mRS的差異只是剛剛達到統(tǒng)計學意義。Heshmatollah等[19]研究分析了有無房顫的EVT患者90 d的mRS評分也未發(fā)現(xiàn)差異。亦有研究發(fā)現(xiàn),在EVT患者中,側支循環(huán)及90 d mRS評分和死亡率之間呈正相關[4]。本研究中這一結果可能與本組患者樣本量偏少有關,也不能排除混雜因素的影響可能。
此外,本研究中頸動脈粥樣硬化性卒中患者比心源性栓塞患者手術時間更長,這可能與頸動脈狹窄時患者手術更困難或此類患者多需要行經皮腔內血管成形術有關。同樣,在頸動脈粥樣硬化性卒中患者中,LVO及其下游區(qū)域初次達到完全再灌注eTICI 3的比例更低,這可能與血栓負荷有關。頸動脈粥樣硬化卒中患者閉塞更常發(fā)生在頸內動脈或頸內動脈遠端,血栓重負荷可能是其主要原因[20,21]。盡管我們沒有對血栓的組織學進行分析,但我們發(fā)現(xiàn)頸動脈粥樣硬化患者更常出現(xiàn)高密度征,但兩組間血栓密度無統(tǒng)計學差異。
總之,由頸動脈粥樣硬化引起的前循環(huán)卒中患者比心源性栓塞引起者在90 d時側支循環(huán)更好,功能結局更佳,但兩組患者在功能獨立性和死亡率方面無統(tǒng)計學差異,導致這一差異的部分原因可能與心源性栓塞患者有更好的治療效果有關。本研究有以下局限性:首先,大多數(shù)心源性栓塞性卒中患者為心房纖顫,但心房纖顫僅占所有心源性栓塞的50%[22]。其次,本研究未對血栓大小和血栓成分進行評估,這也可能導致對側支狀態(tài)評估的不全面,因為較小的血栓可能會增加新生血管生成,增加側支循環(huán)評分,在血栓負荷過重患者中,評估側支循環(huán)分數(shù)可能會偏低[23]。

