短期饑餓對(duì)雜交石斑魚(Epinephelus fuscogutatus♀×E. polyphekadion♂)幼魚消化酶活性與血清生化指標(biāo)的影響
鄧文鑫 張健東 黃建盛 王忠良 潘傳豪 施鋼 湯保貴 陳剛


摘 要:為了解短期饑餓對(duì)雜交石斑魚 (Epinephelus fuscogutatus♀×E. polyphhekadion♂) 幼魚消化酶活性和血清生理生化指標(biāo)的影響,對(duì)雜交石斑魚幼魚進(jìn)行短期饑餓處理(0 d、5 d、10 d、15 d),分別為S0組、S1組、S2組和S3組,并以S0組為對(duì)照組。結(jié)果表明,隨著饑餓時(shí)間的延長,各種消化酶活性呈下降趨勢(shì),淀粉酶活性呈先上升后下降趨勢(shì)。血清碳水化合物、膽固醇、甘油三酯、總蛋白、白蛋白等生化指標(biāo)在饑餓前期顯著降低(P< 0.05),隨后維持在相對(duì)穩(wěn)定的水平。AST、ALT、ALP活性呈“下降-上升-下降”趨勢(shì)。分析表明,在短期饑餓過程中,雜交石斑魚幼魚早期主要消耗碳水化合物和脂肪物質(zhì),后期主要以蛋白質(zhì)代謝能量來維持生命活動(dòng),短期饑餓并沒有對(duì)雜交石斑魚造成不可逆轉(zhuǎn)的肝臟損傷。
關(guān)鍵詞:雜交石斑魚(Epinephelus fuscogutatus♀×E. polyphhekadion♂);饑餓;消化酶活性;血清生理生化指標(biāo)
自然環(huán)境下,由于季節(jié)更迭、環(huán)境變化或者是食物散布不均勻等影響,魚類在實(shí)際成長中存在顯著的食物缺口,進(jìn)而導(dǎo)致饑餓的困境[1]。人工養(yǎng)殖的場(chǎng)景之中,魚類也會(huì)因餌料不足、養(yǎng)殖密度過大等問題導(dǎo)致饑餓[2]。饑餓脅迫下,魚類會(huì)依靠調(diào)控機(jī)體之中的酶活性、生化代謝等多種模式,降低耗能從而維持生命活動(dòng)[3]。消化酶活性影響魚類最終的消化與吸收效果,進(jìn)一步?jīng)Q定魚類的發(fā)育狀況,因此關(guān)于消化酶活性的相關(guān)研究一直是魚類消化生理的重要研究內(nèi)容[4]。而研究魚類的血液生理生化指標(biāo)可直接反映魚類健康狀態(tài)、生理和營養(yǎng)狀況[5]。
石斑魚(Epinephelus spp.)隸屬鱸形目(Perciformes),鱸亞目(Percoidei),鮨科(Serranidae),石斑魚亞科(Epinephelinae)。其味道鮮美,營養(yǎng)豐富,為我國沿海地區(qū)廣泛養(yǎng)殖魚種[6]。本試驗(yàn)魚為雜交石斑魚,是褐點(diǎn)石斑魚(E.fuscogutatus♀)和清水石斑魚(E.polyphekadion♂)雜交子代,目前對(duì)雜交石斑魚的研究較少,研究的內(nèi)容包括鹽度對(duì)受精卵孵化和卵黃囊仔魚形態(tài)及活性的影響[7];子代幼魚形態(tài)性狀對(duì)體質(zhì)量影響的通徑分析[8];干擾素調(diào)節(jié)因子3(IRF3)基因的克隆及表達(dá)分析[9];生長激素、生長激素受體及雌激素受體的分子識(shí)別、生物信息學(xué)和表達(dá)譜分析[10]等。短期饑餓對(duì)雜交石斑魚幼魚消化酶活性的影響的研究尚未有學(xué)者涉足,所以論文計(jì)劃分析該場(chǎng)景中的消化酶活性以及血液生化指標(biāo)的具體變動(dòng)規(guī)律,同時(shí)初步研究饑餓場(chǎng)景中的魚體代謝指標(biāo)、能源運(yùn)用的次序與營養(yǎng)狀態(tài),為雜交石斑魚養(yǎng)殖生產(chǎn)提供科學(xué)且有價(jià)值的參考資料。
1 材料和方法
1.1 試驗(yàn)材料
試驗(yàn)用魚為取自廣東海洋大學(xué)湛江海洋高新科技園養(yǎng)殖所培育的褐點(diǎn)石斑魚(♀)×清水石斑魚(♂)雜交子一代幼魚,運(yùn)回實(shí)驗(yàn)室后在50 cm×70 cm×60 cm的養(yǎng)殖桶內(nèi)暫養(yǎng)一周。暫養(yǎng)期間,養(yǎng)殖用水為經(jīng)24 h曝氣的自然海區(qū)海水,鹽度(27±1.0)‰,水溫(28±1.0) ℃,溶氧質(zhì)量濃度保持在6 mg/L以上,自然光照。每日于8:00、12:00、18:00三個(gè)時(shí)間點(diǎn)投喂配合飼料(“粵海牌”石斑魚配合飼料4#,顆粒直徑5 mm),每次達(dá)到飽食,投喂半個(gè)小時(shí)后通過虹吸清理殘餌和糞便,每天換水1~2次,每次1/3~1/2,換水溫差不超過1 ℃,保持水質(zhì)清新。
1.2 試驗(yàn)設(shè)計(jì)
暫養(yǎng)結(jié)束后,選用200尾體表無傷、體格健壯、體長為(12.42±0.93) cm、體重為(52.23±11.17)g的雜交石斑魚幼魚,進(jìn)行短期饑餓處理(0、5、10、15 d),分別為S0組、S1組、S2組和S3組,并以S0組為對(duì)照組,各個(gè)組別設(shè)置3個(gè)平行,單個(gè)平行涉及15尾幼魚,實(shí)際數(shù)量為180尾。同時(shí)選擇20尾魚作為相應(yīng)的連續(xù)饑餓備用。
1.3 樣品的制備及測(cè)定
1.3.1 血樣制備及測(cè)定 各個(gè)試驗(yàn)組別饑餓完成的情況下,針對(duì)多個(gè)組別各個(gè)平行,運(yùn)用隨機(jī)的方式選擇5尾魚,取樣操作之前用 MS-222 進(jìn)行麻醉操作。用 2.5 mL 注射器取用相應(yīng)的血液1~2 mL,放入到離心管內(nèi)在4 ℃環(huán)境下存儲(chǔ)12 h,后續(xù)再置于4 000 r/min離心處理 10 min,取相應(yīng)的上層血清運(yùn)用深圳雷杜生命科技Chemray 800分析儀開展后續(xù)的指標(biāo)測(cè)試。
1.3.2 酶液的制備及測(cè)定
針對(duì)麻醉取血處理之后的幼魚,迅速解剖剝離獲取腸胃及肝臟,剔除內(nèi)容物及腸系膜后,用預(yù)冷的生理鹽水沖凈,迅速放入液氮中冷藏,待所有魚取樣完成后,按編號(hào)轉(zhuǎn)入冰箱(-80 ℃)儲(chǔ)存?zhèn)溆谩谋渲腥〕龃郎y(cè)樣品,4 ℃下解凍,用剪刀剪成小塊,加入10倍體積預(yù)冷生理鹽水,在高速組織勻漿機(jī)中冰浴勻漿,勻漿液經(jīng)2 500 r/ min的速率離心10 min后取上清液,并置于4 ℃冰箱中保存,進(jìn)行酶活性檢測(cè)。用試劑盒測(cè)試肝、腸、胃3 類組織的三類酶活性指標(biāo),并且用考馬斯亮藍(lán)染色法來確認(rèn)其中具體的蛋白濃度指標(biāo)。
蛋白酶活性:37 ℃狀態(tài)下,實(shí)際取用的每mg組織蛋白,持續(xù)1 min分解獲得相應(yīng)的1 mg氨基酸,代表其擁有1個(gè)酶活單位(U);淀粉酶活性:37 ℃狀態(tài)下,實(shí)際取用的每mg組織蛋白和底物之間產(chǎn)生作用30 min水解10 mg淀粉,代表其擁有1個(gè)酶活單位(U);脂肪酶活性:37 ℃狀態(tài)下,實(shí)際取用的每mg組織蛋白在該反應(yīng)系統(tǒng)之中和底物之間反應(yīng)1 min,每消耗相應(yīng)的1 μmol底物,代表其擁有1個(gè)酶活單位(U)。酶活性運(yùn)用相應(yīng)的比活性(每mg蛋白活性單位,U·mg-1)的方式進(jìn)行表述。
1.4 數(shù)據(jù)處理
用SPSS19.0軟件進(jìn)行生物統(tǒng)計(jì)分析,采用單因素方差分析和Duncan檢驗(yàn)法進(jìn)行多重比較。結(jié)果用“平均值±標(biāo)準(zhǔn)差(Meant±SD) ”表示,P<0.01表示具有極顯著性差異,P<0.05 表示具有顯著性差異。
2 結(jié)果
2.1 短期饑餓對(duì)雜交石斑魚幼魚消化酶活性的影響
測(cè)定結(jié)果見圖1。各饑餓組蛋白酶活性和脂肪酶活性變化明顯,均隨饑餓時(shí)間的延長持續(xù)降低,饑餓處理S0組的腸、肝、胃的蛋白酶活性均高于其它各組(P<0.05),肝臟中的蛋白酶變化最小。脂肪酶活性饑餓前期下降幅度顯著(P<005),后期降幅緩慢(P<0.05)。腸、肝、胃三個(gè)組織的淀粉酶活性較低,整體隨饑餓時(shí)間的延長呈現(xiàn)先上升后下降的趨勢(shì),腸淀粉酶活性S1組顯著高于其它各組(P<0.05)。
2.2 短期饑餓對(duì)雜交石斑魚幼魚能量代謝指標(biāo)的影響
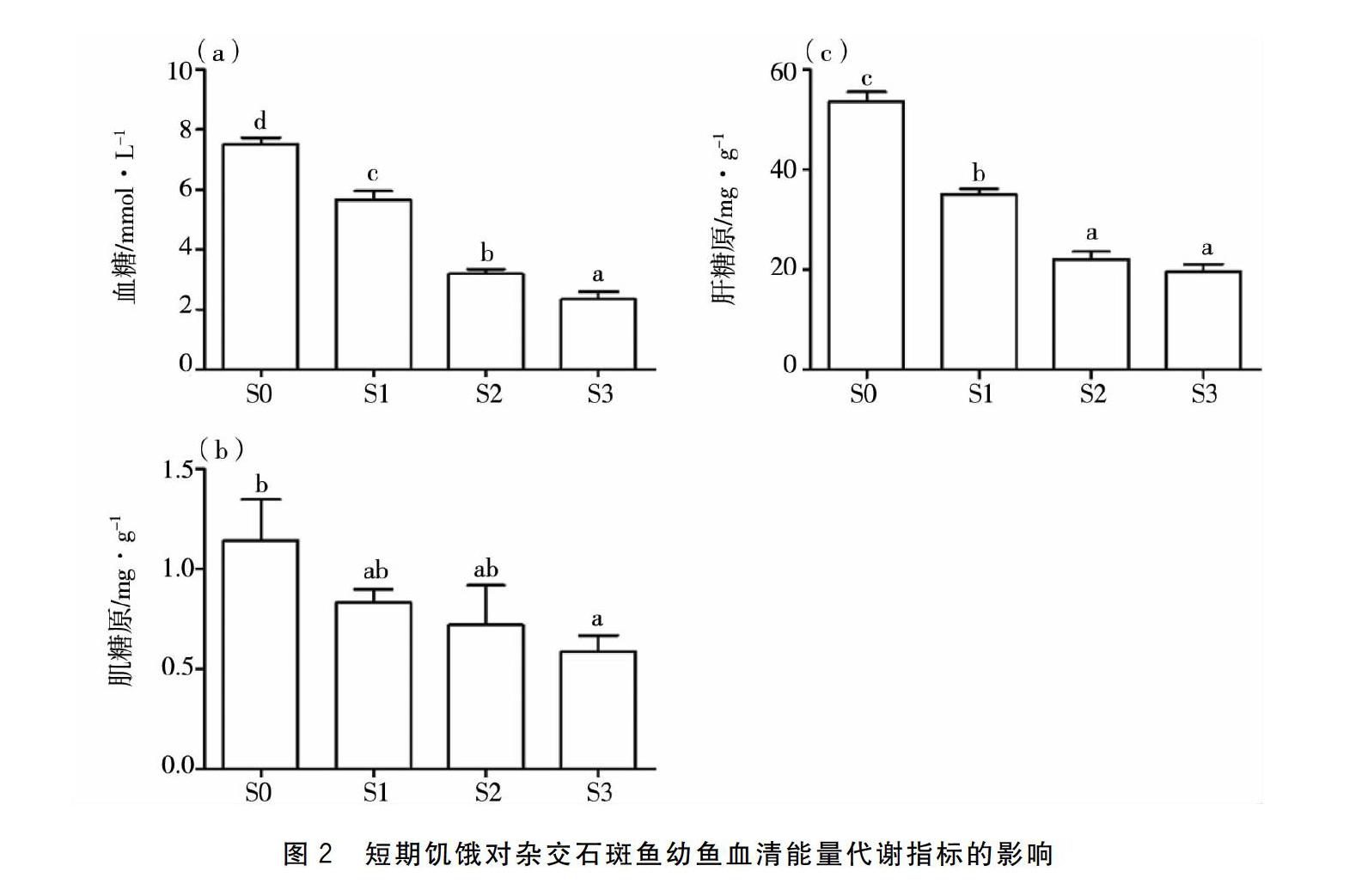
各饑餓組對(duì)雜交石斑魚幼魚能量代謝測(cè)定結(jié)果見圖2。糖類物質(zhì)代謝總體隨饑餓時(shí)間的延長而持續(xù)下降,之后維持在相對(duì)穩(wěn)定的水平。雜交石斑魚的血糖對(duì)饑餓比較敏感,饑餓5 d后,血糖含量顯著降低(P<0.05)。隨饑餓時(shí)間的延長,血糖一直處于顯著低于對(duì)照組的水平(P<005);肝糖原含量S2與S3組差異不顯著(P>0.05);肌糖原含量S1與S2組差異不顯著(P>0.05)。
2.3 短期饑餓對(duì)雜交石斑魚幼魚肝功能指標(biāo)的影響
在饑餓脅迫下,雜交石斑魚幼魚肝功能指標(biāo)的變化情況見圖3。堿性磷酸酶(ALP)和谷丙轉(zhuǎn)氨酶(ALT)活性隨饑餓時(shí)間延長呈現(xiàn)先降低再升高后下降的趨勢(shì);谷草轉(zhuǎn)氨酶(AST)則隨饑餓時(shí)間延長而持續(xù)下降(P<0.05),S1組與S2組差異不顯著(P>0.05)。
2.4 短期饑餓對(duì)雜交石斑魚幼魚血清脂代謝和蛋白質(zhì)代謝指標(biāo)的影響
饑餓脅迫對(duì)雜交石斑魚幼魚血清生化指標(biāo)的變化情況見圖4。膽固醇和白蛋白隨饑餓時(shí)間延長而不斷下降,S1與S2組間差異不明顯(P>005);總蛋白和甘油三酯隨饑餓時(shí)間延長下降幅度顯著(P<0.05),呈現(xiàn)階梯性下降。
3 討論
3.1 短期饑餓對(duì)雜交石斑魚幼魚消化酶活性的變化分析
饑餓脅迫下的魚類,依靠調(diào)控消化酶活性的方式來調(diào)動(dòng)身體中的營養(yǎng),進(jìn)而適應(yīng)環(huán)境的改變和維持機(jī)體的正常生理活動(dòng)[1]。因此,消化酶活性的變化在一定程度上反應(yīng)魚類生長與環(huán)境條件之間的關(guān)聯(lián)[11]。本試驗(yàn)中,雜交石斑魚幼魚的肝、腸和胃中3種消化酶(蛋白酶、脂肪酶、淀粉酶)活性均隨饑餓時(shí)間的延長而逐漸下降,此結(jié)果與千年笛鯛幼魚(Lutjanus sebae)[12]饑餓實(shí)驗(yàn)結(jié)果相一致。原因是在饑餓脅迫下,雜交石斑魚幼魚為了維持生命所需的各種基本生理需要,從而降低能量損耗。而淀粉酶整體呈現(xiàn)先上升后下降的趨勢(shì),分析可能為雜交石斑魚幼魚受到饑餓的脅迫,為了更好地吸收體內(nèi)殘留的淀粉和糖原而導(dǎo)致淀粉酶活性上升。蛋白酶活性變化明顯,腸、肝、胃三個(gè)組織的蛋白酶活性對(duì)照組(饑餓處理0 d)始終高于其它各組,總體呈現(xiàn)下降的趨勢(shì)。這與錢云霞13]的研究結(jié)果一致,與蘇慧等[2]研究結(jié)果相反,這說明饑餓對(duì)不同魚類蛋白酶活性的影響也不同。本試驗(yàn)中胃蛋白酶活性顯著高于腸和肝,肝蛋白酶活性最低; Das等[14]看來肝胰腺重點(diǎn)分泌蛋白酶原,所以活性相對(duì)較低乃至于不存在活性。本研究結(jié)果與此相符合,雜交石斑魚蛋白酶活性胃最高,腸次之,肝臟最低,這說明可能胃是雜交石斑魚幼魚蛋白酶消化的主要部位。饑餓前期,脂肪酶活性下降顯著;饑餓10 d后,雜交石斑魚腸、肝、胃三個(gè)組織的脂肪酶活性基本趨于平緩,試驗(yàn)結(jié)果與Furné[15]和張怡波等[16]相一致,分析可能是雜交石斑魚幼魚為了適應(yīng)饑餓脅迫以及配合其它種類的消化酶,對(duì)脂肪酶活性作出了調(diào)整,以便長時(shí)間適應(yīng)饑餓脅迫環(huán)境并生存下去。
魚類在受到饑餓脅迫時(shí),由于只能利用消耗體內(nèi)的殘留物質(zhì)和自身能源物質(zhì),為了適應(yīng)饑餓環(huán)境,繼續(xù)生存,需要通過調(diào)節(jié)自身各種消化酶活性來消耗體內(nèi)貯藏的營養(yǎng)物質(zhì),以維持生命。本試驗(yàn)中,消化酶活性呈總體下降狀態(tài),分析原因有三種,一是在饑餓脅迫環(huán)境下,魚類的消化系統(tǒng)沒有接收到食物的機(jī)械刺激信號(hào),所以消化酶的分泌會(huì)減少[1];二是饑餓脅迫下的魚類,因沒有受到視覺、嗅覺、味覺等感覺的刺激,中樞神經(jīng)系統(tǒng)不分泌激素促使消化腺分泌[17];三是饑餓脅迫損傷了魚類消化道組織結(jié)構(gòu),致使組織結(jié)構(gòu)萎縮,消化功能衰退[18-19]。
3.2 短期饑餓對(duì)雜交石斑魚幼魚血清生理生化的變化分析
魚類生化指標(biāo)可判斷適應(yīng)狀況與營養(yǎng)信息[20]。恒定的血糖濃度對(duì)維持魚類正常生命活動(dòng)有重要的作用。饑餓 5 d后血糖大幅降低,后續(xù)保持相對(duì)平穩(wěn)的狀態(tài),和刀鱭(Coilia nasus)[21]的數(shù)據(jù)基本相同,主要原因?yàn)轸~體中有保持血糖固定的調(diào)節(jié)體系。在遭遇饑餓的情況下,魚類無法通過食物獲得相關(guān)碳水、脂質(zhì)等營養(yǎng),因此血糖重點(diǎn)依靠糖異生來維持穩(wěn)定[22]。通常情況下,脂肪與糖原作為核心的儲(chǔ)能,禁食場(chǎng)景中重點(diǎn)耗費(fèi)兩類物質(zhì)[23],魚體糖類運(yùn)用糖原的模式位于肝臟與肌肉。魚的饑餓場(chǎng)景之中,并不存在外部供養(yǎng),饑餓最開始階段耗費(fèi)的能源源自糖原以及內(nèi)臟周邊所存儲(chǔ)的脂肪[24]。
血清實(shí)際的甘油三酯以及總膽固醇指標(biāo),用于表述具體的利用脂質(zhì)信息[25]。分析得出,短期饑餓脅迫下,雜交石斑魚幼魚血清總膽固醇和甘油三酯水平顯著下降。該結(jié)果表明,饑餓脅迫下雜交石斑魚可能持續(xù)利用體內(nèi)存儲(chǔ)的脂肪為機(jī)體提供能量,隨饑餓時(shí)間延長,存儲(chǔ)脂肪含量下降,可利用的甘油三酯含量降低,雜交石斑魚難以通過脂肪代謝為機(jī)體提供充足能量。
魚體中血液蛋白含量與新陳代謝、能量消耗以及免疫強(qiáng)弱有關(guān)。當(dāng)受到外界脅迫時(shí)新陳代謝加強(qiáng),能量消耗加快,導(dǎo)致血液中的蛋白含量下降,免疫能力也隨之下降[26]。饑餓5 d,雜交石斑魚幼魚血清白蛋白下降顯著,之后緩慢下降,組間差異不顯著。白蛋白含量的減少可能會(huì)導(dǎo)致整體免疫水平的下降,總蛋白含量的相對(duì)穩(wěn)定是魚體自身調(diào)節(jié)的表現(xiàn),也與實(shí)驗(yàn)有關(guān),因?yàn)槌囸I外并無其它脅迫,魚體不需要維持高的代謝和能量消耗[27-28]。
血清中 AST、ALT 和 ALP 的活性一般被用作判斷肝功能是否正常的指標(biāo)[29],當(dāng)組織發(fā)生損傷或病變時(shí),特別是肝損傷,其活性會(huì)迅速升高。相關(guān)分析得出血清轉(zhuǎn)氨酶活性下降與維生素B6不足存在密切聯(lián)系,堿性磷酸酶的下降和鋅缺乏存在密切聯(lián)系[30]。關(guān)于魚類饑餓的分析得出,饑餓造成哲羅魚[31]和南方鲇[32]的這三種酶活顯著降低,與本試驗(yàn)的研究結(jié)果一致,表明短期饑餓脅迫尚未造成雜交石斑魚肝損傷。亦有和試驗(yàn)結(jié)果有所區(qū)別的分析,類似于饑餓對(duì)鮭魚血漿AST指標(biāo)并未產(chǎn)生影響[33];饑餓對(duì)鲇血清ALP指標(biāo)并沒有產(chǎn)生影響[34],代表多種魚類所遭遇的影響有區(qū)別,原因或許是不同種類的魚類實(shí)際蓄積的營養(yǎng)與承受饑餓的能力有所區(qū)別。
參考文獻(xiàn):
[1]
謝小軍,鄧?yán)瑥埐?饑餓對(duì)魚類生理生態(tài)學(xué)影響的研究進(jìn)展[J].水生生物學(xué)報(bào),1998(2):181-188.
[2] 蘇慧,區(qū)又君,李加兒,等.卵形鯧鲹消化酶活力的研究Ⅵ饑餓對(duì)幼魚存活和消化酶活力的影響[J].海洋漁業(yè),2012,34(1):45-50.
[3] MCCUE M D.Starvation physiology:Reviewing the different strategies animals use to survive a common challenge[J].Comparative Biochemistry & Physiology Part A Molecular & Integrative Physiology,2010,156(1):1-18.
[4] 江麗華,朱愛意,苑淑賓.饑餓對(duì)褐菖鲉消化道指數(shù)及消化酶活力的影響[J].水產(chǎn)科學(xué),2011,30(4):187-191.
[5] 林浩然.魚類生理學(xué)[M].廣州:廣東高等教育出版社,1999:185-188.
[6] 孫穎.棕點(diǎn)石斑魚(♀)×鞍帶石斑魚(♂)雜交F1代生長優(yōu)勢(shì)的轉(zhuǎn)錄組學(xué)研究[D].廣州:中山大學(xué),2016.
[7] 黃建盛,陳剛,張健東,等.鹽度對(duì)雜交石斑魚受精卵孵化和卵黃囊仔魚形態(tài)及活力的影響[J].中國水產(chǎn)科學(xué),2017,24(3):507-515.
[8] 黃建盛,張敬威,陳剛,等.褐點(diǎn)石斑魚(♀)×清水石斑魚(♂)雜交子代幼魚形態(tài)性狀對(duì)體質(zhì)量影響的通徑分析[J].廣東海洋大學(xué)學(xué)報(bào),2017,37(3):23-28.
[9] 盧曉穎,黃寶松,馬騫,等.雜交石斑魚干擾素調(diào)節(jié)因子3(IRF3)基因的克隆及表達(dá)分析[J].生物技術(shù)通報(bào),2019,35(10):144-151.
[10] AMENYOGBE E.雜交石斑魚(褐點(diǎn)石斑魚♀×清水石斑魚♂)生長激素、生長激素受體及雌激素受體的分子識(shí)別、生物信息學(xué)和表達(dá)譜分析[D].湛江:廣東海洋大學(xué),2019.
[11] PEDRO N D,DELGADO M J,GANCEDO B,et al.Changes in glucose,glycogen,thyroid activity and hypothalamic cate-chola mines in tench by starvation and refeeding [J].Journal of Comparative Physiology B:Biochemical,Systemic,and Environmental Physiology,2003,173(6):475—481.
[12] 區(qū)又君,劉澤偉.饑餓和再投喂對(duì)千年笛鯛幼魚消化酶活性的影響[J].海洋學(xué)報(bào)(中文版),2007(1):86-91.
[13] 錢云霞.饑餓對(duì)養(yǎng)殖鱸蛋白酶活力的影響[J].水產(chǎn)科學(xué),2002,(3):6-7.
[14] DAS K M,TRIPATHI S D.Studies on the digestive enzymes of grass carp,Ctenopharyngodon idella(Val.)[J].Aquaculture,1991,92(1):21-32.
[15] FURN M,GARGA-GALLEGO M,HIDALO M C,et al.Effect of starvation and refeeding ondigestive enzyme activities in sturgeon(Acipenser naccarii)and trout(Oncorhynchusmykiss)[J].Comparative Biochemistry and Physiology,2008,149(4):420-425.
[16] 張怡波,呂慧明,袁子,等.饑餓再投喂對(duì)黑鱾幼魚消化酶活性與血液生理生化指標(biāo)的影響[J].寧波大學(xué)學(xué)報(bào)(理工版),2019,32(5):12-16.
[17] 錢國英.不同馴食方式對(duì)鱖魚胃腸道消化酶活性的影響[J].浙江農(nóng)業(yè)大學(xué)學(xué)報(bào),1998(2):99-102.
[18] EHRLICH K F,BLAXTER J H S,PEMBERTON R.Morphological and histological changes during the growth and starvation of herring and plaice larvae[J].Marine Biology,1976,35(2):105-118.
[19] SUN S M, SU Y L, YU H,et al.Starvation affects the intestinal microbiota structure and the expression of inflammatory-related genes of the juvenile blunt snout bream,Megalobrama amblycephala[J].Aquaclture,2020,517:734764.
[20] 胡麟,吳天星.饑餓對(duì)魚類生理生化的影響[J].水利漁業(yè),2007,27(1):7-9.
[21] 金鑫,徐鋼春,杜富寬,等.饑餓脅迫對(duì)刀鱭形體、體成分及血液生化指標(biāo)的影響[J].動(dòng)物學(xué)雜志,2014,49(6):897-903.
[22] GILLIS T E,BALLANTYNE J S.The effects of starvation onplasma free a mino acid and glucose concentrations in lake sturgeon[J].Journal of Fish Biology,1996,49(6):1306-1316.
[23] 杜震宇,劉永堅(jiān),田麗霞,等.饑餓對(duì)于鱸肌肉、肝臟和血清主要生化組成的影響[J].動(dòng)物學(xué)報(bào),2003,49(4):458-465.
[24] 程超,施光美.饑餓對(duì)鯽魚血液生理生化指標(biāo)和流變學(xué)性質(zhì)的影響[J].中國農(nóng)學(xué)通報(bào),2008,24(1):516—519.
[25] 孫紅梅.饑餓對(duì)黃顙魚血液指標(biāo)及免疫機(jī)能的影響[D].長春:吉林農(nóng)業(yè)大學(xué),2004.
[26] 封功能,楊文平,王愛民,等.饑餓脅迫對(duì)鯉形體、體成分及血液生理指標(biāo)的影響[J].上海海洋大學(xué)學(xué)報(bào),2011,20(6):814-819.
[27] 許源劍,孫敏.環(huán)境脅迫對(duì)魚類血液影響的研究進(jìn)展[J].水產(chǎn)科技,2010(3):27-31.
[28] 桂遠(yuǎn)明,吳垠,祝國芹,等.幾種養(yǎng)殖魚類越冬生理生化指標(biāo)的變化Ⅰ─—血液指標(biāo)及代謝率[J].大連水產(chǎn)學(xué)院學(xué)報(bào),1994(3):15-27.
[29] GHOLIZDEH Z T B,BANAEE M,JOURDEHI Y A,et al.Effects of selenium (Sel-Plex) supplement on blood biochemical parameters of juvenile Siberian sturgeon (Acipenser baerii) [J].Iranian Journal of Fisheries Sciences.2018,17(2):300-312.
[30] WANER T,NYSKA A.The toxicological significance of decreased activities of blood alanine and aspartate a minotransferase [J].Veterinary Research Communications,1991,15(1):73-78.
[31] 楊成輝,蔡勛,劉霞,等.饑餓和再投喂對(duì)哲羅魚幼魚血液生理生化指標(biāo)的影響[J].淡水漁業(yè),2009,39(1):36-40.
[32] 陳曉耘.饑餓對(duì)南方鯰幼魚血液的影響[J].西南農(nóng)業(yè)大學(xué)學(xué)報(bào),2000,22(2):167-169.
[33] 羅波,馮健,蔣步國,等.饑餓對(duì)太平洋鮭生長、機(jī)體組成及血漿相關(guān)生化指標(biāo)變化研究[J].水生生物學(xué)報(bào),2010,34(3):541-546.
[34] 喬志剛,張建平,牛景彥,等.饑餓和再投喂對(duì)鲇血液生理生化指標(biāo)的影響[J].水生生物學(xué)報(bào),2008,32(5):631-635.
Effects of short-term starvation on digestive enzyme activities and serum biochemical indexes of juvenile hybrid grouper (Epinephelus fuscogutatus♀×E. polyphekadion♂)
DENG Wenxin1, ZHANG Jiandong1,2,3, HUANG Jiansheng1,2,3, WANG Zhongliang1,2,3,PAN Chuanhao1, SHI Gang1, TANG Baogui1,2,3, CHEN Gang1,2,3
(1.Fishery College, Guangdong Ocean University, Zhanjiang 524088, China; 2.Southern Marine Science and Engineering Guangdong Laboratory (Zhanjiang), Zhanjiang 524025, China;3. Guangdong Provincial Key Laboratory of Pathogenic Biology and Epidemiology for Aquatic Economic Animals, Zhanjiang 524088, China)
Abstract:This experiment was conducted to study the effects of short-term starvation on digestive enzyme activities and serum physiological and biochemical indices of juvenile hybrid grouper (Epinephelus fuscogutatus♀×E. polyphekadion♂).Juvenile hybrid groupers were starved for a short time (0d,5d,10d,and 15d),the fish were grouped into two namely,control and experimental groups,with replicates of 3 per group and 15 fish per replicate (S0 as control,S1,S2 and S3 as experimental groups respectively).The digestive enzyme activities and serum indices of juvenile hybrid groupers were determined using S0 group as a control group.The results showed that digestive enzyme activities decreased with the prolonging of starvation time,and the activities of amylase increased first and then decreased.Serum carbohydrate,cholesterol,triglyceride,total protein,albumin,and other biochemical indices were significantly decreased in the early starvation period (P<0.05) and then maintained at a relatively stable level.AST,ALT,and ALP activities showed a serrated step decrease.According to the analysis,in the process of short-term starvation,juvenile hybrid grouper mainly consumed carbohydrate and fatty substances in the early stage and metabolized energy based on protein in the later stage to maintain life activities,and short-term starvation did not cause irreversible liver damage to hybrid grouper.
Key words:hybrid grouper;starvation;digestive enzyme activites;serum biochemical indices
(收稿日期:2021-01-26)

