煤化學鏈氣化制甲醇工藝模擬與技術經濟分析
雷昕儒,孫 喆
(安徽大學 化學化工學院,安徽 合肥 230601)
對于當前“煤炭富裕、燃氣匱乏、油品短缺”的能源現狀,發展以煤炭為主的能源化工局面必將會應勢而生。 因此研究以煤制甲醇的技術不僅促進化工行業的多元化,而且有效保障了國家能源安全戰略。 隨著科技的不斷進步,煤制甲醇的研究越來越多,Wang等[1]提出基于流化床煤氣化的煤制甲醇生產系統引起了關注,在系統中煤被熱解,揮發分轉化為合成氣在燃燒室中燃燒, 熱能被用來發電,其余的殘留物在氣流床氣化爐中氣化生成合成氣,然后轉化成甲醇。Gao等[2]對煤基甲醇制烯烴過程進行了生命周期分析,研究節能和排放控制等方面的減排能力。Li等[3]對煤制甲醇系統的環境評價進行了研究。 基于以上研究,煤制甲醇的生產技術引入化學鏈氣化技術來改善其工藝。
化學鏈氣化(Chemical-Looping Gasification,CLG)是在化學鏈燃燒(Chemical-Looping Combustion,CLC)技術的理念上所提出的可以有效分離和捕集CO2,降低能量損失并減少NOx等有害氣體排放的新型氣化技術。Huang等[4]研究了基于赤鐵礦的生物質直接化學鏈氣化制取合成氣的反應特性,結果表明鐵礦石載氧體的存在加速了生物質中碳的轉化,并提高了合成氣產率。Niu等[5]和Tian等[6]在煤化學鏈氣化過程中通過載體床料和反應控制,實現了定向調控煤氣化品質。 該技術系統簡單、能效高、運行成本低,開發該技術對我國能源清潔高效利用有較為深遠的意義。
本文對常規煤氣化制甲醇和煤化學鏈氣化制氫制甲醇兩種技術進行了模擬和經濟性分析,通過引入化學鏈氣化技術和化學鏈制氫技術來替代空分和常規氣化以及水煤氣變換,以經濟性的方法計算出兩種工藝制甲醇的生產成本。
1 煤氣化制甲醇工藝原理
圖1所示為兩種煤氣化制甲醇技術的工藝流程原理示意圖。 圖1(a)中,常規煤氣化制甲醇的工藝包括空分單元、煤氣化、酸性氣體脫除、水煤氣變換、甲醇合成。 圖1(b)中,煤化學鏈氣化制氫制甲醇的工藝包括了煤化學鏈氣化、煤化學鏈制氫、酸性氣體脫除、甲醇合成。
2 煤氣化制甲醇流程模擬
2.1 常規煤氣化制甲醇
(1)空分單元(ASU)
在模擬過程中, 模擬的物性方法選擇PENGROB, 所用到的模塊有分離器Split模塊、 壓縮機Compr 模 塊、 換 熱 器MHeatX 模 塊 和 空 分 精 餾 塔RadFrac模塊。
(2)煤氣化(CG)
該過程的模擬,物性方法選用PENG-ROB。首先將煤熱解為C、H2、O2、N2、H2O、S、Cl2、Ash(灰分)等組分,然后將空分單元中制成的純氧氣利用壓縮機和泵Pump模塊所輸送的H2O混合送入RGibbs反應器完成氣化過程。 利用RGibbs反應器的目的是分相后吉布斯自由能最小化的原則計算平衡不需要規定化學反應計量系數[7]。
(3)酸性氣體脫除(AGR)
在凈化過程中所用到的酸性氣體脫除劑是甲基二乙醇胺(MEDA)[8],用MEDA水溶液從氣體中吸收H2S、有機硫化物和CO2。 此過程在用高活性銅基催化劑的低壓法合成甲醇情況下,所用到的模型是Radfrac模型,物性方法是ELECNRTL。
(4)水煤氣變換(WGS)
在水煤氣變換過程中用REquil模型模擬變換反應爐,用HeatX模型模擬換熱器,在進行變換反應模擬過程時使用的物性方法是PENG-ROB。 發生的反應在Co-Mo催化劑作用下進行[9]。研究中通過此過程調節CO和H2的物質的量比到2左右來制甲醇, 反應見式(1)[10],用到的模塊是HeatX模塊和REquil模塊。
(5)甲醇合成(MS)
本研究采用魯奇甲醇合成工藝建立過程模型,PENG-ROB是此工藝的物性方法。 發生的主要反應見式(2)、式(3)[9]。 用到的模塊是REquil模塊。 精餾用RadFrac模塊。
2.2 煤化學鏈氣化制氫制甲醇
化學鏈氣化(CLG)和化學鏈氣化制氫(CLGH)中所用的物性方法是PENG-ROB, 所用到的模塊主要有RGibbs模塊、RStoic模塊、SSplit模塊,然后制得合成氣和氫氣。 煤化學鏈氣化制氫制甲醇中酸性氣體脫除和甲醇合成與常規煤氣化制甲醇流程模擬所用物性方法及單元操作模型相同,不再描述。
2.3 常規煤氣化制甲醇的工藝流程圖
如圖2所示為常規煤氣化制甲醇過程的工藝流程圖。空分單元制得的氧氣由壓縮機(C-O2)輸送進入煤氣化單元中,通過換熱器(HEX-O2)換熱,過程中H2O由泵(PUMP1)輸送,經過換熱器HEX-H2O換熱后,與煤通過熱解罐(STOI)熱解之后的產物一起進入氣化爐(GASIFIER)進行反應,出來的合成氣與灰分(ASH)通過氣固分離器(SEP)分離,氣體經過換熱和冷凝(COOL2)之后進入酸性氣體脫除過程在吸收塔(AB)中與MEDA反應,再進入脫除塔(R)中脫除H2S和CO2等腐蝕性氣體, 清潔氣由換熱器(HEAT2)換熱進入水煤氣變換反應器(REQ1)中進行變換反應,蒸汽是通過(HEAT1)換熱得到的。 變換后的氣體與(SPLIT3)中分離出來的循環氣混合經C-GAS6壓縮進入到甲醇合成的過程在反應器(REQ2)中反應,經閃蒸罐(FLASH)最后通過精餾塔(DT)精餾得到純甲醇。
圖3所示為煤化學鏈氣化制氫制甲醇的工藝流程圖。 在煤化學鏈氣化過程中,煤經熱解罐(STOI)熱解后進入燃料反應器(FR)進行氣化反應,主要產生CO、H2、CO2、H2O等以及FeO和灰分,FeO進入空氣反應器(AR)與氧氣反應生成Fe2O3,通過氣固分離器(SEP1)分離固體物質Fe2O3進入燃料反應器進行反應,以提高合成氣的產率。 在煤化學鏈制氫模擬中,煤經過熱解罐(STOI)熱解進入燃料反應器(FR)與Fe2O3反應產生氣體GAS2以及FeO和灰分,FeO進入蒸汽反應器(SR)反應,生成Fe3O4和氫氣以及蒸汽產物,Fe3O4進入空氣反應器(AR)進行燃燒反應生成Fe2O3, 氫氣進行下一個工段調解H2/CO的比例來合成甲醇,蒸汽(從蒸汽反應器分離出來的)與補入的水在蒸汽反應器中進行反應。 利用氣固分離器(SEP2)分離出Fe2O3進入燃料反應器中進行反應。氣體GAS1和GAS2進入下一個工段進行酸性氣體的脫除和變換反應以及甲醇合成的反應。 表1是煤氣化制甲醇的主要技術參數。
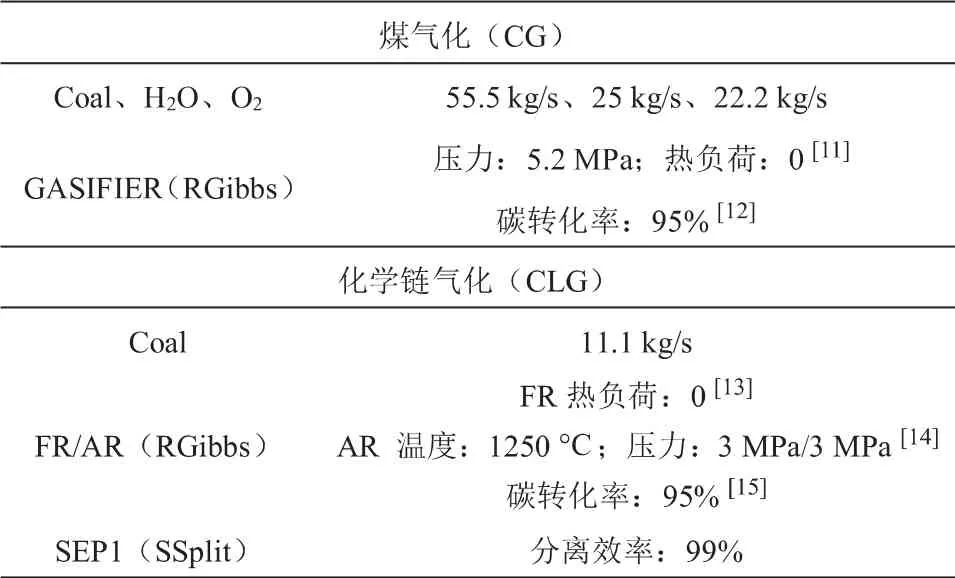
表1 煤氣化制甲醇的主要技術參數
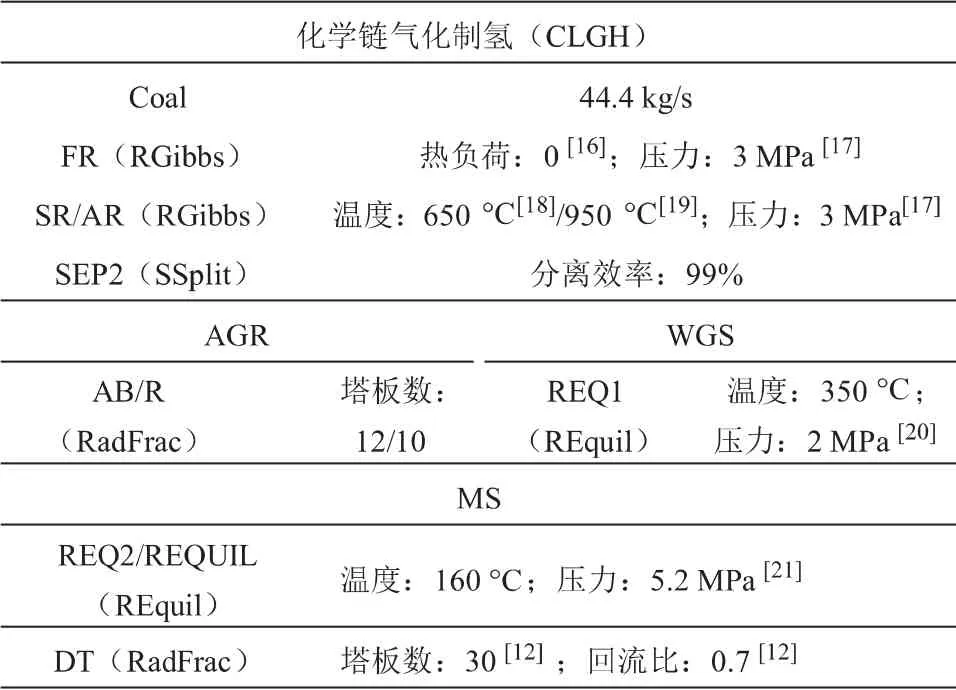
表1(續)
3 模擬結果分析
3.1 常規煤氣化制甲醇的數據分析
從圖4(a)中可知,隨著氣化壓力的增加,H2O體積分數由3.4%增加至5.4%,CO體積分數由49.1%降低至48.6%,CO2體積分數由1.6%增加至2.0%,H2體積分數由44%降低至42%,CH4體積分數趨于平穩狀態。 綜合來看,氣化壓力的改變對粗煤氣的影響不明顯。 從圖4(b)中可知,氧煤質量比(以下簡稱氧煤比) 從0.4變化到2.2,H2和CO的體積分數逐漸減小,H2O和CO2的體積分數逐漸增加,其導致的原因是由于氣化爐中CO與H2不斷的反應,相對于CH4,其體積分數基本沒有變化。 為了讓甲醇含量最大化,此工況取氧煤比0.4才能使粗煤氣中CO和H2的體積分數達到最大。 從圖4(c)中可知,水煤質量比(以下簡稱水煤比)從0.45增加到1.35,CO和H2的體積分數逐漸減小,CO的體積分數減小是因為水增加, 導致此現象有兩個方面的原因: 一個是CO參與了重整反應;另一個是CO的變換反應。 CO2和H2O的體積分數隨著水煤比的增加而增加。 經過分析可知,當水煤比在0.45左右時,粗煤氣的體積分數為最佳狀態。從圖4(d)中可知,氣化爐溫度由600 ℃變化到1200 ℃,CO2和CH4的體積分數減小,CO和H2的體積分數增加, 從1200 ℃以后CO和H2的體積分數增加趨于穩定狀態,H2O的體積分數從600 ℃變化到800 ℃是增加的,在800 ℃時達到最大值,之后又減小。 通過上述分析,當溫度到1200 ℃左右時,各產物的體積分數不再變化。
3.2 煤化學鏈氣化制氫制甲醇的數據分析
從圖5(a)中可知,隨著氣化壓力的增加,H2O體積分數由6%增至7%,CO體積分數由57.3%降至56%,CO2體積分數由9.6%增至12%,H2體積分數由24.8%降至19.4%,CH4體積分數趨于平穩狀態,所以氣化壓力選定為3 MPa。 從圖5(b)中可知,當溫度由650 ℃變化到1450 ℃時,粗煤氣成分中CO2和CH4的體積分數逐漸減小,650 ℃到1250 ℃之間,CO、H2以及H2O的體積分數增加, 在1250 ℃以后都處于穩定狀態。通過上述的描述,當溫度到1250 ℃左右時,各產物的體積分數不再變化。 從圖5(c)中可知,煤載氧體質量比在0.18之前, 粗煤氣組分CO和CO2的體積分數沒有變化,H2和H2O的體積分數增加,在煤載氧體質量比達到0.18之后,CO和H2的體積分數減小,CO2的體積分數增加,CH4的體積分數隨著煤載氧體質量比的增加在減小。 固體組分FeO和Fe隨著煤載氧體質量比的增加,FeO的體積分數增加,Fe的體積分數減小,所以在煤載氧體質量比為0.18時,各組分基本趨于最佳的狀態。
4 技術經濟分析
本研究以單位甲醇總投資和生產成本為評價指標,進行技術經濟分析。 表2為規模為1.7 × 106t/a的常規煤氣化制甲醇和1.1 × 106t/a的煤化學鏈氣化制氫制甲醇裝置的單位甲醇生產成本估算假設,表3為常規煤氣化制甲醇設備投資基礎數據[22,23],表4為煤化學鏈氣化制氫制甲醇設備投資基礎數據[24],表5為投資中各部分的比例系數[24],計算見式(4)~式(6)[25]。
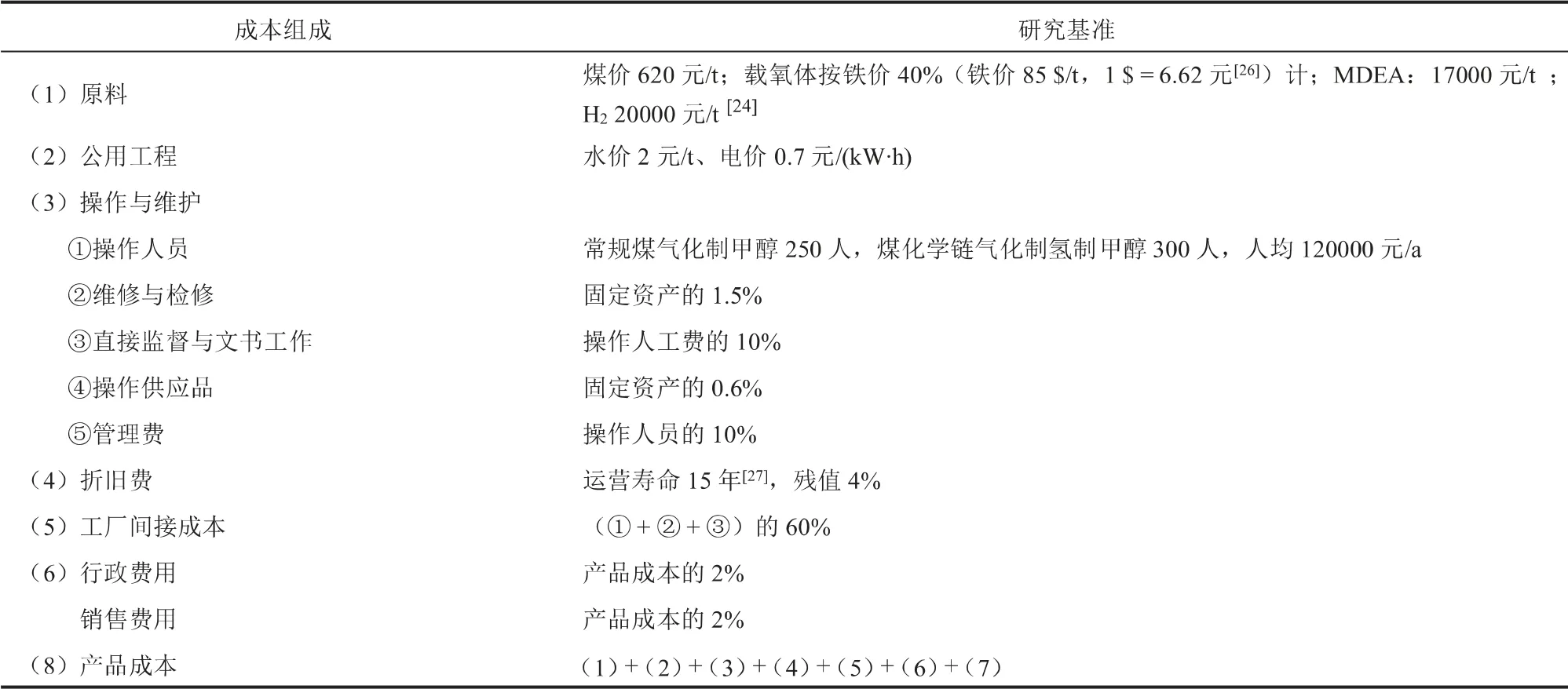
表2 煤氣化制甲醇的單位甲醇生產成本估算假設
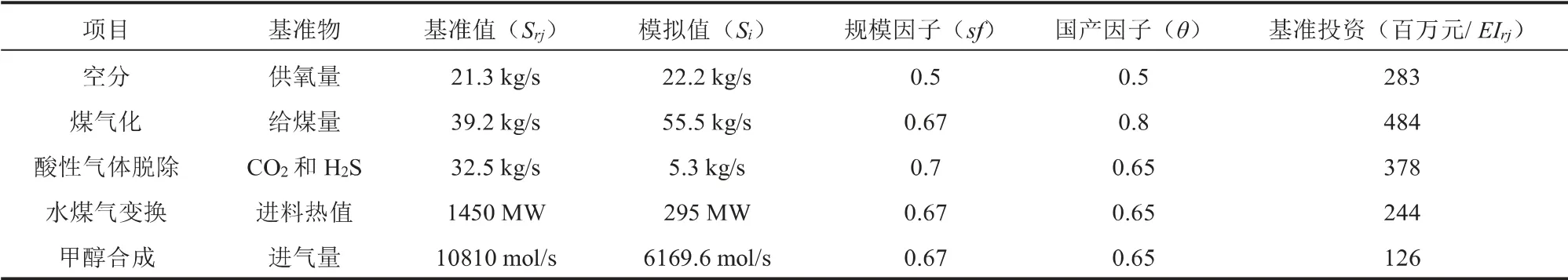
表3 常規煤氣化制甲醇設備投資基礎數據
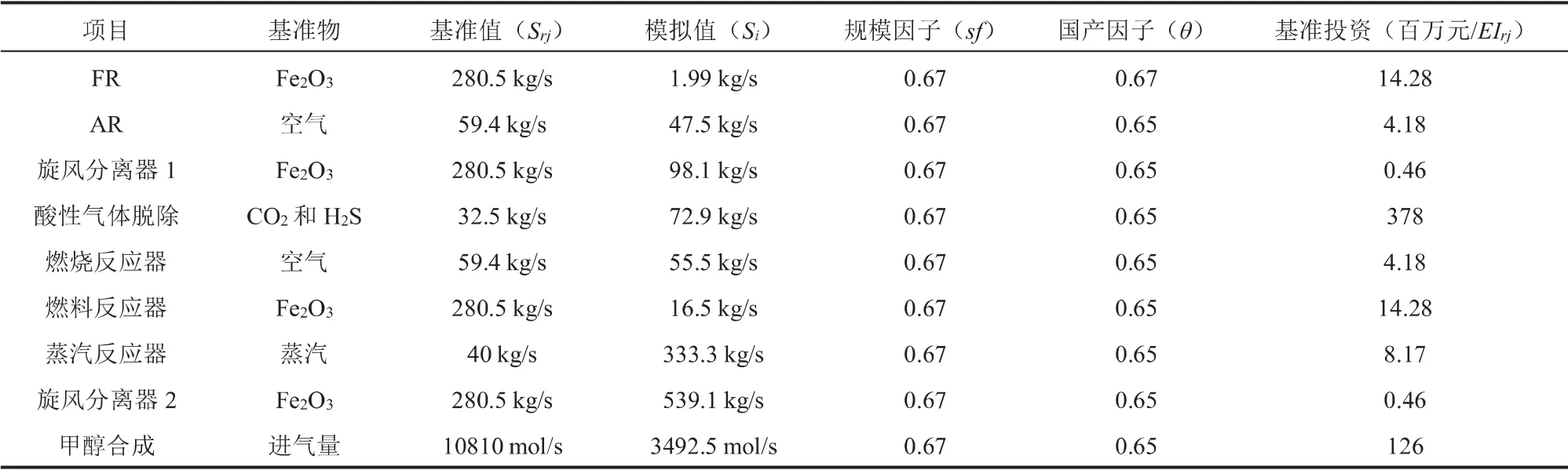
表4 煤化學鏈氣化制氫制甲醇設備投資基礎數據
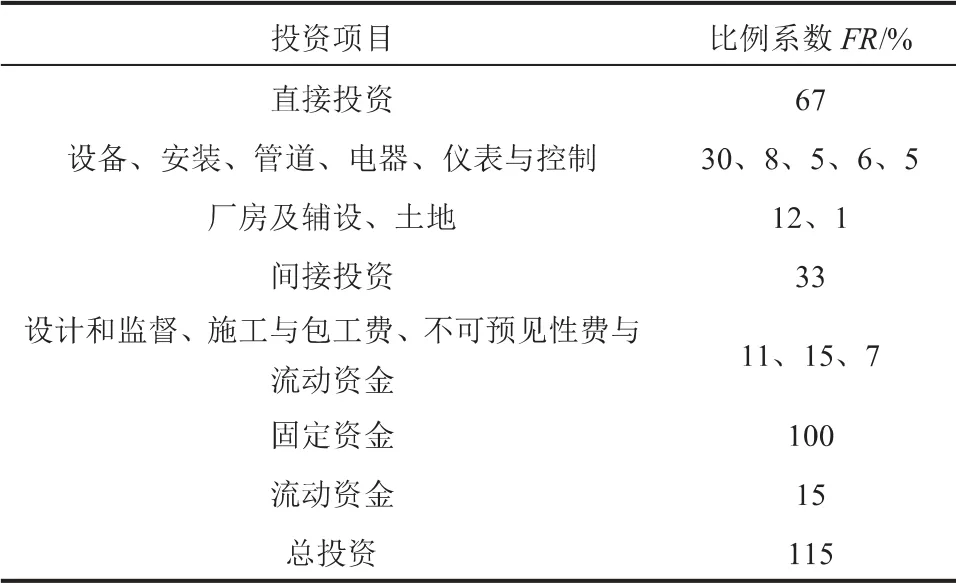
表5 投資中各部分的比例系數
式中,EI為設備投資, 百萬元;TCI為總投資, 百萬元;PC為產品成本,百萬元;CR為原材料成本,百萬元;CU為公用工程費,百萬元;CO&M為操作與維修費,百萬元;CD為折舊費,百萬元;CPOC為工廠間接成本,百萬元;CAC為行政費用,百萬元;CDSC為銷售成本,百萬元。
如圖6所示, 常規煤氣化制甲醇的單位甲醇生產成本為1647.4 元/t, 煤化學鏈氣化制氫制甲醇的單位甲醇生產成本為2116.6 元/t。但是,在煤化學鏈氣化制氫制甲醇中氫氣調節H2/CO比例的過程中還有剩余氫氣,H2的年剩余量是38313 t, 按照H2的價格20000 元/t對H2進行出售,則每噸甲醇銷售剩余氫可獲收益696.6 元,從總成本除去獲得的收益,最終煤化學鏈氣化制氫制甲醇的單位甲醇生產成本為1420 元/t。 比常規煤氣化制甲醇的成本低227.4 元/t。
如圖7所示, 常規煤氣化制甲醇裝置的單位甲醇總投資為2889.4 元/t, 煤化學鏈氣化制氫制甲醇裝置的單位甲醇總投資為2756 元/t,前者單位甲醇總投資高,主要在于前者是傳統的氣化工藝,多了一部分空分裝置和水煤氣變換,所以煤化學鏈氣化制氫制甲醇的投資有優勢。
5 結論
本文對常規煤氣化制甲醇和煤化學鏈氣化制氫制甲醇兩種工藝進行模擬與技術經濟分析,得到如下結論:
(1)常規煤氣化最優操作條件為:水煤質量比為0.45、氧煤質量比為0.4,氣化溫度為1200 ℃,氣化壓力為2.5~5.2 MPa。 煤化學鏈氣化最優條件為:煤載氧體質量比為0.18,空氣煤質量比為4.3,反應器的壓力為3 MPa,空氣反應器溫度為1250 ℃。
(2)以規模為1.7 Mt/a的常規煤氣化制甲醇和1.1 Mt/a的煤化學鏈氣化制氫制甲醇裝置的單位甲醇產品投資量來分析制甲醇的經濟性,常規煤氣化制甲醇裝置的單位甲醇總投資為2889.4 元/t, 甲醇生產成本為1647.4 元/t; 煤化學鏈氣化制氫制甲醇裝置的單位甲醇總投資降低為2756 元/t、甲醇生產成本降低為1420 元/t。 煤化學鏈氣化制氫制甲醇投資低主要是因為省去了空分制氧和水煤氣變換環節,而生產成本低則是由于副產高價值的氫氣。

