鈦摻雜BiFeO3光催化劑的制備及其催化性能
孟 帥,孫鵬凱,沈延群,孫 軍,王麗麗,譚 芳
(1. 長(zhǎng)春大學(xué) 理學(xué)院,吉林省材料設(shè)計(jì)與量子模擬實(shí)驗(yàn)室,吉林省人體健康狀態(tài)辨識(shí)與機(jī)能增強(qiáng)重點(diǎn)實(shí)驗(yàn)室, 長(zhǎng)春 130022;2. 長(zhǎng)白朝鮮族自治縣北疆硅藻土新材料科技有限公司,吉林 白山 134400)
0 引言
隨著工業(yè)社會(huì)的不斷發(fā)展,消耗化石能源導(dǎo)致了溫室效應(yīng)和環(huán)境污染,太陽能作為一種綠色、清潔、可再生的能源,已引起人們廣泛關(guān)注. 半導(dǎo)體光催化技術(shù)的迅速發(fā)展,使人們可利用太陽能高效治理有機(jī)污染物廢水[1-3]. 半導(dǎo)體光催化是指半導(dǎo)體在受到光子能量等于或大于其禁帶寬度的光照射后,載流子會(huì)經(jīng)歷產(chǎn)生、遷移、復(fù)合和轉(zhuǎn)化的過程,當(dāng)光能等于或大于半導(dǎo)體禁帶寬度時(shí),價(jià)帶電子可被激發(fā)到導(dǎo)帶,在價(jià)帶中留下帶正電的空穴,產(chǎn)生光生電子-空穴對(duì). 光生電子和空穴生成后會(huì)經(jīng)歷多個(gè)變化途徑,主要是遷移(或分離)和復(fù)合兩個(gè)競(jìng)爭(zhēng)過程. 電子和空穴遷移過程的速率和可能性取決于導(dǎo)帶和價(jià)帶各自的位置和被吸附物的氧化還原電位. 異相的存在使其與主相間由于能帶位置的差異產(chǎn)生電位差,光生電子和空穴在電位差的作用下實(shí)現(xiàn)遷移,提高了載流子的分離效率,抑制了電子-空穴對(duì)的復(fù)合. 分離后的電子和空穴在氧氣和水的參與下發(fā)生氧化還原反應(yīng)轉(zhuǎn)化為活性物質(zhì),最終完成有機(jī)污染物的降解. 圖1為兩相間載流子轉(zhuǎn)移示意圖.
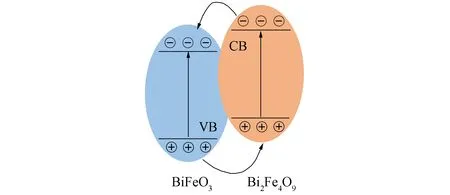
圖1 兩相間載流子轉(zhuǎn)移示意圖Fig.1 Schematic diagram of carrier transfer between two phases
傳統(tǒng)的光催化劑TiO2具有高催化率、穩(wěn)定、無毒、無二次污染等優(yōu)點(diǎn),但TiO2的禁帶寬度較大,只能利用太陽光中波段范圍較小的紫外光,導(dǎo)致太陽能的利用率較低. 鐵酸鉍(BiFeO3)是一種廣泛應(yīng)用于多鐵存儲(chǔ)器的多鐵材料,由于其具有窄帶隙(2.2~2.5 eV)、低成本、高化學(xué)穩(wěn)定性等特性,因此是一種具有潛在應(yīng)用前景的光催化劑. BiFeO3材料在可見光照射下具有高效的光催化活性[4-7]. 在BiFeO3光催化劑存在的情況下,當(dāng)太陽光照射染料分子的水溶液時(shí),催化劑表面受激產(chǎn)生電子-空穴對(duì),經(jīng)氧化還原反應(yīng)產(chǎn)生的羥基自由基等活性物質(zhì)最終將染料分子降解為無機(jī)小分子[8]. 但BiFeO3自身電子-空穴對(duì)具有高復(fù)合率的缺點(diǎn),限制了其在光催化領(lǐng)域的應(yīng)用.
為解決BiFeO3在實(shí)際應(yīng)用中的不足,摻雜金屬離子是一種簡(jiǎn)單且有效提高光催化性能的方法. 通過引入雜質(zhì)能級(jí)提高光生電子和空穴的分離效率,進(jìn)而提高光催化活性. 此外,BiFeO3的帶隙也可通過元素局部替換進(jìn)行調(diào)控,主要是Al3+,Ca2+,Sr2+,La3+等元素的Bi位替換以及Co2+,Mn2+,Cr3+,Ti4+等元素的Fe位替換[9-13]. 目前,BiFeO3的制備方法較多,如溶膠-凝膠法[14-16]、水熱法[17-18]、共沉淀法[19-20]、燃燒合成法[21-22]和超聲化學(xué)法[23-24]等,這些方法廣泛用于制備特定尺寸和形貌的BiFeO3微粒. 其中,溶膠-凝膠法具有相純度高、操作簡(jiǎn)單方便、可重復(fù)性好等優(yōu)點(diǎn).
由于Ti4+具有與Fe3+相似的離子半徑(Ti4+半徑為68 pm,F(xiàn)e3+半徑為64 pm),容易實(shí)現(xiàn)Fe位的離子替換,因此選擇Ti4+摻雜BiFeO3納米顆粒(Ti-BiFeO3),以提高材料的光催化性能. 本文用溶膠-凝膠法制備Ti-BiFeO3催化劑,通過改變煅燒溫度對(duì)Ti-BiFeO3進(jìn)行調(diào)控,并考察Ti-BiFeO3催化劑在太陽光照射下,光催化降解羅丹明-B(RhB)的反應(yīng)性能.
1 實(shí) 驗(yàn)
1.1 藥品和儀器
Bi(NO3)3,Fe(NO3)3和鈦酸四丁酯(分析純,上海阿拉丁生化科技股份有限公司);濃硝酸和無水乙醇(分析純,北京化工廠).
電子天平(BSA124S型,賽多利斯科學(xué)儀器有限公司);數(shù)控超聲波清洗器(KQ5200DA型,昆山市超聲儀器有限公司);氙燈光源(PLS-SXE300DUV型,北京泊菲萊科技有限公司);多頭磁力加熱攪拌器(HJ-4型,常州國(guó)華電器有限公司);恒溫磁力攪拌器(85-2型,常州國(guó)華電器有限公司);醫(yī)用離心機(jī)(H1650型,長(zhǎng)沙高新技術(shù)產(chǎn)業(yè)開發(fā)區(qū)湘儀離心機(jī)有限公司);電熱鼓風(fēng)干燥箱(DHG-9000型,上海一恒科學(xué)儀器有限公司);高溫爐(KSL-1700X-A2型,合肥科晶材料技術(shù)有限公司);X射線衍射儀(TD-3000型,丹東通達(dá)儀器有限公司);掃描電子顯微鏡(JEOL-7800F型,日本電子株式會(huì)社);紫外-可見分光光度計(jì)(UV-3600plus型,日本電子株式會(huì)社).
1.2 制 備
所有試劑均為分析純?cè)噭褂们拔唇?jīng)進(jìn)一步純化. 用溶膠-凝膠法合成一系列Ti摻雜摩爾分?jǐn)?shù)為10%的不同燒結(jié)溫度處理的BiFe0.9Ti0.1O3納米粒子. 先按化學(xué)計(jì)量比將Bi(NO3)3·5H2O和Fe(NO3)3·9H2O樣品溶于90 mL去離子水中,混合均勻后逐滴加入鈦酸四丁酯溶液,再取10 mL濃硝酸作為礦化劑緩慢加入上述溶液中,置于80 ℃磁力攪拌器連續(xù)攪拌2 h,形成黃棕色凝膠物質(zhì). 將所得凝膠轉(zhuǎn)移至100 ℃烘箱中烘干6 h后,于150 ℃烘干3 h至形成固體物質(zhì). 將所得前驅(qū)體研磨后,分別置于高溫爐中(600,650,700 ℃)煅燒2 h,升溫速率為10 ℃/min.
1.3 光催化實(shí)驗(yàn)
用RhB作為模擬染料進(jìn)行Ti-BiFeO3的光催化染料降解. 取0.5 g的Ti摻雜BiFeO3樣品于19.8 mL去離子水中,超聲處理10 min. 將0.2 mL質(zhì)量濃度為1 mg/mL的RhB溶液加入上述溶液中,懸濁液于黑暗環(huán)境中達(dá)到吸附-解吸平衡后,用功率為300 W的氙燈模擬太陽光源照射,每隔10 min取1 mL懸濁液,高速離心后取上清液,測(cè)定樣品的吸光度.
2 結(jié)果與討論
用X射線衍射(XRD)儀測(cè)試樣品的組成和相結(jié)構(gòu);用掃描電子顯微鏡(SEM)觀察納米顆粒的分布及形狀;用能譜分析(EDS)確定原子種類及比例;用紫外-可見分光光度計(jì)測(cè)試計(jì)算樣品的光催化性能,獲得樣品的吸收能力指標(biāo).
2.1 XRD結(jié)果

圖2 不同煅燒溫度下?lián)诫s摩爾分?jǐn)?shù) 為10%Ti的BiFeO3顆粒XRD譜Fig.2 XRD patterns of BiFeO3 particles with Ti-doped mole fraction of 10% at different calcination temperatures
圖2為摻雜摩爾分?jǐn)?shù)為10%Ti的BiFeO3顆粒在不同溫度下煅燒制得樣品的XRD譜. 由圖2可見,在22.1°,32.2°,39.5°,45.7°,52.1°,57.0°,67.1°,70.6°,75.9°處出現(xiàn)樣品的主要衍射峰,所有衍射峰均可與R3c (JCPDS No.21-0619)空間群BiFeO3相的(101),(012),(021),(202),(113),(122),(220),(303),(312)晶面相對(duì)應(yīng),表明已成功制備BiFeO3材料. 除與BiFeO3菱形結(jié)構(gòu)相對(duì)應(yīng)的衍射峰外,在樣品中27.5°,28.9°,33.7°,35.8°,37.1°,61.8°處檢測(cè)到Bi2Fe4O9的衍射峰,分別對(duì)應(yīng)Bi2Fe4O9相的(121),(002),(130),(310),(202),(004)晶面,表明元素間并未完全反應(yīng). 隨著溫度的升高,Bi2Fe4O9相的含量逐漸增大. 不同煅燒溫度下Bi2Fe4O9相的含量不同,可能是由于溫度升高加快了Bi元素?fù)]發(fā),導(dǎo)致Bi2Fe4O9含量不同. 測(cè)試結(jié)果表明,Bi2Fe4O9的相含量可通過改變煅燒溫度調(diào)控. 產(chǎn)生Bi2Fe4O9可能是Bi元素在制備過程中揮發(fā),誘導(dǎo)形成氧空位,從而形成了Bi2Fe4O9[25].
2.2 SEM與EDS結(jié)果
圖3為不同煅燒溫度下?lián)诫s摩爾分?jǐn)?shù)為10%Ti的BiFeO3顆粒的SEM照片. 由圖3可見,所有納米顆粒呈直徑為300~800 nm的不規(guī)則塊狀結(jié)構(gòu). 塊狀的空間結(jié)構(gòu)增大了反應(yīng)中與有機(jī)污染物的接觸面積,增加了納米材料的比表面積及反應(yīng)的活性位點(diǎn),有利于光催化反應(yīng)的進(jìn)行和光催化效率的提高[26]. 煅燒溫度為650 ℃和700 ℃的顆粒尺寸大于600 ℃煅燒的顆粒尺寸,證實(shí)了提高煅燒溫度對(duì)顆粒尺寸有粗化作用. 與700 ℃的顆粒相比,煅燒溫度為650 ℃的顆粒表面相對(duì)蓬松,樣品的比表面積大,增加了反應(yīng)的活性位點(diǎn),進(jìn)一步提高了光催化活性.

圖3 不同煅燒溫度下?lián)诫s摩爾分?jǐn)?shù)為10%Ti的BiFeO3顆粒SEM照片F(xiàn)ig.3 SEM images of BiFeO3 particles with Ti-doped mole fraction of 10% at different calcination temperatures
在Ti-BiFeO3納米顆粒中,Bi,F(xiàn)e,Ti元素的能譜分析列于表1. 由表1可見,隨著煅燒溫度從600 ℃增加到700 ℃,w(Bi)∶w(Bi+Ti)逐漸減小,該結(jié)論進(jìn)一步證明適當(dāng)升高煅燒溫度可促進(jìn)Bi揮發(fā),誘導(dǎo)形成氧空位,從而形成Bi2Fe4O9相.

表1 Ti-BiFeO3納米顆粒中Bi,F(xiàn)e,Ti元素的質(zhì)量比
2.3 UV-Vis結(jié)果
為研究光催化劑的光吸收特性,測(cè)試了Ti-BiFeO3的紫外-可見(UV-Vis)光譜,如圖4所示. 由圖4可見,所有樣品的最大吸光度均位于可見光范圍內(nèi)(λ=550 nm附近),隨著時(shí)間的增加,吸光度逐漸降低,表明Ti-BiFeO3降解RhB的過程. 此外,BiFe0.90Ti0.10O3的最高吸收峰出現(xiàn)一定程度的紅移,這是由于光降解過程中,RhB分子發(fā)生了脫乙基反應(yīng)所致[27].
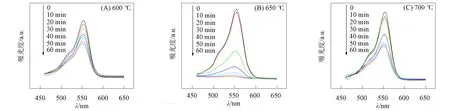
圖4 不同煅燒溫度下Ti-BiFeO3顆粒的UV-Vis光譜Fig.4 UV-Vis spectra of Ti-BiFeO3 particles at different calcination temperatures
2.4 對(duì)RhB降解的影響
圖5為不同煅燒溫度下Ti-BiFeO3顆粒的RhB降解曲線. 由圖5可見,650 ℃煅燒下的Ti-BiFeO3具有最高的降解活性,反應(yīng)30 min后,降解效率約為75%~80%;600,700 ℃煅燒下制得的樣品光催化活性明顯下降,60 min后溶液質(zhì)量濃度約為初始質(zhì)量濃度的30%和45%. 由于650 ℃煅燒得到的Ti-BiFeO3納米顆粒具有適中的Bi2Fe4O9含量和最高的光催化活性,因此適量的Bi2Fe4O9相可有效提高樣品的光催化效率. 此外,隨著煅燒溫度的升高,Bi2Fe4O9的光催化活性呈先升高后降低的趨勢(shì),可能是由于BiFeO3或Bi2Fe4O9結(jié)構(gòu)被Bi2Fe4O9納米材料覆蓋,導(dǎo)致光催化效率降低[28].
綜上,本文用溶膠-凝膠法制備了Ti-BiFeO3納米顆粒,并研究了不同煅燒溫度對(duì)樣品結(jié)構(gòu)及光催化性能的影響. 結(jié)果表明:引入適量的Bi2Fe4O9可提高Ti-BiFeO3材料的光催化性能,煅燒溫度可調(diào)控Bi2Fe4O9的含量;Ti-BiFeO3催化劑為不規(guī)則的塊狀結(jié)構(gòu),且煅燒溫度為650 ℃的顆粒表面相對(duì)蓬松,有利于光催化反應(yīng)的進(jìn)行和光催化效率的提高;煅燒溫度為650 ℃的Ti-BiFeO3具有優(yōu)異的降解活性,在60 min內(nèi)達(dá)到85%的降解效率.

