磁性鎳基氮摻雜多壁碳納米管對雙酚A的吸附性能及機理研究
孔 佳,王學東,劉婷婷,2,顧海東,2*
(1.蘇州科技大學 環境科學與工程學院,江蘇 蘇州 215009;2.江蘇省環境科學與工程重點實驗室,江蘇 蘇州 215009)
雙酚A(BPA)是一種典型的有機污染物,是生產環氧樹脂和聚碳酸酯塑料不可或缺的添加劑,含有BPA的塑料廣泛用作食品及飲料包裝的內側涂層[1]。近年來,在廢水、地下水、地表水甚至飲用水中都檢測到了BPA[2]。BPA具有一定的雌激素活性,結構與生物體內激素類似,具有內分泌干擾效應,對人體的生殖系統和免疫力系統有危害作用[3-4]。因此,水體中BPA的有效去除成為研究的熱點。
目前,水體中BPA的去除方法主要有光催化降解法[5]、物理法(膜過濾和吸附法)[6]、生物降解法[7]、化學氧化法[8]等。相比于其他方法,吸附法具有操作簡單,不易產生二次污染等優點。利用納米材料進行吸附被認為是目前去除廢水中BPA的有效途徑之一。碳基納米材料具有比表面積大、合成成本低等優點,是理想的吸附劑[9-10]。但傳統碳基納米材料在吸附完成后,往往需借助過濾、離心等繁瑣步驟才能與廢水分離。為了簡化分離操作,提高分離效率,對吸附材料進行磁化和摻入氮、硼等雜原子改性處理成為研究熱點。傳統的磁性吸附材料多以Fe3O4作為磁核,但裸露的Fe3O4的磁性和理化性質不穩定[11],大大限制了其應用范圍。為保證材料在擁有較強吸附性能的同時保持磁性穩定,Song等[12]通過煅燒鎳基金屬有機骨架制備了新型吸附劑Ni@C納米復合材料,并將其用于羅丹明B的吸附研究,室溫下10 min內的吸附率可達99%。Xu等[9]制備了氮摻雜多孔碳納米結構吸附劑(N-dope FPC)用于水溶液中磺胺甲嘧啶的吸附,298 K下5 min即可達到吸附平衡,吸附容量達610 mg/g。研究表明,磁性金屬鎳的引入可簡化吸附劑分離過程中的繁瑣步驟,提升處理效率;同時,摻雜的氮原子為碳納米管引入了空缺位,從而提高了吸附效率[13]。
目前,含鎳的氮摻雜磁性碳納米管狀材料在BPA的吸附應用中少見報道。基于此,本實驗以醋酸鎳和雙氰胺為前驅體,通過高溫煅燒法一步制得了具有較大比表面積,較多缺陷位點及較強磁性的氮摻雜磁性多壁碳納米管狀材料Ni-NMCNTs,對Ni-NMCNTs的微觀形貌及結構進行研究,并將其用于水中BPA的吸附。結合液相色譜/熒光檢測法考察了不同反應條件對吸附性能的影響,并通過傅里葉變換紅外光譜、X射線光電子能譜等測試對吸附機理進行了深入研究。
1 實驗部分
1.1 主要試劑與儀器
雙酚A(BPA)購于日本WAKO公司,四水合醋酸鎳(Ni(CH3COO)2·4H2O)、N,N-二甲基甲酰胺(DMF)、色譜級乙腈均購于瑞士Adamas公司,雙氰胺(C2H4N4)、調節pH值所用的氫氧化鈉(NaOH)和鹽酸(HCl)均購于上海阿拉丁試劑有限公司,配制BPA溶液所用的色譜級甲醇(CH3OH)購于上海滬試公司,清洗和合成材料所用的無水乙醇和硫酸均為分析純,購于太倉周氏化學試劑有限公司。
KQ-500DE數控超聲波清洗器(昆山市超聲儀器有限公司),OTF-1200X管式爐(合肥科晶材料技術有限公司),DHG-9070A電熱鼓風干燥箱(上海夕聞生物科技有限公司),B15-3多功能恒溫恒速磁力攪拌器(上海司樂儀器有限公司),THZ-92A臺式恒溫振蕩箱(上海躍進醫療器械有限公司),Quanta FEG250掃描電子顯微鏡、Tecnai G2F30 透射電子顯微鏡(美國FEI公司),Nicolet 6700傅里葉變換衰減全反射紅外光譜儀、K-Alpha+型X射線光電子能譜儀(美國Thermo Fisher Scientific公司),Bruker D8 Advance X射線衍射儀(德國Bruker公司),MPMS XL-7磁滯回線測試儀(美國Quantum Design公司),V-Sorb 2800P 比表面積及孔徑分析儀(北京金埃譜科技有限公司),LC-20AT高效液相色譜儀(日本島津公司)。
1.2 Ni-NMCNTs的制備
稱取0.209 g Ni(CH3COO)2·4H2O和1.009 g C2H4N4加入到約30 mL DMF中,將混合液于80 ℃,500 r/min下攪拌至蒸干,得到棕黃色前驅體粉末。將前驅體粉末在N2保護下,700 ℃高溫煅燒2 h,冷卻后得到的黑色粉末先用200 mL 1 mol/L H2SO4酸洗24 h,再用超純水洗滌3次,最后于60 ℃下烘干,得到Ni-NMCNTs。
1.3 材料表征
利用掃描電子顯微鏡(SEM)和透射電子顯微鏡(TEM)觀察Ni-NMCNTs的形貌特點;利用傅里葉變換紅外光譜(FT-IR)研究材料的官能團;利用X射線衍射儀(XRD)和X射線光電子能譜技術(XPS)分別研究材料的晶格結構及化學成分;利用比表面積及孔徑分析儀(BET)測試Ni-NMCNTs的比表面積和孔徑分布;利用磁滯回線測試儀(VSM)測量吸附前后Ni-NMCNTs的磁性變化。
1.4 Ni-NMCNTs材料吸附BPA實驗
在一系列含有100 mL BPA溶液(20 mg/L)的250 mL錐形瓶中分別加入20 mg Ni-NMCNTs,將錐形瓶置于25 ℃,振蕩速度200 r/min的恒溫振蕩箱中,分別于10、30、60、90、120 min時各取1 mL溶液,采用磁鐵將吸附劑與樣品溶液分離。
通過高效液相色譜/熒光法測定BPA的濃度,色譜柱為安捷倫Eclipse XDB C18,柱溫為30 ℃,流動相為50%乙腈和50%超純水,流速為0.8 mL/min,激發波長為233 nm,發射波長為303 nm。
2 結果與討論
2.1 材料的表征


圖1 Ni-NMCNTs的SEM(A)和TEM(B)

根據吸附等溫線計算得出Ni-NMCNTs吸附前后的比表面積分別為201.36 m2/g和171.94 m2/g(圖3A),由孔徑分布(BJH)模型(圖3A內插圖)計算得到Ni-NMCNTs的孔徑主要集中于3.8 nm,累積孔體積為0.766 9 m3/g。表明該材料具有介孔結構及較大的比表面積和孔隙體積,可有效增加與BPA的接觸面積,為吸附過程提供更多的活性位點[22]。VSM(圖3B)測試結果顯示,吸附前后Ni-NMCNTs材料的飽和磁通量分別為14.71、13.35 emu/g,表明Ni-NMCNTs具有明顯的超順磁性,且吸附前后磁性的變化很小,可保證完成吸附后將其快速分離。
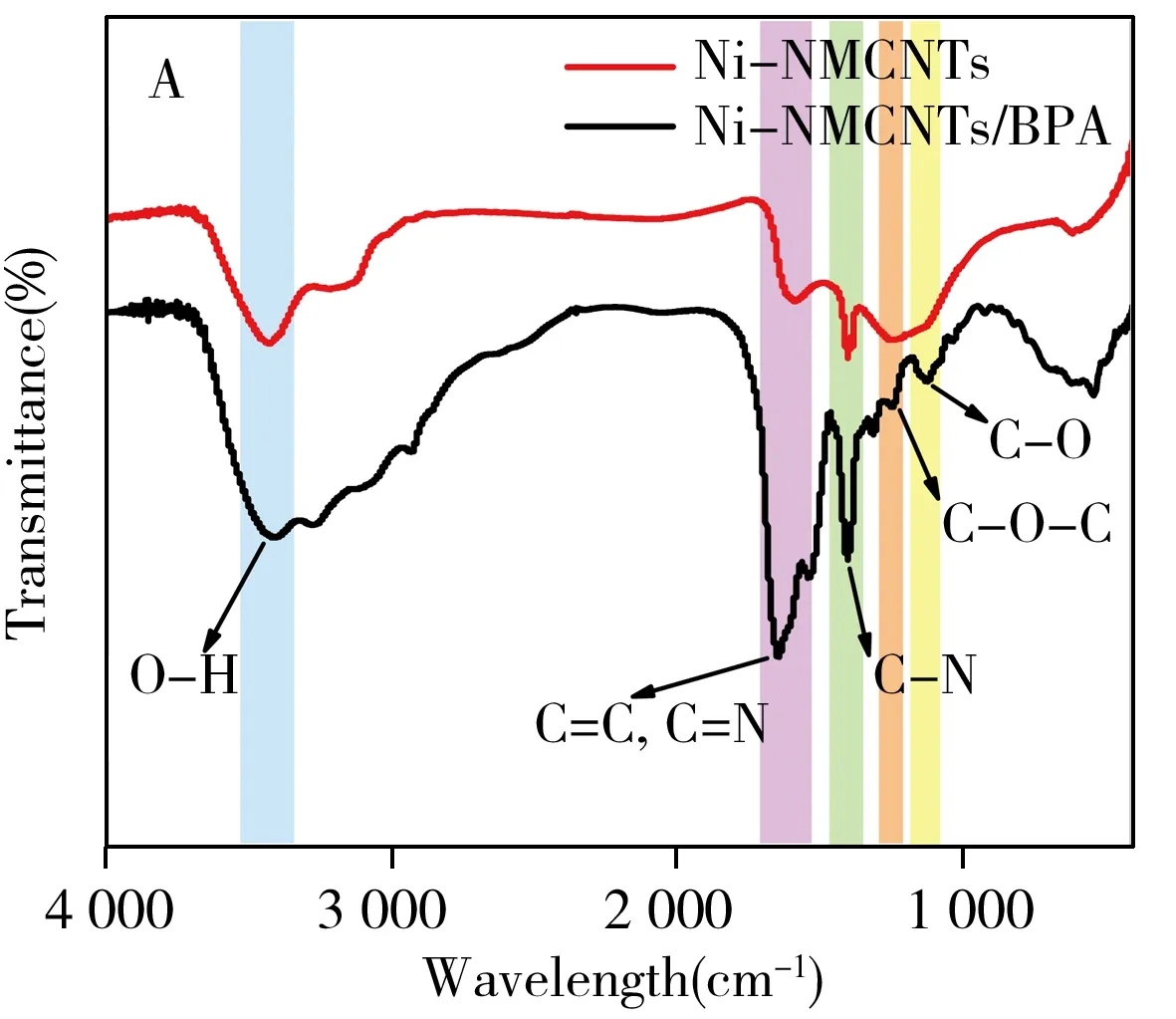
圖2 Ni-NMCNTs的結構表征

圖3 Ni-NMCNTs的BET圖(A)和VSM圖(B)

圖4 pH值對吸附BPA的影響
2.2 Ni-NMCNTs吸附性能的影響因素
2.2.1 pH值的影響在一系列100 mL BPA溶液(20 mg/L)中分別加入20 mg Ni-NMCNTs,用HCl(0.1 mol/L)或NaOH(0.1mol/L)調節pH值(2.0、4.0、6.0、8.0、10.0)。如圖4所示,隨著pH值的增加,吸附效率呈先上升后下降的趨勢,酸性條件下BPA的吸附率普遍高于堿性條件,pH 6.0時Ni-NMCNTs對BPA的吸附率可達86.6%。這是因為,BPA在水溶液中的解離常數pKa為9.59~11.30,pH 2.0~6.0時,隨著pH 值的升高,H+與BPA之間的相互競爭逐漸降低[23];而堿性條件下,溶液中的BPA主要以游離態的形式存在,容易被質子化形成陰離子,并在pH 8.0時發生一級電離形成HBPA-,pH 9.0時則發生二級電離形成BPA2-,與被Ni-NMCNTs吸附的BPA發生靜電作用,從而導致吸附率下降[24-25]。因此,偏酸性條件更利于Ni-NMCNTs對BPA的吸附。
2.2.2 投加量的影響合理的吸附劑投加量是影響吸附效果的另一重要因素。配制100 mL BPA溶液(20 mg/L),向其中分別加入5、10、15、20、25、30 mg Ni-NMCNTs,研究吸附劑投加量對吸附實驗的影響。結果顯示,Ni-NMCNTs的投加量為5 mg時,BPA的吸附率為43.5%,投加量為20 mg時吸附率增至86.1%,將投加量繼續增加至35 mg,吸附率變化不明顯,保持在86.5%左右。這可能是由于隨著吸附劑投加量的增加,吸附劑的活性位點相應增加,當投加量增至20 mg時吸附達到飽和,吸附率基本穩定[14]。因此,選擇最佳投加量為20 mg進行后續研究。
2.3 吸附等溫線
將20 mg Ni-NMCNTs復合材料分別投加到100 mL不同質量濃度(5、10、15、20、25、30 mg/L)的BPA溶液中,于恒溫振蕩箱中在不同溫度(25、35、45 ℃)下以200 r/min振蕩,經磁鐵分離后,采用HPLC測定BPA的濃度。分別采用Langmuir(式1)和Freundlich(式2)等溫吸附方程對實驗數據進行線性擬合:
(1)
式中,Ce為吸附平衡濃度,mg/L;b為平衡時的吸附常數,L/mg;Qe為平衡時的吸附量,mg/g;Qm為理論最大吸附量,mg/g。
(2)
式中,Ce為吸附平衡濃度,mg/L;Qe為平衡時的吸附容量,mg/g;k為吸附常數,L/mg,n為溫度相關的特征常數。
由圖5可知,Ni-NMCNTs對BPA的吸附更符合Freundlich 等溫吸附方程。25 ℃時的回歸系數R2為0.997 9,理論最大吸附量為31.63 mg/g,表明表面吸附位點分布不均勻。由圖6可知,隨著溫度的升高,Ni-NMCNTs對BPA的吸附量減小,這是由于BPA在水中的溶解度隨著溫度的升高而增加,而整個吸附過程為放熱過程,溫度的降低有利于Ni-NMCNTs對BPA的吸附[25]。因此,選擇室溫25 ℃進行吸附研究。

圖5 Langmuir(A)和Freundlich(B)等溫吸附擬合結果

圖6 不同溫度下Ni-NMCNTs對BPA的等溫吸附曲線

圖7 Ni-NMCNTs 對BPA的吸附動力學曲線
2.4 吸附動力學
選擇準一級動力學方程和準二級動力學方程對吸附實驗進行擬合。準一級動力學公式:
(3)
其中,qe為平衡時的吸附容量,mg/g;qe,exp為理論飽和吸附量,mg/g;qt為t時刻的吸附容量,mg/g;k1為吸附速率常數,g/(mg·min)。
(4)
其中,qt為t時刻的吸附容量,mg/g;k2為吸附速率常數,g/(mg·min)。
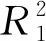

表1 吸附熱力學參數
2.5 吸附熱力學研究
在吸附等溫線的基礎上,計算了吸附過程的自由能(ΔG)、焓變(ΔH)、熵變(ΔS),結果如表1所示。ΔH為負值,表明整個吸附過程為放熱過程;吸附熱低于40 kJ/mol,可知吸附過程中發生氫鍵力作用。Ni-NMCNTs中的氮原子和含氧官能團可與BPA中的羥基之間形成氫鍵;同時,材料表面存在豐富的π電子,可與BPA結構中苯環上的π電子形成π-π共軛,表明在該吸附過程中存在物理吸附,與文獻報道結論相符[25-26]。ΔG為負值,表明Ni-NMCNTs對BPA的吸附自發進行;ΔS為負值,表明Ni-NMCNTs對BPA的吸附隨著吸附量的增加逐漸趨于穩定。
2.6 材料的重復利用
為了驗證Ni-NMCNTs 的可重復使用性,將吸附后的材料回收并利用乙醇和超純水交替洗滌3次,于60 ℃下烘干后繼續用于BPA吸附實驗。結果發現,每經一次循環后,吸附量和吸附率均有所下降,循環5次后的最大吸附量為73.48 mg/g,為初始最大吸附量的87.9%,吸附率從86.8%下降至79.4%,表明合成的Ni-NMCNTs吸附劑具有良好的可重復利用性。
3 結 論
本研究采用高溫煅燒法制備了磁性鎳基氮摻雜多壁碳納米管材料(Ni-NMCNTs),并用于BPA的吸附研究。結果證明,酸性條件更有利于Ni-NMCNTs 對BPA的吸附,而Ni-NMCNTs中空的納米結構和大的比表面積可增大其與溶液的接觸面積,提高吸附率;氮元素的摻雜和材料中豐富的含氧官能團有助于形成氫鍵,增強π-π共軛效應,也有利于吸附效率提高。磁性金屬鎳的引入則使材料更利于分離并重復利用。動力學研究表明,Ni-NMCNTs對BPA的吸附更符合準二級動力學方程,即吸附過程主要為化學吸附。熱力學研究表明,Ni-NMCNTs對BPA的吸附更符合Freundlich模型,整個吸附過程為放熱過程且自發進行,吸附過程中存在物理吸附。