酸棗仁-五味子藥對配比篩選及半仿生提取工藝研究
冉建新 胡等慧 王曉杰
1.北京市第六醫院藥劑科,北京 100007;2.北京中醫藥大學中藥學院,北京 102488;3.北京電子科技職業學院生物工程學院,北京 100176
失眠又稱為睡眠障礙(sleep deprivation,SD),是指睡眠時間和質量下降不能滿足人們日常社會活動的一種睡眠障礙綜合征[1],屬中醫范疇內“不寐”“不得眠”“不得臥”等,是目前臨床較為難治的疾病之一[2-3]。酸棗仁、五味子兩藥在中醫經典安神方劑中多配伍使用,是臨床常用的安神藥對之一,具有滋陰養血、安神鎮驚、消除疲勞等功效,可用于各種與失眠有關的病癥,如神經衰弱等[4-10]。北京市第六醫院(以下簡稱“我院”)臨床應用酸棗仁-五味子混合粉末口服給藥的鎮靜催眠效果較為理想,與文獻報道相一致;但二者最佳配比,未見有相關報道[11-13]。鑒于此,選取臨床常用的酸棗仁-五味子3 個配比(15 g∶6 g、12 g∶6 g、6 g∶6 g)進行考察,篩選方便、安全、高效的半仿生提取法的提取工藝參數。
1 材料與方法
1.1 試劑與設備儀器
1.1.1 試劑
酸棗仁、五味子購買于河北安國藥材市場;戊巴比妥鈉(國藥集團化學試劑有限公司,批號:WS20060 401);艾司唑侖(山東信誼制藥有限公司,批號:180905);谷氨酸(Glu,貨號:CSB-E05129r)、γ-氨基丁酸(GABA,貨號:SA8240)、谷氨酰胺(Gln,貨號:CSB-E12692h)、5-羥色胺(5-HT,貨號:CSB-E14956r)、5-羥吲哚乙酸(5-HIAA,貨號:CEB005Ge-2),上述酶聯免疫吸附試驗(ELISA)試劑盒均購于上海碧云天生物科技有限公司。
1.1.2 設備儀器
VT05404-0998 全自動酶標儀(美國伯騰儀器公司);YY/T0657-2008 高速冷凍離心機(湖南赫西儀器公司);KQ-250E 多功能粉碎機(鉑歐五金廠);DHG-9030A(101)電熱恒溫鼓風干燥箱(上海齊欣科學儀器有限公司);S1-2002 電子天平(丹佛儀器有限公司)。
1.2 實驗動物
SPF 級昆明種小鼠購于北京斯貝福實驗動物有限公司,雄性,5 周齡,體重(25±5)g,合格證號:SCXK9(京)2017-0002。實驗動物喂養環境:SPF 級動物房,自由飲水,相對濕度:40%~70%,室溫:20~26℃。
1.3 實驗方法
1.3.1 酸棗仁-五味子配比篩選
1.3.1.1 供試品溶液的制備 根據2015 版《中華人民共和國藥典》一部[4]規定人體臨床用量及我院常用的配比進行分析,確定制備3 份不同配比的供試品溶液,其中酸棗仁與五味子配比依次為:15 g∶6 g、12 g∶6 g、6 g∶6 g。模擬臨床使用中所采取的酸棗仁-五味子混合粉末口服的給藥形式,上述不同配比藥物打粉制備混懸液以備實驗使用。
1.3.1.2 實驗分組及給藥 依據隨機數字表法,將50 只小鼠分為空白組、陽性藥組、酸棗仁:五味子(15 g∶6 g)組、酸棗仁:五味子(12 g∶6 g)組、酸棗仁:五味子(6 g∶6 g)組,每組10 只。空白組給予蒸餾水,陽性藥組給予0.13%艾司唑侖水溶液,給藥組給予相應配比混懸液,連續給藥14 d。
1.3.1.3 閾下劑量戊巴比妥鈉致小鼠睡眠 各組小鼠適應性3 d 后,于實驗第1 天開始灌胃給予藥物,給藥60 min 后,腹腔注射閾下濃度戊巴比妥鈉,0.1 mL/10 g,觀察30 min 內入睡小鼠只數(翻正反射消失1 min以上)。
1.3.1.4 閾劑量戊巴比妥鈉致小鼠睡眠 試驗期間每天定時給藥,第13 天,各組小鼠灌胃給予對應藥物60 min 后,腹腔注射閾上濃度戊巴比妥鈉,0.1 mL/10 g,計算各組小鼠睡眠潛伏期和睡眠持續時間(以注射后小鼠翻正反射消失為入睡指標,小鼠翻正反射恢復為蘇醒指標)。
1.3.1.5 小鼠大腦內GABA、Glu、Gln、5-HT 和5-HIAA含量檢測 試驗最后1 d,5 組小鼠給藥60 min 后注射閾劑量戊巴比妥鈉,12 h 后處死,制備10%的腦組織液,按照試劑盒說明書嚴格操作,分別測定腦組織液中GABA、Glu、Gln、5-HT 和5-HIAA 含量。
1.3.2 半仿生提取工藝優化
1.3.2.1 Box-Behnken 響應面法實驗設計 將上述篩選得到的藥對配比,進行半仿生提取工藝的優化。根據前期預實驗結果,利用BBC 設計原理,選取人工胃液的用量和提取時間,人工腸液的用量和提取時間4 個為自變量為考察因素,以GABA 和5-HT 的綜合評分為響應值,設計四因素三水平的響應面優化實驗,見表1。利用Design-Expert 軟件進行響應面分析,確定酸棗仁與五味子半仿生提取工藝的最佳條件。
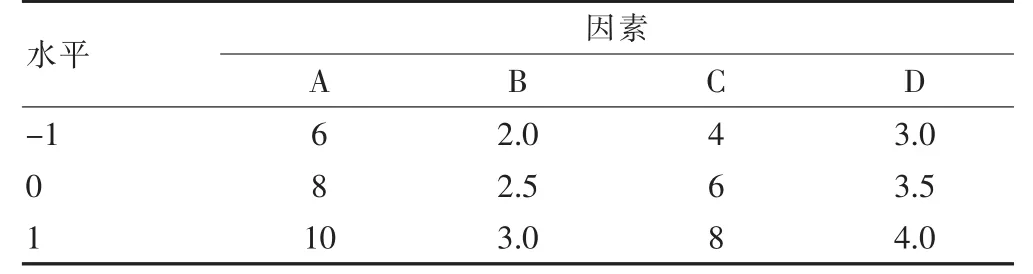
表1 四因素三水平中心組合實驗因素水平編碼表
1.3.2.2 供試品溶液的制備及分組給藥 參考上述實驗,選取GABA 和5-HT 為考察指標,設計藥效試驗,操作同上,每組5 只小鼠,將仿生提取液減壓濃縮為1 g/mL 灌胃給藥,于第14 天末次給藥60 min 后處死,制備腦組織液,測定GABA 和5-HT 含量。
1.4 統計學方法
采用SAS 8.2 統計學軟件進行數據分析,計量資料用均數±標準差()表示,多組間比較采用單因素方差分析,兩兩比較采用LSD-t 檢驗。以P < 0.05 為差異有統計學意義。
2 結果與分析
2.1 酸棗仁、五味子配比篩選結果
2.1.1 閾下劑量戊巴比妥鈉對各組小鼠入睡的影響
與空白組比較,陽性藥組、15 g∶6 g 組、12 g∶6 g組以及6 g∶6 g 組小鼠入睡率均有一定程度提高,其中以陽性藥組療效最佳,15 g∶6 g 組次之,12 g∶6 g 及6 g∶6 g 組效果相近。見表2。
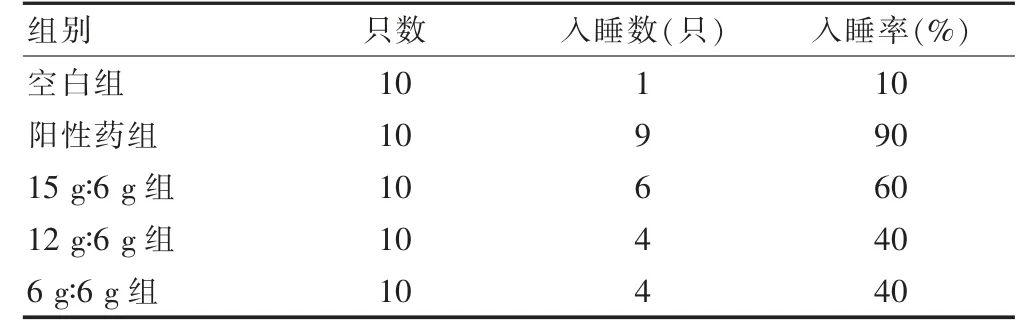
表2 閾下催眠劑量戊巴比妥鈉對各組小鼠入睡的影響
2.1.2 閾劑量戊巴比妥鈉對各組小鼠睡眠時間的影響
與空白組比較,陽性藥組、15 g∶6 g 組以及6 g∶6 g組小鼠睡眠潛伏期明顯縮短、睡眠持續時間明顯延長,差異有統計學意義(P <0.05 或P <0.01)。與陽性藥組比較,12 g∶6 g 組睡眠潛伏期明顯延長,差異有統計學意義(P <0.05)。與15 g∶6 g 組比較,12 g∶6 g 組睡眠潛伏期明顯延長,差異有統計學意義(P <0.05)。見表3。
表3 閾劑量戊巴比妥鈉對各組小鼠睡眠的影響(min,)
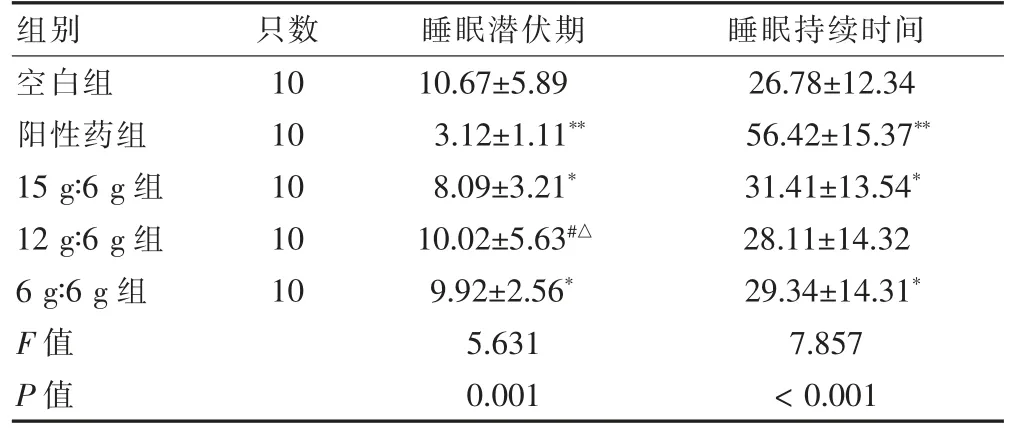
表3 閾劑量戊巴比妥鈉對各組小鼠睡眠的影響(min,)
注:與空白組比較,*P <0.05、**P <0.01;與陽性藥組比較,#P <0.05;與15 g∶6 g 組比較,△P <0.05
2.1.3 藥物對各組小鼠腦組織GABA、Glu及Gln含量的影響
與空白組比較,陽性藥組和15 g∶6 g 組小鼠腦內GABA 含量增加、Glu 和Gln 含量減少,差異有統計學意義(P <0.05 或P <0.01)。與陽性藥組比較,12 g∶6 g 組和6 g∶6 g 組GABA 含量減少、Glu 和Gln 含量增加,差異有統計學意義(P <0.05)。與15 g∶6 g 組比較,12 g∶6 g 組GABA 含量減少;6 g∶6 g 組Gln 含量增加,差異有統計學意義(P <0.05)。見表4。
表4 藥物對各組小鼠腦組織中GABA、Glu 及Gln 的影響()
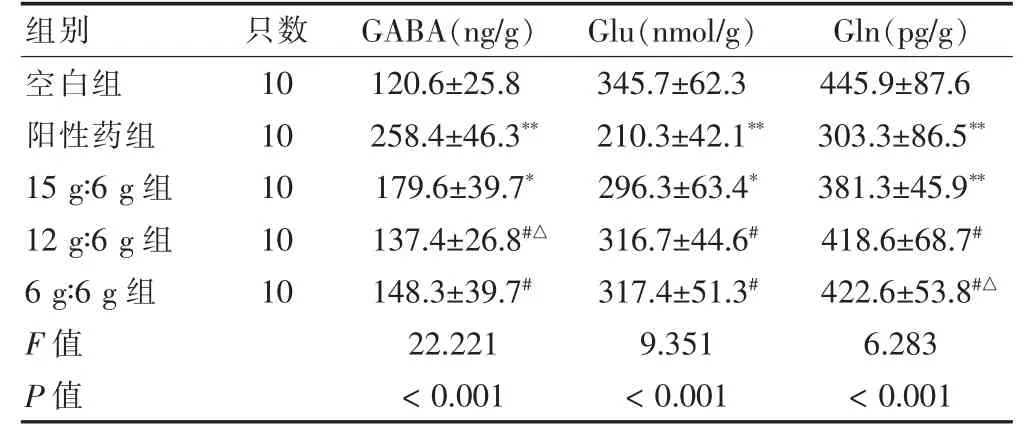
表4 藥物對各組小鼠腦組織中GABA、Glu 及Gln 的影響()
注:與空白組比較,*P <0.05、**P <0.01;與陽性藥組比較,#P <0.05;與15 g∶6 g 組比較,△P <0.05。GABA:γ-氨基丁酸;Glu:谷氨酸;Gln:谷氨酰胺
2.1.4 藥物對各組小鼠腦內5-HT 及5-HIAA 的影響
與空白組比較,陽性藥組、15 g∶6 g 組、12 g∶6 g組和6 g∶6 g 組的5-HT 含量增加,差異有統計學意義(P <0.05 或P <0.01)。與陽性藥組比較,12 g∶6 g組5-HT 含量減少,差異有統計學意義(P <0.05)。與15 g∶6 g 組比較,12 g∶6 g 組5-HT 含量減少,差異統計學意義(P <0.05)。與空白組比較,陽性藥組5-HIAA 含量減少,差異有統計學意義(P <0.05)。與陽性藥組比較,15 g∶6 g 組、12 g∶6 g 組、6 g∶6 g 組5-HIAA 含量增加,差異有統計學意義(P <0.05 或P <0.01)。見表5。
表5 藥物對各組小鼠腦組織中5-HT 及5-HIAA 的影響(pg/g,)
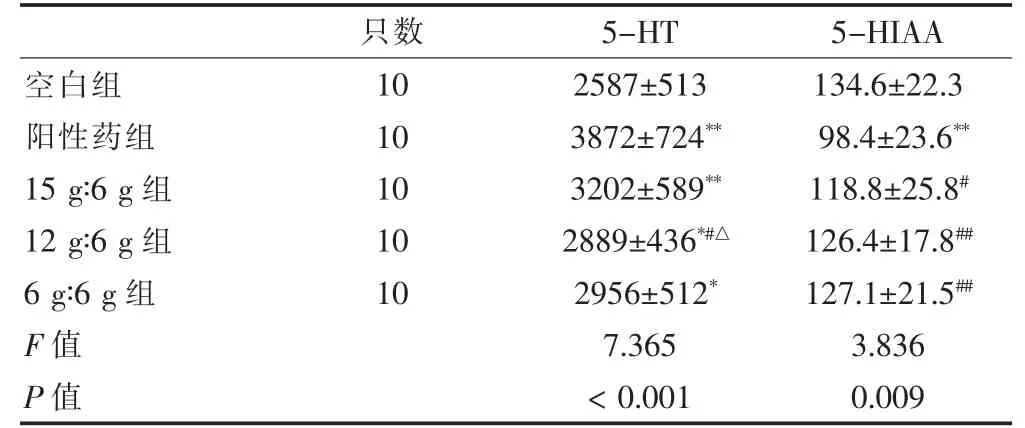
表5 藥物對各組小鼠腦組織中5-HT 及5-HIAA 的影響(pg/g,)
注:與空白組比較:*P <0.05,**P <0.01,與陽性藥組比較:#P <0.05;與15 g∶6 g 組比較,△P <0.05。5-HT:5-羥色胺;5-HIAA:5-羥吲哚乙酸
綜上所知,酸棗仁與五味子不同配比均能對小鼠起到一定的鎮靜催眠作用,其中以15 g∶6 g 組療效最好,6 g∶6 g 組次之,12 g∶6 g 組最差,且6 g∶6 g 組與12 g∶6 g 組效果與15 g∶6 g 組相差較大,最終確定15 g∶6 g 組為最佳配比。
2.2 半仿生提取工藝優化結果
根據預實驗結果,利用Box-Behnken 中心組合實驗的設計原理,設計四因素三水平的29 個實驗點。各實驗點GABA 和5-HT 的含量測定結果見表6。
2.2.1 回歸模型的建立與擬合
采用Design-Expert 軟件對上面數據進行分析,以Y 對變量進行模型擬合,并通過系數(R2)等對擬合自模型進行評價,通過比較各擬合方程的擬合度,建立四元二次回歸方程Y=0.98+0.052A+0.0075B-0.0008C+0.025D+0.010AB+0.012AC+0.013AD+0.0075BC-0.060BD-0.022CD-0.042A2-0.059B2-0.051C2-0.068D2,運用Design-Expert 軟件對上述實驗點的響應值進行方差分析。
由表7 可以看出,回歸模型P <0.01,F=11.41,提示模型具有高度差異性,同時該模型具有較高的相關系數(R2=0.9194),擬合度大于90%,且失擬值P >0.05,說明該模型能夠反映響應值的變化,誤差小,因此可用該回歸方程代替實驗真實點對實驗結果進行分析和預測。
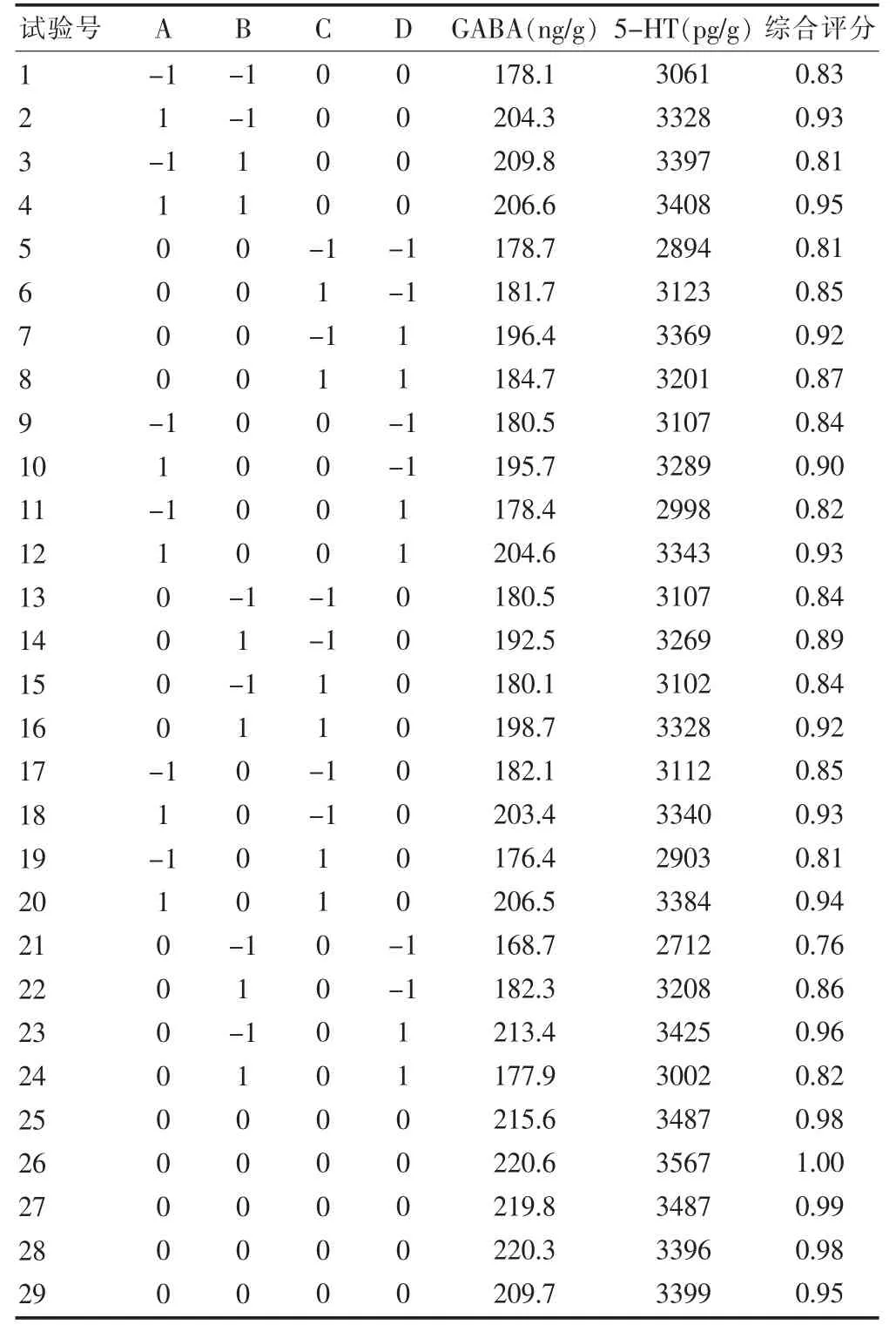
表6 四因素三水平中心組合實驗方案與結果
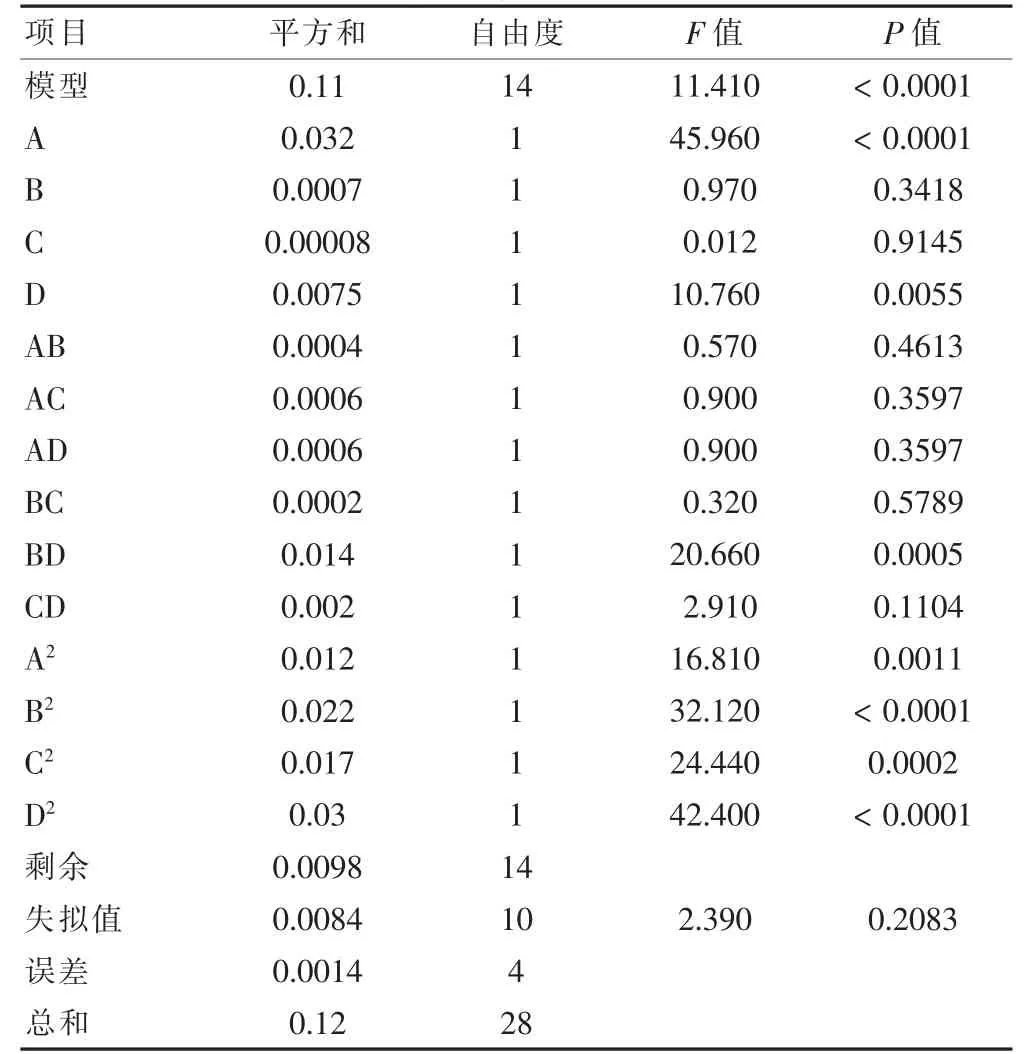
表7 方差分析
2.2.2 效應面優化分析
用Design-Expert 8.2.0 軟件對表6 實驗結果擬合分析,所得響應面等高線曲面圖,見圖1。曲面陡表明該因素對綜合評分影響顯著,曲面平緩則表明該因素對綜合評分影響不顯著。
由圖1 可以看出,A、B、C、D 四個因素對綜合評分的影響均成拋物線關系。分析各圖,從圖①可以看出,A 曲面較陡,B 曲面較平緩,說明人工胃液的用量對綜合評分的影響顯著,而提取時間的影響不顯著。同理,從圖②可以看出,A 對綜合評分影響顯著,C 影響不顯著;從圖③可以看出,A 對綜合評分影響顯著,D 影響較顯著;從圖④可以看出,B 影響不顯著,D 影響較顯著;從圖⑤可以看出,B 和D 二者的提取時間交互作用顯著,說明BD 項對綜合評分影響顯著;從圖⑥可以看出C 不顯著,D 較顯著。
綜上可知,影響半仿生提取的主要因素為A,其次為D,其中以B、D 交互作用最為顯著。
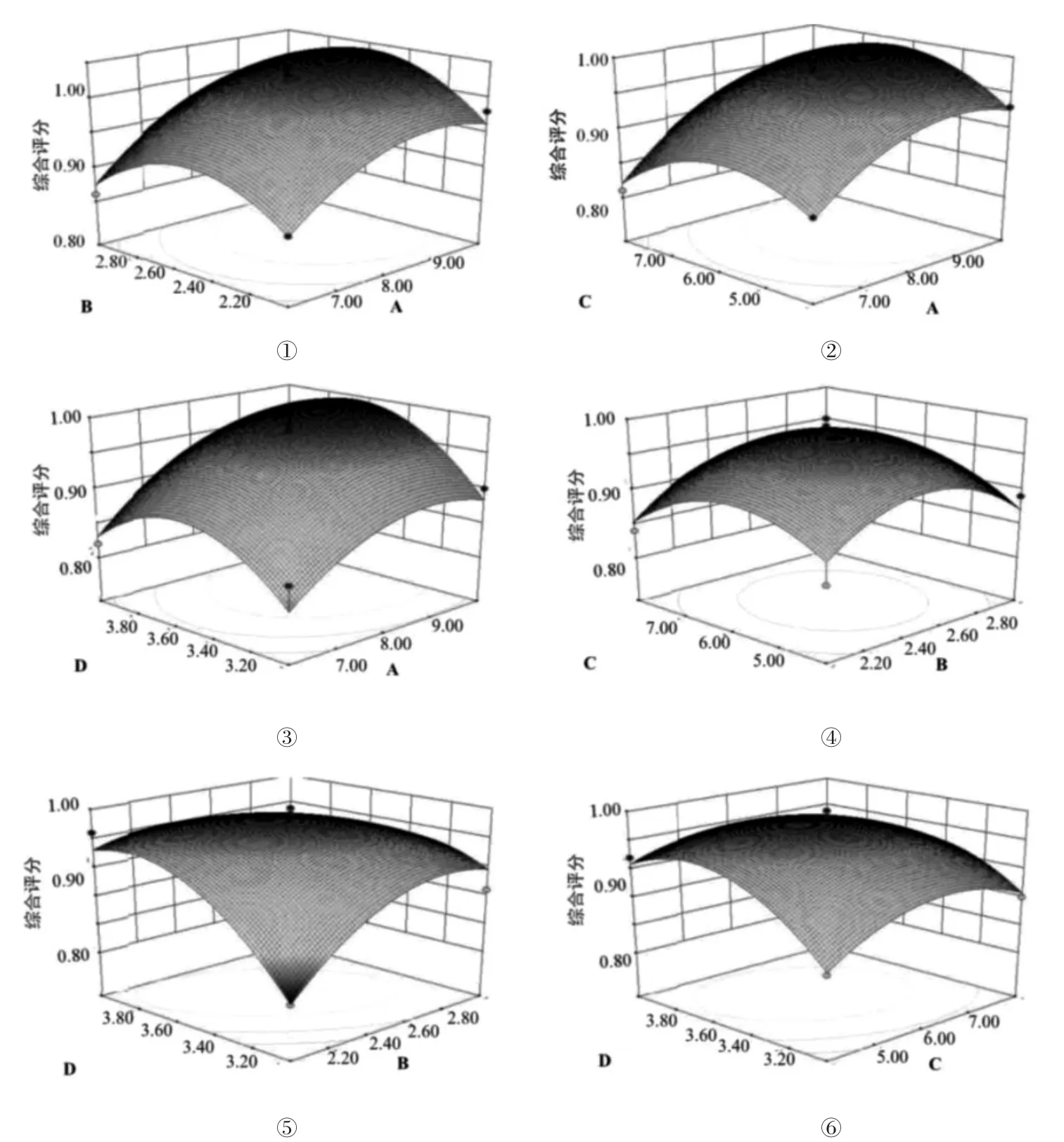
圖1 A、B、C、D 四因素等高線圖和響應面圖
2.2.3 提取工藝優化結果及驗證試驗
根據回歸模型分析可知,半仿生提取的最佳條件為:第1 次提取人工胃液用量9.45 倍、時間2.43 h;第2 次提取人工腸液用量6.02 倍、時間3.65 h。按照優化的處方劑量,結合實際操作情況,各因素值保留為整數,即第1 次提取人工胃液用量9.5 倍、時間2.5 h,第2 次提取人工腸液用量6.0 倍、時間3.6 h。在此條件下,按照中試規格要求,藥材用量采用處方量1000 倍進行3 次平行實驗,見表8。GABA 和5-HT 的含量的平均值分別為216.60 ng/g 和3508.11 pg/g,與理論值221.21 ng/g 和3533.38 pg/g 比較接近。說明該回歸方程與實際情況擬合較好,該最佳工藝切實可行,可操作性強。

表8 驗證試驗表
3 討論
中藥藥對配伍是基于中醫基礎理論將兩味藥合用,通過藥物間的復雜配伍作用,有機地組合而成。酸棗仁與五味子藥對配伍以酸棗仁為主,但最佳配伍比例并不確定,本實驗基于鎮靜催眠作用篩選酸棗仁-五味子的最佳配比。結果顯示,酸棗仁與五味子不同配比均能對小鼠起到一定的鎮靜催眠作用,其中以酸棗仁:五味子(15 g∶6 g)療效最好,12 g∶6 g 組、6 g∶6 g 組療效雖然相差無異,但6 g∶6 g 組耗費藥材少。綜合分析可知:15 g∶6 g 組配比雖然用量大,但療效最佳,6 g∶6 g 組雖然給藥量小但效果等同于12 g∶6 g組,不及15 g∶6 g 組,又因五味子每天最大給藥量上限為6 g,故最終確定最佳配比為15 g∶6 g。
Glu 能夠在相應合成酶谷氨酰胺的作用下轉變成Gln,屬于人體內少有的興奮性氨基酸;而GABA屬于抑制性氨基酸,部分鎮靜催眠藥物的發揮作用主要與加強GABA 功能有關[15-17]。同時,神經遞質5-HT及其代謝產物5-HIAA 兩者變化也可影響人體的睡眠[18-19],所以本研究除上述3 種物質外,也同時測定5-HT、5-HIAA 含量,以判斷酸棗仁-五味子不同配比的鎮靜催眠作用。
半仿生提取法是一種新的中藥提取技術,該法模擬胃腸道環境,采用接近于胃腸道PH 的酸性溶液和堿性溶液依次提取,提取簡便、不破壞有效成分、提取率高,能在一定程度上節約成本,較一般提取法的有效成分含量更高[20-22];而且經歷了模擬胃腸道環境的處理,生物活性有所增強,口服不存在胃腸道破壞情況。另外,酸棗仁五味子單獨提取時,采用半仿生提取法的鎮靜催眠效果明顯優于傳統提取法[23-25]。

