頭孢噻肟所致藥品不良反應文獻分析*
趙,張東梅,姜,宗黎瓊,郭 澄,張劍萍
(上海交通大學附屬第六人民醫院藥劑科,上海 200233)
頭孢菌素類為經典殺菌劑,作用機制為結合青霉素結合蛋白,抑制細菌細胞膜的細胞壁合成,破壞膜結構。第3 代頭孢菌素類及其復方制劑占臨床治療的主導地位[1]。頭孢噻肟屬第3 代頭孢菌素類,隨著臨床的廣泛應用,其引發的藥品不良反應(ADR)也較多。為此,將相關ADR 文獻進行統計分析,供臨床合理用藥參考。
1 資料與方法
以“頭孢噻肟”為檢索詞,檢索萬方數據庫1998 年至2019 年有關頭孢噻肟致ADR 的文獻資料,納入無重要信息缺失、可進行因果評價的病例報道,排除重復報道、超量用藥、藥物配伍不當或非病例報道。共得有效文獻144 篇、病例169 例。將患者的年齡、性別、原患疾病、給藥途徑、ADR 發生時間、預后等相關信息錄入Excel表格,并歸納分析。
2 結果
2.1 病例及ADR 基本情況
結果見表1 至表3。呼吸系統感染為主要原患疾病,居前三位的為肺炎(25 例,14.79% ),氣管炎、支氣管炎(24 例,14.20%),呼吸道感染、上呼吸道感染(22 例,13.02% );靜脈滴注(155 例,91.72% )為主要給藥途徑,其次為靜脈注射(13 例,7.69% )、皮下注射(1 例,0.59%)。
2.2 過敏史、預后與轉歸
56 例(33.14%)無過敏史;9 例(5.33% )有過敏史,其中6 例對青霉素過敏,3 例對其他頭孢菌素類過敏,含對多種藥物過敏者1 例;其余患者過敏史不詳。行皮膚過敏試驗(簡稱皮試)者 59 例(34.91% ),其中,頭孢菌素類皮試陰性42 例,含1 例青霉素皮試陽性;青霉素皮試陰性 13 例、陽性 2 例。15 例(8.88% )有頭孢菌素類用藥史,包括2 例有頭孢噻肟用藥史,5 例有青霉素用藥史;另有7 例(4.14%)有青霉素用藥史。經停藥并對癥治療后,164 例緩解或痊愈,其中132 例(80.49%)于 1 min 至 24 h 內緩解或痊愈,14 例(8.54% )于 3 d 內痊愈,其余 18 例(10.98% )均于 90 d 內痊愈。5 例(2.96% ,男 3 例、女 2 例)死亡,包括過敏性休克 4 例和急性喉頭水腫1 例;發生于用藥首日5 min 內及用藥次日各2 例,均于ADR 發生當日即死亡。
2.3 因果關系評價
依據國家藥品不良反應監測中心的ADR 報告表中有關ADR 分析的5 個問題,對收集匯總的病例進行關聯性評價。在169 例病例中,評價結果為“肯定有關”的有 10 例 (5.92% ),“很 可 能 有 關 ”的 有 155 例(91.72%),“可能有關”的有 4 例(2.37% )。
3 討論
3.1 ADR 發生的基本特點
由表1 至表3 可見,頭孢噻肟所致ADR 多見于11 歲以內患兒;發生時間以用藥后第1 天最多,尤其是用藥后30 min 內,發生于用藥5 min 內的有41 例,其中用藥后即刻發生的有10 例;靜脈滴注是主要用藥途徑。建議臨床對患者用藥前后的癥狀及體征進行觀察,尤其是靜脈滴注用藥患者,應適當調節其初始用藥的滴速;11 歲以內的少年兒童為重點關注人群,首次用藥前30 min為重點關注時段。
3.2 ADR 的臨床類型
過敏性休克:是頭孢噻肟所致ADR 的主要表現形式,也是抗菌藥物致藥源性死亡的首要原因[2]。本調查中 72 例過敏性休克患者中,男 38 例、女 34 例;25 例(34.72% )無過敏史,1 例(1.39% )有頭孢菌素類過敏史,5 例(6.94% )有青霉素過敏史,其中 2 例同時對至少1 種頭孢菌素類過敏;10 例(13.89%)有頭孢菌素類用藥史,5 例(6.94% )有青霉素用藥史;21 例頭孢菌素類皮試陰性,7 例青霉素皮試陰性;靜脈滴注(64 例,88.89%)是主要用藥途徑。60 例(83.33% )發生于用藥首日,其中,用藥 5,10 min 內發生的分別為 36 例(50.00% )、20 例(27.78% );其余病例均于用藥 6 d 內發生。經停藥并對癥治療后,于當日好轉或痊愈的67 例(93.06% ),其中 40 例(55.56% )為 120 min 內即好轉或痊愈;1 例于第 3 天痊愈。另有 4 例(5.56% )死亡。提示除有藥物過敏史的患者外,過敏性休克的重點關注人群還應包括無用藥史、無過敏史的首次靜脈滴注用藥患者;重點關注時段為用藥的前10 min。
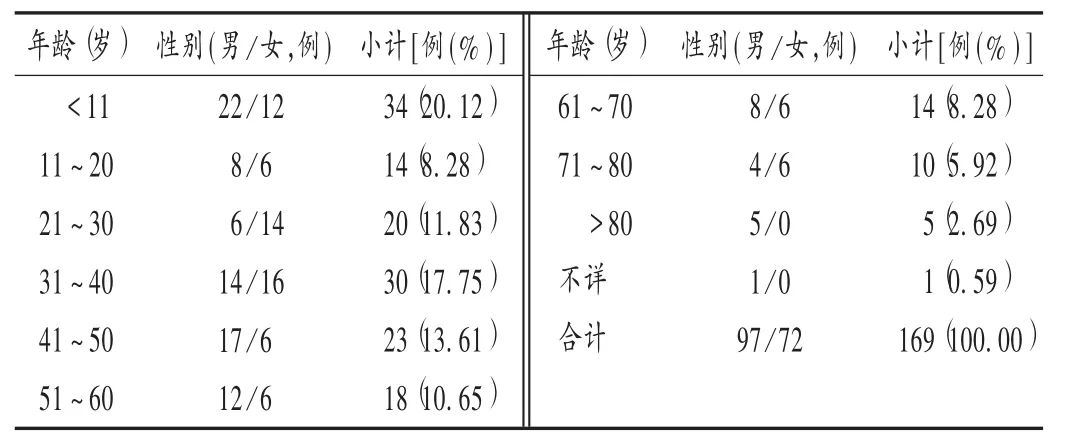
表1 ADR 患者性別與年齡分布(n =169)Tab.1 Distribution of the gender and age of patients with ADRs(n =169)
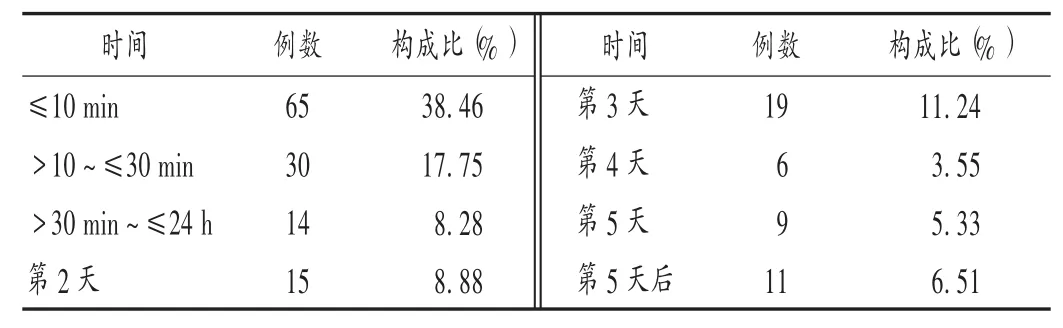
表 2 ADR 發生時間分布(n =169)Tab.2 Distribution of the onset time of ADRs(n = 169)
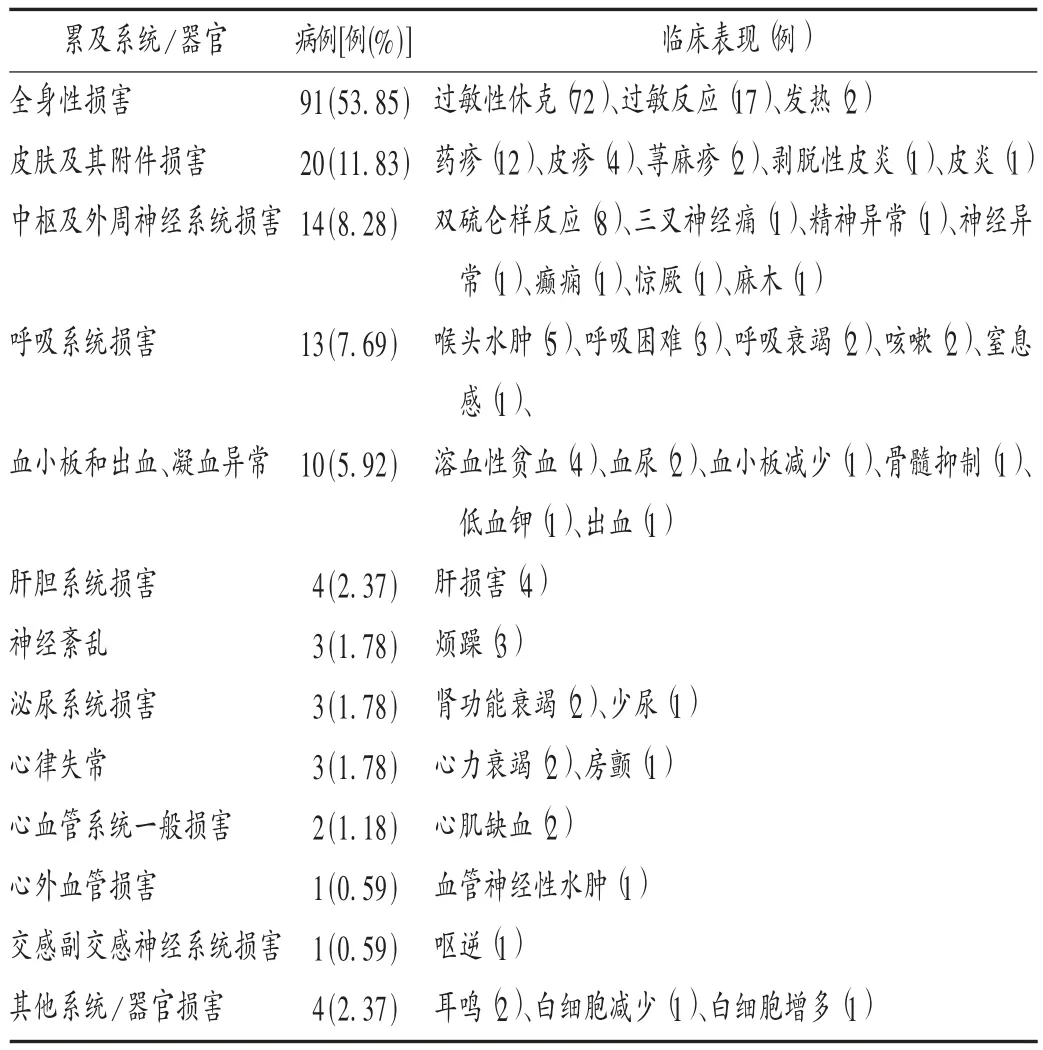
表 3 ADR 累及系統 /器官(n =169)Tab.3 Systems/organs involved in ADRs(n = 169)
血小板和出血、凝血異常:藥物引起的血液學改變約占全部藥源性疾病的10% ,而據世界衛生組織(WHO)藥物不良反應監測中心的估計,藥源性溶血性貧血(DHA)約占藥源性血液學反應的 10%[3]。頭孢菌素類在引起溶血性貧血的抗菌藥物中居首位[3]。本調查中,發生溶血性貧血的為靜脈滴注用藥的4 例患者(男、女各2 例),且其中3 例發生于用藥后的5 d 內;停藥并對癥治療后,均于1 個月內痊愈。藥源性免疫性貧血、藥物氧化性溶血性貧血、三重復合物學說,是DHA 發生的3 種可能機制[3]。免疫復合物型是頭孢菌素引起的溶血性貧血的可能機制。在反復使用頭孢菌素類藥物后,機體受刺激產生抗體(藥物依賴性),其與頭孢菌素(或其代謝產物)形成可與紅細胞膜上的特異性靶蛋白相結合的免疫復合物,激活補體,發生抗體抗原免疫反應,導致紅細胞破裂,引起溶血反應,常在血管內發生溶血[4-5]。提示若需長期使用頭孢菌素類藥物,應定期監測血常規、尿常規、凝血功能等指標。16 歲以下青少年兒童包括血液系統在內的各項機體功能尚未發育完全,是重點關注對象。
肝腎系統ADR:出現肝腎損害的有7 例(男6 例、女1 例),均發生于用藥后的5 d 內,經停藥并對癥支持治療后,于半個月內好轉或痊愈,未出現死亡病例。藥物引起腎臟ADR 主要是由于藥物的直接腎毒性(與藥物濃度及劑量相關)影響腎臟代謝過程或造成尿路梗阻所致[6]。頭孢菌素類藥物導致的腎毒性不表現為過敏性損傷,而是表現為藥物濃度過高導致的肝腎損害,近曲小管細胞是發生腎損傷的主要部位[7]。可能的因素有大多數頭孢菌素類藥物經腎排泄,抑制、干擾腎小管細胞酶活性,引起急性腎小管壞死而致血尿[5],而頭孢噻肟約有80%的給藥量經腎臟排泄;頭孢噻肟要求快速靜脈滴注,短時間內流經肝臟和腎臟的血流中血藥濃度較高,更易結晶,刺激或損害肝腎細胞。1% ~11% 的患者在使用注射用頭孢菌素類藥物后,其轉氨酶、堿性磷酸酶水平均會輕度升高,但停藥后大多數患者可自行恢復[7]。因此,頭孢菌素類藥物用藥前后有必要監測患者的肝腎功能,一旦發現異常,及時停藥是關鍵。
呼吸系統ADR:血管神經性水腫屬Ⅰ型變態反應,是由于血管擴張和體液外滲導致的真皮、結締組織或黏膜的水腫,發生于咽喉部的血管神經性水腫為喉頭水腫。喉頭水腫是呼吸系統ADR 的主要表現形式,本研究中共發現 5 例(38.46% ),其中男 4 例、女 1 例;均為靜脈滴注用藥,與周正東[8]的研究結果相符;頭孢菌素類皮試陰性4 例(含1 例青霉素皮試陽性者),青霉素皮試陰性1 例;均發生于用藥2 d 內,其中發生于用藥首日15 min 內的有3 例;除1 例于當日死亡外,其余均于當日痊愈。抗菌藥物是引起藥源性水腫最多的藥物(31.21% )[8-9],β - 內酰胺類藥物(以第 3 代頭孢菌素類居多)是主要藥物[8-10]。鑒于喉頭水腫會導致嚴重后果,對于靜脈滴注患者,若在用藥過程中或用藥后30 min出現呼吸窘迫及哮鳴音,臨床應注意鑒別是否為喉頭水腫所致。保持患者的呼吸道通暢、及時改善通氣是防治喉頭水腫的關鍵。
3.3 頭孢菌素類藥物的皮試
頭孢菌素類藥物為β-內酰胺酶藥物,其有共同的結構基礎,發生過敏反應的抗原決定簇結構主要和各自的側鏈結構有關,用某種頭孢菌素類藥物代替所有品種的皮試,易導致臨床誤判;青霉素的6 位側鏈和頭孢菌素類藥物的7 位側鏈是二者交叉過敏的基礎,二者側鏈結構的相似性,決定了交叉過敏反應發生的概率,用青霉素代替,不僅假陽性多,且陰性結果也不完全可靠[11];用同種頭孢菌素類皮試,鑒于不同廠家(尤其是進口的與國產的)的生產工藝的差異與質量控制的波動性,難以避免假陽性或假陰性結果。提示為保障醫療安全需進行皮試時,皮試液應以同廠家同批號的新鮮配制原藥為宜,以確保皮試結果的準確性。
3.4 合理用藥要點
建議臨床使用頭孢噻肟前,應嚴格把握使用指征,詳細詢問過敏史、用藥史;使用時注意觀察患者的體征變化;使用后,注意監測血常規、尿常規、凝血指標的變化,對于需長期使用者,應定期監測各項指標的變化。重點關注人群為青少年兒童(尤其是11 歲以下者)和靜脈用藥患者,重點關注首次用藥后的前30 min(過敏性休克為用藥后的前10 min),防止嚴重ADR 發生。

