多維突破元素知識 原創試題提升復習效率
湖南
1 高考背景
2019年6月19日國務院辦公廳發布的《國務院辦公廳關于新時代推進普通高中育人方式改革的指導意見》中關于深化考試命題改革中明確要求“創新試題形式,加強情境設計,注重聯系社會生活實際,增加綜合性、開放性、探究性試題”,2020年1月份教育部考試中心發布的《中國高考評價體系》和《中國高考評價體系說明》成為“后考綱”時代高考復習教學的重要參考文件。
元素化合物知識是高考題中較關鍵的部分,通常會滲透于理論與實驗,生活與生產等具體問題中,重點考查知識的應用能力。近五年全國卷工藝流程題與實驗題中主要載體元素見表1及表2。
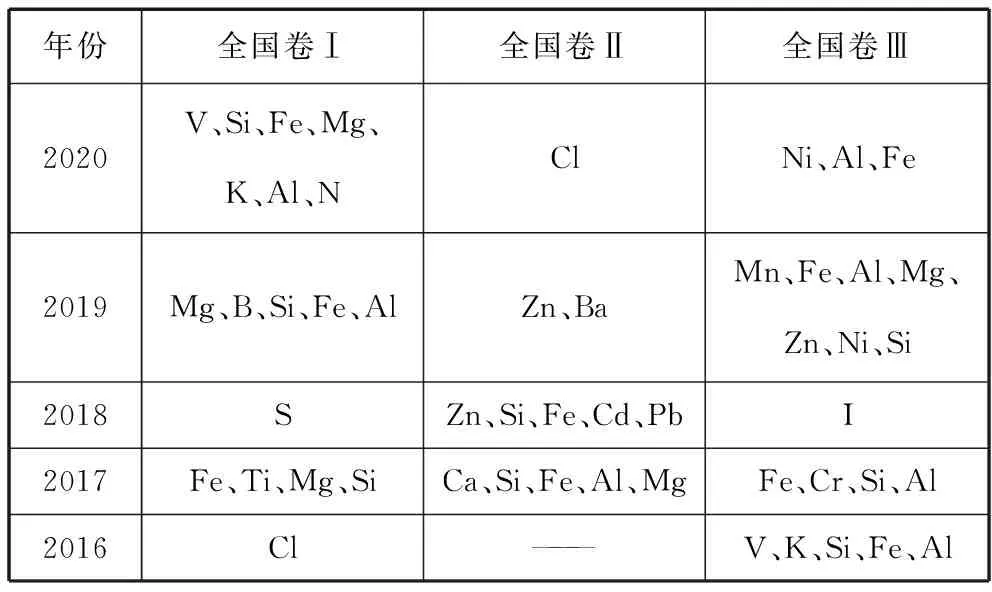
表1 近五年全國卷工藝流程題元素考查情況匯總

表2 近五年全國卷實驗題主要載體元素
2 利用原創試題突破元素化合物知識的復習
《普通高中化學課程標準(2017年版2020年修訂)》提出高中主要掌握的元素有Na、Fe、Cl、N、S,共5種。在復習過程中一般分為金屬及其化合物、非金屬及其化合物兩個模塊。在2020年新冠肺炎的影響下,全國卷化學非常注重難度調控,關注學生切身感受。故復習中進行試題命制時,需在保證試卷總體區分度的前提下,提高學生的感受度和學生答題的積極性,因此,筆者認為可從2個方面科學合理地調控試題難度,第一,試題選取的元素應貼近學生學習實際;第二,改變某類試題的考查方式,例如2020年全國卷Ⅱ36題對同分異構體的考查,由原來的寫出同分異構體數目改為以選擇題的形式呈現;再比如,計算題可只要求給出計算式。
2.1 創“填空題”夯實元素基礎
教材是學生突破高考試題的基礎,是思維的來源,如今高考題越發新穎的原因就是希望改變“靠刷題就能得高分”的現狀,故教師們需要采用“授之以漁”的方式通過創設新穎的試題夯實基礎,同時為進階學習提供契機。
筆者以硫及其化合物為例,以提高學生能力為目的,創設了如下題目。
【硫及其重要化合物】填空題
1.硫元素在周期表中的位置:________。用硫粉和亞硫酸鈉反應制Na2S2O3時,一般會在溶液中加入乙醇的目的是:。
2.寫出硫單質分別與Fe、Cu單質反應方程式:
______________;____________________。
3.向硫代硫酸鈉溶液滴入稀硫酸,有淡黃色沉淀產生,請寫出相關離子方程式:________________________。硫代硫酸鈉可用于吸收Cl2,寫出相應的離子方程式:____________________。已知:NaHSO3過飽和溶液脫水結晶得到焦亞硫酸鈉(Na2S2O5)固體,寫出相應的化學方程式:____________________,葡萄酒中常需要加入適量的焦亞硫酸鈉(Na2S2O5),目的是____________________,可用碘標準溶液滴定,確定是否超標,滴定原理的離子方程式為____________________。
4.碳單質與濃硫酸加熱反應的化學方程式:
________________,硫單質與濃硫酸加熱反應的化學方程式:____________________,體現了濃硫酸具有________性。濃硫酸能否干燥H2S、SO2氣體________,若不能,請用化學方程式解釋原因。
銅單質與濃硫酸加熱反應的化學方程式:
,
體現了濃硫酸具有________性。能否使用pH試紙測濃硫酸的pH________。
5.在水溶液中,Ag2SO4與單質S作用,沉淀變為Ag2S,分離后,向所得溶液中加碘水不褪色。則Ag2SO4與單質S作用的離子方程式為________________。在酸化的KI溶液中通入SO2,觀察到溶液出現淡黃色沉淀且溶液顯棕黃色,寫出相應反應的離子方程式:________________,繼續通SO2,溶液變為無色,寫出相應反應的離子方程式:________________。總反應方程式為________________,說明KI在反應中的作用________。
6.已知I2易溶于KI溶液是由于能夠反應生成一定量的KI3,寫出該反應的離子方程式:____________________;單質S可溶于Na2S溶液,黃色固體消失得到Na2S2溶液。向所得溶液中加入稀鹽酸,溶液中產生淡黃色沉淀,寫出整個過程發生反應的離子方程式:____________________。
通過這樣的練習,學生既能夯實基礎,同時也提升了學習能力,比如其中一些陌生情境的創設就凸顯了對學生學習能力的考查。
那么,該如何創編這樣的填空題呢?
1.基于教材和教輔材料梳理命制題目的主干部分,并有所涉及部分相關的化學反應理論,可側重實驗和工藝流程的基礎知識。
2.合理設空,注重前后的邏輯關系,不可“一空到底”,例如在考查物質性質時,可先要求學生書寫方程式,然后再對其性質設問,這樣可提高學生感受度,起到循序漸進的作用。
3.多關注拓展性的元素知識,巧妙設置已知信息,例如以上填空題中的5題,從而提高學生獲取信息并解決問題的能力。
在創設過程中,應摒棄“死記硬背”的方式,注重發展學生的思維方式。
2.2 創“流程題”助力元素應用
2.2.1 探索高考命題規律 確定試題命制方向
表3為近五年全國卷工藝流程題的考查內容及頻次。

表3 近五年全國卷高考試題工藝流程題的設問方向及頻次
2.2.2 以科技論文或專利為工藝流程題的主體素材
筆者在命制工藝流程題時,首先預設了該題需要考查的考點,選取素材方向。此類試題主要有兩種形式,即“產品包含的元素是陌生的,雜質包含的元素是熟悉的”和“產品、雜質包含的元素均是熟悉的”,大多數題中涉及的原料為固體礦物質,由于地殼中含量最多的前四位元素為O、Si、Al、Fe,故常見雜質含有的非氧元素為Si、Al、Fe,因此在命制過程中“產品元素陌生,雜質元素熟悉”是該題的主流形式。
1.選擇鋰離子電池的正極材料為素材。鋰離子電池在新能源發展中具有較大的潛力,因而對所用材料的合成研究也非常之多,故筆者初步確定從正極材料角度進行文獻篩選。
2.選擇科研論文,在百度學術或知網上進行查找,筆者最終確定以鐘燕萍的《以廢棄二次電池為原料制備α-Ni(OH)2正極材料的研究》為參考資料進行試題設計。
3.預設考查角度為化合價的計算、反應方程式的書寫、原理的分析和反應條件的控制等,通過化合價、方程式書寫等基礎內容考查學生的必備知識,通過原理的分析、反應條件的控制等來考查學生的信息處理、分析、整合等關鍵能力,同時設問均取材于真實的科技論文,具有較強的科學依據。
4.由于該文獻篇幅較大,筆者選擇了文中主要的研究方式——濕法處理工藝流程,該過程較其他方式而言降低了復雜性,原料的選取也突出了綠色化學的要求,符合高考命題的特點。在具體命制過程中需要注重文獻的科學性及設問的簡單化,如由于廢舊二次電池原料過于復雜,酸浸后的成分采用了直接給出離子種類的方式,同時對稀土復鹽進行了有效“屏蔽”,減少了學生的困惑。
根據以上過程最終命題成文如下:
LiNiO2是一種前景極好的鋰離子電池正極材料。回答下列問題:
已知:LiNiO2在850℃左右開始分解
(1)LiNiO2中Ni的化合價為________,利用電池級的Ni(OH)2與LiOH,在空氣氣氛中,700~800℃煅燒可制得LiNiO2。寫出該過程的化學方程式
,
加熱溫度不宜過高的原因是
,
可用LiNO3代替LiOH,存在的缺點是。
(2)以廢棄二次電池為原料回收利用合成電池級Ni(OH)2的工藝如圖1所示:
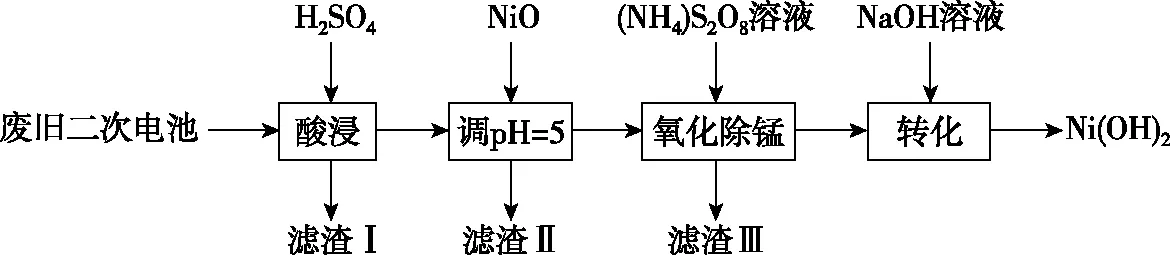
圖1
已知:酸浸后濾液中含有Ni2+、Al3+、Fe3+、Mn2+;
Ksp[Fe(OH)3]=4.0×10-38,Ksp[Al(OH)3]=1.0×10-33,Ksp[Ni(OH)2]=1.6×10-14;
①“濾渣Ⅱ”為________。
②“氧化除錳”即將錳元素最終轉化為MnO2而除去,反應歷程如下:

ⅱ.
(用離子方程式表示)。
③“轉化”后,產品需經過洗滌、烘干,則檢驗Ni(OH)2是否洗滌干凈的實驗操作是。
④“調pH=5”時,已知溶液中Ni2+濃度為2 mol·L-1,則“濾渣Ⅱ”中是否存在Ni(OH)2沉淀?
(列式計算)。


③取最后一次洗滌液,先加稀鹽酸酸化,再滴加BaCl2溶液,若無白色沉淀產生,則洗滌干凈
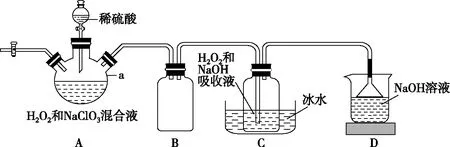
④pH=5,濾液中c(OH-)=10-9mol·L-1,Qc=c2(OH-)·c(Ni2+)=(10-9)2×2=2×10-18 【說明】筆者認為原創工藝題時要注意以下幾點: 1.明確該題的產物及原料; 2.多方查找文獻,以最新研究為主,深入研究其中素材,將其簡化、試題化,同時可以綜合多篇文獻,對除雜、分離提純等階段進行基于學生學情的綜合替換或拼接; 3.反復核實,保證不出現科學性或知識性差錯; 4.注重對學生信息處理、整合、應用能力的考查設問。 2.3.1 明晰實驗主體——氣體或溶液 近年高考試題逐步呈現出以溶液實驗為主的趨勢,這比較符合教材的真實情況。教材實驗大多以試管實驗為主,有氣體參與的綜合性實驗較少,在創新大賽中,實驗往往以“微、精、簡”為主流。故在考查過程中,溶液類實驗更能全面體現高中化學必備知識與關鍵能力。 2.3.2 基于真實情境命制實驗試題 實驗題與工藝流程題實際上均有實驗操作,前者側重元素化合物知識在實驗中的應用,以實驗基本操作、原理、實驗現象、實驗條件等為主要考查方向,后者更側重元素化合物知識本身,如方程式書寫、成分分析等。二者有較多相似點,這兩種題型是元素化合物知識復習的重要載體。前文已經對工藝流程題的命制作了分析,下面來講講實驗題。 首先要確定命制實驗題的類型:制備類、性質探究類、定量計算類、原理探究類,其次是素材的選取,通過搜索多個科研論文確定目標,最后再根據考查內容設問。 筆者確定題目類型為制備類,以NaClO2的合成為目標,篩選文獻,最終選擇專利——《亞氯酸鈉的制備方法》為主要參考資料。 最終命制試題如下: 亞氯酸鈉(NaClO2)是一種高效含氯消毒劑和漂白劑,主要用于自來水、污水等水環境的殺菌消毒,也常用作紙漿、砂糖、油脂的漂白劑。圖2為目前生產亞氯酸鈉的流程之一(夾持裝置省略),所得NaClO2具有純度高的優點。 圖2 已知:NaClO2飽和溶液在低于38℃時會析出NaClO2·3H2O,高于38℃時析出NaClO2,高于60℃時NaClO2分解成NaClO3和 NaCl。 試回答下列問題: (1)儀器a的名稱為________。 (2)裝置A用來制取ClO2,發生反應的離子方程式為____________________。 圖3 (4)C裝置采用“冰水浴”的目的是。 (5)充分反應后,從產品溶液中獲取NaClO2晶體的操作是:55℃恒溫減壓蒸發結晶、趁熱過濾、________℃水洗滌、干燥。 (本題部分內容已應用于教學考試優師計劃研發項目) 【說明】本題為筆者命制的2020年常德市高考模擬試題中的一道實驗題。為了給試題創設亮點,命制過程中對NaClO2的生成條件進行了文獻查詢,最終設計了(3),原文獻包含兩個圖像,但筆者有意圖創設雙縱坐標圖像,效仿了與 2020年全國卷Ⅰ13題。在圖像設置中要注意降低學生形成錯誤思維可能性,本題的設問是選擇合適的實驗條件,對于學生來講有一定的難度,原因在于不少學生沒有考慮生產成本,故此問可幫助學生加深綠色化學的理念。因而還有一種設問方式即為何選用c(NaOH)=0.8 mol·L-1最為合適?筆者又在第(6)問涉及了文獻中含量測定時常出現的角色——滴定度,設計了相關問題,較好的考查了學生分析、解決問題和整合信息的能力。因此,本題具備了良好的區分度。 通過關注與學科相關的新聞,關注與學科相關網站,查找教材、雜志、報刊等角度挖掘新材料,具體可以有兩種形式,第一,以現有習題的目標物質為目標,搜索相關科技文獻,重新組織題干與設問;第二,以目前少見的物質合成為目標編制新題,但要確保試題的嚴謹性與真實性。 注重試題設問角度,通過拼接、模仿、套用、反轉、變形等手段進行再創造,但要注意保證試題不偏、不怪。命題應以“改編為主,創新為輔”的形式,逐步向“創新為主、改編為輔”的形式轉變。2.3 創“實驗題”助力元素探究
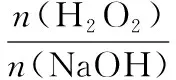



3 命制優秀試題的方向
3.1 保證試題命制的材料新
3.2 注重試題設問角度的再創造
4 結語


