涂層下金屬管道縫隙腐蝕瞬態的數值模擬
白浩然,饒永超,王樹立,孫 琪,李立軍,賈 茹
(1. 常州大學 石油工程學院,常州 213164; 2. 榆林學院 化學與化工學院,榆林 719000)
現階段,石油與天然氣主要通過埋地管道進行長距離輸送,管道腐蝕是威脅其安全運行的最重大因素之一。對于埋地金屬管道,國內外主要采用涂層和陰極保護技術二者結合的方法來防止其腐蝕[1-2]。然而在管道安裝過程中,由于管道補口噴涂和不可避免的機械損傷等可能會使管道涂層出現缺陷,在埋地環境中缺陷處受到侵蝕,隨著時間的推移缺陷處的涂層可能失效并在管道表面形成狹窄的縫隙[3]。腐蝕介質(氣體、電解質、含硫微生物等)進入縫隙可能引發縫隙腐蝕,進一步加快管道腐蝕,縮短管道壽命。目前,世界公認最有效的管道防腐蝕方法是在管道表面施加陰極保護,但是在涂層下,縫隙內腐蝕過程主要取決于離子的傳質和電化學反應。由于縫隙寬度過于狹窄,現有的測量探頭或電極無法深入縫隙內[4],現階段關于縫隙內電位分布和傳質過程的理論研究仍然有限,縫隙內陰極保護作用機制仍是一個有爭議的問題[5]。通過試驗了解縫隙腐蝕以及陰極保護的有效性是遠遠不夠的。數值模擬技術日益完善,可以高效對數據進行分析,大大提高了縫隙腐蝕的理論研究效率。
現如今國內外學者對縫隙腐蝕的數學模型已經進行了大量的研究[6-9]。例如, KENNELL等[10]提出了一種結合臨界縫隙解理論(CCST)和IR降理論的一維穩態縫隙腐蝕模型,認為物質的傳質和電位在縫隙內外都會下降,陰極反應很可能發生在縫隙口處。XIAO等[11]建立了定量相位模型研究鹽水中鐵的縫隙腐蝕,考慮了六種離子和一些相關的化學反應,分析了不同電位下與腐蝕相關的理化性質。但是相當多的研究只針對穩態下縫隙腐蝕的形成機理和化學狀態,且側重于沒有陰極保護條件下縫隙腐蝕的潛伏期及其發展過程,而對瞬態條件下縫隙腐蝕過程的研究還不夠充分,且有無陰極保護條件下,縫隙腐蝕的電化學過程完全不同。SONG[12]針對可變縫隙(即間隙隨著縫口距離變化而變化)開發了一種預測管道化學性質的數學模型,在有(無)陰極保護兩種條件下,探究了管道表面縫隙中化學反應和腐蝕速率的變化。CHEN等[13]和WANG等[14]開發了在陰極保護條件下的縫隙腐蝕模型,以研究瞬態的電化學過程,但兩種模型都只考慮了x方向的數值變化。近些年來新開發的瞬態模型,大部分都只考慮一個維度(即忽略寬度對電位和化學參數的影響)。因此,針對有陰極保護的縫隙腐蝕,研究其瞬態的化學狀態,同時盡可能在空間維度上貼近實際,分析其局部溶液環境中的電化學過程,得到更加準確的模擬結果,對研究陰極保護機理以及防止涂層下的金屬腐蝕十分重要。
本工作主要在前人工作基礎上,建立了一個二維瞬態模型,研究涂層下施加陰極保護的縫隙腐蝕,綜合考慮了縫隙內離子傳質、化學反應和水電離等問題,利用有限元軟件模擬涂層下縫內環境中化學和電化學的瞬時狀態,并根據模擬結果分析縫隙腐蝕的陰極保護機理,為研究縫內腐蝕過程提供了理論依據,并將模擬結果與試驗結果進行對比,以期確定合理的陰極保護電位,優化管道的防護措施,從而減輕管道腐蝕,節約成本,防止在使用過程中管道發生災難性事故。
1 理論研究
1.1 幾何模型
由于縫隙腐蝕是一個復雜的電化學過程,在模擬過程中會進行近似假設和簡化,如圖1所示。該模型在縫口處添加一個電解質域,避免模擬時電解質的電位邊界與電極表面相連接,從而防止電位梯度奇點導致的迭代步數收斂。縫口坐標(0,0)為起點,縫寬(δ)1 mm,縫隙深度(L)200 mm。

圖1 縫隙腐蝕幾何模型Fig. 1 Geometry model of crevice corrosion
1.2 模型條件
模擬電解質溶液為經過土壤地下水稀釋的Na2SO4溶液,根據無限稀釋理論的基本假設,模型中電解質域內為無限體積的Na2SO4溶液,且溶液中的化學物質含量是恒定不變的。縫隙內外溶液被空氣飽和,在施加陰極保護電流的情況下,氧氣會從縫口進入縫隙內部且被不斷消耗。除此之外,為簡化模型,還進行了如下假設:
(1) 在施加陰極保護電流的情況下,縫隙內陽極溶解反應受到抑制,縫內主要反應為氧氣還原反應,且縫隙內溶液變為堿性溶液,反應式如下:

(1)
(2) 縫內溶液處于停滯狀態,并且由于縫隙寬度過于狹窄,化學物質對流忽略不計,在縫隙內化學物質通過擴散和電遷移進行傳質;
(3) 傳質過程考慮四種化學物質:OH-、SO42-、Na+、O2;
(4) 在初始狀態下縫隙溶液中各化學物質的濃度沿x和y方向均勻分布,反應過程中縫隙寬度不變,且不考慮沉淀和管道鋼表面的腐蝕形變;
(5) 化學物質傳質過程滿足紐曼電中性原則[15]:
∑zici=0
(2)
式中:i是溶液中的化學物質;ci是濃度(mol·L);zi是電荷數;
(6) 模型考慮到水的電離平衡:

c(OH-)c(H+)=Kw
(3)
-lgKw=14.94-0.042 09(T-273.15)+
0.000 171 8(T-273.15)2
(4)
Kw=10-lgKw
(5)
式中:Kw為水的離子積常數;T為溫度。
(7) 金屬表面的電雙層厚度足夠小,可忽略不計。
1.3 反應方程式
1.3.1 傳質方程
在縫隙內,化學物質的運輸受到三種機制控制:離子電遷移、擴散和對流。化學物質i的質量流量(Ni)由式(6)給出[15]:

(6)
式中:Ni是i的質量流量(mol·cm-2·s-1);ui是遷移率(m·V-1);F是法拉第常數(96 500 C·mol-1);φ是縫隙內鋼的局部電位(V);Di是擴散系數(cm2·s-1);v是對流速度(m·s-1)。
因此,在等式的右側存在第一遷移項,第二擴散項和第三對流項。
假設模型為靜態,對流速度為零。因此,縫隙內的質量流量可寫成如下形式[15]:

(7)
在以往的研究中,一般只考慮沿縫隙x軸方向的反應[16-18]。在本模型中,考慮了沿x和y軸的二維傳質和堆積效應。如圖2所示,當離子以恒定速度從x1移動到x2、從y1移動到y2時,其凈流量為[19]:
ρividydz|x+dx-ρividydz|x+ρividxdz|y+dy-
ρividxdz|y=nidydz|x+dx-nidydz|x+
nidxdz|y+dy-nidxdz|y
(8)
式中:ρi是密度(kg·m-3);ni是質量速度(kg·m-2·s-1)。

圖2 二維傳質積累示意圖Fig. 2 Diagram of 2D mass transfer accumulation


(9)
式(9)可以用摩爾表達,可得式(10):

(10)
式中:Nim為m(m=x,y)方向上i的摩爾通量(mol·m-2·s-1)。
由于以上所述可以忽略對流效應,根據能斯特-普朗克方程,離子的質量流量Ni為:

(11)
縫內質量守恒方程可以表示為[13]:

(12)
式中:t為時間(s);Ri為化學反應中i產生或者消耗的速率,主要為氧氣的還原反應,有:

(13)
式中:JO是氧氣交換電流密度(A·cm-2);n是電極反應的化學計量系數。
因此式(12)可以如下表示:

(14)
1.3.2 電化學動力學方程
縫隙中氧還原由電化學控制擴散[13]:

(15)

因此式(12)、(13)可以寫成:

(16)
1.4 初始條件與邊界條件
1.4.1 邊界條件
根據以往學者的研究,在縫隙口處所有化學成分是恒定且不隨時間變化的,而應用的陰保電位可以作為固定值給出[20]。

(i=O2,OH-,SO42-,Na+,0≤x≤L,0≤y≤δ)
(17)
在x=0處,所有化學物質的濃度與本體溶液化學物質的濃度相同,并且電勢與施加的陰極保護電勢(Ecp)相同:

(18)
在x=L處,因為沒有物質穿過邊界邊緣,縫隙的末端和所有物質的通量均為零:
x=L,ci=0,E=0
(19)
1.4.2 初始條件
根據矩形二維縫隙,結合以往研究得到陰極保護下縫隙腐蝕的數學模型,以1.2節所敘述的模型條件和電解質的理化性質為基礎,同時利用PARSTAT 2273電化學工作站測定極化曲線,擬合曲線獲得X70管線鋼的陰極塔菲爾斜率以及交換電流密度,如圖3所示。本體溶液為0.01 mol·L-1的Na2SO4溶液。基于無限稀釋定律,縫隙外的本體溶液含量恒定且體積無限大。pH受陰極電流和本體溶液的影響。表1為初始條件。

圖3 X70管線在土壤中的極化曲線Fig. 3 Polarization curve of X70 pipeline in soil

表1 初始條件Tab. 1 Initial conditions
1.5 數值處理
式(12)、(14)是一組非線性的二階偏微分方程,需要相互關聯[21]。然而在方程中,ci和E相互耦合,不可能有解析解,但是可以得到數值解。所以數值模擬技術可以解決此類問題,有限差分法(FDM)因其剖分簡單、編程計算方便,通常用于求解具有數值解的偏微分方程。首先,將方程和初始邊界條件做無量綱化處理;其次,剖分網格、劃分時間差量;最后,通過數值迭代求解方程[13]。方程由有限元軟件Comsol求解,Comsol對模型幾何體的網格劃分靈活,由于縫隙口附近電位梯度和濃度梯度很大并且傳質效應顯著,所以網格尺寸需要足夠小,以獲得準確的模擬結果。同時考慮水的自電離效應,選用水基電中性環境防止縫口處電位梯度奇點導致迭代步數收斂,將本體溶液進行區域化,縫隙外電解質的電位邊界與管體表面氧化還原反應邊界不接觸。
2 結果與討論
2.1 縫內電位分布
由圖4可見,縫口處的電位和陰極保護電位大致相同,均為-1 V,隨著時間的推移,延縫隙每個點的電位均向正方向移動。同一時間點下,縫隙深處的電位要高于縫口處的。100 h后,縫隙最深處的電位最值為-0.79 V,低于埋地管道最低保護電位-0.85 V。根據模擬情況分析,在100 h內縫口處可以完全被陰極保護電流覆蓋,隨著縫隙深度的增加和時間的推移,陰極電流逐漸向縫內流入,由于縫隙的特殊性和溶液的IR降(存在于管道和電解質電位測試過程中的電壓降)下降,陰極電流無法到達縫隙最深處。縫隙內部和外部的電位梯度隨著時間的延長逐漸減小。從模擬結果來看,縫隙深度超過約150 mm后,陰極保護電流將無法生效,縫隙內部的電場呈陰性,因此陰離子(SO42-)遷移出縫隙,縫口處的電位梯度比縫內的高,且陰離子遷移率遠高于縫內的。

圖4 電位與縫隙深度隨時間的變化Fig. 4 Variation of potential and crevice depth with time
2.2 縫內溶液pH
溶液pH受cOH-的影響,OH-在縫隙內的運動方式主要為擴散和電遷移,這受到縫隙形狀和極化電流的制約[22]。其擴散的主要形式是從縫內向縫口部分擴散,電遷移速率反應為電位梯度的大小,電位梯度高,OH-的遷移速率越高[23]。pH與cOH-的關系式如下:
pH=14+lg(cOH-)
(20)
如圖5和圖6所示,縫隙中每個點的pH隨著時間的延長而增加,在施加極化電流后的5 h之內,溶液的pH迅速從6.8升高到10以上;隨著時間的繼續延長,溶液pH逐漸穩定。溶液pH隨縫隙深度的增加而升高,約100 h后其pH穩定在12左右,在距離縫口約15 mm處溶液pH出現峰值。

圖5 至縫隙口不同距離處溶液pH隨時間的變化Fig. 5 Variation of solution pH with time at different distances to the crevice mouth

圖6 不同時間下溶液pH隨縫隙深度的變化Fig. 6 Variation of solution pH with crevice depth at different times
從以往的研究結果來看,由于縫口處離子的電遷移和擴散效應方向相同,縫口處的濃度梯度和電位梯度比縫內的要強很多,陰離子要用更慢的速度達到穩定值。而縫內溶液中離子的擴散和電遷移方向相反,縫隙越深濃度梯度和電位梯度越小,溶液pH可以達到更高[20]。由圖6可知,由于縫口處發生還原反應,氧氣濃度降低,OH-濃度迅速升高,而縫隙內過于陜窄,傳質效應在縫內受限,所以縫隙口附近的溶液pH比縫隙內的變化更快,故縫隙內溶液pH會更快達到穩定值而不再變化。
2.3 溶解氧濃度分析
縫內溶液pH主要受溶解氧(DO)的影響,縫隙內的氧氣主要被鋼表面發生的還原反應消耗。在模擬過程中,氧氣的還原反應是影響腐蝕速率的最重要因素,氧氣還原速率直接影響金屬的腐蝕速率,如圖7所示。
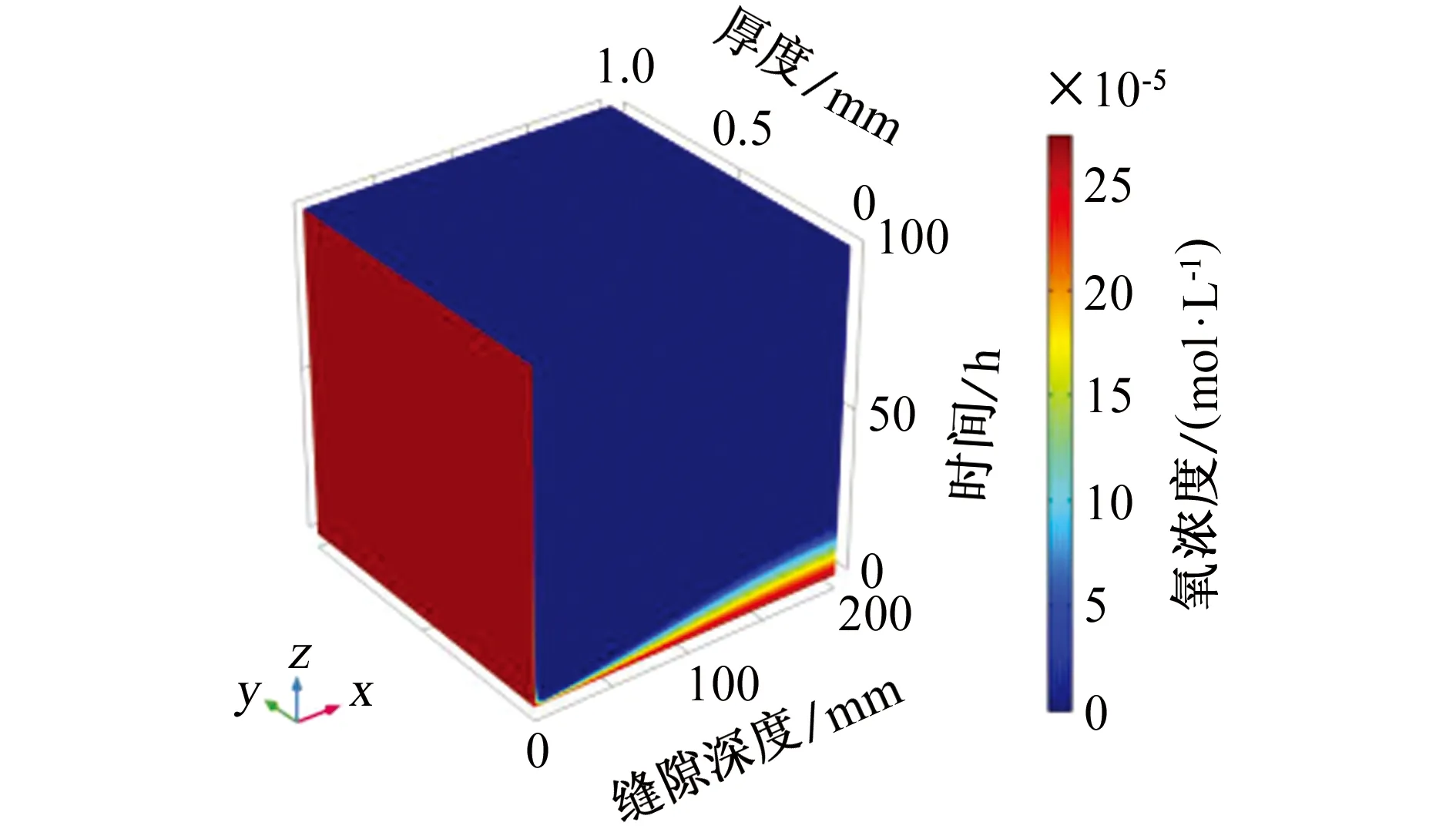
圖7 縫內溶解氧濃度隨時間和深度的變化Fig. 7 Variation of dissolved oxygen concentration in the crevice with time and depth
由圖7可以看出,在縫口處溶解氧濃度沒有發生變化,這是因為外部溶液為無限稀釋溶液,氧氣可以從外部溶液中不斷得到補充。在縫隙中由于氧氣被還原反應消耗,縫口處的氧氣在較短時間內被消耗,縫內溶液中溶解氧的消耗速度遠大于氧氣擴散的補充速度,溶解氧濃度隨著時間的推移而急劇下降。這是陰極保護效應開始時溶解氧濃度分布的一個典型現象。隨著縫隙深度的增加,縫內溶解氧消耗的速度逐漸變緩,這是由于只有少量的氧氣擴散到縫隙深處,并且縫隙深處還原反應速率比較低,當溶解氧消耗殆盡時,外部氧氣無法及時擴散到縫隙深處,這和以往的試驗研究結果相同。
2.4 電化學影響下的縫內離子濃度
由于縫隙內只存在氧氣的還原反應,并且產生OH-,溶液中的陰離子和陽離子會發生遷移以保持電中性原則。如圖8所示,可以更直觀地展現出金屬陽離子在溶液中的濃度變化情況。模擬結果表明,在距縫口約30 mm處Na+濃度達到峰值,約為外部溶液濃度的6.6倍,隨著縫隙深度的增加,Na+濃度急劇降低,在縫隙最深處Na+濃度的最小值和縫隙外部的保持一致。縫隙深處由于縫隙過于狹窄,Na+的擴散速率急劇降低,因此無法向縫內傳質,Na+的遷移導致陰極電流無法到達縫隙深處,影響了陰極保護的效果。

圖8 縫內Na+濃度與初始條件下Na+濃度的比值隨時間和縫隙深度的變化Fig. 8 Variation of the ratio of Na+ concentration in crevice to Na+ concentration under initial condition with time and crevice depth
根據電中性條件的假設,隨著縫隙內OH-濃度的增加,SO42-應向縫隙外部遷移,從圖9中可以看出,縫隙深度為0~25 mm,SO42-濃度比下降到0.3以下,最低值為0.12。可見陰離子濃度受傳質效應控制,縫隙口的電位梯度大,并且縫口與縫隙外部溶液中離子的擴散傳質受縫隙形狀影響較小,所以SO42-濃度迅速下降。在縫隙深處由于受到環境限制,SO42-濃度變化較慢。

圖9 縫內SO42-濃度與初始條件下SO42-濃度的比值(簡稱濃度比)隨時間和縫隙深度的變化Fig. 9 Variation of the ratio of SO42- concentration in crevice to SO42- concentration under initial condition with time and crevice depth
根據以往的模擬和試驗結果,由于溶液保持電中性,Na+向縫隙內部遷移,同時向縫隙外部擴散,Na+濃度與OH-濃度近似相等[24-25],這與本模型的模擬結果基本一致。
2.5 溶液電導率的影響
模型中電導率(σ)可以用如下方程表示[15,26]:

(21)
從上式中了解到,溶液的電導率與陰陽離子濃度密切相關,從圖10中可以直觀地看出縫內溶液電導率的變化,縫隙中電導率整體呈現上升趨勢,且隨著時間的增加而增加、隨深度的增加而減小,這與WANG等[14,27]的試驗結果相一致。根據前面章節的數據分析,由于縫隙內發生了氧氣的還原反應,造成了OH-濃度的升高,為了保持縫內溶液的電中性,陽離子(Na+)向縫內遷移,陰離子(SO42-)向縫外擴散,因此在縫口處的離子傳質運動劇烈,造成電解質溶液電導率大大增加,最大值約為本體溶液的4.2倍。但是縫隙底部的電位梯度和電流密度遠遠小于縫隙口附近的,所以電導率雖然因離子的傳質而增加但是遠沒有縫口附近電導率增加的快。與此同時,由于受到縫隙形狀和電位梯度的限制,Na+和SO42-只能在距縫口大約100 mm有限距離內進行傳質運動。綜上分析可知,電解質電導率的模擬結果與前幾節得到的結果一致。

圖10 溶液電導率與初始條件下溶液電導率的比值隨縫隙深度和時間的變化Fig. 10 Variation of the ratio of solution conductivity to solution conductivity under initial condition with time and crevice depth
3 模擬計算結果與試驗測量結果的比較
本工作參考了CHEN等[28]的試驗研究,并與之進行比較,以說明模擬的準確性。試驗采用X70管線鋼,試驗條件如下:以0.01 mol/L Na2SO4溶液作為土壤模擬溶液,pH為6.8,溫度為室溫(22 ℃),縫隙深度為30 cm,厚度為0.9 mm,陰極保護電位為-1 000 mV。
如圖11、圖12和圖13所示,通過數據對比,模擬結果和試驗結果的平均誤差為1.8%,這種偏差可能是模型的假設與實際情況仍存在差距所致。

圖11 72 h后模擬和試驗所得的溶液pHFig. 11 Solution pH obtained by simulation and test after 72 h

圖12 72 h后模擬和試驗所得的縫內電位Fig. 12 Potential in crevice obtained by simulation and test after 72 h

圖13 72 h后模擬和試驗所得溶液的氧質量濃度Fig. 13 Oxygen concentration of solution obtained by simulation and test after 72 h
4 結論
(1) 在結合前人的數學模型的基礎上,開發了一個涂層下縫隙腐蝕的二維瞬態模型,將縫隙內化學物質的傳質、還原反應和水的電離統一,利用有限差分法解決了方程的求解問題,模擬了陰極保護條件下,縫隙內化學和電化學反應隨時間的演變,模擬結果與試驗數據吻合度較好,兩者平均誤差為1.8%。
(2) 當縫內溶液含有溶解氧時,縫內發生氧的還原反應,氧氣被消耗,在有陰極保護電流的情況下,在距縫口1.5 mm處溶液pH出現峰值,此處氧氣被消耗殆盡,并且由于電中性和縫隙形狀的特殊性,使得氧氣無法進一步向縫內擴散。
(3) 本模型添加水的電離效果,當溶解氧被還原生成OH-的同時還有少部分OH-來自水的電離,這使模擬效果更佳貼合實際。在陰極保護條件下,縫內溶液的pH顯著上升,在縫隙口處達到峰值,并隨著時間的推移逐漸趨于穩定。而在高堿性環境中,縫隙內部的金屬表面會形成鈍化膜從而使其腐蝕速率降低,即使縫隙深處未受到陰極保護也能延緩腐蝕的發生。
(4) 縫隙中由于電遷移傳質和濃度梯度影響下的擴散,使陽離子向內、陰離子向外運動,同時由于還原反應使縫口處OH-濃度迅速升高,導致溶液電導率隨時間的延長而增加,并且隨著深度的增加而減小。

