衰弱楊梅樹根際土壤微生物多樣性研究
汪兆,任海英,鄭錫良,俞浙萍,張淑文,戚行江*
(1.西北農林科技大學 園藝學院,陜西 楊凌 712100; 2.浙江省農業科學院 園藝研究所,浙江 杭州 310021)
楊梅(MyricarubarSieb.et Zucc.)是我國重要的亞熱帶經濟果樹,果實酸甜可口,富含花青素、維生素C和多種抗氧化物質[1]。近年來,在楊梅產區發現楊梅樹體衰弱現象,該現象具有危害重、地域廣等特點。該癥狀的發生以盛產期果園為主,在發生癥狀當年,樹體年生長量減少、葉小且顏色變淺、落葉嚴重,結果量增多而果實品質下降,而后癥狀逐年加重。病情嚴重的果園中樹體衰弱率可達50%以上,80%左右葉片脫落,樹體頂端雖有少量葉片暫存,但葉色暗綠無光澤;在后期,根系出現腐爛,經過2~4 a樹體死亡。目前,衰弱現象在各楊梅產區都有不同程度的發生,梅農損失嚴重,由于其成因仍不明確,尚無法采取有效防控措施。
隨著對微生物功能的不斷了解,研究發現,微生物菌劑是調理土壤環境、減少病害發生的有效措施,而研究植物根際微生物菌群的變化則是使用微生物技術防治植物病害的前提[2]。在對根際土壤進行深入研究后,發現根際是植物-微生物-土壤相互作用、進行物質能量交換和信號傳遞的重要界面。唐鑫等[3]發現,土壤真菌群落結構的變化與天麻患褐腐病密切相關;丁亞茹等[4]發現,健康與易感病煙田根際土壤微生物群落組成存在差異,易感病煙田中存在較多潛在病原菌,可通過調控措施改善土壤性質及微生物群落結構,減少病原菌定殖;武華周等[5]發現,抗青枯病桑樹根際土壤富集了大量類諾卡氏菌屬、芽胞桿菌屬、鞘氨醇單胞菌屬等生防菌。在農業生產中,分析根際微生物多樣性以及微生物群落結構特征有利于深入研究和有效防治植物病害。目前,高通量測序技術被廣泛應用于微生物群落結構的研究[6-8]。本研究采用微生物群落測序技術,對不同地區樹勢衰弱與健康楊梅的根際土壤樣品進行分析,研究根際微生物群落結構和多樣性,為探究楊梅樹勢衰弱成因及根際功能菌株的篩選提供理論依據。
1 材料與方法
1.1 果樹樣品的收集和指標測定
2016年7月選取樹勢衰弱嚴重的浙江省臨海市弘寶楊梅園、仙居縣西爐村楊梅園和瑞安高樓鄉楊梅基地為取樣點,在各地區同一果園分別選取有代表性的3棵健康植株和衰弱植株的東、南、西、北4個方向春梢各5支,共20支嫩梢,測量其梢長、梢粗。選取30片葉子,利用SPAD-502便攜式葉綠素儀測定葉綠素含量,每片葉重復測3次。4個方位各采集成熟楊梅果實50顆,隨機選擇5顆用電子分析天平稱量其質量,同時用手持糖度計(Pocket refractometer pal-1)測定可溶性固形物含量。VC采用2-6二氯靛酚滴定法[9]進行含量測定,總糖用蒽酮比色法[10]進行含量測定,可滴定酸采用酸堿滴定法[11]進行含量測定。
1.2 土壤樣品的收集和測定
每個地區各選擇3棵有代表性的健康與發病楊梅樹,在地面以下10~20 cm處尋找楊梅細根,每棵樹選擇3個土壤采樣點,去除易被抖落的土壤后裝于無菌自封袋中,置于裝有干冰的泡沫盒中,快速運至實驗室[12]。在無菌工作臺中,去除根部松散的土壤,使用無菌刷子從根部收集殘留土壤。將每個地區取樣的健康樹和衰弱樹根際土壤樣本等量混勻,轉移至10 mL離心管,標記樣本信息后經液氮速凍,置于-80 ℃冰箱保存,共計6個樣品。
1.3 基因組DNA提取、PCR擴增、文庫構建和上機測序
采用CTAB法提取根際土壤微生物基因組DNA,用1%瓊脂糖凝膠電泳進行DNA質量檢測。利用New England Biolabs公司的High-Fidelity PCR Master Mix with GC Buffer和高保真酶進行PCR擴增。16S V4區引物選擇515F和806R;ITS1區引物選擇ITS5-1F-F和ITS1-1F-R。PCR反應體系為DNA模板1 μL,10×Buffer 5 μL,2.5 mmol·L-1dNTPs 4 μL,Taq DNA聚合酶0.5 μL,上、下游引物各1.5 μL,無菌超純水補至50 μL。擴增程序為94 ℃預變性5 min;94 ℃變性50 s,50~60 ℃退火50 s(根據引物設計不同的退火溫度),72 ℃延伸1.5 min,30個循環;72 ℃延伸10 min,4 ℃保存。對PCR產物進行瓊脂糖凝膠電泳檢測,并利用QIAGEN公司的膠回收試劑盒對目的條帶進行回收。使用TruSeq?DNA PCR-Free Sample Preparation Kit建庫試劑盒進行文庫構建,構建好的文庫經過Qubit和q-PCR定量來檢測文庫質量,文庫合格后,使用NovaSeq6000進行上機測序。采用Qiime、Uparse、Mothur等分析軟件對測序結果進行微生物多樣性分析[13]。
1.4 數據分析
根據Barcode序列和PCR擴增引物序列從下機數據中拆分出各樣本數據,截去Barcode和引物序列后使用FLASH對每個樣本的reads進行拼接,得到的拼接序列為原始Tags數據(Raw Tags);將拼接得到的Raw Tags過濾處理得到高質量的Tags數據(Clean Tags)。參照Qiime的Tags質量控制流程,進行Tags截取和Tags長度過濾得到Tags,再進行去除嵌合體序列的處理,將Tags序列與物種注釋數據庫進行比對檢測嵌合體序列,并最終去除其中的嵌合體序列,得到最終的有效數據(Effective Tags)。
利用Uparse軟件對所有樣本的全部Effective Tags進行聚類,默認以97%的一致性(Identity)將序列聚類成為OTUs,同時會選取OTUs的代表性序列,依據其算法原則,篩選OTUs中出現頻數最高的序列作為代表序列。對OTUs序列進行物種注釋,用Mothur方法與SILVA132的SSUrRNA數據庫進行物種注釋分析(設定閾值為0.8~1.0),獲得分類學信息并分別在界、門、綱、目、科、屬、種各個分類水平統計各樣本的群落組成。使用MUSCLE軟件進行快速多序列比對,得到所有OTUs代表序列的系統發生關系。最后以樣本中數據量最少的為標準進行均一化處理。
使用Qiime軟件計算Observed-otus、Chao1、Shannon、Simpson、ACE、Goods-coverage指數。真菌的功能預測用FunGuild真菌環境功能數據庫,查詢文獻中已有的物種在環境中的生態功能;細菌的功能預測用FAPROTAX原核生物環境功能數據庫,基于擴增子物種注釋結果,對數據庫進行查詢,獲得已有文獻支持的物種的環境功能信息。
2 結果與分析
2.1 健康與衰弱楊梅樹體表型和果實品質
本研究對3個楊梅產地健康和衰弱樹的葉片、枝條和果實的表型進行測定(表1)。在樹體生長上,3個產地衰弱樹的葉綠素含量、梢長、梢粗均低于健康楊梅樹,其中葉綠素含量、梢長和梢粗的變化率依次為2.08%~11.10%、6.34%~35.59%和12.36%~16.96%(變化率=(衰弱樣品數值-健康樣品數值)/健康樣品數值×100%)。仙居地區衰弱樹葉綠素含量、梢長、梢粗的變化率最大。3個產地衰弱樹的單果重、總糖、VC含量均低于健康樹,其中單果重、總糖和VC含量的變化率依次為1.51%~9.89%、2.64%~6.48%和5.95%~8.59%;衰弱樹果實的可溶性固形物含量低于健康樹,臨海地區降低3.09%,瑞安地區降低7.98%;衰弱樹果實的可滴定酸含量均高于健康樹。
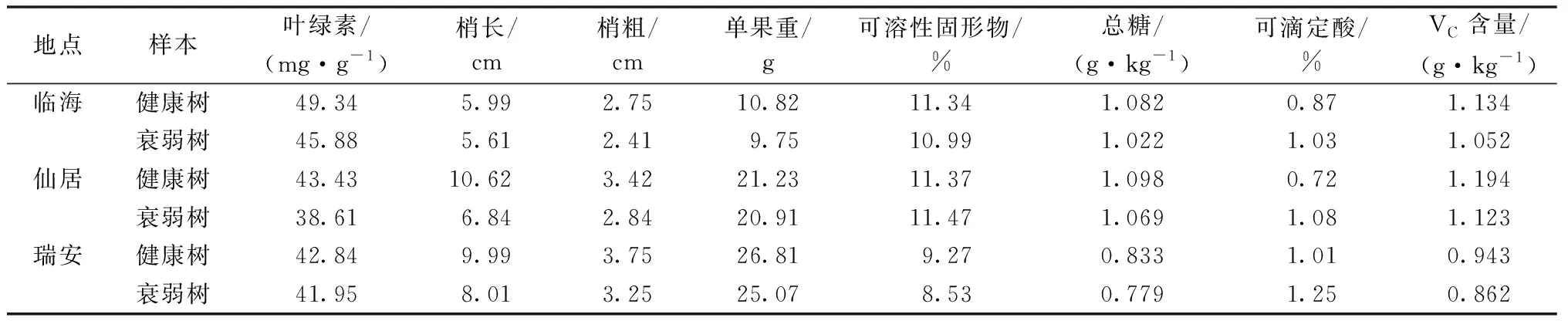
表1 健康和衰弱楊梅的表型和品質分析
2.2 楊梅根際土壤微生物α多樣性分析
本研究對3個產地健康和衰弱樹的根際土壤微生物進行了α多樣性分析(表2),各樣品的測序深度指標(Goods-coverage)均高于0.98,表明數據準確可用于后續分析。Shannon與Simpson指數值越大,表明群落多樣性越高;Chao1與ACE指數越大,表明群落豐富度越高[14]。本研究中,臨海地區健康樹土壤細菌和真菌的Shannon、Chao1、ACE指數高于衰弱樹。仙居地區健康樹土壤細菌Shannon和Simpson指數均低于衰弱樹,而健康樹細菌Chao1與ACE指數值均高于衰弱樹,仙居地區健康樹土壤真菌4種α多樣性指數均高于衰弱樹。瑞安地區健康樹的細菌Chao1和真菌Simpson指數值高于衰弱樹,其他健康樹的α多樣性指數值均低于該地區衰弱樹土壤微生物α多樣性指數值。綜合3個地區的土壤微生物α多樣性來看,4種α多樣性指數值并未呈現出與樹體健康狀況相關聯的規律。

表2 衰弱、健康楊梅樹根際土壤細菌和真菌α多樣性分析
2.3 健康與衰弱楊梅樹土壤微生物豐度比較
2.3.1 門和科水平細菌豐度分析
對3個產地健康和衰弱楊梅樹的根際土壤進行微生物豐度分析,在平均相對豐度最高的10種細菌門中,4種細菌門在3個產地健康與衰弱樹中呈基本一致的變化趨勢,這4種細菌門分別是變形菌門、酸桿菌門、疣微菌門和擬桿菌門。變形菌門在臨海、仙居和瑞安地區衰弱樹土壤中的相對豐度均低于健康樹。酸桿菌門、疣微菌門和擬桿菌門的相對豐度在3個地區均呈現出衰弱樹高于健康樹的趨勢(表3)。
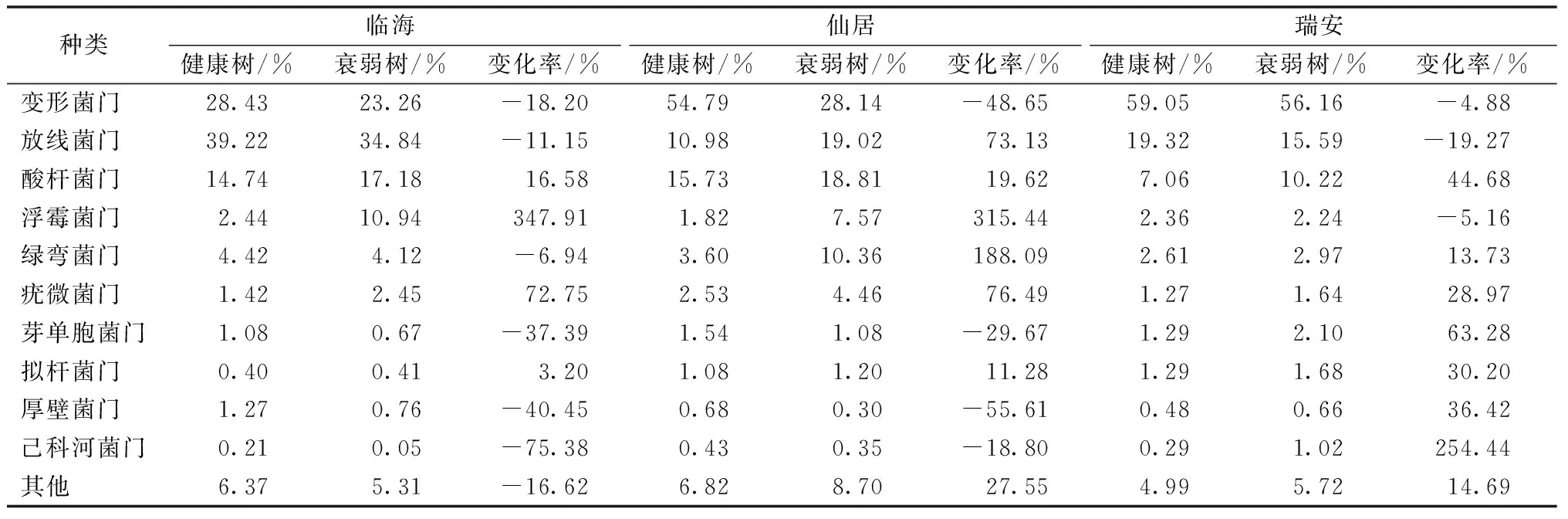
表3 門水平平均豐度最高的10類細菌相對豐度差異比較
對3個產地健康和衰弱樹的根際土壤細菌在科水平進行相對豐度分析,在平均相對豐度最高的15種細菌中,3種細菌在3個產地健康與衰弱樹中呈基本一致的變化趨勢,其余12種細菌隨著地區變化在健康與衰弱樹中呈現不同的變化趨勢(表4)。在臨海、仙居和瑞安地區的健康樹土壤中伯克氏菌的豐度分別為6.48%、23.79%和15.69%,而在對應地區衰弱樹土壤中豐度分別為4.85%、2.66%和8.56%。鏈霉菌科在臨海、仙居和瑞安的健康樹土壤中豐度分別為12.68%、1.06%和4.28%,均低于相應的健康樹。貝耶林克菌在健康樹土壤中的相對豐度均高于衰弱樹。以上結果表明,伯克氏菌、鏈霉菌科和貝耶林克菌等細菌在健康樹土壤中的相對豐度均顯著高于衰弱樹(圖1)。

表4 科水平平均豐度最高的10類細菌相對豐度差異比較

LHH代表臨海地區健康樹土樣,LHD代表臨海地區衰弱樹土樣;XJH代表仙居地區健康樹土樣,XJD代表仙居地區衰弱樹土樣;RAH代表瑞安地區健康樹土樣,RAD代表瑞安地區衰弱樹土樣。
2.3.2 門和屬水平真菌相對豐度分析
對各土壤樣品在門水平平均相對豐度前10的真菌進行分析,子囊菌門在6份樣品中的平均相對豐度為79.18%,最高為仙居衰弱樹(92.80%),最低為臨海衰弱樹(67.49%)(表5)。被孢霉門在3個地區的衰弱樹土壤相對豐度高于健康樹,該菌門在全部樣品中的平均相對豐度為3.82%。在10種相對豐度最高的真菌門中,臨海地區健康樹土壤中未發現壺菌門、卡爾卡氏桿菌、捕蟲霉門,衰弱樹土壤中未發現捕蟲霉門。在仙居地區,健康與衰弱樹土壤中均未發現卡爾卡氏桿菌,僅在健康樹土壤中發現了球囊菌門、羅茲菌門、捕蟲霉門。在瑞安地區未發現球囊菌門、卡爾卡氏桿菌、捕蟲霉門,僅在健康樹土壤中發現了羅茲菌門,僅在衰弱樹土壤中發現了壺菌門。

表5 門水平平均豐度最高的10種真菌相對豐度比較
在健康和衰弱樹土壤中,屬水平平均相對豐度最高的10種真菌中,6種真菌在不同地區的健康與衰弱樹中呈不同變化趨勢,青霉菌在3個地區都呈現健康樹土壤中相對豐度高于衰弱土壤趨勢(表6)。潘尼西里佛菌在3個地區的健康土樣中的相對豐度均高于對應地區衰弱樹土壤,此真菌屬目前研究較少。多囊藻屬、被孢霉屬和鐮刀菌屬在3個地區的衰弱樹土壤中的相對豐度均高于健康土樣(圖2)。

圖2 屬水平上有差異的3類細菌相對豐度

表6 屬水平平均豐度最高的10種真菌相對豐度比較
2.4 細菌和真菌微生物功能預測
本研究將3個地區的衰弱樹根際土壤微生物樣本記為D組,健康樹根際土壤微生物樣本記為H組。在對細菌進行FAPROTAX功能預測后,發現衰弱楊梅根際土樣中細菌與植物相關的功能為鐵呼吸、纖維素水解作用、亞硝酸鹽氧化、硫化合物的呼吸作用、硫酸鹽呼吸、硫化合物的暗氧化等,而健康楊梅樹根際土壤中細菌的功能為硝化作用、化學異養、光營養、芳香族化合物降解、芳香烴降解、硝酸鹽還原、含氧光自養、碳氫化合物降解、光自養、脂肪族非甲烷烴降解、好氧化學異養、木質素分解等。
通過對真菌進行FunGuild功能預測,發現衰弱楊梅樹根際土壤樣品中真菌的主要功能為菌根、木材腐生菌、動物病原菌、植物病原菌等;在健康楊梅樹根際土壤樣品中,其功能為動物病原菌、植物病原菌、內生真菌、地衣、木腐菌、外生菌根、木材腐生菌、苔蘚植物等。
由此可見,與健康樹土壤微生物相比,衰弱楊梅樹土壤中關于氮元素轉化的細菌較少,細菌類群較少;在真菌方面,健康楊梅土壤樣品相比于衰弱楊梅土樣增加了地衣、苔蘚等。
3 小結與討論
本研究以3個地區的健康和衰弱楊梅樹為對象,通過分析植株生長、果實品質指標和微生物多樣性測序結果,發現衰弱樹在樹體生長和果實品質方面均差于健康樹,4種α多樣性指數值并未呈現出與樹體健康狀況相關聯的規律。
植物根際微生物群落結構受病原菌和生防微生物等生物因子的影響[15-16],故對根際微生物群落進行分析,可得到與該植物相關的病原菌與生防微生物等微生物信息。對衰弱和健康楊梅根際土壤中細菌科水平的微生物相對豐度進行分析后發現,健康樹的伯克氏菌、鏈霉菌、貝耶林克菌等有益細菌的相對豐度均高于衰弱樹。伯克氏菌能產生揮發性含硫化合物從而抑制病害的發生[17]。鏈霉菌通過產生揮發性有機化合物,降低由真菌引起的植物病害的發病率,但同時會造成不同真菌的形態異常[18]。貝耶林克菌被研究者認為具有明顯的固氮活性[19-20]。此外,纖線桿菌在衰弱土樣中的相對豐度高于健康土樣,但未見有文獻對該菌有過詳細報道。在對真菌屬水平相對豐度進行分析后發現,多囊藻屬、鐮刀菌屬和被孢霉屬在3個地區衰弱土樣中的相對豐度均高于健康土樣。鐮刀菌屬能引起橡膠莖桿潰瘍病[21]、馬鈴薯鐮刀菌根腐病[22]、香蕉枯萎病[23]等病害,而被孢霉屬的相對豐度在大豆、草莓和硒砂瓜連作時會出現大幅增加[24-26]。目前,關于多囊藻屬的研究相對較少,在本研究中,多囊藻屬在衰弱楊梅根際土壤中相對豐度較高,推測其與楊梅衰弱病的發生存在一定關聯。因此,在總結3個地區的真菌和細菌微生物群落變化規律后發現,衰弱癥的發生與土壤中伯克氏菌、鏈霉菌科和貝耶林克菌等有益細菌的減少呈現一致性規律;與土壤中多囊藻屬、鐮刀菌屬、被孢霉屬這3類真菌豐度的增加也呈現一致性規律。進一步對細菌和真菌的功能進行預測分析,發現健康楊梅樹土壤中含有更多關于土壤氮元素轉化的微生物,這與發現衰弱病土壤中具有固氮作用的貝耶林克菌豐度偏低的現象一致。
隨著人們對微生物在農業生產中重要作用的認識不斷加深,利用土壤微生物學特性來評價土壤的健康程度和質量逐漸被認可[27]。本研究從楊梅根際微生物菌群中找到了衰弱與健康楊梅的差異特征菌群,可為預測和防控楊梅衰弱病提供依據。基于本研究結論,利用多囊藻屬、鐮刀菌屬和被孢霉屬等真菌的相對豐度為預測指標,當相對豐度大幅上升則預示楊梅衰弱病的發生。同時,通過施用土壤菌劑來提高土壤中伯克氏菌、鏈霉菌、貝耶林克菌等細菌的豐度,或可以防控楊梅衰弱病。
本研究以浙江3個楊梅產地健康楊梅樹為對照,對衰弱癥狀的楊梅葉片、枝條、果實性狀和根際土壤微生物多樣性進行了分析。結果表明:衰弱楊梅樹的葉綠素含量、梢長、梢粗、單果重、總糖和VC含量均有不同程度的降低,衰弱楊梅樹果實的可滴定酸含量均高于健康樹;進一步對衰弱土樣中細菌和真菌的相對豐度開展研究,發現在衰弱楊梅土壤中伯克氏菌、鏈霉菌、貝耶林克菌等細菌相對豐度降低,而鐮刀菌屬、被孢霉屬和多囊藻屬等真菌相對豐度增加,同時衰弱楊梅樹土壤中關于氮元素轉化的細菌類群較健康植株少。初步推測,衰弱楊梅土壤中有益菌的減少及有害菌的增加可能是造成楊梅樹勢衰弱的重要原因。

