基于鏤空陣列探頭的反射式光聲/熱聲雙模態組織成像*
謝實夢 黃林? 王雪 遲子惠 湯永輝 鄭鑄 蔣華北
1) (重慶郵電大學光電學院, 重慶 400065)
2) (電子科技大學電子科學與工程學院, 成都 611731)
3) (深圳邁瑞生物醫療電子股份有限公司, 醫學影像事業部, 深圳 518057)
4) (南佛羅里達大學醫學工程系, 佛羅里達, 坦帕, 美國 33620)
光聲和熱聲成像技術除激發源不同外, 可共用一套數據采集和處理系統, 具有天然的融合優勢.本文提出了一種基于鏤空陣列的反射式光聲/熱聲雙模態成像技術, 該技術利用光纖與天線, 通過鏤空陣列的開孔進行光聲/熱聲信號激發, 使得激發光、微波和接收超聲信號共軸, 構成明場光聲/熱聲雙模態成像模式.通過對探頭鏤空部分晶元相位和幅值的補償校準, 成功實現了3 mm直徑塑料管、人體手臂、手背和腳背的雙模態成像.實驗結果表明: 系統空間分辨率為0.33 mm, 雙模態成像技術可同時提供組織的光學和微波吸收分布, 有助于腫瘤、糖尿病足等疾病的精準檢測, 具有極廣泛的臨床應用前景.
1 引 言
光聲成像技術通過探測脈沖光激發產生的超聲信號以獲取組織的光學吸收分布, 不僅保留了光學成像的高對比度, 還兼具了超聲成像的高分辨率優勢.光聲成像技術利用人體內不同生色團, 比如:血紅蛋白、黑色素和水等具有的特殊吸收峰, 可以反映上述生色團的相對含量及其變化, 有助于多種疾病的檢測以及功能信息的獲取.目前光聲成像技術已廣泛應用在病理切片[1,2]、動物模型研究[3?5]、臨床前[6]和臨床中[7,8], 被認為有望成為繼MRI,CT和超聲等之后的“第八種生物成像技術”.
此外, 將用于激發產生光聲信號的激光器更換為脈沖微波源, 也同樣可以產生超聲信號用于成像, 即熱聲成像技術.用于熱聲成像的微波波長遠大于光聲成像所用激光波長, 通常在厘米量級, 因而具有更大的成像深度.此外, 由于熱聲成像主要反映與組織水分含量和離子濃度相關的介電特性;因此, 在諸如乳腺癌[9?12]、腦卒中[13]、肌骨[14]、血管[15]、腎臟[16]和前列腺[17]顯像等方面都展現出了一定的優勢.光聲和熱聲成像技術除激發源不同外, 可共用一套數據采集和處理系統, 具有天然的融合優勢.尤其是針對乳腺癌的檢測, 結合光聲和熱聲成像技術將有助于乳腺癌檢測精準度的提升.
2005年, Ku等[18]通過在掃描區域上方放置光路和下方放置微波天線, 分別進行光聲、熱聲激發的單探頭旋轉掃描成像方式, 進行了光聲/熱聲雙模態成像的實驗研究.該研究組[19]進一步通過在喇叭天線側面開小孔進光, 并將由棱鏡和毛玻璃組成的光學組件直接固定于喇叭天線內, 實現了光聲/熱聲的同向激發成像.基于光學組件與微波天線的一體化設計, 2012年研究組[20]進一步發展了一套可用于乳腺成像的光聲/熱聲和超聲三模態成像平臺, 該平臺利用一個相控陣超聲線陣探頭接收光聲和熱聲信號, 以及進行超聲成像; 但因探頭的接收孔徑角限制[21], 使得光聲/熱聲成像質量較差.相比而言, Reinecke等[22]構建的光聲/熱聲和超聲三模態成像平臺采用凹陣探頭接收光聲和熱聲信號, 線陣探頭僅用于超聲成像, 可同時獲得高質量的光聲/熱聲和超聲圖像; 但該平臺有效成像區域有限, 難以開展大動物或者人體實驗.
醫用超聲探頭多采用線陣或者凸陣探頭進行成像檢測, 但該類探頭用于光聲/熱聲成像時, 其有限孔徑角使得難以獲得較好的光聲/熱聲圖像.相比而言, 光聲和熱聲成像除激發源不同以外, 剩余硬件系統和軟件算法均可共用; 且光聲/熱聲成像可使用環形或者半圓形陣列探頭進行信號收集,可以獲得高質量的圖像, 具有一定的臨床應用前景.為進一步探索光聲/熱聲雙模態成像技術的臨床應用潛力, 本文提出了一種基于鏤空陣列的反射式光聲/熱聲雙模態成像技術.該技術利用光纖與天線通過鏤空陣列的開孔進行光聲/熱聲信號激發, 使得激發光、微波和接收超聲信號共軸, 構成明場光聲/熱聲雙模態成像模式.相比于側向照射的暗場成像模式, 本文所提明場成像模式[23], 不僅結構更加緊湊、操作便捷, 而且由于激發光、微波和接收超聲信號共軸的緣故, 也具有更高的信噪比.
2 實驗系統
本文所用光聲/熱聲雙模態成像系統框圖如圖1(a)所示, OPO脈沖激光器(脈寬: 4 ns, 重復頻率: 20 Hz; Surlite I-20, Continuum, USA)和小型化高功率脈沖微波源(脈寬: 550 ns, 峰值功率:< 60 kW, 中心頻率: (3.0 ± 25) MHz, 重復頻率:1—200 Hz; HWK-3050FA, 成都國睿電子科技有限公司, 成都)分別用于光聲和熱聲成像信號激發.反射式光聲和熱聲成像實物圖如圖1(b)和圖1(c)所示, 其中: 鏤空陣列(河北奧索電子科技有限公司)參數為: 陣元, 128; 中心頻率, 2.0 MHz; 帶寬,80%; 半徑, 65 mm; 晶片尺寸, 1.6 × 20.0 mm; 中間32個晶片進行10 mm切割鏤空, 兩側分別剩5 mm晶片.激光通過光纖束輸出, 光纖束輸出端(外觀尺寸: 50 mm × 60 mm × 12 mm, 出光口:40 mm × 1 mm, 成都尚光科技有限公司)實物圖如圖1(c)所示, 經過整形后輸出光為一矩形光斑,實驗中所用激光能量密度低于ANSI (American national standards institute safety limit)規定[24]的20 mJ/cm2.微波通過同軸線纜(1.5 m, 1.2 dB插損, Micable邁可博電子, 福州)輸出至自制的偶極子天線[25], 實驗中所用微波功率密度低于IEEE規定[26]的20 mW/cm2.鏤空陣列接收光聲/熱聲信號, 首先經由自制128通道放大器(帶寬0.2—2.5 MHz, 增益56 dB)放大, 然后經由1∶2多路復用器傳輸至兩張NI 5752B (50 MS/s, 12 Bit, National Instruments, USA)采集卡組成的64通道數據采集系統, 采集后的數據存于計算機中, 利用延遲疊加圖像重建算法進行圖像重建[27].實驗過程中,鏤空陣列探頭用保鮮膜進行密封, 內部裝滿石蠟油由于光聲和熱聲成像耦合; 同時, 待成像物體置于薄膜底部, 通過醫用超聲耦合劑與薄膜緊密接觸,保證良好的超聲耦合.

圖1 (a)為反射式光聲/熱聲雙模態成像系統框圖; (b), (c)分別為反射式光聲和熱聲成像探頭接口實物圖; (d), (e)分別為鏤空探頭俯視和側視實物圖Fig.1.(a) Schematic of the photoacoustic (PA)/thermoacoustic (TA) dual modality imaging system; (b), (c) photograph of the PA and TA imaging system, respectively; (d), (e) Top view and side view of the hollow concave array, respectively.
3 實驗結果與討論
所用陣列探頭第49—80晶元中間被切除10 mm形成鏤空, 相比其他晶元長度方向較少了一半; 因此, 鏤空部分晶元需要進行相位和靈敏度校準.首先以裝有質量分數為0.9%鹽水的3 mm直徑塑料管為研究對象, 通過對該塑料管的熱聲成像實現鏤空陣列探頭的校準.由圖2(a)中第47和48晶元接收到的熱聲信號可知: 相鄰晶元熱聲信號應該具有類似的波形.考慮鏤空部分晶元面積僅為非鏤空部分1/2; 故其接收到的熱聲信號幅值也下降為1/2(圖2(b)中藍色信號).同時, 由于探頭制作過程中, 中間鏤空部分晶元正負電極引線接反, 導致其信號相位也發生了180°偏移.經相位和靈敏度校準后第49晶元波形圖(圖2(b)中黑色信號)與第48晶元波形圖(圖2(b)中紅色信號)相似, 符合圖2(a)中所示相鄰晶元(第47和48晶元)波形規律.在對信號進行0.1—3.0 MHz帶通濾波后, 利用相干因子加權[28]的延遲疊加重建圖像算法得到的塑料管的熱聲圖像, 進一步分析發現: 校準后生理鹽水圖像(圖2(d))幅值大于校準前圖像(圖2(c))幅值, 具有更高信噪比.通過上述實驗實現了對本文所用鏤空陣列的相位和靈敏度校準, 為下一步利用本文所提光聲/熱聲雙模態成像系統開展仿體和人體實驗研究奠定了基礎.
為驗證本文所提光聲/熱聲雙模態成像技術相比于單獨的光聲或者熱聲成像技術更具優越性, 本文對分別裝有質量分數為0.9%的生理鹽水和紅花油的3 mm直徑塑料管進行了成像, 實驗過程示意圖和成像物體實物圖分別如圖3(a)和圖3(b)所示.由于生理鹽水不具有光學吸收性, 只能吸收微波, 因此, 圖3(a)中1號裝有生理鹽水塑料管僅熱聲圖像可見(圖3(d)).然而紅花油因其低的電導率(0.26 s/m)[29], 導致其基本不吸收微波; 但其本身的褐紅色導致其具有一定的光學吸收性; 因此,圖3(a)中2號裝有紅花油塑料管在680 nm激發光照射下光聲圖像可見(圖3(c)).圖3實驗結果表明: 利用光聲/熱聲雙模態成像技術, 可同時獲取成像區域目標物體的光學和微波吸收功能信息(如圖3(e)所示), 可同時反映成像區域生色團(光聲成像對比度來源)與水分、離子含量(熱聲成像對比度來源)的含量變化, 有助于諸如乳腺癌、腦卒中、關節炎等疾病的準確檢測.

圖2 鏤空陣列探頭校準結果圖 (a) 第47和48晶元接收到的熱聲信號波形; (b) 第49晶元所接收熱聲信號校準前和校準后的波形圖, 以及與第48晶元熱聲信號波形圖; (c), (d) 分別為校準前和校準后的熱聲圖像Fig.2.The calibration results of hollow transducer array: (a) TA signal received by the 47 th and 48 th elements; (b) the TA signal before and after calibration of the 49 th element, and the TA signal of the 48 th element; (c), (d) are the TA images before and after calibration, respectively.TAM: Thermoacoustic Amplitude.
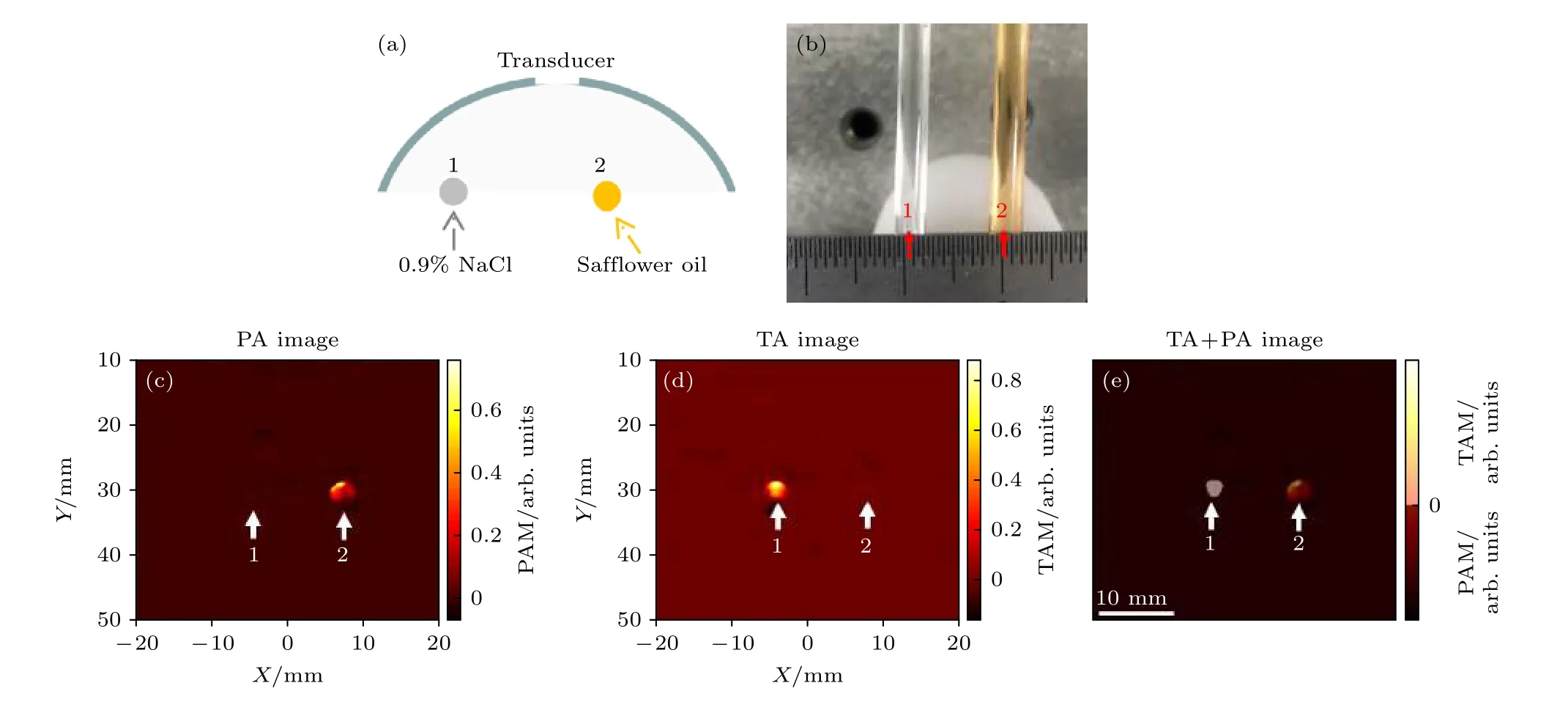
圖3 雙模態成像性能驗證實驗 (a), (b) 分別為待成像物體示意圖和實物圖; (c), (d) 分別為熱聲圖像和680 nm激發波長得到的光聲圖像; (e)融合后的熱聲/光聲雙模態圖像Fig.3.(a), (b) Schematic and photograph of the target, respectively; (c), (d) TA and PA images obtained at 680 nm, respectively;(e) the fused TA/PA image.PAM:Photoacoustic Amplitude.
由于用于熱聲成像激發微波脈沖寬度(550 ns)大于光聲成像所用激發脈沖寬度(4 ns), 所以本文所提系統空間分辨率主要受制于熱聲成像; 為此,對兩根直徑66 μm平行放置的銅絲進行熱聲成像以對系統空間分辨率進行研究.實驗結果如圖4所示, 其中圖4(a)為兩根銅絲的熱聲成像結果, 沿圖中紅色虛線取熱聲圖像一維輪廓分布, 得到圖4(b)所示結果, 進一步[13]定量計算得到本文基于鏤空陣列探頭構建的反射式光聲/熱聲雙模態成像系統空間分辨率為: AB + CD –d= (1.116 – 0.6451)+ (3.462 – 2.945) – 0.66 = 0.33 mm, 其中d為銅絲直徑(66 μm).此外, 由于本文側重點在于研究淺表血管(手臂、手背和腳背)相關疾病, 所以系統成像深度主要受制于激光的穿透深度.前期已有大量研究結果表明, 光聲成像對于淺表血管具有較好的成像能力[1]; 但在針對諸如乳腺疾病等[2]研究時成像深度依然需要定量分析.基于本文所用的鏤空陣列探頭在開展乳腺疾病成像時, 已經對其成像范圍和成像深度進行了詳細研究[30].
目前常用的手持式淺表血管光聲成像技術多將光纖/光纖束固定在探頭兩側進行光聲激發[31],該方法難以對探頭正前方無法被激光照射區域進行光聲成像.而傳統手持式熱聲成像技術, 由于天線尺寸通常較大[32], 也多采用側向輻照進行熱聲激發, 該方法雖能對探頭正前方區域進行熱聲成像; 但由于輻照范圍較大, 使得超聲探頭有效接收孔徑內熱聲信號幅值較低, 且來自周圍非成像區域組織的噪聲也較多, 導致圖像偽影較大.本文提出的基于鏤空陣列的反射式光聲/熱聲雙模態成像技術, 利用光纖與天線通過鏤空陣列的開孔進行光聲/熱聲信號激發, 使得激發光、微波和接收超聲信號共軸, 可以提供更加豐富的信息(比如皮膚輪廓等), 以及更高的圖像信噪比.為對本文所提技術性能進行進一步評估, 在獲得電子科技大學倫理委員會審核同意, 以及受試者知情同意情況下, 本文開展了2例自愿者人體實驗研究.本文實驗研究采用的順序均為先進行熱聲成像, 然后依次進行680,720, 800 nm光激發的光聲成像; 圖像重建首先對信號進行0.1—3.0 MHz帶通濾波, 然后利用延遲疊加重建算法直接成像.
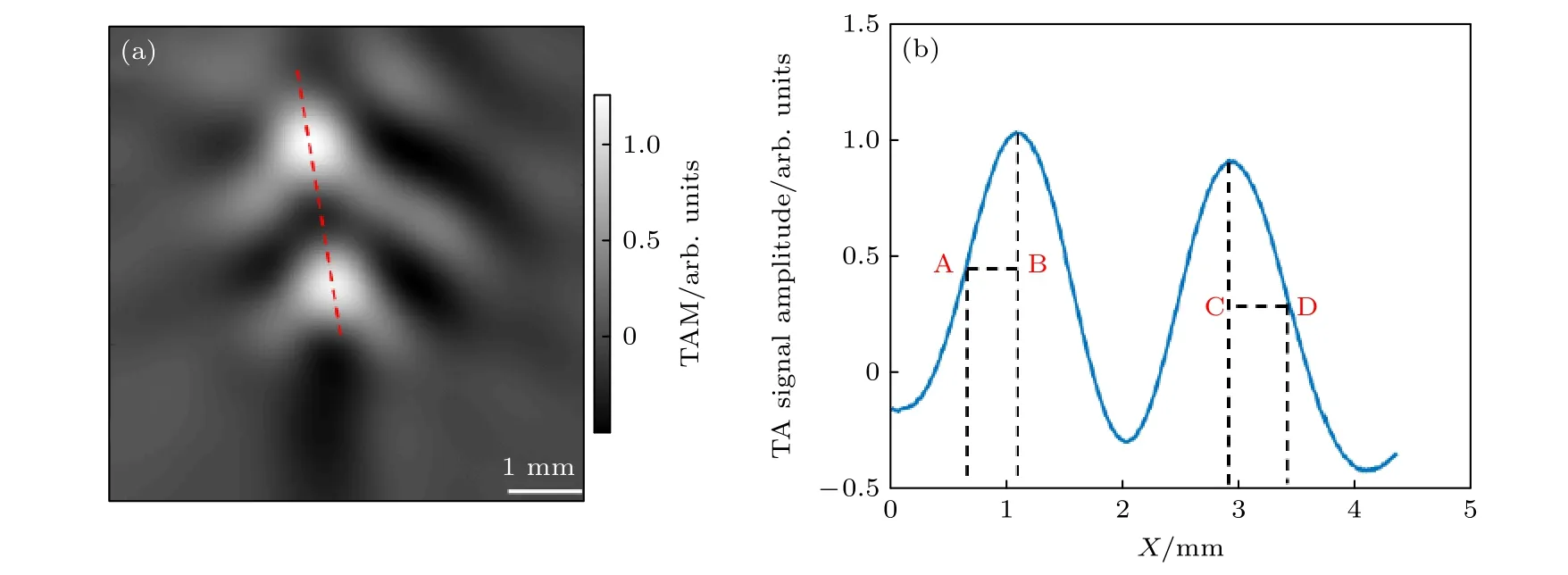
圖4 空間分辨率實驗 (a) 兩根直徑66 μm銅絲的熱聲成像結果; (b) 沿(a)中紅色虛線的熱聲圖像一維輪廓分布Fig.4.TAI of two copper wires for system spatial resolution evaluation: (a) Recovered TA image; (b) recovered microwave absorption profile along the red dashed line shown in (a).TAM: Thermoacoustic Amplitude.
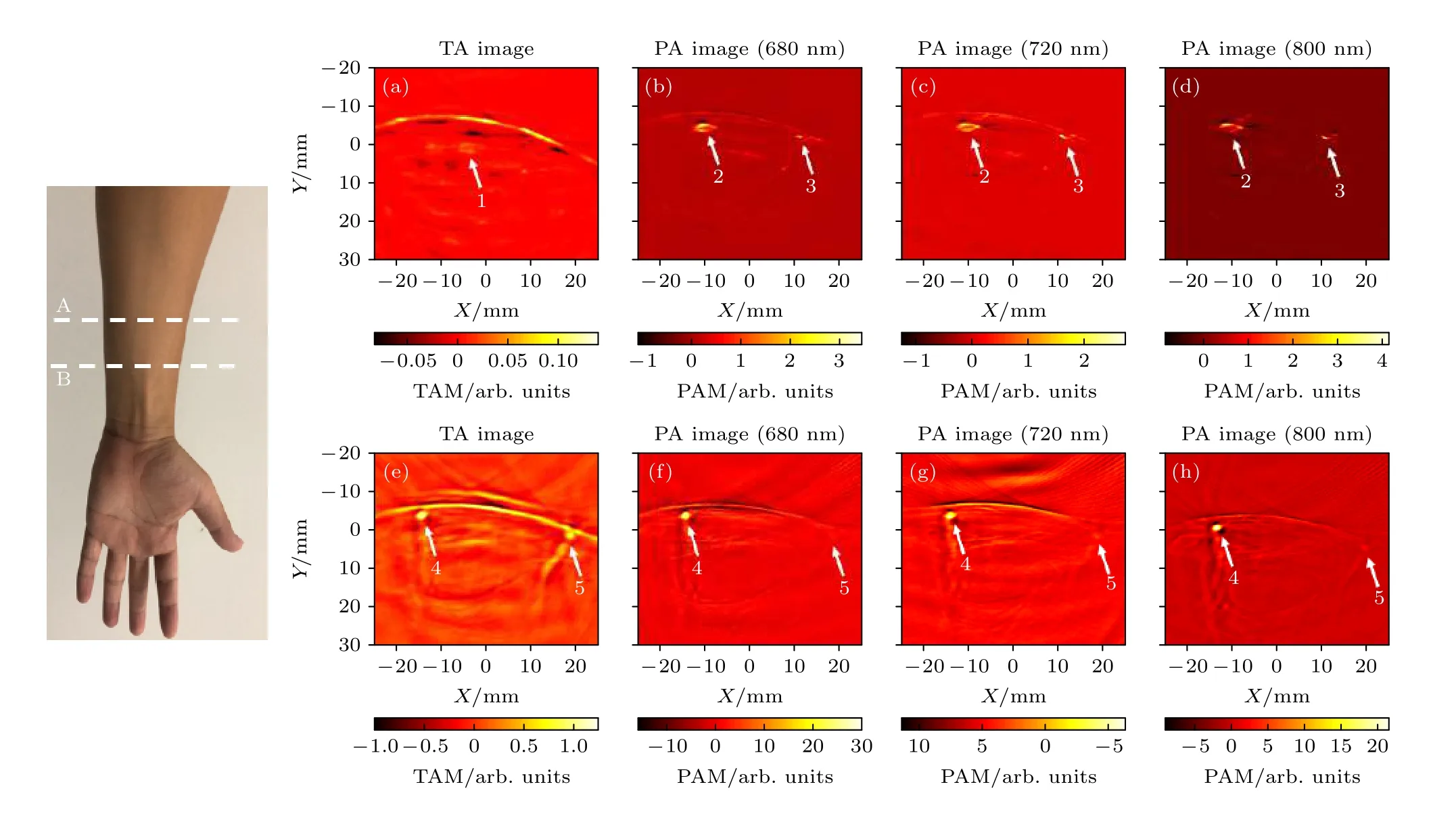
圖5 正常人手臂雙模態成像, 左側為待成像平面示意圖, A和B分別為自愿者1和2待成像手臂平面示意圖; (a)?(d)和(e)?(h)依次為為自愿者1和2手臂的熱聲圖像, 680, 720, 800 nm激發光聲圖像Fig.5.The picture is the schematic of the opisthenar to be imaged, A and B are the detection plan of volunteers 1 and 2, respectively.(a)?(d) and (e)?(f) are TA image, 680 nm PA image, 720 nm PA image and 800 nm PA image of volunteers 1 and 2, respectively.TAM: Thermoacoustic Amplitude, PAM: Photoacoustic Amplitude.
首先, 對自愿者1和2手臂內側進行了雙模態成像實驗, 實驗結果如圖5所示.圖5左側照片給出了自愿者1(A層面)和2(B層面)待成像平面示意圖.由于自愿者1在被試時, 手腕彎曲過大, 且為保證良好的貼合, 鏤空探頭底部薄膜對皮膚擠壓過度, 致使圖5(b)和圖5(c)中2和3號靜脈血管出現阻斷, 導致熱聲信號降低, 難以在圖5(a)熱聲圖像中顯現.但圖5(a)中熱聲圖像顯示出了一些屈肌腱的結構1, 與手指關節熱聲成像結果較吻合[33].針對自愿者1出現的血管阻斷問題, 在進行自愿者2成像研究過程中, 使其盡量處于自然舒張狀態, 且保證鏤空探頭薄膜底部僅輕微擠壓手臂.因此, 圖5(e)—(h)兩根血管4和5均可見, 且血管的光聲和熱聲信號幅值均大于自愿者1的實驗結果, 比如圖5(b)中光聲信號最大值為3, 僅僅是圖5(f)中光聲信號最大值的0.1.此外, 由于熱聲成像天線輻照范圍(大于60 mm × 60 mm)大于光聲成像所用光纖輻照范圍(40 mm × 1 mm); 因此, 熱聲圖像5(e)中兩根血管4和5清晰可見, 而光聲圖像5(f)和5(h)中僅血管4清晰可見.
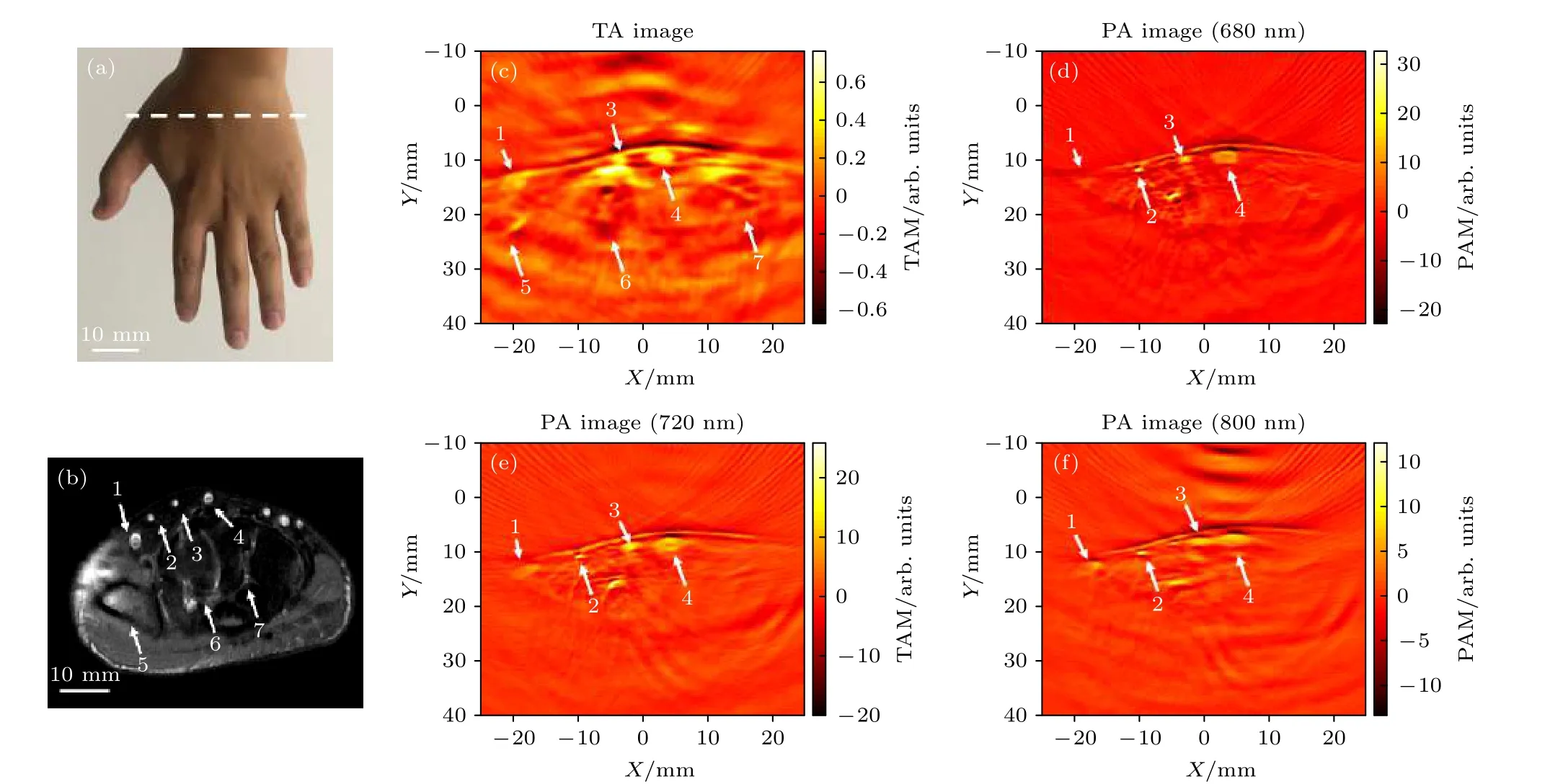
圖6 正常人手背雙模態成像 (a) 待成像平面示意圖; (b) 對應層面MRI圖; (c)?(f) 依次為手背的熱聲圖像, 680, 720和800 nm激發光聲圖像Fig.6.(a) Schematic diagram of the plane to be imaged; (b) the corresponding MRI image; (c)?(f) are TA image, 680 nm PA image, 720 nm PA image and 800 nm image of hand, respectively.TAM: Thermoacoustic Amplitude, PAM: Photoacoustic Amplitude.
進一步, 對自愿者1手背進行了雙模態成像實驗, 實驗結果如圖6所示.圖6(a)和圖6(b)分別給出了自愿者1手背待成像平面示意圖和MRI橫斷位成像結果(OAx fx PD序列, 3.0T, GE).從圖6中可見, MRI中顯示的1, 3和4號血管熱聲成像(圖6(c))和光聲成像(圖6(d)—(f))均可見,但2號血管熱聲成像中未被顯示, 分析原因可能是手背成像過程中有輕微擠壓所致; 在今后的研究中將醫用超聲線陣探頭固定于鏤空部分, 先超聲成像引導調節探頭施壓力度及角度以獲得較好的血管超聲圖像, 再進行光聲和熱聲成像可以有效地提升雙模態技術對淺表血管的顯像能力.此外, MRI成像中(圖6(b))所示5, 6和7號掌骨在熱聲成像(圖6(c))中可見, 光聲成像中不可見.
臨床研究表明腳背外周血管病變和骨質畸變均是糖尿病足的預警標志[34]; 因此, 能同時對腳背外周血管和骨質進行無損成像, 對于糖尿病足的早期預警具有臨床意義.對自愿者1右腳腳背進行了雙模態成像實驗, 實驗結果如圖7所示.其中圖7(a)和圖7(b)為彩色多普勒超聲成像結果, 1,2, 3和4號血管清晰可見.光聲圖像中(圖7(e)—(g)), 1和2號血管清晰可見, 但4號血管處于3號血管正下方(如圖7(b)所示), 在采用反射式光聲激發時其被3號血管遮擋, 因此未能被光聲成像顯示.圖7(a)中1, 2和3號血管由于距離皮膚太近,其熱聲信號與皮膚信號疊加, 導致熱聲圖像7(c)中1, 2和3號血管無法被顯像.同時, 為避免探頭底部薄膜對腳背過度擠壓(如圖7(c)所示), 導致3號血管位置薄膜貼合不緊, 超聲耦合較差; 因此,信號強度較大的光聲圖像(圖7(e)—(g))中3號血管可見, 但在信號強度較小的熱聲圖像(圖7(c))中3號血管難以被熱聲顯像.相比而言, 圖7(b)中4號血管距離皮膚較遠(大于6 mm), 在熱聲成像中清晰可見(圖7(d)); 同時, 超聲成像所示5號跖骨(圖7(b)), 在熱聲成像中(圖7(d))也可見.為此, 基于本文所提反射式光聲/熱聲雙模態成像技術具有同時實現腳背外周血管和骨質無損成像的潛力, 有助于糖尿病足的早期預警和提前干預.
4 結 論

圖7 正常人腳背雙模態成像 (a), (b) 待成像平面彩色多普勒超聲圖; (c)成像層面示意圖; (d)?(g) 依次為腳背的熱聲圖像,680, 720和800 nm激發光聲圖像Fig.7.(a), (b) The color Doppler ultrasound images; (c) the schematic of imaging plane; (d)?(g) TA image, 680 nm PA image,720 nm PA image and 800 nm image of instep, respectively.TAM: Thermoacoustic Amplitude, PAM: Photoacoustic Amplitude.
本文提出了一種基于鏤空陣列的反射式、明場光聲/熱聲雙模態成像技術; 通過對3 mm直徑塑料管熱聲成像, 實現了對探頭鏤空部分晶元相位和幅值的補償校準.同時, 成功實現了人體手臂、手背和腳背的雙模態成像, 光聲成像還進行了多波長成像(本文僅進行了680, 720和800 nm光聲成像).通過與MRI成像結果(圖6)和超聲成像(圖7)結果對比, 結果表明: 本文所提雙模態成像可同時提供組織的光學(比如: 有氧和去氧血紅蛋白)和微波(比如: 皮膚和骨)吸收分布, 有助于諸如乳腺癌、骨癌、糖尿病足等疾病的精準檢測, 具有廣闊的臨床應用前景.
然而, 本文所提光聲/熱聲雙模態成像技術分別依次進行熱聲和光聲成像, 需要更換微波天線和光纖, 不便于操作; 為進一步滿足臨床使用所需,本文后續將設計緊湊型、小型化天線, 使其可以直接與光纖同時固定于鏤空陣列探頭開孔內, 實現手持式、便攜式光聲/熱聲雙模態成像.此外, 光聲/熱聲雙模態成像技術的結構性能力有限, 需借助超聲成像的結構性成像優勢, 提供更為豐富的結構性信息, 以滿足臨床所需; 因此, 本文后續還將基于該鏤空陣列探頭設計超聲成像模塊, 實現超聲/光聲/熱聲的三模態成像, 推動光聲和熱聲成像技術的臨床轉化.

