尾側聯合腸系膜上靜脈優先入路機器人輔助下全結腸系膜切除治療右半結腸癌的效果
連玉貴,周全博,段小飛,王貴憲,袁維堂
鄭州大學第一附屬醫院結直腸外科 鄭州 450052
手術仍是治療可切除右半結腸癌的主要方法。支配右半結腸的供血血管變異較多,且毗鄰胰腺、十二指腸等重要臟器,因此手術難度大,手術風險較高。全結腸系膜切除聯合中央血管結扎是治療右半結腸癌的可選術式之一,強調在胚胎層面銳性游離臟壁層筋膜、保證系膜“信封”完整和腫瘤滋養血管的根部結扎,較傳統手術更能保證系膜的完整,能夠切除更大面積的結腸系膜及獲取更多的淋巴結,降低局部復發率,改善遠期生存狀況[1-3]。
在微創外科時代,全結腸系膜切除手術治療右半結腸癌常見有3種入路:中間入路[4]、頭側入路[5]及尾側入路[6]。有研究[6-7]表明,尾側入路以建立層面優先后離斷血管為特點,首先進入升結腸后間隙及胰腺十二指腸前間隙,相比于其他入路,更加有利于右半結腸變異血管的處理和淋巴結清掃。理論上,機器人手術具有高清3D穩定的視野、靈活可旋轉540°的機器人腕部結構等,使其在進行組織暴露、分離及淋巴結清掃等操作中更為精準。回顧性研究及Meta分析[8-11]結果表明,機器人全結腸系膜切除術較腹腔鏡具有中轉開腹率低、術后恢復快、長期生存更優的特點。尾側聯合腸系膜上靜脈(superior mesenteric vein,SMV)優先入路機器人輔助下全結腸系膜切除術幾乎適用于包括肥胖患者在內的所有病例,其特點在于能確保正確的解剖平面、精確識別關鍵解剖、優化Henle干屬支血管的處理、提高淋巴結切除完整度。本文對該入路方式的技術細節及短期療效進行了詳細分析,報道如下。
1 對象與方法
1.1研究對象回顧性分析鄭州大學第一附屬醫院結直腸外科前瞻性數據庫記錄的2020年3月至12月行尾側聯合SMV優先入路機器人輔助下全結腸系膜切除術20例患者的臨床資料。病例納入標準:①年齡>18歲。②結腸鏡及病理證實為腺癌。③術前CT評估UICC TNM分期為Ⅰ~Ⅲ期。排除標準:①合并其他惡性腫瘤。②M1。③急診手術、拒絕機器人手術、不能耐受麻醉或手術。患者均簽署知情同意書。
20例患者中,男12例,女8例,年齡31~78歲,中位數59歲;體質指數20.6~28.7 kg/m2,中位數24.0 kg/m2;有腹部手術史3例;合并高血壓7例,糖尿病5例;ASA分級Ⅰ、Ⅱ級18例,Ⅲ、Ⅳ級2例;腫瘤位于盲腸5例,升結腸4例,肝區11例;T分期T1、T2期2例,T3、T4期18例;N分期N0期12例,N1、N2期8例。
1.2手術方法所有手術由兩組醫師完成,單個醫生年機器人大腸切除手術量超過150例。仔細分析術前影像學資料,以評估可能存在的遠處轉移、原發腫瘤的T分期以及區域淋巴結轉移情況,確定腸系膜上動脈(superior mesenteric artery,SMA)、SMV屬支血管解剖特征。患者術前均未行機械性腸道準備。均采用氣管插管靜吸復合全身麻醉,頭低5°~15°,同時左傾10°~15°,使小腸移向脾曲,以便于術野的顯露。手術均基于DaVinci SiTMSurgical System平臺完成。Trocar孔位置見圖1。臍部左下方約3 cm處為12 mm鏡頭孔,左側鎖骨中線肋緣下2~3 cm為8 mm主操作孔,置入單極電剪或超聲刀;麥氏點尾側2 cm處為8 mm副操作孔,置入雙擊電凝;在操作孔、鏡頭孔弧形連線上分別建立12、5 mm輔助孔。機器人自患者右側、頭側進入完成對接。整個手術過程不再調整體位。腫瘤位于升結腸肝區或橫結腸近肝區者,行包括幽門下淋巴結及中結腸血管根部淋巴結清掃的擴大切除術;腫瘤位于回盲部或升結腸近端者則行標準右半結腸切除術。手術步驟如下。
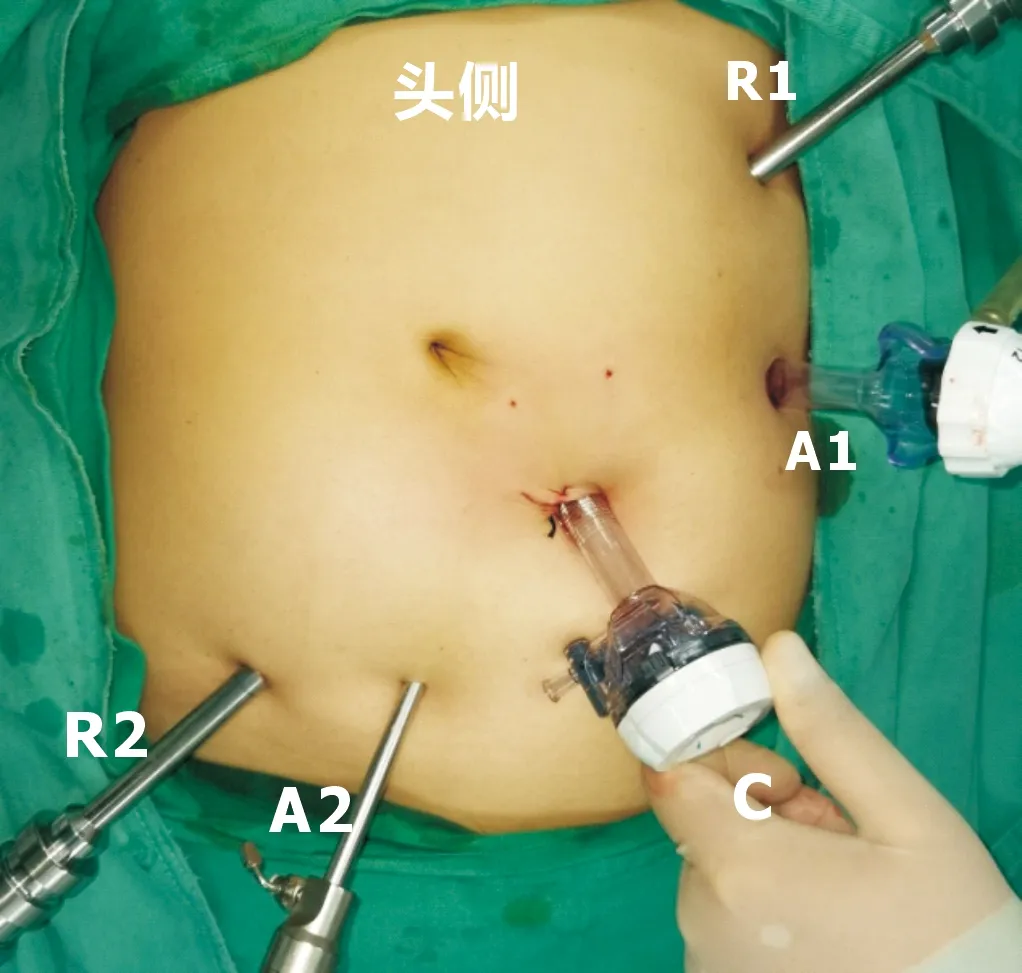
C:12 mm鏡頭孔;R1:8 mm主操作孔;R2:8 mm副操作孔;A1:12 mm主輔助孔;A2:5 mm副輔助孔
①尾側入路:首先識別解剖標志(十二指腸、右髂總動脈),于小腸系膜根部與后腹膜交接處右髂總動脈上方約1 cm處自左向右切開腹膜,進入升結腸后間隙。在十二指腸外側建立平面后繼續向右側擴大平面直至升結腸旁溝,此時可見右側生殖血管與右側輸尿管被腎前筋膜覆蓋(圖2A),避免其損傷。轉向十二指腸水平部,打開原始后腹膜,進入胰腺十二指腸前間隙,此時可顯露SMV、SMA背側面。繼續沿十二指腸降部向頭側游離擴大平面,尋找右結腸或副右結腸靜脈,以其為“路標”向匯入Henle干方向推進(圖2B)。注意在靠近匯入點時有胰十二指腸上前靜脈加入Henle干,在上提升結腸系膜時注意張力,以防其撕裂。在胰十二指腸前方留置小紗布作為標記。
②SMV的顯露:轉向腹側,不調整體位,把小腸移向左下腹及盆腔,暴露術野。牽拉回結腸血管蒂,在其匯入SMV尾側1 cm處切開腹膜。尋找SMV,以SMV左側緣為“路標”向頭側游離至胰腺下緣。一般SMV前方沒有屬支血管,可安全清除SMV前方的淋巴、脂肪組織。通過裸化SMV建立游離平面,同時有利于辨認SMA的右側分支(圖2C),以確保完整的淋巴結清掃。由于整個解剖過程靠近SMV,因此應小心處理,以避免出現血管損傷。為避免出血或血栓形成,不要直接抓持SMV。造成血管損傷的最高風險可能是在分支的匯合處,在解剖過程中應避免過度牽引血管以防意外出血。如果遇到出血,應立即紗布壓迫,視損傷程度和術者技術水平選擇血管縫合線修復縫合或轉換為開放性手術。
③回結腸血管蒂的離斷(203組淋巴結清掃):提起回結腸血管蒂,于其下方1 cm處切開小腸系膜,與尾側游離層面相通。SMV前方已經裸化,回結腸靜脈(Ileocolic vein,ICV)的SMV匯入點很容易顯露。回結腸動脈(Ileocolic artery,ICA)通常位于ICV背側,離斷ICV后更容易顯露及清掃ICA根部淋巴結(圖2D)。SMA一般走行于SMV左后方,ICA走行于ICV后方更為多見。然而,約42%的ICA走行于SMV前方[12],在裸化SMV時應注意這些血管變異。
④中結腸血管蒂的離斷(223組淋巴結清掃):ICV/ICA離斷后繼續向頭側游離至Henle干水平,此時于SMV左側胰腺下緣尋找起源于SMA的中結腸動脈(middle colic artery,MCA),中結腸靜脈(middle colic vein,MCV)通常位于MCA頭側。自MCA根部向遠心端游離至MCA左右支分叉處,根部腫瘤位置決定MCA離斷水平(圖2E)。結腸肝區腫瘤自MCA/MCV根部離斷,其他部位腫瘤可離斷MCA/MCV右支。約60%的患者有單獨的右結腸動脈(right colic artery,RCA)[12],在進行SMV裸化時需要注意。
⑤Henle干屬支的處理:前述手術已沿右結腸靜脈(right colic vein,RCV)游離至Henle干起始部。沿Henle干自左向右解剖血管,顯露屬支。游離并保護胃網膜右靜脈,離斷RCV(圖2F)。此時整個胰十二指腸前間隙處理完畢。第2機器臂可向腹側上壓升結腸系膜,外側游離至升結腸旁溝,頭側游離至膈結腸韌帶,顯露十二指腸起始部。
⑥結腸肝區的游離:自胃網膜中段或距腫瘤10 cm以遠胃網膜血管弓內或弓外離斷胃結腸韌帶進入網膜囊。在胃系膜與橫結腸系膜間隙內自左側向肝區方向游離。在上述留置紗布指引下離斷大網膜、膈結腸韌帶及升結腸側腹膜。至此,整個右半結腸及其系膜已完全游離。
⑦消化道重建:取上腹正中5 cm切口,經此切口切除標本,完成小腸與橫結腸端側或側側吻合,關閉系膜裂孔。沖洗腹盆腔,升結腸旁溝留置引流管一根,關閉各切口,術畢。

A:尾側入路進入升結腸后間隙,可見輸尿管,其被腎前筋膜所覆蓋;B:胰十二指腸前間隙,分別暴露SMV背側及RCV;C: 以SMV左緣為導向向頭側裸化SMV,同時可顯露SMA的分支;D:暴露并清掃ICV、ICA根部淋巴結;E:清掃中結腸血管根部淋巴結,MCV、MCA已離斷;F:暴露Henle干屬支,離斷RCV
1.3手術結果術中出血量30~200(中位數80)mL,手術時間135~240(中位數170) min,淋巴結獲取總數12~37(中位數19)枚;有1例患者術中出現RCV損傷,給予鈦夾夾閉;無中轉開腹。術后首次排氣時間1~3 d,首次進流食時間1~4 d,引流管拔除時間3~7 d,住院時間6~19(中位數8) d。術后無Clavien-DindoⅢ級以上并發癥發生。術后有2例出現并發癥,其中1例出現切口感染換藥后愈合;另1例出現淋巴漏,初始引流量約300 mL,采取禁食加全胃腸外營養支持加生長抑素后痊愈。無圍手術期死亡,無30 d內非計劃再次住院或手術。
2 討論
在傳統開腹時代,外側入路是右半結腸切除的主流入路。在微創外科時代,鑒于器械和手術視野的不同,采取中間入路和尾側入路越來越普遍。Henle干屬支血管變異較多且靜脈壁菲薄,如果Henle干顯露不清、牽拉張力過高或者操作粗暴極易造成Henle干及其屬支的出血,這也是全結腸系膜切除的技術難點。我們采取尾側入路,自小腸系膜根部切開腹膜進入升結腸后間隙,首先顯露右側輸尿管及生殖血管并加以保護。建立起層面后再進入胰十二指腸前間隙,以RCV為導向向SMV方向游離,為后續尋找Henle干和安全離斷RCV創造條件。本研究結果顯示,術中無重要血管損傷,無Clavien-Dindo Ⅲ級以上并發癥發生,與其他研究[8]基本一致。
歐美國家多采取全結腸系膜切除,而日本則采取D3淋巴結清掃術治療Ⅱ、Ⅲ期結腸癌,二者手術理念相似,都取得了顯著的治療效果,但兩者孰優孰劣目前尚無定論[3]。然而,對于右半結腸癌,無論是全結腸系膜切除還是D3淋巴結清掃,均未對淋巴結清掃的內側界有明確的說明。根據淋巴引流規律,中央組淋巴結位于SMA發出右側屬支的根部,理論上以SMA為內側界更為合理。但有研究[7,13]表明,以SMA為導向進行淋巴結清掃有較高的腹瀉及淋巴漏發生率,且對術者有較高的技術要求,長期生存是否獲益仍不明確。因此,目前國際上絕大多數學者均以SMV左緣為手術切除的內側界限[14-15]。尾側入路實質是先建立游離空間,以層面為優先,內側游離終點線恰好為SMV背側的右側緣;而以SMV為導向即是淋巴結清掃需要,也為SMV右側屬支的處理提供便利。兩種入路聯合更加有利于淋巴結清掃和重要血管的保護。本研究詳細描述了尾側聯合腸系膜上靜脈優先入路機器人輔助下全結腸系膜切除治療右半結腸癌的技術細節和短期療效,初步證實了該技術的可行性和安全性。
需要強調的是,機器人輔助下全結腸系膜切除治療右半結腸癌手術難度較高,對術者和助手有較高的要求,存在較長的學習曲線。在開展此術式時需要優化手術操作,選擇合理的手術入路,保證手術安全。該術式的療效仍有待大樣本、多中心的前瞻性研究提供更高級別的循證醫學證據。

