“素養為本”的微項目教學在高中化學實驗中的應用
史培艷

摘要:以二氧化硫制備、性質驗證、噴泉實驗的一體化、封閉式實驗項目為例,開展“素養為本”的微項目教學,發展學生科學探究與創新意識、證據推理與模型認知素養;通過子項目問題交流討論,培養學生化學符號表征及化學進階思維能力。
關鍵詞:素養為本;微項目教學;高中化學實驗;二氧化硫
文章編號:1008-0546(2021)02-0093-05 中圖分類號:G632.41 文獻標識碼:B
doi:10.3969/j.issn.1008-0546.2021.02.023
一、問題的提出
“素養為本”的化學課堂教學,以真實情境為載體,開設實驗為主的多種探究活動,重視教學內容的結構化,改變學生的學習方式,注重學生實踐、創新能力的培養。微項目教學是以學生為中心,以微型項目為載體,在真實情境中開展一系列探究活動的教學形式。微項目教學是實施化學課程,發展學生化學學科核心素養,體現學生個性化的一種新教學方式,具有項目式教學和微課的特點。微項目教學從學生的生活經驗人手,依據學生的認知規律和最近發展區,創設真實生產、生活情境,融合專業知識和技能,提升學生解決實際問題、綜合實踐應用能力。
在科技抗疫的今天,國家重點組建實驗室體系,實現產學研融通創新。農村學校的實驗室儀器和藥品陳舊,有的甚至不能使用,更缺乏現代化、數字化實驗儀器。陳舊的實驗器材阻礙不了教師和學生創新之舉,借助鄉土素材,融合化學知識,助推實驗創新,提升實踐技能。
“二氧化硫的性質與應用”上課前,需要提前制備二氧化硫并把二氧化硫通入水中制得二氧化硫的水溶液。進行實驗探究過程中,二氧化硫的水溶液不穩定,會釋放出具有刺激性氣味、有毒的二氧化硫氣體,導致學生對實驗的興趣削減。為了減少以上弊端,采用微項目教學,設計二氧化硫制備與性質的一體化、封閉式實驗,促進學生對“含硫化合物的性質”的深度學習,提升學生化學學科核心素養。
二、微項目內容主題分析
1.教材分析
“二氧化硫的性質和應用”是蘇教版《化學(必修第一冊)》專題4第一單元第一課時內容。本單元在學習了物質的分類、物質的量濃度、氧化還原反應、離子反應等基礎上學習二氧化硫制備與性質、含硫物質間轉化、硫酸型酸雨成因與防治。根據結構決定性質,性質決定用途這一知識主線,進行有意義二氧化硫知識建構。二氧化硫是酸性氧化物,具有酸性氧化物通性;二氧化硫中硫的化合價為+4價,介于最低價一2價和最高價+6價之間,即有還原性也有氧化性;二氧化硫的特性為漂白性。通過設計實驗方案、改進實驗裝置,進行二氧化硫實驗分組合作探究,并繪制含硫物質之間轉化的價類二維圖。利用價類二維圖促使學生內化氧化還原和物質分類等核心概念。
2.學情分析
學生已經具有分類觀,理解氧化還原反應、離子反應大概念,掌握常見氣體制備、一定物質的量濃度溶液的配制等,能設計氣體制備及性質探究的實驗方案并實施實驗方案,觀察現象,得出實驗結論,也能用相關原理分析陌生情境問題和解決問題。學生已經知道二氧化硫是酸性氧化物,具有氧化性、還原性、漂白性;學生不了解不同酸堿指示劑變色范圍和氧化還原反應的先后順序原因。
3.教學策略
基于學生元認知、生活經驗、最近發展區,給學生提供儀器和藥品、文獻,組織學生閱讀課本和文獻。學生借助身邊的生活素材,在他人對二氧化硫性質改進成果基礎上進行創新。受新冠病毒形狀啟發,設計多彩新冠模型變色實驗。學生分組、分工、合作探究,展示成果并講解各組設計實驗方案、實驗過程、實驗現象、實驗結論及實驗注意問題。
4.專業拓展
利用不同酸堿指示劑不同變色范圍(表1),探究二氧化硫與堿、鹽溶液的變色反應。配制約0.1mol/L堿、鹽溶液,并用精密pH試紙測其pH值(表2)。
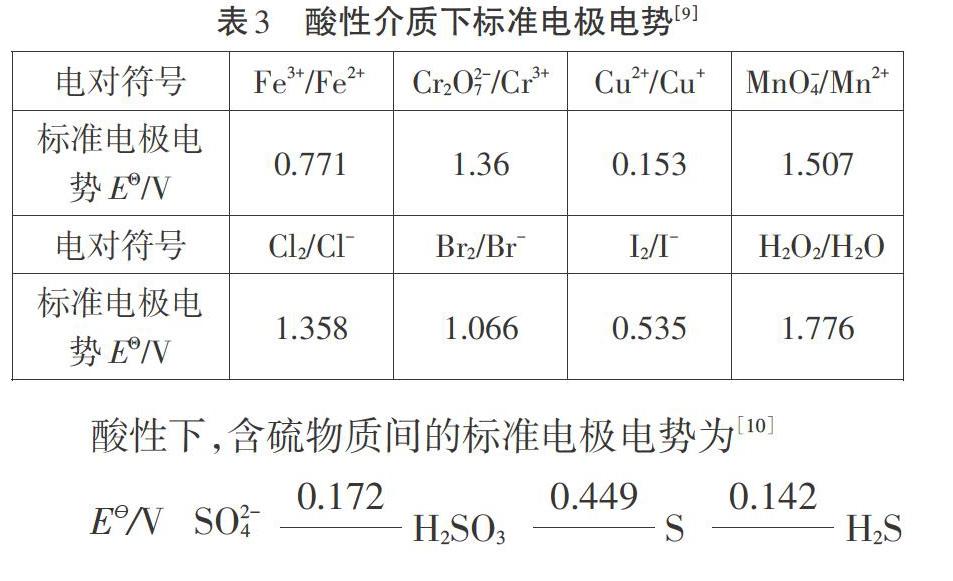
二氧化硫以還原性為主,與常見氧化劑反應的變色順序是不同的,取決于氧化劑的氧化性強弱。通過文獻查閱,298K時標準電極電勢(表3),判斷氧化還原反應的難易程度。
三、微項目教學目標
1.通過改進實驗實現二氧化硫制備與性質的一體化,通過動手實驗、觀察、分析實驗現象,收集實驗證據,得出實驗結論,發展學生證據推理與模型認知素養。
2.能從物質類別、元素價態的角度,認識物質轉化路徑,能用化學符號表征物質的轉化,發展學生變化觀念。
3.基于“綠色化學”理念設計實驗方案,并對實驗進行評價和優化,發展學生科學探究與創新意識、科學態度與社會責任素養。
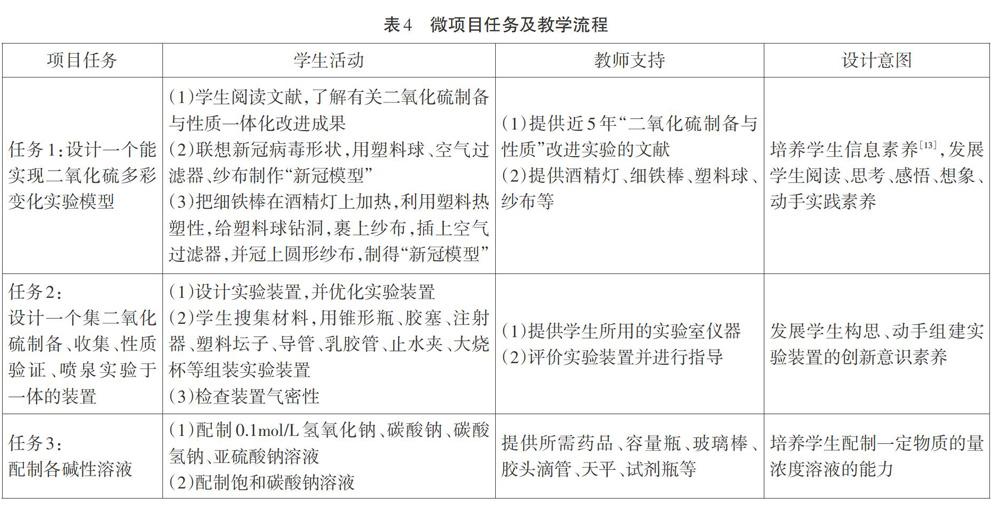
四、微項目任務及教學流程
學生分組、分任務合作實驗,其中1-6任務(表4)課前完成。
五、微項目實施過程及學生學習成果
1.展示學生課前任務成果把學生課前任務成果(圖1)匯總,并展示給學生
觀看。
實驗裝置如圖2:塑料壇子中A、B是兩個空心塑料球,塑料球上插入幾個空氣過濾器(類似冠),這樣形成冠狀病毒形狀。A、B球用紗布包上,各“冠”上冠有紗布。A球紗布浸有NaOH溶液(酚酞),A球“冠”上的紗布按順時針順序分別浸有Na2CO3溶液(中性紅)、NaHCO3溶液(甲基紅)、Na2SO3溶液(溴甲酚綠與甲基紅3:1混合)、飽和Na2CO3溶液(溴百里香酚藍)、紫色石蕊、Na2S溶液、品紅溶液(A7在最上方,檢驗二氧化硫是否收集滿);B球紗布浸有FeCl3(KSCN)溶液,B球“冠”上的棉花按順時針順序分別K2Cr2O7溶液、FeCl3溶液、CuClz溶液、12/淀粉溶液、酸性KMnO4溶液、廣泛pH試紙(水濕);A、B形成多彩的“新冠模型”。塑料小壇子中導管上粘有雙氧水和氯化鋇溶液浸濕的廣泛pH試紙。
2.實驗過程
實驗過程如表5及圖3所示。
3.實驗現象變化原因分析
學生分組、合作討論實驗現象變化的原因。
子任務1:兩處品紅溶液顏色變化慢、快原因。
學生成果:亞硫酸鈉與75%硫酸溶液反應是放熱反應,生成熱的二氧化硫氣體,熱的二氧化硫氣體難能使品紅溶液褪色;二氧化硫經導管進入塑料壇中,經冷卻,易使品紅溶液褪色;導管中是浸有品紅的棉花,成團狀,二氧化硫與品紅接觸面較小,而塑料壇中是浸有品紅的單層紗布,成片狀,二氧化硫與品紅接觸面大,后者反應速率快,褪色快。
子任務2:二氧化硫與同濃度不同溶液反應顏色變化快慢原因(A新冠模型)
學生成果:二氧化硫使紫色石蕊變紅,說明二氧化硫是酸性氧化物,與水反應生成亞硫酸。0.1mol/LNaOH、Na2CO3、NaHCO3、Na2SO3溶液pH分別為13.0、11.6、8.3、10.0,堿性不同,c(OH-)大小不同,二氧化硫與它們反應本質是與OH-反應,c(OH-)大的反應快,顏色變化快。
子任務3:二氧化硫與同濃度不同氧化劑變色快慢不同原因(B新冠模型)
學生成果:同濃度不同氧化劑的標準電極電勢不同,電極電勢越大,其氧化性越強,與二氧化硫反應就越快。
子任務4:二氧化硫分別使酸性高錳酸鉀溶液、品紅溶液褪色原理相同嗎?
學生成果:不同,二氧化硫與酸性高錳酸鉀溶液因發生氧化還原反應而使之褪色,二氧化硫與水反應生成亞硫酸,亞硫酸與品紅結合為不穩定無色物質,前者利用二氧化硫的還原性,后者利用二氧化硫的漂白性。
子任務5:兩處廣泛pH試紙變紅程度不同原因
B6冠上廣泛pH試紙呈紅色,是因為SO2+H2O=H2SO3=H+HSO3-導管上廣泛pH試紙呈紅色且顏色深,是因為H2O2+SO2=H2SO4;H2SO3為弱酸,H2SPO4是強酸,酸性不同,廣泛pH試紙紅色深度不同。
子任務6:燒杯中是藍色溶液,為什么形成黃色噴泉呢?
學生成果:打開止水夾b,多余二氧化硫與氫氧化鈉溶液作用,c(OH-)減小,pH減小。溴百里香酚藍變色pH范圍是6.2-7.6,顏色變化為黃一綠一藍。溶液由藍變綠,再變黃,說明二氧化硫稍過量。向錐形瓶中加水,止水夾a是打開狀態,整個裝置是相通的,二氧化硫因溶于水且部分被擠壓入氫氧化鈉溶液導致裝置內壓強減小,外壓大,形成黃色噴泉。
子任務7:通過實驗現象說明含硫物質之間具有怎樣的關系?
學生成果:同種價態含硫物質之間、不同價態的含硫物質之間能相互轉化,如圖4價-類二維關系。
五、微項目教學反思及改進建議
1.以學生為主體,教師為主導
微項目教學過程中,教師為主導,是組織者、指導者、點撥者;學生為主體,是親歷者、體驗者、探究者。整個過程中,學生通過項目,動手實驗體驗知識的產生過程。教師為學生提供活動的場所、空間、材料,適時針對學生存在的問題進行指導。
2.以學定項,難易適中
選擇的項目不僅符合課程標準要求,還要適合學情,根據學生的認知規律及最近發展區選擇難易適度的項目。過難的項目,學生很難完成,會產生挫敗感,興趣降低;過易的項目,學生容易完成,沒有挑戰性,不能激發學生潛力。適中的項目,學生既有挑戰性又能完成,有成就感和自豪感,樂意去做,能發揮學生內在動力。
3.利于學生學科核心素養發展
在真實情境中解決真問題,利于學生科學探究、宏觀辨識、微觀探析、變化觀念等素養的發展,利于學生化學思維能力的培養,利于學生完成任務共同體意識的強化。
4.存在問題及改進建議
鄉村中學班級人數多,分組合作時,有的學生不積極參加微項目學習;鄉村中學實驗藥品較久,失效,導致有的實驗現象不明顯;實驗室沒有網絡,不能及時、適時搜索資料等。改進建議:教學小班化、網絡化、微型化;資源時代化、更新化、跟進化。

