一株高濃度氨氮耐受的除氨氮菌篩選、鑒定及發(fā)酵條件優(yōu)化
谷雅文,于鯤鵬,任玉文,閆 珂,周曉輝,
(1.河北科技大學(xué),河北石家莊 050018;2.河北大美環(huán)境修復(fù)科技股份有限公司,河北石家莊 050000)
隨著工農(nóng)業(yè)的快速發(fā)展,我國的水土環(huán)境受到嚴(yán)重氨氮污染[1]。氨氮[2]主要指水體中以銨離子和游離氨形式而存在的氮,是一種高耗氧污染物,通過使水體富含營養(yǎng)素而導(dǎo)致水體的富營養(yǎng)化[3]。氨氮污染不僅會(huì)造成魚類等其他水體生物大量死亡,給水產(chǎn)養(yǎng)殖業(yè)帶來嚴(yán)重威脅[4];同時(shí),生活用水的氨氮污染也會(huì)嚴(yán)重危害人類的身體健康。氨氮來源廣泛,與農(nóng)藥化肥[5]、牲畜糞便[6]等傳統(tǒng)氨氮排放途徑相比,化工、醫(yī)藥和食品加工等工業(yè)產(chǎn)生的氨氮質(zhì)量濃度大于500 mg/L的廢水正成為我國水體氨氮污染的重要來源,據(jù)統(tǒng)計(jì),高濃度氨氮工業(yè)廢水的排放約占總氨氮來源的30%[2]。我國食品企業(yè)普遍存在規(guī)模小、技術(shù)落后的發(fā)展現(xiàn)狀,企業(yè)無力建設(shè)高額的環(huán)保處理設(shè)備,因此亟需尋找快速高效低成本去除氨氮的有效手段。
近半個(gè)世紀(jì)以來,為解決氨氮廢水問題,國內(nèi)外學(xué)者做了大量研究工作。目前報(bào)道最多的有物化法和生物法。羅宇智等[7]利用化學(xué)沉淀法去除稀土工業(yè)廢水中的氨氮;Chen等[8]在微波作用下,利用活性炭吸附廢水中的氨氮;Li等[9]采用離子交換法去除水體中的氨氮。這些方法工藝成熟、除氨氮效率高,但是耗能大、經(jīng)濟(jì)效益低且藥劑投入量大,會(huì)對(duì)水體造成新污染[10-12]。生物法[13-15]是指利用微生物處理氨氮廢水,具有成本較低、條件溫和、無二次污染等優(yōu)點(diǎn)。目前,生物法多集中于氨氮濃度范圍為50~100 mg/L的中低氨氮濃度廢水研究,該濃度范圍已有大量氨氮去除微生物菌株被報(bào)道:陳猛等[16]研究發(fā)現(xiàn)一株對(duì)氨氮廢水具有較好去除效果的芽孢桿菌ZF2-3,在第24 h時(shí)氨氮去除率為85.7%;陳紅菊等[17]研究發(fā)現(xiàn)一株24 h氨氮去除率為98.5%的凝結(jié)芽孢桿菌除氨氮菌株,但菌株鹽度耐受性差,水體中鹽度超過3%時(shí)菌株生長受到抑制;陳錦豪等[18]從對(duì)蝦養(yǎng)殖水體中分離到一株枯草芽孢桿菌DS5,5 d內(nèi)氨氮去除率最高為36%;此外還有解淀粉芽孢桿菌、假單胞菌、紅球菌、溶桿菌、反硝化細(xì)菌等,這些菌株對(duì)氨氮的去除能力各不相同,普遍存在耐受力低、應(yīng)用成本高和接種量大等缺點(diǎn),不適用于處理高氨氮濃度工業(yè)廢水。近期,張冠根等[19]研究發(fā)現(xiàn)一株解淀粉芽孢桿菌,在氨氮濃度500 mg/L的模擬高氨氮濃度廢水中,氨氮降解率僅為21.90%。
本研究利用以NH4Cl為唯一氮源的選擇性培養(yǎng)基,通過平板馴化篩選的方法以期從受發(fā)酵工業(yè)污水污染嚴(yán)重的土壤中篩得一株具有高濃度氨氮耐受的高效除氨氮菌株,對(duì)其進(jìn)行菌株形態(tài)分析、菌種鑒定、菌株除氨氮性質(zhì)研究以及菌株的高氨氮耐受能力測定,并通過單因素、正交試驗(yàn)優(yōu)化確定菌株最佳氨氮去除條件,為其未來可能開展的工業(yè)化應(yīng)用提供理論基礎(chǔ)。
1 材料與方法
1.1 材料與儀器
污染土壤 2018年9月于石家莊欒城區(qū)采集受發(fā)酵工業(yè)污水污染嚴(yán)重的土壤,用采樣鏟刮去表面0.5~1.0 cm的表層土壤后垂直向下切取約1.0~10.0 cm深度的土壤,約200 g放入無菌采樣袋中;C2H3NaO2上海麥克林生化科技有限公司;胰蛋白胨、酵母粉、瓊脂、NaCl、MgSO4·7H2O 北京索萊寶科技有限公司;K2HPO4天津市鼎盛鑫化工有限公司;MnSO4·4H2O 天津市河?xùn)|區(qū)紅巖試劑廠;FeSO4北京市奧博星生物技術(shù)有限責(zé)任公司;NH4Cl 北京市奧博星生物技術(shù)有限責(zé)任公司。
T1000電子天平 常熟市雙杰測試儀器廠;ME104/02分析天平 梅特勒-托利多(上海)有限公司;STARTER3100/F電子pH計(jì) 奧豪斯(上海)有限公司;HJ-4AS磁力攪拌器 江蘇省金壇市榮華儀器公司;移液器 大龍醫(yī)療設(shè)備有限公司;BCD-189WDPV冰箱 海爾公司;DW-HL100超低溫冷凍儲(chǔ)存箱 中科美菱;SW-CJ-1FD單人單面垂直凈化工作臺(tái) 上海博訊實(shí)業(yè)有限公司醫(yī)療設(shè)備廠;YXQ-30SII立式壓力蒸汽滅菌器 上海博訊實(shí)業(yè)有限公司醫(yī)療設(shè)備廠;ZWYR-4912恒溫培養(yǎng)振蕩器 上海智城分析儀器制造有限公司;UV-5800(PC)紫外可見分光光度計(jì) 上海元析儀器有限公司;BA410E顯微鏡 麥克奧迪實(shí)業(yè)集團(tuán)有限公司。
1.2 實(shí)驗(yàn)方法
1.2.1 培養(yǎng)基配制 LB培養(yǎng)基(g/L):胰蛋白胨10.0,酵母粉5.0,NaCl 10.0,pH7.0;
微量元素液(g/L):CoCl2·6H2O 0.1,MnCl2·4H2O 0.425,ZnCl20.05,NiCl2·6H2O 0.01,CuSO4·5H2O 0.015,Na2MoO4·2H2O 0.01,Na2SeO4·2H2O 0.01;
富集培養(yǎng)基(g/L):NH4Cl 0.352,胰蛋白胨10.0,酵母粉5.0,NaCl 10.0,pH7.0;
初篩無機(jī)鹽培養(yǎng)基(g/L):C2H3NaO22.0,MgSO4·7H2O 0.05,K2HPO40.2,NaCl 0.12,MnSO4·4H2O 0.01,F(xiàn)eSO40.01,NH4Cl 1.76,微量元素液1 mL,pH7.0;
復(fù)篩無機(jī)鹽培養(yǎng)基(g/L):C2H3NaO22.0,MgSO4·7H2O 0.05,K2HPO40.2,NaCl 0.12,MnSO4·4H2O 0.01,F(xiàn)eSO40.01,NH4Cl 0.176,微量元素液1 mL,pH7.0;
斜面培養(yǎng)基:100 mL富集培養(yǎng)基加1.0 g瓊脂;
初始培養(yǎng)基(g/L):C2H3NaO22.0,MgSO4·7H2O 0.05,K2HPO40.2,NaCl 0.12,MnSO4·4H2O 0.01,F(xiàn)eSO40.01,NH4Cl 0.352,微量元素液1 mL,pH7.0;
高濃度氨氮培養(yǎng)基(g/L):C2H3NaO211.0,MgSO4·7H2O 0.25,K2HPO41.0,NaCl 0.60,MnSO4·4H2O 0.05,F(xiàn)eSO40.05,NH4Cl 1.76,微量元素液5 mL,pH8.0。
1.2.2 菌株分離篩選 取10 g土壤樣品加入到含玻璃珠的100 mL無菌水中,手動(dòng)振蕩打碎10 min,靜止片刻后取10 mL液體加入到90 mL富集培養(yǎng)基中于28 ℃,160 r/min培養(yǎng)24 h,獲得富集菌液,然后將富集菌液按5%的接種量接種于初篩無機(jī)鹽培養(yǎng)基中,重復(fù)篩選兩次。通過稀釋涂布平板法將篩選后的菌液以10-3、10-4、10-5、10-6四個(gè)濃度梯度涂布于斜面培養(yǎng)基固體平板上,28 ℃倒置培養(yǎng)進(jìn)行初篩[20]。獲得單菌落后對(duì)菌落進(jìn)行純化(重復(fù)2~3次劃線)并保存。
1.2.3 菌株生長特性及除氨氮能力分析 將初篩得到的6株單菌株接入LB培養(yǎng)基中,160 r/min,28 ℃培養(yǎng)至OD600nm值為1.0,將菌液離心沉淀,棄去上清液,并重懸于相等體積的復(fù)篩無機(jī)鹽培養(yǎng)基中;按照接種量為5%吸取2.5 mL菌懸液加入到裝液量50 mL/250 mL、氨氮初始濃度為50 mg/L的復(fù)篩無機(jī)鹽培養(yǎng)基中,160 r/min,28 ℃培養(yǎng),每隔2 h測定培養(yǎng)基OD600nm,取6株單菌株發(fā)酵20 h時(shí)的發(fā)酵液各10 mL,12000 r/min離心15 min獲取上清液,利用納氏試劑光度法[21]測定上清液中氨氮的含量,根據(jù)式(1)進(jìn)行氨氮去除率計(jì)算,并繪制菌體生長曲線和6株菌20 h氨氮去除情況表格,來驗(yàn)證不同菌株的生長繁殖能力和對(duì)氨氮的去除性能,確定最優(yōu)氨氮去除菌株。
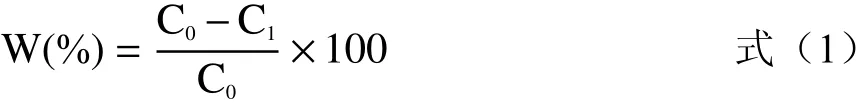
式中:W為氨氮去除率,%;C0為初始氨氮濃度,mg/L;C1為剩余氨氮濃度,mg/L。
將篩選獲得的最優(yōu)除氨氮菌株重復(fù)上述培養(yǎng)操作,每隔2 h取樣,氨氮(NH4+-N)的測量方法為納氏試劑光度法,根據(jù)參考文獻(xiàn)[21-22];NO2-N用N-(1-萘基)乙二胺光度法測定,NO3-N用紫外分光光度法測定。根據(jù)測定的氨氮、硝酸鹽氮、亞硝酸鹽氮含量,繪制菌株除氨氮特性圖。
1.2.4 菌株鑒定 將篩得的最優(yōu)單菌株N-2接種于LB培養(yǎng)基中,28 ℃、160 r/min過夜培養(yǎng),取1 mL培養(yǎng)液置于離心管中,經(jīng)12000 r/min離心2 min后,棄上清液,收集菌體,經(jīng)無菌水漂洗后的菌體,用細(xì)菌基因組試劑盒提取DNA。
細(xì)菌16S rRNA基因擴(kuò)增通用引物為27F(5'-AGAGTTTGATCCTGGCTCAG-3')和1492R(5'-GGTTACCTTGTTACGACTT-3'),PCR反應(yīng)體系為20 μL(10×PCR Buffer 2 μL,10 μmol/L引物各0.5 μL,(10 mmol/L)dNTP 0.5 μL,DNA模板2 μL,ddH2O 14 μL,Taq Plus DNA Polymerase(5 U/μL)0.5 μL),PCR擴(kuò)增條件:95 ℃ 5 min;94 ℃ 30 s;57 ℃30 s;72 ℃ 90 s;30個(gè)循環(huán);最后72 ℃延伸8 min。PCR產(chǎn)物經(jīng)1.5%瓊脂糖凝膠電泳檢測后,委托生工生物工程(上海)股份有限公司對(duì)細(xì)菌序列進(jìn)行雙向測序。將測序完成并拼接后的1481 bp的16S rRNA基因序列上傳至NCBI獲得登錄號(hào)GenBank accession number MT084039,并進(jìn)行BLASTn(www.ncbi.nlm.nih.gov/BLAST)相似性比對(duì)。下載BLAST比對(duì)序列相似性較高的菌株序列,利用MEGA 5.05軟件計(jì)算序列相似度,同時(shí)用鄰接法(neighbor-joining method)構(gòu)建菌株系統(tǒng)發(fā)育樹,確定物種的系統(tǒng)發(fā)育地位。
1.2.5 N-2菌株氨氮濃度耐受性分析 將初始培養(yǎng)基中0.352 g/L的NH4Cl分別調(diào)整為0.176、0.352、1.76、3.52、7.04、10.56、14.08、21.12和28.16 g/L,乙酸鈉和其他成分含量也做相應(yīng)調(diào)整,使培養(yǎng)基中氨氮濃度分別為50、100、500、1000、2000、3000、4000、6000和8000 mg/L,制備高濃度氨氮(50 mg/L除外)模擬廢水。
將N-2單菌株接入LB培養(yǎng)基中,160 r/min,28 ℃培養(yǎng)至OD600nm值為1.0,按照接種量為5%,分別吸取2.5 mL菌液離心棄上清后重新懸浮于2.5 mL無菌初始培養(yǎng)基中,加入到上述不同氨氮濃度50 mL/250 mL模擬廢水中,160 r/min,28 ℃培養(yǎng)10 h測定剩余氨氮的含量,驗(yàn)證N-2菌株對(duì)高濃度氨氮的耐受和去除能力。
1.2.6 不同培養(yǎng)條件對(duì)氨氮去除率的影響 將單克隆菌株N-2接種于LB培養(yǎng)基中,在28 ℃、160 r/min條件下培養(yǎng)至OD600nm值為1.0,收集70 mL培養(yǎng)液在12000 r/min離心2 min,棄上清液,用初始培養(yǎng)基重懸至70 mL后作為種子液備用。
1.2.6.1 不同pH對(duì)氨氮去除率的影響 將種子液以5%接種量接種于氨氮濃度為100 mg/L的初始培養(yǎng)基中,pH設(shè)置為5.0、6.0、7.0、8.0和9.0這5個(gè)梯度,28 ℃、160 r/min振蕩培養(yǎng)10 h,考察pH對(duì)菌株N-2氨氮去除率的影響。
1.2.6.2 不同溫度對(duì)氨氮去除率的影響 將種子液以5%接種量接種于氨氮濃度為100 mg/L的初始培養(yǎng)基中,溫度設(shè)置為28、30、34、37和40 ℃這5個(gè)梯度,28 ℃、160 r/min振蕩培養(yǎng)10 h,考察溫度對(duì)菌株N-2氨氮去除率的影響。
1.2.6.3 不同碳氮比對(duì)氨氮去除率的影響 將種子液以5%接種量接種于氨氮濃度為100 mg/L的初始培養(yǎng)基中,將初始培養(yǎng)基的C/N設(shè)置為5、10、15、20和25這5個(gè)梯度,28 ℃、160 r/min振蕩培養(yǎng)10 h,考察培養(yǎng)基C/N對(duì)菌株N-2氨氮去除率的影響。
1.2.6.4 不同轉(zhuǎn)速對(duì)氨氮去除率的影響 將種子液以5%接種量接種于氨氮濃度為100 mg/L的初始培養(yǎng)基中,搖床轉(zhuǎn)速設(shè)置為160、180、220、260和300 r/min 5個(gè)梯度,28 ℃振蕩培養(yǎng)10 h,考察轉(zhuǎn)速對(duì)菌株N-2氨氮去除率的影響。
1.2.6.5 不同裝液量對(duì)氨氮去除率的影響 將種子液以5%接種量接種于氨氮濃度為100 mg/L的初始培養(yǎng)基中,搖瓶裝液量設(shè)置為25、50、75、100和125 mL/250 mL5個(gè)梯度,28 ℃、160 r/min振蕩培養(yǎng)10 h,考察裝液量對(duì)菌株N-2氨氮去除率的影響。
1.2.7 正交試驗(yàn)優(yōu)化N-2菌株氨氮去除率 在培養(yǎng)條件單因素試驗(yàn)結(jié)果的基礎(chǔ)上,選擇對(duì)菌株N-2氨氮去除率影響相對(duì)較大的溫度、碳氮比、裝液量,另外增加一列空列共4個(gè)因素,設(shè)置3個(gè)水平,進(jìn)行正交試驗(yàn)(表1)。以培養(yǎng)10 h菌株對(duì)初始氨氮濃度100 mg/L模擬廢水的氨氮去除率為參考指標(biāo),發(fā)酵試驗(yàn)設(shè)計(jì)3次重復(fù),取3次試驗(yàn)的平均值作為發(fā)酵培養(yǎng)條件優(yōu)化的試驗(yàn)結(jié)果。
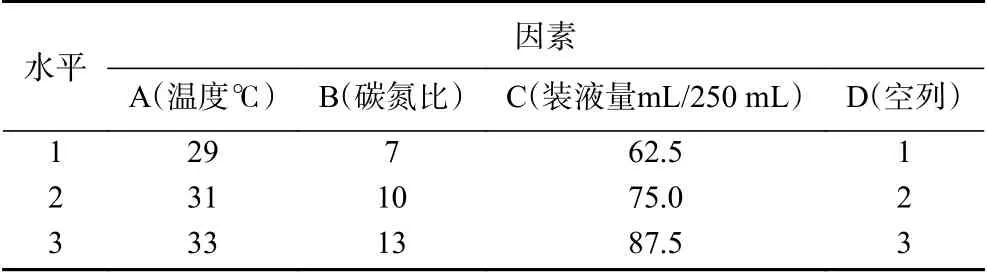
表1 正交試驗(yàn)因素與水平Table 1 The factors and levels of orthogonal experiment
1.3 數(shù)據(jù)處理
各數(shù)據(jù)均為三組的平均值,用平均值±標(biāo)準(zhǔn)差表示。利用Minitab18軟件設(shè)計(jì)正交試驗(yàn)并進(jìn)行正交試驗(yàn)結(jié)果分析,利用SPSS 22.0以及Excel對(duì)試驗(yàn)數(shù)據(jù)處理分析并進(jìn)行圖表制作。
2 結(jié)果與分析
2.1 除氨氮菌株的篩選與鑒定
2.1.1 除氨氮菌株的篩選 通過初步篩選培養(yǎng),獲得6株生長情況良好、菌落較大、可利用NH4Cl為唯一氮源的單菌株,分別命名為N-1、N-2、N-3、N-4、N-5和N-6。按照1.2.3中的方法測定6株菌的生長曲線及20 h氨氮去除率。由表2可得,與其他四株菌相比,N-2、N-3菌株氨氮去除率相對(duì)較高,可達(dá)82.90%、81.36%,具有較好的氨氮去除能力;由圖1可得,在穩(wěn)定期OD600nm大體一致的情況下,與N-3相比,N-2菌株指數(shù)期較短,能更快進(jìn)入穩(wěn)定期,生長繁殖相對(duì)較快,故將繁殖速度快且氨氮去除率高的菌株N-2保存于-80 ℃超低溫冰箱中備用。
2.1.2 N-2菌株除氨氮特性 由圖2可知,2~8 h時(shí)菌株N-2處于生長指數(shù)期,OD600nm快速增長,生長繁殖速度最快,同時(shí),模擬廢水中氨氮含量也在快速下降;8 h之后菌株達(dá)到穩(wěn)定期,OD600nm與模擬廢水中的氨氮含量均趨于穩(wěn)定,結(jié)果表明菌株生長狀況與氨氮去除情況同步;另外由圖2可以發(fā)現(xiàn)在整個(gè)氨氮去除過程中硝酸鹽氮與亞硝酸鹽氮未見明顯積累,說明氨氮并沒有轉(zhuǎn)化為硝酸氮和亞硝酸氮,菌株N-2是由細(xì)菌的同化作用將氨氮轉(zhuǎn)化為自身所需營養(yǎng)物質(zhì)。同時(shí)N-2菌株具有較快的氨氮去除性能,在10 h對(duì)初始氨氮濃度50 mg/L的氨氮模擬廢水可達(dá)到最大氨氮去除效果,此時(shí)氨氮剩余量為9.4 mg/L,利用式(1)算得氨氮去除率為81.2%,遠(yuǎn)優(yōu)于劉亞樵等[23]培養(yǎng)5 d時(shí)氨氮去除率78%的去除效果。
2.1.3 N-2菌株的鑒定 在LB固體培養(yǎng)基上菌株N-2的菌落形態(tài)為乳白色半透明狀、質(zhì)地軟且菌落表面濕潤、形狀為扁圓形、邊緣不規(guī)則;通過革蘭氏染色表明菌株N-2是革蘭氏陽性菌,在光學(xué)顯微鏡下呈短桿狀,單個(gè)隨機(jī)分布(圖3)。將測定的N-2菌株16S rRNA基因序列GenBank accession number MT084039在NCBI數(shù)據(jù)庫中進(jìn)行序列相似性比對(duì),選取BLAST中相似度最高的10株細(xì)菌序列,利用MEGA 5.05計(jì)算細(xì)菌序列相似度,并利用鄰接法(neighbor-joining method)構(gòu)建細(xì)菌系統(tǒng)發(fā)育樹,如圖4所示。菌株N-2與球形賴氨酸芽孢桿菌(Lysinibacillus sphaericusNR 042073.1)親緣關(guān)系最近。

表2 6株菌培養(yǎng)20 h時(shí)氨氮去除率Table 2 Degradation rate of ammonia nitrogen of six strains cultured for 20 h
2.2 N-2菌株對(duì)氨氮濃度耐受性分析
按照1.2.5方法通過調(diào)節(jié)水樣中銨離子濃度來測定N-2菌株對(duì)不同氨氮濃度的耐受能力和去除能力,分析結(jié)果如表3所示。結(jié)果可見,當(dāng)氨氮濃度為50 mg/L時(shí),培養(yǎng)10 h后,氨氮去除率可達(dá)82.1%;氨氮濃度為100 mg/L時(shí),培養(yǎng)10 h氨氮去除率為68.2%;當(dāng)氨氮濃度高達(dá)500 mg/L時(shí),仍有54.6%的氨氮去除率;當(dāng)氨氮濃度大于1000 mg/L,菌株N-2生長繁殖受到一定程度的抑制,OD600nm值不再隨著氨氮濃度的增高而增高,且此時(shí)氨氮去除率較低,氨氮去除效果不明顯;當(dāng)氨氮濃度達(dá)到8000 mg/L時(shí),菌株繁殖量下降。結(jié)果表明,菌株N-2具有極高的氨氮耐受性,當(dāng)氨氮濃度為6000 mg/L時(shí),菌株仍具有一定的生長繁殖能力;在氨氮去除能力方面,當(dāng)模擬廢水氨氮濃度為1000 mg/L時(shí),菌株仍具有36.5%的氨氮去除效果。為了發(fā)掘菌株N-2除氨氮的潛力,并考慮到培養(yǎng)基中其他成分對(duì)于菌株繁殖的供給能力,將培養(yǎng)條件優(yōu)化實(shí)驗(yàn)的培養(yǎng)基氨氮濃度設(shè)置為100 mg/L。此時(shí),在初始培養(yǎng)條件下菌株N-2對(duì)氨氮的去除率為68.2%。

圖1 6株菌生長曲線對(duì)比圖Fig.1 Comparison of growth curves of six strains
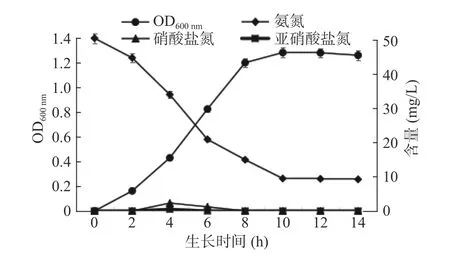
圖2 N-2菌株的生長量、氨氮、硝酸鹽氮、亞硝酸鹽氮變化情況Fig.2 N-2 strain growth, ammonia nitrogen, nitrate nitrogen,nitrite nitrogen changes
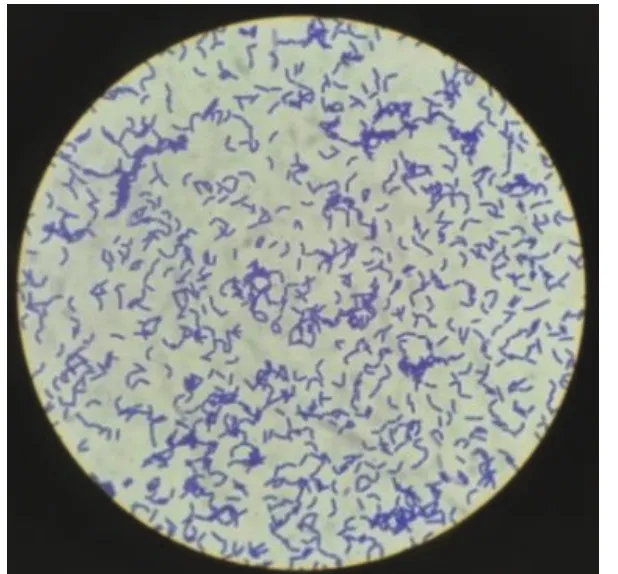
圖3 光學(xué)顯微鏡下菌株N-2革蘭氏染色圖Fig.3 Gram stain photo of N-2 under light microscope
2.3 不同培養(yǎng)條件對(duì)氨氮去除率的影響
2.3.1 不同pH對(duì)N-2菌株氨氮去除率的影響 微生物各項(xiàng)生命活動(dòng)都與酶反應(yīng)息息相關(guān),pH直接影響各種酶活力,在最適pH條件下,才可能發(fā)揮最佳酶活。如圖5A所示,當(dāng)培養(yǎng)基pH為5時(shí),菌體生長繁殖受到明顯抑制,氨氮去除率幾乎為0;當(dāng)pH大于6時(shí),氨氮去除能力不斷提高,pH為8時(shí),氨氮去除率最大,達(dá)到77.0%。實(shí)驗(yàn)結(jié)束時(shí),測定初始pH為6.0、7.0、8.0和9.0四組發(fā)酵液的終止pH,均為7.8左右。結(jié)果表明,N-2菌株最適pH為8.0左右,說明N-2菌株適合在微堿性環(huán)境下生長代謝。
2.3.2 不同溫度對(duì)N-2菌株氨氮去除率的影響 發(fā)酵溫度主要影響細(xì)胞酶活力,溫度過高或過低都會(huì)降低酶活;發(fā)酵溫度適宜,菌株才會(huì)最大限度利用培養(yǎng)基中營養(yǎng)物質(zhì)。如圖5B所示,當(dāng)N-2菌株在培養(yǎng)溫度為28~30 ℃時(shí),生長量逐漸增多,氨氮去除率不斷增大;當(dāng)N-2菌株在培養(yǎng)溫度為30~40 ℃時(shí),生長量呈下降趨勢,氨氮去除率不斷降低。結(jié)果表明,最適溫度為30 ℃,此時(shí)對(duì)氨氮的去除能力達(dá)到最大值82.0%。

圖4 菌株N-2基于16S rRNA基因序列的系統(tǒng)發(fā)育樹Fig.4 Phylogenetics tree based on 16S rRNA gene sequence of strain N-2
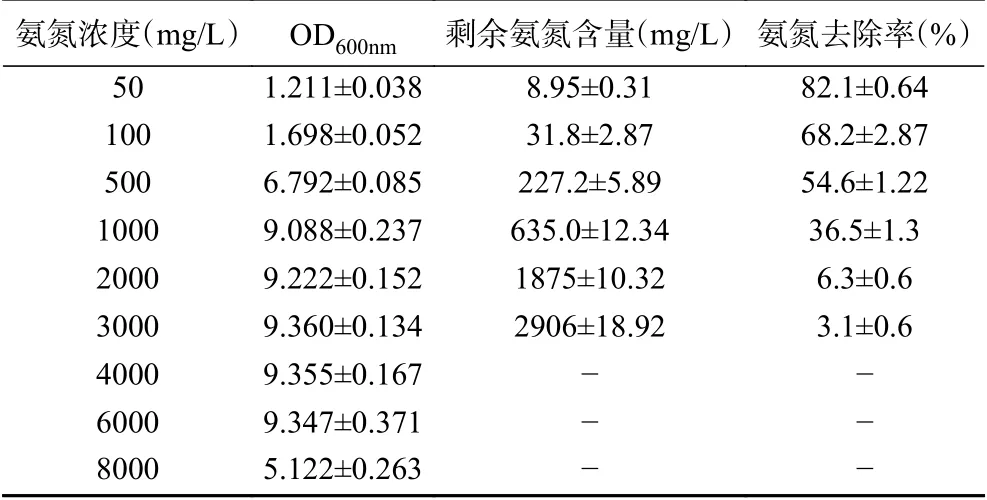
表3 菌株N-2在不同氨氮條件下的生長和去除性能Table 3 The growth and removal situation of strain N-2 under different concentrations of ammonia nitrogen
2.3.3 不同碳氮比對(duì)N-2菌株氨氮去除率的影響 碳氮比(C/N)是指培養(yǎng)基配制時(shí),碳元素與氮元素物質(zhì)的量比值。在微生物發(fā)酵培養(yǎng)中,C/N會(huì)直接影響微生物生長和發(fā)酵產(chǎn)量。如圖5C所示,當(dāng)N-2菌株在C/N為5~10時(shí),生長量逐漸增多,氨氮去除率不斷增大;當(dāng)N-2菌株在C/N為10~25時(shí),生長量呈下降趨勢,氨氮去除率不斷降低。結(jié)果表明,C/N為10時(shí)更適于N-2菌株的生長繁殖,此時(shí)氨氮去除率最大達(dá)到81.0%。
2.3.4 不同轉(zhuǎn)速對(duì)N-2菌株氨氮去除率的影響 N-2菌為異養(yǎng)好氧型芽孢桿菌,培養(yǎng)過程需要保證氧氣的供給。搖床轉(zhuǎn)速與溶氧量呈正相關(guān)。如圖5D所示,通過調(diào)整搖瓶培養(yǎng)轉(zhuǎn)速,觀察溶氧對(duì)N-2除氨氮的影響。當(dāng)轉(zhuǎn)速由160 r/min提高到180 r/min時(shí),隨著溶氧量增高,菌體生長量增高,氨氮去除率有所提高,由67.6%提高到73.5%;但當(dāng)轉(zhuǎn)速進(jìn)一步提高后,隨著溶氧量的急劇升高,細(xì)菌會(huì)產(chǎn)生大量的代謝產(chǎn)物,影響菌體生長,氨氮去除率降低。結(jié)果表明,最適轉(zhuǎn)速為180 r/min,此時(shí)對(duì)氨氮的去除能力也達(dá)到最大值73.5%。
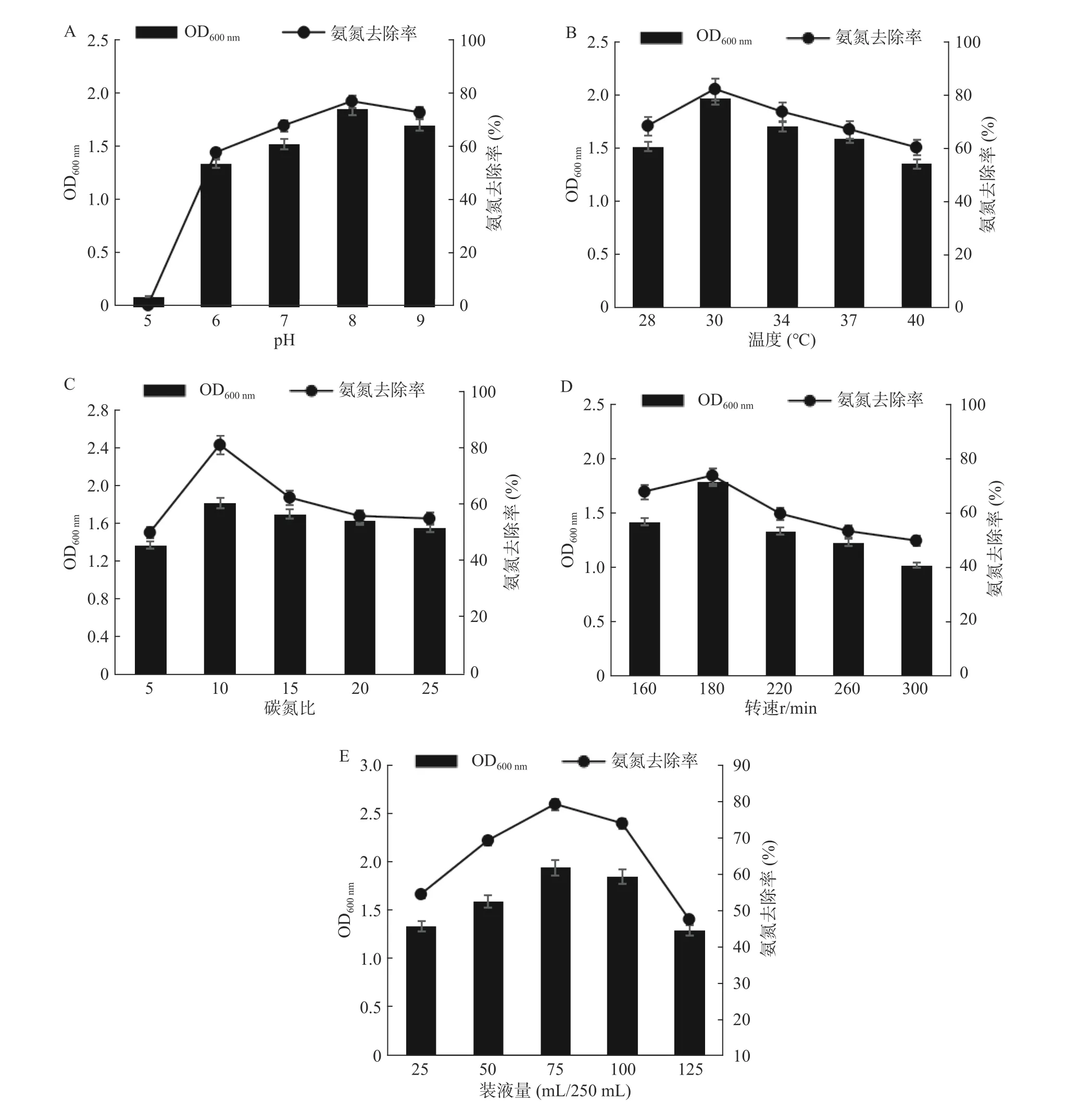
圖5 不同pH(A)、溫度(B)、碳氮比(C)、轉(zhuǎn)速(D)、裝液量(E)對(duì)N-2菌株發(fā)酵量及氨氮去除率的影響Fig.5 The effects of different pH (A), temperature (B), carbon-to-nitrogen ratio (C), rotation speed (D), and liquid volume (E) on the fermentation amount and ammonia nitrogen removal rate of N-2 strain
2.3.5 不同裝液量對(duì)N-2菌株氨氮去除率的影響 提高搖瓶裝液量在為細(xì)菌生長繁殖提供更多營養(yǎng)物質(zhì)和資源的同時(shí),也影響了溶氧量,因此適宜的裝液量有利于更好的發(fā)揮菌株性能。如圖5E所示,當(dāng)N-2菌株在裝液量為25~75 mL/250 mL時(shí),菌體生長量逐漸增多,氨氮去除率也在不斷增加;當(dāng)裝液量為75~125 mL/250 mL時(shí),菌體生長量呈下降趨勢,氨氮去除率不斷降低。結(jié)果表明,在最適裝液量75 mL/250 mL時(shí),營養(yǎng)物質(zhì)與溶氧量達(dá)到很好的平衡,菌體量最多,因此N-2氨氮去除能力達(dá)到最大值79.2%。
2.4 培養(yǎng)條件的正交試驗(yàn)結(jié)果
由上述單因素實(shí)驗(yàn)結(jié)果可知,在其他培養(yǎng)條件相同的情況下,分別進(jìn)行pH為8、轉(zhuǎn)速180 r/min、裝液量75 mL/250 mL、培養(yǎng)基C/N 10以及培養(yǎng)溫度30 ℃的單因素優(yōu)化調(diào)整后,菌株N-2對(duì)氨氮的去除率依次為77.0%、73.5%、79.2%、81.0%和82.0%。其中裝液量、培養(yǎng)基C/N和培養(yǎng)溫度對(duì)菌株N-2氨氮去除率影響較大,因此,對(duì)這三個(gè)因素做進(jìn)一步優(yōu)化處理。根據(jù)正交表L9(34),設(shè)計(jì)一個(gè)四因素三水平的正交試驗(yàn)。
在正交試驗(yàn)中,各優(yōu)化條件極差的大小反映了各個(gè)條件對(duì)菌株N-2除氨氮能力影響的主次,極差越大,影響越主要。由表4中的極差R可看出,初始溫度、碳氮比和裝液量這3個(gè)條件對(duì)除氨氮菌株發(fā)酵影響的主次因素依次為:C(裝液量)>B(碳氮比)>A(溫度);由表4中各因子的k值來看,最優(yōu)組合為A2B2C1,即溫度31 ℃,碳氮比10,裝液量62.5 mL/250 mL。由表5可得,在α=0.05的水平上,碳氮比與裝液量對(duì)菌株N-2去除氨氮有顯著性影響(P<0.05),溫度影響不顯著(P>0.05)。
鑒于其最優(yōu)組合A2B2C1不在正交試驗(yàn)設(shè)計(jì)表中,故對(duì)其最優(yōu)組合進(jìn)行試驗(yàn)驗(yàn)證,試驗(yàn)重復(fù)3次。結(jié)果表明,在最優(yōu)條件下培養(yǎng),對(duì)氨氮濃度為100 mg/L的模擬廢水10 h時(shí)氨氮去除率為91.90%(圖6A),高于其他實(shí)驗(yàn)組,結(jié)果可靠。因此,菌株N-2的最佳氨氮去除條件為接種量5%,培養(yǎng)基C/N 10,pH8.0,裝液量為62.5 mL/250 mL,溫度31 ℃,轉(zhuǎn)速180 r/min。
為有效驗(yàn)證N-2菌株在低、中、高不同氨氮濃度廢水中的最佳氨氮去除效能,以正交優(yōu)化最優(yōu)氨氮去除條件為基礎(chǔ),分別在氨氮濃度為50、100、500 mg/L的模擬廢水中培養(yǎng)10 h后取樣測定菌株氨氮去除率,結(jié)果見圖6。結(jié)果表明在此最優(yōu)培養(yǎng)條件下,菌株N-2對(duì)水體中氨氮的去除能力有了大幅度提高。初始氨氮濃度為100 mg/L時(shí),由68.2%提高為91.0%(圖6A),增幅為33.4%;初始氨氮濃度為50 mg/L時(shí),由81.2%提高為97.7%(圖6B),增幅為20.3%;初始氨氮濃度為500 mg/L時(shí),由54.6%提高為71.7%(圖6C),增幅為30.2%。

表4 正交試驗(yàn)結(jié)果Table 4 Results of orthogonal test
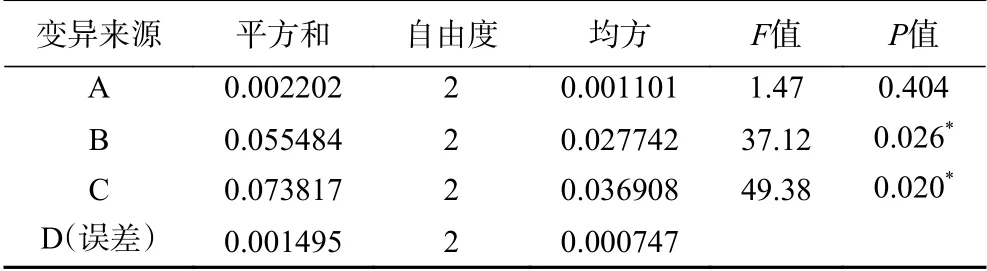
表5 正交設(shè)計(jì)方差分析Table 5 Orthogonal design variance analysis
3 結(jié)論與討論
目前廢水中氨氮的生物法去除多以利用菌株的硝化與反硝化作用為基礎(chǔ),生物硝化反硝化[24]法中無論是自養(yǎng)型還是異養(yǎng)型的硝化細(xì)菌都生長緩慢且有效菌體濃度低,并且對(duì)溫度、pH和有機(jī)物濃度等外界因素敏感,直接影響硝化作用效果[25],菌株代謝產(chǎn)生的亞硝酸鹽和N2O仍會(huì)污染環(huán)境,需二次處理。在氨氮廢水處理方面,雖已有很多其他除氨氮菌被研究發(fā)現(xiàn),但多由于氨氮耐受能力差或培養(yǎng)成本高而不適用于工業(yè)廢水的處理。
為找到更適用于高濃度氨氮工業(yè)廢水污染治理的菌種資源,本研究從受發(fā)酵工業(yè)污水污染嚴(yán)重的土壤中,通過初篩、復(fù)篩等一系列實(shí)驗(yàn)手段獲得一株高濃度氨氮耐受的除氨氮球形賴氨酸芽孢桿菌(Lysinibacillus sphaericus)N-2。通過菌株N-2氨氮濃度耐受力測定結(jié)果表明,菌株N-2具有極強(qiáng)的氨氮耐受力和去除能力,在氨氮初始濃度達(dá)到500 mg/L時(shí),該菌氨氮去除率為71.7%,明顯高于張冠根等[19]21.90%的去除效果;在氨氮濃度為6000 mg/L時(shí)菌株N-2仍能大量繁殖,8000 mg/L時(shí)稍顯抑制,該濃度已遠(yuǎn)高于通常情況下1000 mg/L左右氨氮濃度的工業(yè)廢水,菌株N-2表現(xiàn)出了潛在的處理高濃度氨氮工業(yè)廢水的產(chǎn)業(yè)化應(yīng)用價(jià)值;在菌株N-2的整個(gè)發(fā)酵過程中并未發(fā)現(xiàn)硝酸鹽氮和亞硝酸鹽氮的積累,因此推測其是利用細(xì)菌的同化作用將氨氮轉(zhuǎn)化為自身所需的營養(yǎng)物質(zhì);菌株N-2較其他已報(bào)道的可去除氨氮的芽孢桿菌[26-27]去除更加快速,為更好地發(fā)揮菌株性能,以菌株氨氮去除率為指標(biāo),通過單因素、正交試驗(yàn)對(duì)N-2菌株氨氮去除條件進(jìn)行優(yōu)化,優(yōu)化后在C/N為10,溫度為31 ℃,pH8.0,轉(zhuǎn)速180 r/min和裝液量62.5 mL/250 mL的培養(yǎng)條件下培養(yǎng)10 h,該菌對(duì)100 mg/L氨氮的最大去除率為91.0%,對(duì)50 mg/L的氨氮最大去除率可達(dá)97.7%,對(duì)500 mg/L的氨氮最大去除率可達(dá)71.7%。
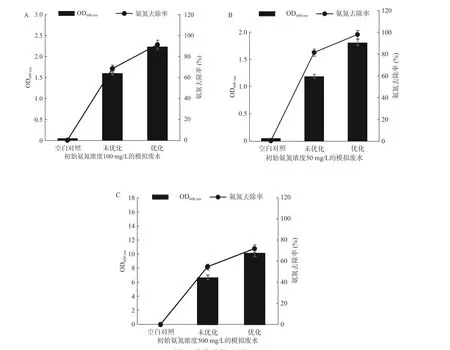
圖6 優(yōu)化效果對(duì)比圖Fig.6 Comparison chart of optimization effect
綜上所述,菌株N-2在模擬高濃度氨氮的廢水處理中表現(xiàn)優(yōu)異,具有潛在的處理高濃度氨氮工業(yè)廢水的能力,是不可多得的優(yōu)秀菌種資源。但菌株N-2吸收氨氮的機(jī)理及細(xì)胞內(nèi)氨氮的轉(zhuǎn)化途徑仍需進(jìn)一步研究,培養(yǎng)成本仍可進(jìn)一步降低,針對(duì)具體的高濃度氨氮工業(yè)廢水水質(zhì)需研發(fā)最適宜的菌劑劑型及接種方式,距離實(shí)際應(yīng)用仍具有較大差距。

