紅島蛤蜊肉酶解工藝優化及其產物降血壓功能研究
曹廷鋒,劉金麗 ,樊 芳,尹德翠,鄒圣燦
(1.青島琛藍醫藥科技發展有限公司,山東青島 266200;2.青島頤圣康和生物制藥有限公司,山東青島 266100)
蛤蜊肉的特點是高蛋白、高微量元素、高鈣、高鐵、低脂肪、低糖[1-2]。紅島蛤蜊(Ruditapes philippinarum)是青島地區極具地域特色的蛤蜊品種,除有一般蛤蜊的營養特點外,還具有皮薄、肉嫩、出肉率高的特點,并且富含優質氨基酸和豐富的寡糖[3-4]。目前人們對蛤蜊肉主要是以鮮食為主,精深加工的蛤蜊產品較少,不僅不能滿足市民對蛤蜊新產品的需求,而且蛤蜊資源沒有得到充分利用,阻礙了蛤蜊產業化進程[5]。因此,如何將高蛋白的蛤蜊資源高值化利用,對于蛤蜊產業的發展具有重要意義。
伴隨著近年來海洋科技的興起,酶工業技術在水產品中的應用越來越廣泛,利用蛋白酶制劑將水產品中的大分子蛋白水解為易吸收的小分子多肽,在食品行業中的優勢逐漸凸顯[6]。這類小分子活性肽通常還具有降血壓、降血脂、預防糖尿病、抗氧化及增強免疫力的作用[7-11]。然而酶解底物的種類及來源、酶制劑選擇以及酶解工藝不同都影響著酶解效果、產物的生物活性。如朱俊向等[12]通過動物蛋白水解酶制備南極磷蝦多肽,優化的工藝條件為50 ℃、pH8.0、加酶量2000 U/g、酶解3 h,得到的產物具有一定抗氧化能力,可清除羥自由基和還原鐵離子。陳啟航等[13]采用木瓜蛋白酶對金槍魚進行酶解,在56 ℃、加酶量300 U/g、酶解4 h的條件下可得到的金槍魚調味汁色香味俱佳。曹文紅等[14]優化的牡蠣肽酶解工藝為風味蛋白酶加酶量5000 U/g、pH6.5、酶解5 h,此工藝下的酶解產物分子量小于1000 Da的占比為43.13%。目前海洋源肽的制備主要以南極磷蝦、牡蠣、海參、鮑魚等高值水產品為原料,而有關經濟水產品蛤蜊酶解制備多肽的報道較少。此外,據相關蛤蜊肽研究報道[1,4-5],目前研究主要集中在酶解工藝的優化,鮮有對蛤蜊肽的相對分子量分布及降血壓活性的報道。
本研究以紅島蛤蜊為原料,以水解度為指標,首先篩選出適宜于紅島蛤蜊水解蛋白酶,通過單因素和正交試驗對酶解工藝進行優化,得到富含小分子多肽的蛤蜊肽粉。并對肽粉相對分子量分布和ACE抑制率進行測定,研究其降血壓功能,為蛤蜊肉的精深加工和高值化利用提供實驗依據。
1 材料與方法
1.1 材料與儀器
新鮮紅島蛤蜊 青島城陽區西大洋社區市場;復合蛋白酶 40萬U/g、中性蛋白酶 30萬U/g、風味蛋白酶 10萬U/g 滄州夏盛酶生物技術有限公司;堿性蛋白酶 40萬U/g、木瓜蛋白酶 100萬U/g 武漢秉德生物科技有限公司;硫酸銅、硫酸鉀、硼酸、氫氧化鈉、鹽酸 分析純,國藥集團;甲醇、乙腈 色譜純,北京沃凱生物科技有限公司;血管緊張素轉化酶 0.1 U 美國Sigma公司。
bamix GASTRO 200/PRO-3勻質機 瑞士Bamix公司;L550離心機 湘儀離心儀器有限公司;752型紫外可見分光光度計 上海舜宇恒平科學儀器有限公司;JJ-1A數顯精密增力電動攪拌器 上海雙捷實驗設備有限公司;SKD-100凱氏定氮儀 上海市沛歐分析儀器有限公司;Agilent LC1260液相色譜儀美國安捷倫公司;InertSustain AQ-C18色譜柱 日本島津公司;TSK gel G2000 SWXL 色譜柱 日本東曹株式會社。
1.2 實驗方法
1.2.1 原料預處理 將新鮮蛤蜊開殼取肉后用純水清洗干凈,瀝水后分裝,置-20 ℃冰箱保存。
1.2.2 紅島蛤蜊肉酶解工藝 參照馮金曉等[4]的工藝略有修改。稱取一定量的蛤蜊肉原料,勻漿后按設定的料液比加入純水,用1 mol/L NaOH溶液和1 mol/L HCl溶液調節最適的pH,然后加入適量的酶制劑,置于恒溫水浴鍋中攪拌酶解。酶解4 h后,沸水浴滅酶10 min,冰水冷卻后4000 r/min離心30 min,取上清液,得蛤蜊肽酶解液。
1.2.3 紅島蛤蜊肉營養成分的測定 水分含量的測定:直接干燥法[15];總蛋白含量測定:凱氏定氮法[15];灰分測定:高溫灼燒法[15];粗脂肪測定:索氏抽提法[15];氨基酸態氮含量測定:中性甲醛電位滴定法[15];總糖測定:苯酚硫酸法[16]。
1.2.4 蛋白酶制劑篩選與單因素實驗
1.2.4.1 蛋白酶制劑的篩選 稱取200 g蛤蜊肉,勻漿,按料液比1:1加入純水。選取了5種蛋白酶制劑:復合蛋白酶、風味蛋白酶、中性蛋白酶、堿性蛋白酶、木瓜蛋白酶。在加酶量1000 U/g以及各酶的建議pH和溫度下水解2 h,具體酶解條件見表1。以水解度為指標,選出紅島蛤蜊肉酶解的最佳蛋白酶。
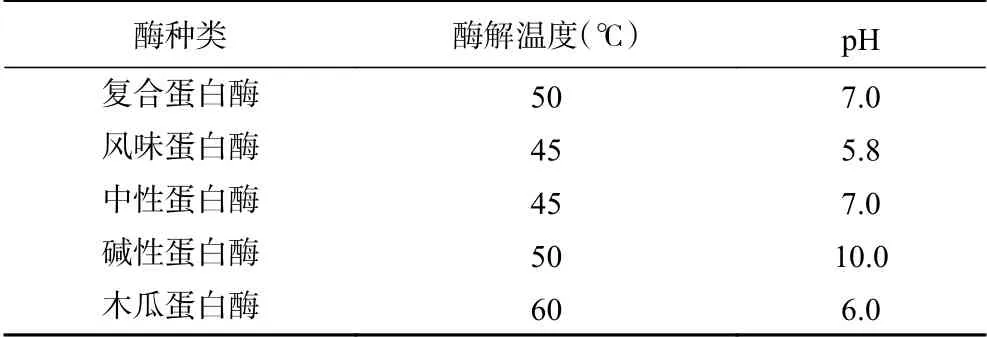
表1 不同蛋白酶水解條件Table 1 Hydrolysis conditions of different proteases
1.2.4.2 酶解溫度的影響 稱取200 g蛤蜊肉5份,分別勻漿,按料液比1:2加純水混勻。溫度設定為45、50、55、60、65 ℃,調節pH7.0,選擇復合蛋白酶,加酶量1000 U/g原料肉,酶解時間為4 h。其余步驟按“1.2.2”操作。取酶解液測水解度。
1.2.4.3 初始pH的影響 稱取200 g蛤蜊肉5份,勻漿。初始pH分別為5.0、6.0、7.0、8.0、9.0,溫度為單因素實驗中最適值,其他酶解條件同“1.2.4.2”。取酶解液測水解度。
1.2.4.4 料液比的影響 稱取200 g蛤蜊肉5份,勻漿,依次按料液比1:1、1:1.5、1:2、1:2.5、1:3加純水攪勻,溫度和pH為單因素實驗中最適值,其他酶解條件同“1.2.4.2”。取酶解液測水解度。
1.2.4.5 加酶量的確定 稱取200 g蛤蜊肉5份,勻漿。加酶量分別為600、800、1000、1200、1400 U/g原料肉,酶解溫度、pH和料液比為單因素實驗中最適值,其他酶解條件同“1.2.4.2”。取酶解液測水解度。
1.2.4.6 酶解時間的影響 稱取200 g蛤蜊肉5份,勻漿。酶解時間設定為2、4、6、8、10 h,酶解溫度、pH、料液比和加酶量為單因素實驗中最適值,其他酶解條件同“1.2.4.2”。酶解結束后測定酶解液水解度。
1.2.5 紅島蛤蜊肉酶解正交試驗 在單因素酶解實驗的基礎上,選擇對酶解結果影響較關鍵的溫度、時間、料液比三因素,以水解度為指標,進行L9(34)正交試驗進行酶解工藝的優化,試驗因素與水平見表2。

表2 正交試驗設計因素水平表Table 2 Factors and levels of orthogonal test
1.2.6 水解度的測定和計算 水解度的測定參見文獻[14]中的方法,水解度的計算公式為:

式中:A:原料中總氮含量,g/100 g; B:水解液中氨基氮含量,g/100 g;C:原料游離的氨基氮含量,g/100 g;D:原料中非蛋白氮含量,g/100 g。
1.2.7 蛤蜊肽分子量分布的檢測
1.2.7.1 酶解蛤蜊肽樣品的制備 按優化后的工藝條件制備的酶解液,經滅酶、真空抽濾分別通過0.8、0.45 μm的微濾膜,然后經冷凍干燥制得蛤蜊肽粉,用于分子量分布及降血壓功能分析。
1.2.7.2 分子量分布的檢測 采用高效液相色譜法[14,17]測定蛤蜊肽分子量分布情況。測定條件:色譜柱為TSKgel G2000 SWXL(7.8 mm×300 mm)凝膠柱;流動相為乙腈:水:三氟乙酸=45:55:0.1(體積比);紫外檢測器的波長設為220 nm;泵流速設為0.5 mL/min;柱溫設為30 ℃;進樣體積為10 μL。肽標準品:細胞色素C(Mw 12355)、抑肽酶(Mw 6511)、桿菌酶(Mw 1422)、乙氨酸-乙氨酸-酪氨酸-精氨酸(Mw 451)、乙氨酸-乙氨酸-乙氨酸(Mw 189),將各多肽標準品用流動相配制成1.0 g/L的溶液,經0.22 μm聚四氟乙烯膜過濾后進樣,以各標準品相對分子量對保留時間作圖,得到標準曲線和線性回歸方程。將蛤蜊肽粉配制成5 mg/mL的樣品,相同條件下進行色譜分析,利用GPC數據分析計算分子量分布。
1.2.8 體外ACE抑制率的檢測 將蛤蜊肽按Cushman等[18]改進的方法制備反應液,一定量的蛤蜊肽粉溶解在5 mmol/L的硼酸緩沖液(pH8.3,0.3 mol/L NaCl)中,取20 μL樣品加入50 μL 2.5 mmol/L馬尿酸-組氨酰-亮氨酸(Hip-His-Leu, HHL),混勻,37 ℃預熱6 min,加入10 μL 0.1 U ACE,37 ℃反應30 min,加入100 μL 1 mol/L HCl終止反應。空白對照采用5 mmol/L硼酸緩沖液代替樣品。
采用高效液相色譜法測定蛤蜊肽ACE抑制率[19],色譜條件如下:InertSustain AQ-C18色譜柱(4.6 mm×150 mm),流動相:A,含0.1%三氟乙酸的純水;B,乙腈。按如下梯度洗脫:0~10 min,5%~60%B;10~12 min,60%B;12~13 min,60%~5%B;13~17 min,5%B。抑制率計算公式為:
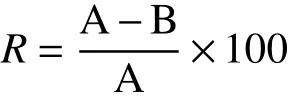
式中:R:酶解樣品對ACE的抑制率,%;A:空白對照組中馬尿酸的峰面積;B:添加蛤蜊肽粉樣品組中馬尿酸的峰面積;IC50值:當ACE抑制率為50%時的肽粉溶液濃度,mg/mL。
1.3 數據處理
每次實驗設3組平行,數據采用 表示,用Excel、Origin 8.0、SPSS統計分析軟件對數據進行分析處理及圖表的制作。GPC數據分析軟件統計不同分子量占比,ELISA數據擬合處理軟件對數據進行多項式擬合。

表3 紅島蛤蜊營養成分表Table 3 Nutrients in Hongdao clam
2 結果與分析
2.1 紅島蛤蜊肉營養成分
紅島蛤蜊是一類營養豐富,味道鮮美的海洋貝類,為更好地了解和利用蛤蜊中的營養成分,對其組成成分進行分析,見表3。紅島蛤蜊除水分外的主要成分是蛋白質,含量17.68%±0.38%,換算干基重為68.81%±1.46%,高于一般陸地動物肉的蛋白含量[20],在常見貝類中也屬于較高的水平[21]。蛤蜊肉脂肪含量低于普通肉類食品,是低脂食品的優選。蛤蜊肉總糖中含有較高的低分子量寡糖和低聚糖,這可能是紅島蛤蜊風味偏甜順口的主要原因。灰分占比較高,換算干基重為6.67%±0.02%,高于一般肉類產品,說明紅島蛤蜊中含豐富的無機礦物質。綜上而言,紅島蛤蜊是一種高蛋白、低脂肪的高營養健康食品。
2.2 蛋白酶制劑的篩選
蛋白酶是可以水解蛋白質肽鍵的一類酶的總稱,不同蛋白酶對蛤蜊肉蛋白的水解位點不同,水解度也會有差異。本研究選取了酶解水產品常用的5種蛋白酶:復合蛋白酶、中性蛋白酶、風味蛋白酶、堿性蛋白酶、木瓜蛋白酶,以水解度為指標,酶解結果如圖1所示。復合蛋白酶對蛤蜊肉的水解度最高,為50.29%±0.21%,因此選擇復合蛋白酶進行酶解實驗。
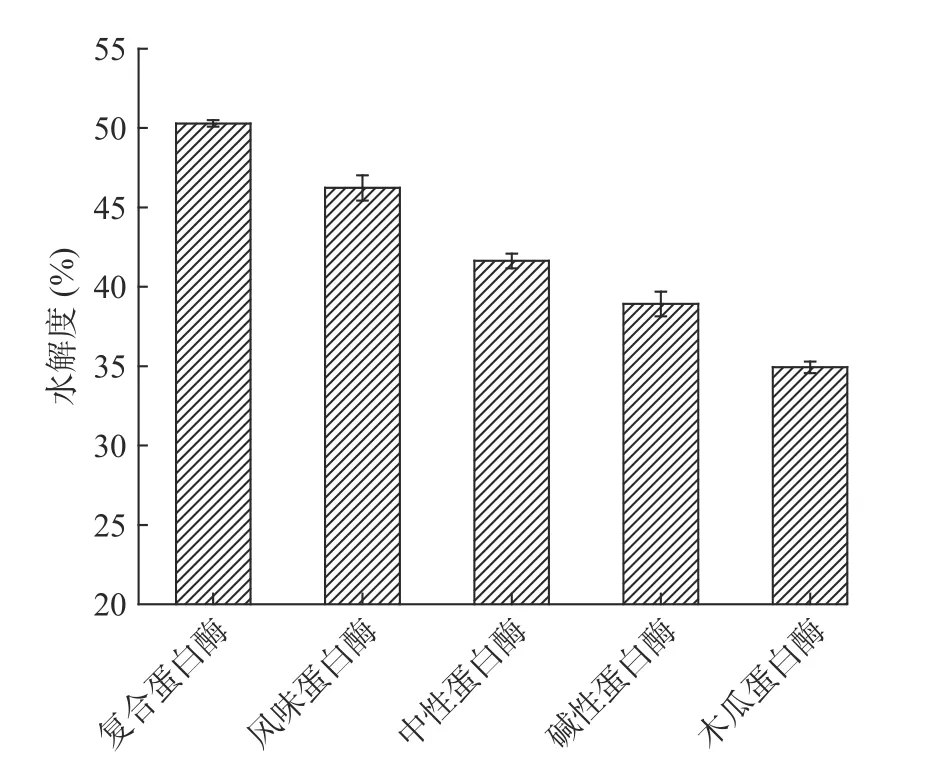
圖1 不同蛋白酶對水解度的影響Fig.1 Effects of different proteases on the degree of hydrolysis
2.3 單因素實驗結果
2.3.1 酶解溫度的影響 酶解溫度對水解度影響如圖2所示。當溫度在45~55 ℃時,隨溫度升高,酶活增大,水解度持續增加,55 ℃時水解度達到最大值66.52%±0.65%。當溫度繼續升高,水解度下降,這主要是因為酶解溫度過高,導致部分蛋白酶的結構遭到破壞、變性,酶活降低。因此復合蛋白酶酶解紅島蛤蜊肉的適宜溫度為55 ℃。

圖2 酶解溫度對水解度的影響Fig.2 Effect of hydrolysis temperature on the degree of hydrolysis
2.3.2 初始pH的影響 酶解初始pH對水解度的影響如圖3所示。隨pH的升高,酶解液的水解度首先呈迅速升高趨勢,pH7.0時,水解度為65.40%±0.21%。當pH大于8.0時水解度顯著下降(P<0.05),可能是堿性環境破壞了酶的空間結構,造成酶活降低。在復合蛋白酶可耐受pH7.0~8.0的范圍內,水解度無顯著性差異(P>0.05),且pH=7.0最接近原料肉的自然pH,同時中性環境對生產設備損害較小,故選擇酶解體系最適pH為7.0,正交試驗中不再對這一因素進行優化。
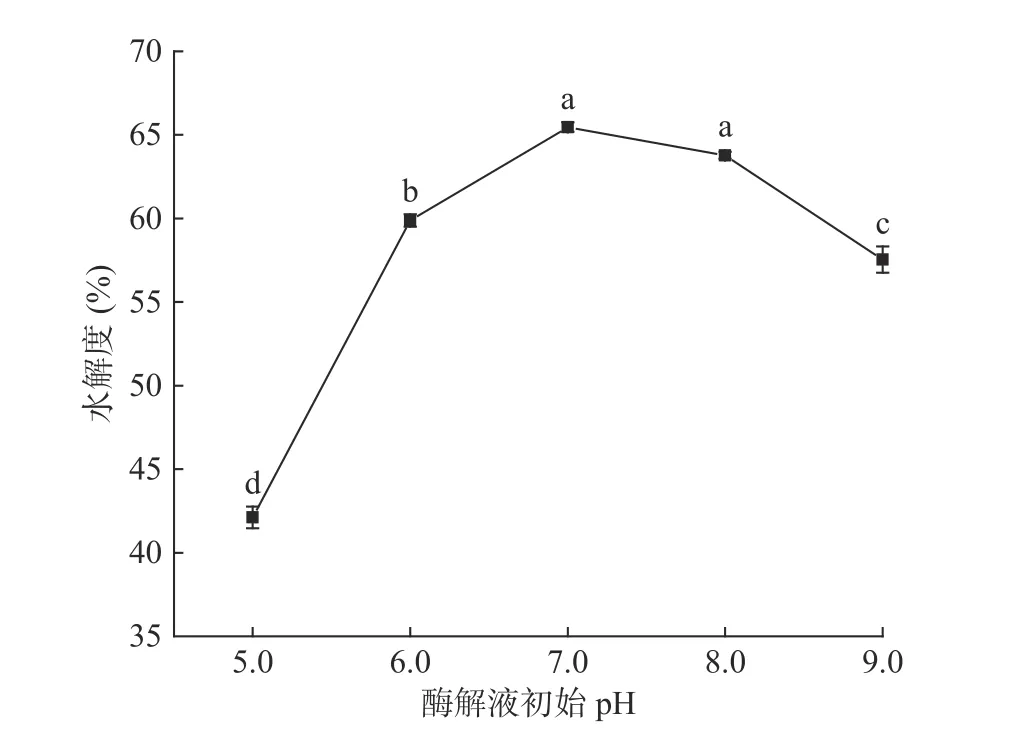
圖3 初始pH對水解度的影響Fig.3 Effect of initial pH on the degree of hydrolysis
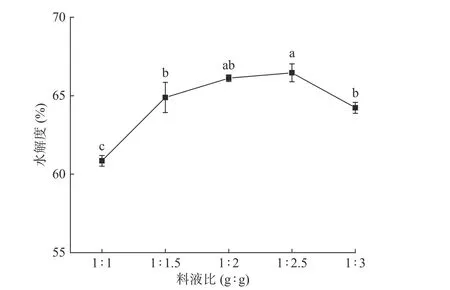
圖4 料液比對水解度的影響Fig.4 Effect of material liquid ratio on the degree of hydrolysis
2.3.3 料液比的影響 料液比對蛤蜊肉酶解產物水解度的影響如圖4所示。結果表明,酶解液水解度隨料液比增大呈現先上升后下降的趨勢,當料液比為1:2.5時,水解度達到最大值為66.46%±0.57%,但與料液比為1:2時無顯著性差異(P>0.05)。當料液比較小時,酶解體系較黏稠,流動性差,阻礙蛋白酶分子與酶解底物的擴散[22],使酶與底物無法充分結合。隨料液比增大,復合蛋白酶分子充分參與到酶解反應中,料液比處于1:1.5~1:2.5之間,水解度趨于平緩。料液比繼續增大到1:3時,水解度下降,推測是體系中底物濃度降低,酶與底物接觸不充分[23],不利于酶解。因此選擇水解度最高的料液比1:2。
2.3.4 加酶量的確定 紅島蛤蜊肉酶解液的水解度隨復合蛋白酶用量的增加變化趨勢如圖5所示。結果顯示在選擇的加酶量范圍內,水解度隨加酶量的增多而增大,加酶量為1000 U/g時,水解度為66.27%±0.28%,之后繼續增加酶量,水解度趨于平穩。酶解開始時,增加酶用量會增加酶與底物的接觸率,促進水解反應,當酶量增加到一定程度,過多的酶解產物可能對酶解反應產生反饋抑制作用[24]。合理的酶添加量不僅可以達到滿意的酶解效果,同時避免酶的浪費。由以上分析可知,加酶量為1000 U/g時,加酶量趨于飽和,因此,加酶量選擇1000 U/g,在正交試驗中不再對此因素進行優化。

圖5 加酶量對水解度的影響Fig.5 Effect of enzyme dosage on the degree of hydrolysis
2.3.5 酶解時間的影響 酶解時間對紅島蛤蜊肉酶解效果的影響如圖6所示。酶解初始階段2~4 h,水解度迅速增加,4 h已達水解度66.13%±0.70%,時間繼續延長,水解度變化趨緩。因為反應剛開始時,酶和底物濃度均較高,酶解速度較快,隨反應進行,酶解產物逐漸積累,一方面是游離肽的增多導致產物的抑制作用增強,另一方面可能是因為酶解體系的pH發生變化使酶活降低。綜合考慮,選擇酶解時間為4 h左右。
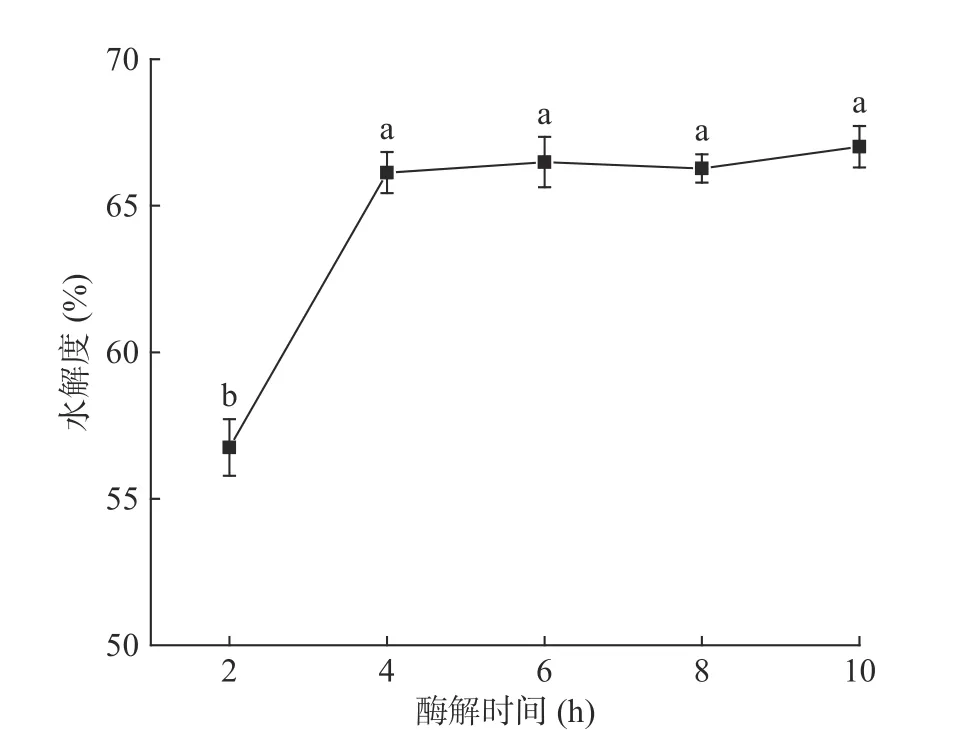
圖6 酶解時間對水解度的影響Fig.6 Effect of hydrolysis time on the degree of hydrolysis
2.4 正交試驗優化酶解工藝
2.4.1 酶解工藝參數優化正交試驗結果 復合蛋白酶水解紅島蛤蜊肉的正交試驗結果及方差分析見表4、表5。由直觀分析結果可以看出,對水解度影響的大小順序為:B(酶解時間)>C(料液比)>A(酶解溫度)。復合蛋白酶酶解紅島蛤蜊肉的最佳工藝參數為:A3B3C2。方差分析顯示,酶解時間對水解度有顯著影響,酶解溫度與料液比影響均不顯著。故以直觀分析結果作為最佳優化條件,即:酶解溫度58 ℃、酶解時間6 h、料液比1:2,在此條件下,水解度為71.58%。
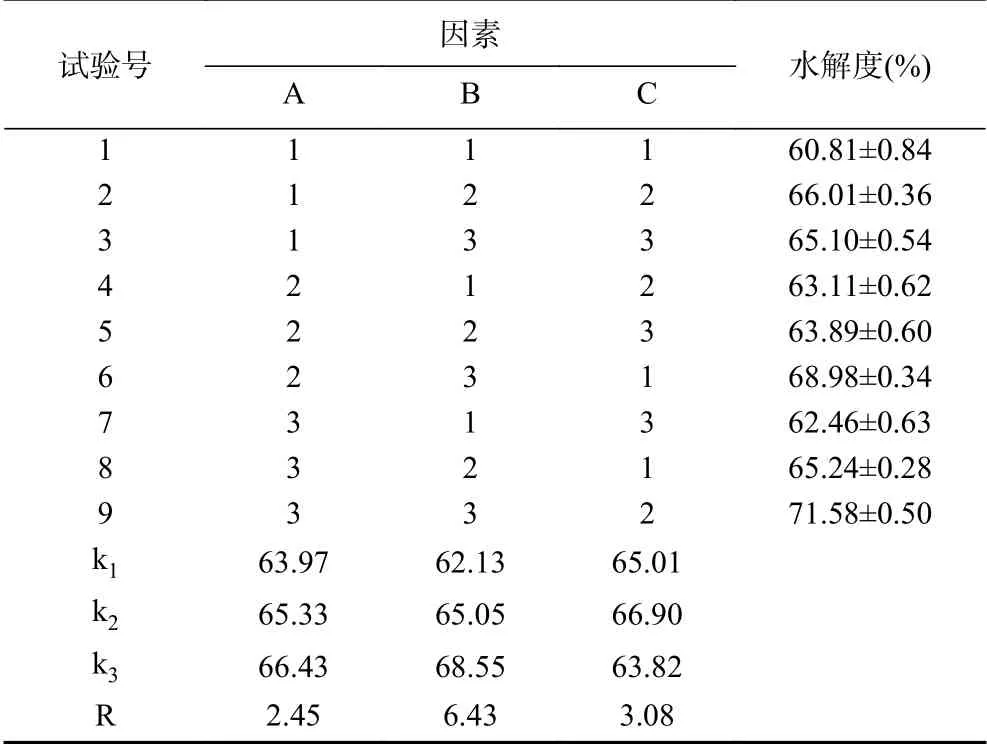
表4 正交試驗設計及結果Table 4 Design and results of orthogonal test
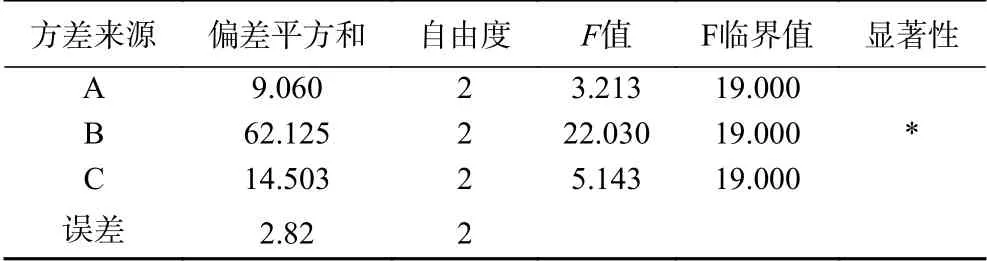
表5 正交實驗方差分析Table 5 Analysis of variance of orthogonal test
2.4.2 最優組合條件驗證 稱取200 g紅島蛤蜊肉,勻漿后調節pH7.0,按料液比1:2加入純水,加酶量1000 U/g,于58 ℃下水解6 h后,制備酶解液。重復驗證三次,測得蛤蜊肉的水解度為71.03%±0.69%,高于正交試驗中其他組合,表明優化條件穩定可信。
2.5 蛤蜊肽分子量分布
為研究蛤蜊肽降血壓活性,首先對蛤蜊肽進行分子量分布的研究,分子量分布如圖7與表6所示。結合分子質量標準曲線,利用GPC數據處理軟件計算得出:多肽Mr≤1000 Da所占比例94.29%;1000<Mr≤3000所占比例5.41%;Mr>3000所占比0.16%。結果表明在優化的工藝條件下,復合蛋白酶對紅島蛤蜊肉酶解較充分,多數蛋白大分子已被酶解為1000 Da以下的寡肽,又稱小分子活性肽,易被腸道吸收利用。有關生物肽的研究顯示[11-12],具生物活性的多肽分子質量大部分在3000 Da以下或1000 Da以下。
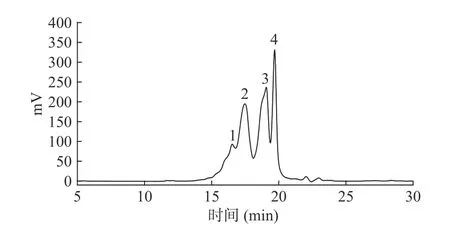
圖7 蛤蜊肽溶液分子量分布色譜圖Fig.7 Chromatogram of the molecular weight distribution of calm peptide
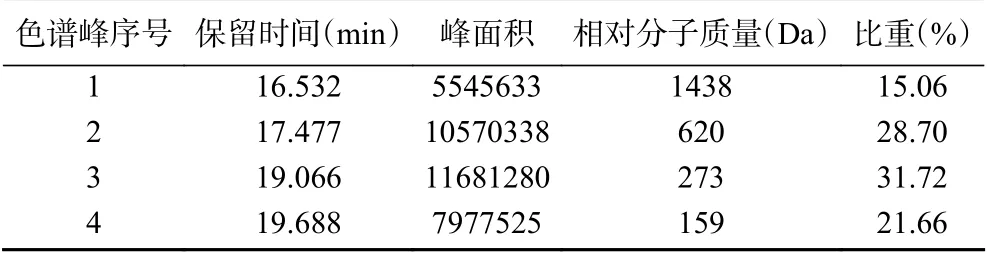
表6 蛤蜊肽相對分子質量分布Table 6 The molecular weight distribution of calm peptide
2.6 蛤蜊肽降血壓活性
蛤蜊肽的降血壓活性是通過測定體外ACE抑制率來實現的。ACE抑制肽是通過抑制ACE酶活性,來阻礙血管緊張素Ⅱ的生成以及抑制血管緩激肽的分解以達到降血壓的作用[25-27]。紅島蛤蜊肽對ACE抑制結果如圖8所示。ACE抑制率隨肽粉濃度的增加而增大,最后逐漸趨于穩定,經ELISA數據擬合并計算其IC50值為0.67 mg/mL。這表明復合蛋白酶酶解制得的紅島蛤蜊肽具有較高的ACE抑制活性。相關研究表明,食源性降壓肽主要由2~12個氨基酸組成[28],具有安全性高、分子量小、易被吸收的特點[29],因此蛤蜊肽的ACE抑制活性可能與小分子多肽有很大關系,尤其是Mr<1000 Da的寡肽在ACE活性抑制中可能起到關鍵作用。
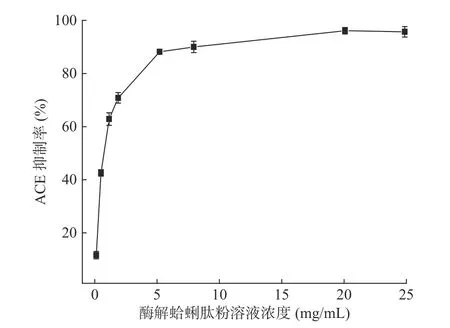
圖8 蛤蜊肽粉溶液濃度對ACE抑制率的影響Fig.8 Effect of the clam peptide content on the inhibitory rate of ACE
3 結論
紅島蛤蜊鮮肉營養豐富,是一類高蛋白低脂肪優質水產品。在篩選的5種蛋白酶中,復合蛋白酶酶解的紅島蛤蜊肉酶解效果最好。通過單因素實驗和正交試驗設計,最終優化的酶解工藝參數為:酶解溫度58 ℃、酶解時間6 h、pH為7.0、料液比1:2、加酶量1000 U/g,在此工藝條件下,水解度可達71.03%。將最優酶解工藝條件下的蛤蜊肽進行分子量分布和降血壓功能分析表明,多肽中分子量低于1000 Da的占比高達94.29%,且蛤蜊肽顯示出良好的ACE抑制率,其IC50值為0.67 mg/mL。蛤蜊肽的降血壓活性可能與分子量小于1000 Da的肽段有關,具體作用機制有待進一步研究。作為海洋來源的ACE抑制肽,蛤蜊肽有作為健康食品和功能食品生物活性原料的潛能,具有廣闊的開發和應用空間。

