黃芩及其有效成份抗腫瘤作用新進展
焦玉菡 孫四海 辛銘 徐娟娟 蔣敬敬 賈秀芹
惡性腫瘤是臨床常見疾病,因其發病率和死亡率逐年上升,已成為人類疾病三大主要死亡原因之首[1-2]。目前由于其難以治愈,且生存率低,亟需研究開發新的抗腫瘤藥物,以延長患者的生存期,提高患者的生存質量。中藥作為新型抗腫瘤藥物在臨床腫瘤藥物治療方面已顯示出其獨特優勢,如增強機體抗炎抗病毒、扶正培本、活血化瘀及避免化療藥物使用產生的毒副作用,最終達到疾病治愈和生活質量提升的目的。因此,中藥研發將為未來抗癌藥物發現及臨床應用提供新的化學庫[3]。
黃芩(ScutellariabaicalensisGeorgi)是一種廣泛應用于臨床的傳統中藥,據《神農本草經》記載,黃芩為黃芩屬草本植物,以根入藥[4],其藥用歷史悠久,具有清熱燥濕、瀉火解毒、安胎、止血、降血壓、降血脂等功效。黃芩含有多種活性成分,包括黃酮類、皂苷類、多糖類等,其藥理作用包括抗炎抗病毒、抗腫瘤、抗心血管疾病和呼吸道系統疾病等[5]。現代藥理學研究表明,黃芩中有效成分黃酮類化合物具有非常顯著的抗腫瘤作用[6],且其不同的有效成分在不同類型腫瘤細胞中顯示出不同的抗腫瘤作用機制(如表1~3所示)。黃酮類化合物迄今為止分離并鑒定了40多種,具體包括黃芩素、漢黃芩素、黃芩苷、漢黃芩苷、千層紙素A、黃芩黃酮Ⅰ、黃芩黃酮Ⅱ等[7-8]。最新研究顯示,黃芩及其有效成分抗腫瘤活性除了涉及經典的增殖、凋亡機制外,還有誘導腫瘤細胞自噬、新生血管生成、調節腫瘤微環境等。因此,本文擬從黃芩及其有效成分的抗腫瘤作用及其機制新進展進行綜述,以期為黃芩在臨床抗腫瘤方面的應用提供參考。
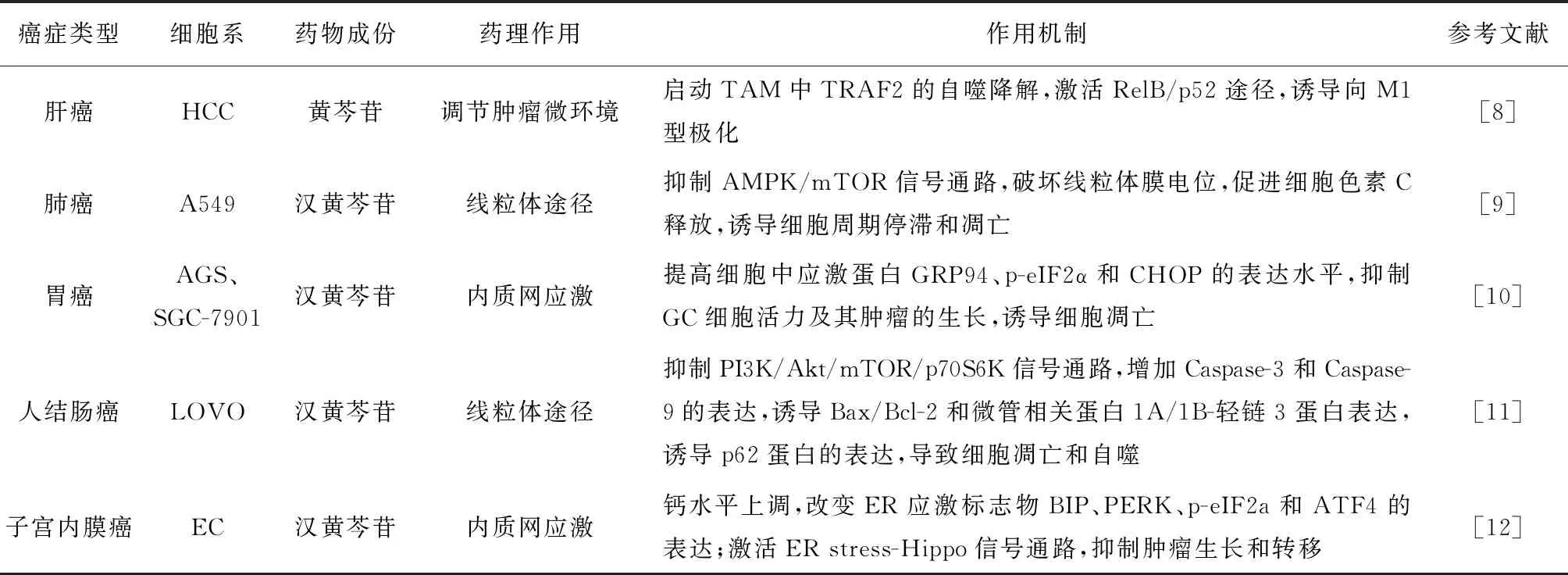
表1 黃芩苷和漢黃芩苷抗腫瘤藥理作用研究概況
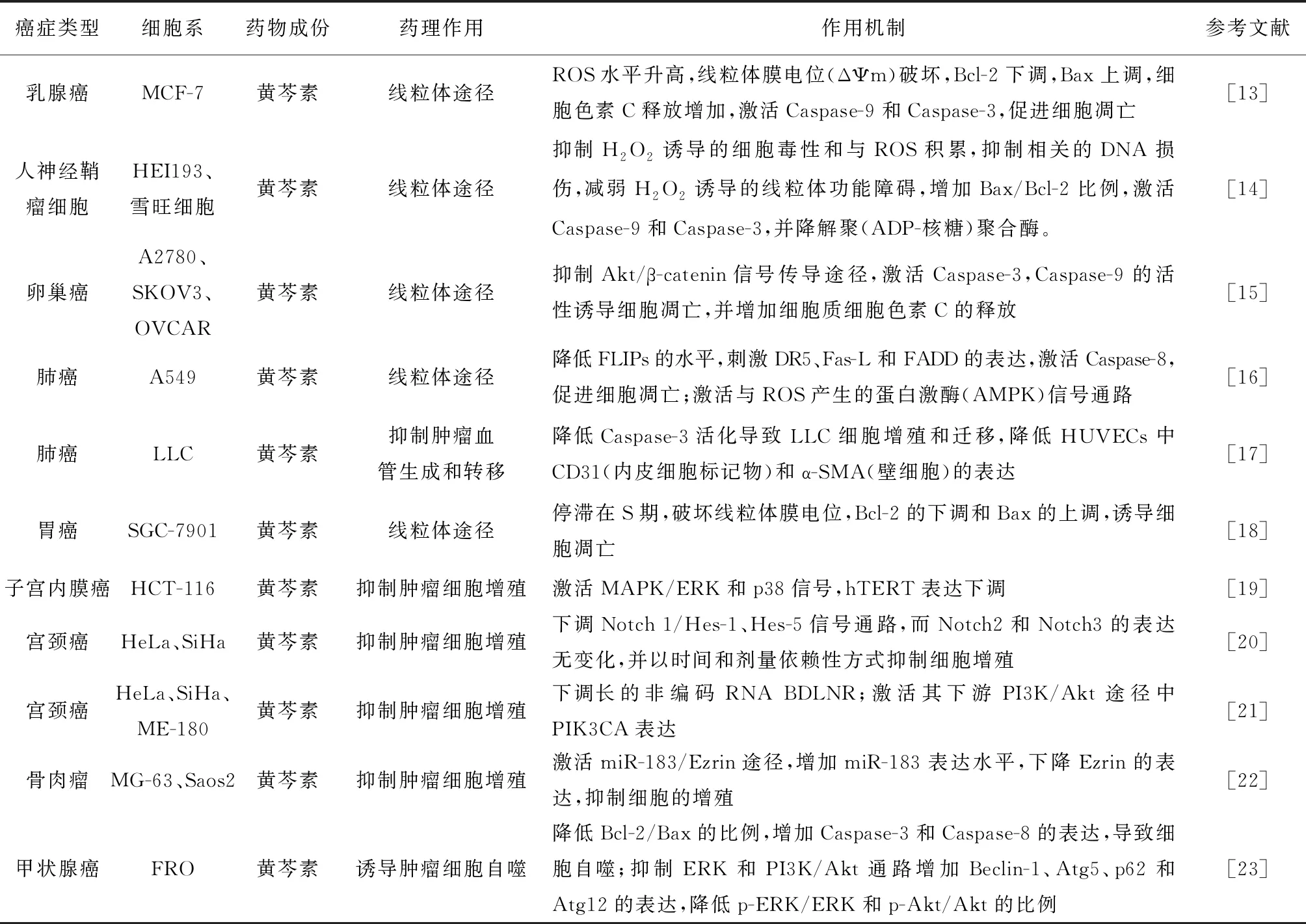
表2 黃芩素抗腫瘤藥理作用研究概況

表3 黃芩其他有效成分抗腫瘤藥理作用研究概況
1 黃芩及其有效成分可誘導腫瘤細胞凋亡
細胞受到外界刺激,在相關基因作用下通過激活內源性(線粒體)或外源性(死亡受體)途徑啟動半胱氨酸天冬氨酸蛋白酶(Caspase)家族發生級聯反應從而誘導細胞凋亡[30]。黃芩及其有效成分作用在細胞膜上的死亡受體,通過細胞凋亡主要途徑,即線粒體途徑、內質網途徑、死亡受體途徑誘導腫瘤細胞死亡。
1.1 經線粒體途徑誘導細胞凋亡
線粒體在細胞生命活動調控過程中起著關鍵作用。黃芩及其有效成分通過影響Bcl-2家族成員、細胞凋亡誘導因子(apoptosis inducing factor,AIF)、第2個線粒體衍生的半胱天冬蛋白酶激活劑(second mitochondria-derived activator of Caspases,Smac)、活性氧(reactive oxygen species,ROS)、腫瘤內蛋白p53(tumor protein P53,p53)等影響因子,參與激活Caspase凋亡途徑從而造成線粒體功能障礙,改變線粒體膜通透性,釋放細胞色素C和其他相關蛋白誘導腫瘤細胞凋亡[31-32]。黃芩素作為一種抗氧化劑可通過動員細胞內銅和生成ROS來觸發人乳腺癌細胞MCF-7的線粒體凋亡途徑,導致細胞內線粒體膜電位破壞,ROS水平升高,Bcl-2/Bax的比例降低,細胞色素C釋放增加,觸發MCF-7細胞凋亡機制[13]。黃芩素還可通過抑制HEI193雪旺細胞中H2O2誘導的細胞毒和ROS的積累,有效抑制相關的DNA損傷,減弱H2O2誘導的線粒體功能障礙,因此黃芩素可能通過Nrf2/HO-1信號通路依賴性機制實現抗氧化功能[14]。
1.2 經內質網途徑誘導細胞凋亡
內質網應激(endoplasmic retieulum stress,ERS)是內質網內Ca2+或內質網蛋白的過量積累,導致ER內穩態失衡,從而造成細胞損傷。而通過未折疊蛋白反應(unfolded protein response,UPR)可減少ERS引起的細胞損傷,多種類型的癌癥中已應用此機制,如宮頸癌、乳腺癌、肺癌、胃癌和胰腺癌等。黃芩及其有效成分可破壞腫瘤細胞內環境嚴重失衡,刺激ERS誘導腫瘤細胞凋亡[33]。研究發現漢黃芩苷可誘導胃癌細胞產生ERS,提高細胞中應激蛋白葡萄糖調節蛋白94 (glucose regulated protein 94,GRP94),磷酸化α亞基的真核起始因子2(phosphorylated α subunit of eukaryotic initiation factor 2,p-eIF2α)和CHOP的表達水平,造成細胞損傷,導致細胞凋亡[10]。漢黃芩素可通過ERS促使S315和S376位點上的P-p53表達增加,促進p53的細胞質定位,從而誘導細胞凋亡[27]。
1.3 經死亡受體途徑誘導細胞凋亡
細胞中的死亡受體主要包括轉鐵蛋白受體1(transferrin receptor-1,TFR-1)、Fas受體、死亡受體(death receptors,DR)3、DR4和DR5五種類型,所涉及誘導細胞凋亡的信號通路主要包括腫瘤壞死因子(tumor necrosis factor,TNF)相關凋亡誘導配體(TNF-related apoptosis-inducing ligand,TRAIL)、Fas受體/Fas配體(FAS ligand,FAS-L)、腫瘤壞死因子受體(tumor necrosis factor receptor,TNFR)等三條途徑。黃芩及其有效成分通過相關信號通路促使死亡受體與其特定死亡配體結合,從而誘導細胞凋亡[34]。黃芩提取物可通過誘導人乳腺癌細胞MCF-7的sub-G1期比率增加,線粒體膜電位改變,ROS的生成增加,誘導細胞凋亡,但其對Fas、FAS-L或TNF-α的表達水平沒有影響[26]。黃芩乙醇提取物可通過對多磷酸酰肌醇-3-羥基酶(phosphatidylinositol3-hydroxy Kinase,PI3K)/Akt信號傳導通路的抑制,增強人白血病U937細胞中DR及其相關配體的表達[28]。
2 黃芩及其有效成分抑制腫瘤細胞增殖
黃芩及其有效成分通過抑制相關信號通路阻滯腫瘤細胞分裂周期、抑制腫瘤細胞增殖從而阻止腫瘤惡化。HU等[20]對黃芩素在人宮頸癌中的抗腫瘤作用機制研究中,探討了黃芩素治療是否影響人宮頸癌的Notch信號通路,結果表明黃芩素處理可下調Notch受體(Notch Receptor,Notch)1/Hes-1,Hes-5信號通路,而Notch 2和Notch 3的表達沒有明顯變化,并以劑量依賴性方式抑制SiHa細胞和HeLa細胞的增殖。Dou等[19]研究了黃芩素和黃芩苷是否抑制人結腸癌細胞的生長和增殖,結果顯示兩者均可誘導細胞周期停滯,抑制腫瘤細胞集落的形成和遷移,揭示黃芩素可通過抑制腫瘤細胞中端粒酶逆轉錄酶表達從而誘導腫瘤細胞衰老,而黃芩苷是通過絲裂原活化蛋白激酶(mitogen-activated protein kinase,MAPK)/細胞外調節蛋白激酶(extracellular regulated protein kinases,ERK)和p38信號通路調節結腸癌細胞凋亡和衰老。
3 黃芩及其有效成分誘導腫瘤細胞自噬
自噬(autophagy)是細胞內物質和能量進行循環的重要過程,其通過自噬泡包裹錯誤蛋白或受損細胞器,經溶酶體酸性水解酶水解作用產生氨基酸等生物分子,最終被細胞再利用過程[35]。研究發現,自噬既能抑制腫瘤的發生,減少DNA損傷和氧化應激,從而維持基因組穩定,也能保護腫瘤細胞在營養能量匱乏的環境下生存,并且也是產生腫瘤耐藥的重要途徑之一[36]。研究發現黃芩中總黃酮苷元提取物可通過PI3K/Akt/mTOR信號通路誘導胰腺癌細胞自噬[29]。黃芩素可通過降低Bcl-2/Bax的比例和增加Caspase-3和Caspase-8的表達,誘導未分化甲狀腺癌細胞FRO細胞自噬[23];同時黃芩素可顯著增加自噬相關蛋白Beclin-1、Atg5、p62和Atg12的表達,降低p-ERK/ERK和p-Akt/Akt的比例,表明黃芩素可通過抑制PI3K/Akt和ERK信號通路從而誘導細胞自噬。
4 黃芩及其有效成分抑制腫瘤新生血管生成和轉移
研究發現,抑制腫瘤生長和轉移的最新研究熱點是以腫瘤血管內皮細胞為研究靶點,抑制腫瘤血管生成從而阻斷腫瘤細胞新陳代謝所必須的氧氣和營養的供應,因此通過調控血管生成相關的蛋白或基因,如血管內皮生長因子(vascular endothelial growth factor,VEGF)和基質金屬蛋白酶(matrix metalloprotinase,MMP)[37],抑制為腫瘤血管供養的途徑,從而導致腫瘤不能生長轉移甚至死亡。研究表明,黃芩苷和漢黃芩素可降低VEGF的表達和活性,抑制血管生成,并在體內外對癌細胞活力和增殖產生影響[38]。而黃芩素可通過降低Caspase-3活化導致B16F10和LLC細胞增殖和遷移并誘導腫瘤細胞死亡;還可使臍靜脈內皮細胞HUVECs中的血小板—內皮細胞黏附分子(platelet endothelial cell adhesion molecule-1,PECAM-1/CD31)和α-平滑肌肌動蛋白(α-Smooth muscle actin,α-SMA)的表達降低,表明黃芩素可通過破壞腫瘤血管發育從而抑制腫瘤新生血管生成和細胞遷移[17]。因此,黃芩及其有效成分是潛在的抑制腫瘤新生血管生成和轉移的治療藥物。
5 黃芩及其有效成分調節腫瘤微環境
5.1 通過免疫逃逸調節腫瘤微環境
調控腫瘤生長轉移和免疫治療反應的關鍵因素是腫瘤細胞和腫瘤微環境的代謝重編程。快速增殖的腫瘤細胞、腫瘤浸潤淋巴細胞(tumor infiltrating lymphocytes,TIL)和血管內皮細胞三者共同競爭氧氣和營養物質,并產生免疫抑制代謝物,導致腫瘤細胞免疫逃逸。研究發現腫瘤細胞代謝可影響腫瘤微環境[39-40],腫瘤浸潤淋巴細胞與腫瘤細胞之間存在營養物質的代謝競爭,糖酵解過程抑制TIL中T細胞的葡萄糖消耗,導致T細胞衰竭和免疫逃逸[41]。除競爭營養物質外,腫瘤細胞代謝產物還可對微環境中的免疫細胞產生影響,如乳酸是腫瘤細胞中有氧糖酵解增加產生的副產物,其可通過自噬因子FIP200的表達降低,并誘導天然T細胞的凋亡,同時也抑制NK細胞和T細胞轉錄因子活化T細胞核因子(nuclear factor of activated T cells,NFAT)的活性,從而導致γ-干擾素(interferon,IFN-γ)分泌減少,誘導腫瘤發生[42]。此外,乳酸可以通過穩定缺氧誘導因子1α多肽(hypoxia-inducible factor 1-alpha,HIF-1α)促進巨噬細胞向M2型極化[43]。
5.2 通過腫瘤相關巨噬細胞調節腫瘤微環境
腫瘤相關巨噬細胞(tumor-associated macrophages,TAMs)在腫瘤進展中發揮重要作用,包括形成免疫抑制微環境,促進腫瘤發生和轉移,促進腫瘤新生血管生成等[44]。研究發現,在具有免疫功能的腫瘤微環境中,腫瘤發生涉及的TAMs參與腫瘤微環境浸潤過程,TAMs由M2型向M1表型的轉表征有助于腫瘤消退,且此表型的逆轉是誘導抗腫瘤免疫應答的直接有效方法。體內外研究發現黃芩苷通過誘導TAMs由M2型向M1型極化,進而抑制肝癌的生長。同時,黃芩苷啟動TAMs中腫瘤壞死因子受體相關因子2(TNF receptor-associated factor 2,TRAF2)的自噬降解并激活RelB/p52途徑,從而誘導向M1型極化。因此,黃芩苷可能抑制HCC的發生[8]。研發還發現含有黃芩苷的仿生納米顆粒,其包含抗原肽(Hgp 10025-33)和toll樣受體9種激動劑(CpG),其通過誘導的CD4+T和CD8+T細胞向腫瘤部位的浸潤增加,表現出免疫激活作用和增強T細胞的免疫應答作用,有效抑制了體內黑素瘤腫瘤的生長[45]。因此,黃芩苷仿生納米顆粒有效地將TAM表型從M2型逆轉為M1型,從而改善了腫瘤免疫微環境,并促進了腫瘤免疫治療。
6 含黃芩復方的抗腫瘤作用機制研究探索
黃芩是中藥經典復方的重要組成成分之一,如:黃芩湯、小柴胡湯和黃連解毒湯等。上述經典復方通常用于治療腫瘤相關癥狀,并受到世界廣泛關注。黃芩湯出自《傷寒論》[46],是有望第一個獲得美國食品藥品監督管理局(food and Drug Administration,FDA)批準的傳統復方中藥制劑,目前已進入腸癌、肝癌、胰腺癌等Ⅱ期臨床研究中,且臨床前研究效果顯著。Liu等[47]通過分子建模技術研究黃芩湯(YIV-906)抑制雙特異性蛋白磷酸酶(dual specificity protein phosphatase, DUSP)的機制,模擬結果發現YIV-906中的有利配體硫酸鹽和羧基部分可以占據酶的催化位點,抑制ERK1/2與DUSPs的結合,減少ERK1/2的去磷酸化,停滯腫瘤細胞周期,最終誘導腫瘤細胞凋亡。GAO等[37]在研究小柴胡湯在體內外誘導人肝癌HUH7細胞凋亡機制中發現,其減少腫瘤的大小和質量,并通過改變Bax、Bcl-2、CDK4和cyclin-D1的表達,促進細胞凋亡。除了經典復方,現代中藥復方制劑同樣顯示出潛在的抗腫瘤活性。如中藥復方PC-SPESⅡ,其以靈芝為君藥,配以黃芩、冬凌草、大青葉等為臣藥,前期體內藥效學表明通過雄激素受體信號轉導通路來抑制前列腺癌細胞LNCaP的增殖,并阻滯細胞于G2/M期,誘導細胞凋亡[25]。目前發現關于含黃芩復方的研究相對較少,推測可能與復方有效成分的鑒定復雜、作用機制交叉相關,因此明確復方、單味藥有效成分,以及在此基礎上的有效成分之間的配伍組合,甚至和療效明確的腫瘤分子靶向藥物的組合運用,可能是今后重要研究方向。
7 思考與展望
綜上所述,黃芩中有效成分黃酮類化合物通過相關分子機制如促進腫瘤細胞凋亡、誘導腫瘤細胞增殖、誘導腫瘤細胞自噬、新生血管生成和調節腫瘤微環境等實現抗不同類型腫瘤的作用,其作用機制呈現出多靶點、多途徑的特點,使其具有良好的研究及應用前景。然而,其存在選擇性較低、細胞毒性較大、抗腫瘤機制研究不夠深入等問題。因此,對黃芩及其有效成分做進一步的改良及官能團修飾,篩選出活性更高、選擇性更強、細胞毒性更低的衍生物,進行藥理活性評價及其機制研究,將成為未來的研究重點及熱點。

